经结肠系膜入路TaTME治疗直肠癌的疗效及安全性研究
2021-04-09周仲鹏刘丹南嘉玮
周仲鹏,刘丹,南嘉玮
1.富平县中西医结合医院外科,陕西渭南711700;
2.咸阳市第一人民医院普外科,陕西咸阳712000
直肠癌是临床上常见的消化道恶性肿瘤之一,发病原因和日常饮食习惯、环境、遗传等相关,我国目前的发病中位年龄在45岁左右,但近年来在青年人群中也有发病升高的趋势[1-2]。早期接受手术切除病灶是延长患者生存期、改善生活质量的重要手段。经肛全直肠系膜切除术(TaTME)是一种新型的自然腔道内镜手术,但TaTME术中选择何种入路方式仍是临床医师探讨的问题[3-4]。本研究旨在观察经结肠系膜入路在TaTME术中的应用效果。
1 资料与方法
1.1 一般资料回顾性分析2016年1月至2018年1月陕西省富平县中西医结合医院接诊的90例直肠癌患者的诊疗情况。纳入标准:①通过直肠镜检组织病理学、盆腔磁共振检查、盆腔CT检查等确诊为直肠癌,肿瘤分期T1~3N0M0[5];②肿瘤下缘距离肛缘≤7 cm;③机体状况良好,可耐受手术;④临床资料完整,配合完成随访。排除标准:①经检查显示肿瘤侵犯肛提肌或者肛门括约肌;②已出现远处转移;③已出现肿瘤所致的肠穿孔、肠梗阻等并发症;④肿瘤远端肠管手术扩张能力缺乏;⑤既往接受过腹部手术;⑥合并其余恶性肿瘤;⑦合并其余重大疾患。按照手术不同入路方式分为观察组和对照组,每组45例,两组患者的一般资料比较差异均无统计学意义(P>0.05),具有可比性,见表1。本研究已获得我院医学伦理委员会批准。
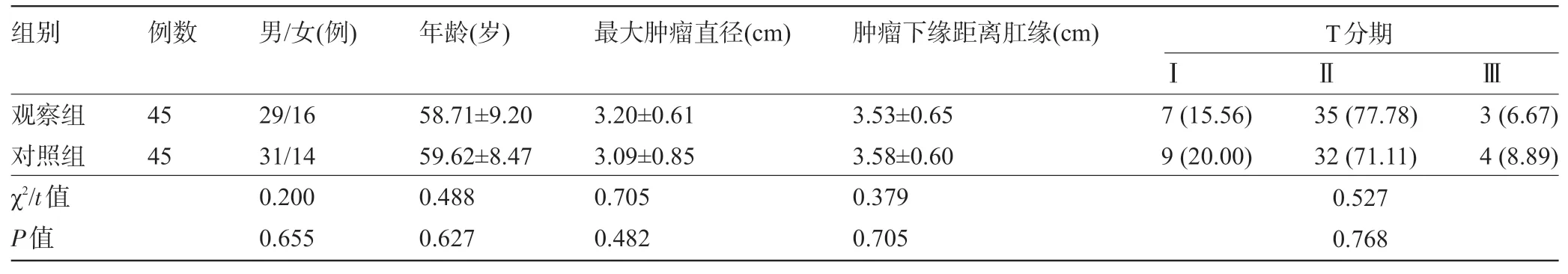
表1 两组患者的一般资料比较[x±s,例(%)]
1.2 方法
1.2.1 对照组该组患者采用传统腹腔镜直肠全系膜游离方式。具体方法:①患者选择全身麻醉,取截石位,常规消毒铺巾,建立气腹和操作平台;②探查腹腔,助手将乙状结肠提起,在乙状结肠系膜根部右侧黄白交界线的部位,将腹膜切开,进入直肠后间隙;③对肠系膜下血管进行游离,保留左结肠动脉,对第253组淋巴结和脂肪组织进行清扫;④将肠系膜下静脉和直肠的上动脉切断,并游离Toldt间隙,将乙状结肠外侧的黏连处分离,切开乙状结肠外侧的腹膜位置;⑤根据全直肠系膜切除的手术原则,将直肠游离至腹膜反折后,沿着乙状结肠血管弓内侧1 cm的部位,裁剪系膜直到距离肿瘤近端10 cm左右的位置,裸化肠管,使用自锁式尼龙扎带对肠管进行阻断,完成经腹游离。
1.2.2 观察组该组患者采用经结肠系膜入路。具体方法:①患者选择全身麻醉,取截石位,常规消毒铺巾,建立气腹和操作平台;②探查腹腔,将乙状结肠和左侧腹壁之间的黏连分离,提起乙状结肠,将肿瘤近端肠管10 cm的位置进行标记,作为近切缘,使用超声刀切断此系膜、边缘血管弓部位,裸化肠管,使用自锁式尼龙扎带将肠管阻断;③助手左手将自锁式尼龙扎带提起,右手将近端乙状结肠提起,令乙状结肠边缘的血管弓部位暴露,于距离边缘内侧1 cm的位置,使用电刀将标记系膜切缘切开;④系膜切开后,从远到近,依次对乙状结肠动静脉进行游离,再切断,游离降结肠系膜,保证结扎部位的血管可轻易下拉至骶骨岬远侧15 cm的位置;⑤通过乙状结肠系膜根部内侧的黄白交界线部位,将腹膜切开,进入TaTME手术间隙,对肠系膜下血管直到根部的部位进行游离,并仔细清扫第253组淋巴结;⑥对裸化肠系膜的下动脉和左结肠动脉进行远端游离,保留左结肠动脉,将直肠上动脉切断后,再游离肠系膜下静脉,于左结肠静脉交汇处进行切断;⑦于直肠后方的位置进行游离,直至到达第3骶椎或尾椎的部位,前方直至精囊腺或者阴道后穹窿的部位,两侧直至盆丛神经下方部位,完成经腹游离。两组患者经肛游离和吻合方式均相同,完成手术后均于腹腔镜下冲洗盆腔,常规放置引流管。术中手术切除原则均严格按照《中国结直肠癌诊疗规范(2017年版)》[5]中相关标准。
1.3 观察指标①术中情况:比较两组患者的经腹游离时间、手术时间、术中出血量、淋巴结清扫数量以及肿瘤标本至远端和近端的切缘长度、系膜完整率、环周切缘阳性率(<1 mm)情况;②术后情况:比较两组患者的尿管留置时间、初次肛门排气时间及住院时间;③并发症:比较两组患者术后并发症发生情况;④预后:比较两组患者2年内局部复发、远处转移及死亡情况。
1.4 统计学方法应用SPSS18.0软件进行数据统计学分析,计量资料以均数±标准差(x-±s)表示,组间比较采用t检验,计数资料比较采用χ2检验,以P<0.05表示差异具有统计学意义。
2 结果
2.1 两组患者术中情况比较两组患者均顺利完成手术,均无中转开腹患者。两组患者的术中出血量、淋巴结清扫数量、肿瘤标本至远端切缘长度、环周切缘阳性情况比较差异均无统计学意义(P>0.05);观察组患者的经腹游离时间、手术时间明显短于对照组,肿瘤标本至近端切缘长度、系膜完整率明显长于/高于对照组,差异均有统计学意义(P<0.05),见表2。
表2 两组患者术中情况比较(±s)
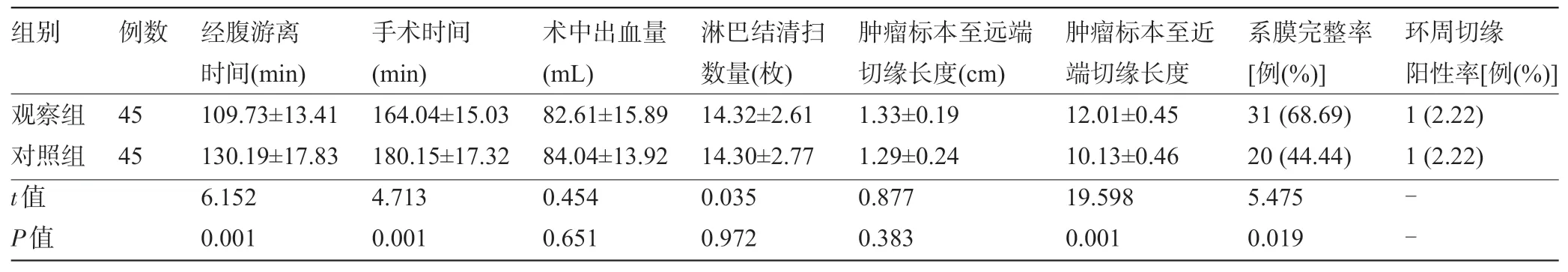
表2 两组患者术中情况比较(±s)
?
2.2 两组患者术后情况比较观察组患者术后尿管留置时间、初次肛门排气时间及住院时间明显短于对照组,差异均有统计学意义(P<0.05),见表3。
表3 两组患者术后情况比较(±s)
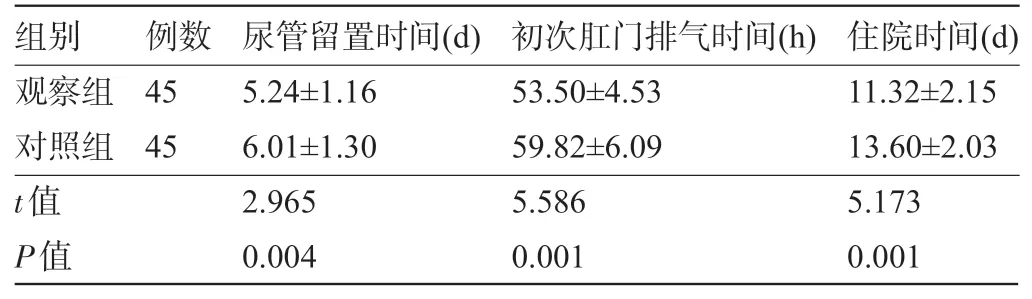
表3 两组患者术后情况比较(±s)
?
2.3 两组患者术后并发症比较两组患者术后吻合口瘘、乳糜漏、感染、肠梗阻经比较差异均无统计学意义(χ2=1.111,P=0.292>0.05),见表4。所有患者上述并发症均给予对症处理后予以好转出院,无围术期死亡患者。
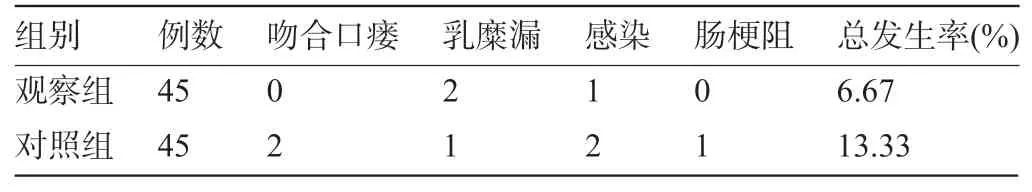
表4 两组患者术后并发症比较(例)
2.4 两组患者的预后情况比较术后2年随访结果显示,随访期间无非肿瘤相关性死亡患者,两组患者的局部复发、远处转移、死亡率比较差异均无统计学意义(P>0.05),见表5。
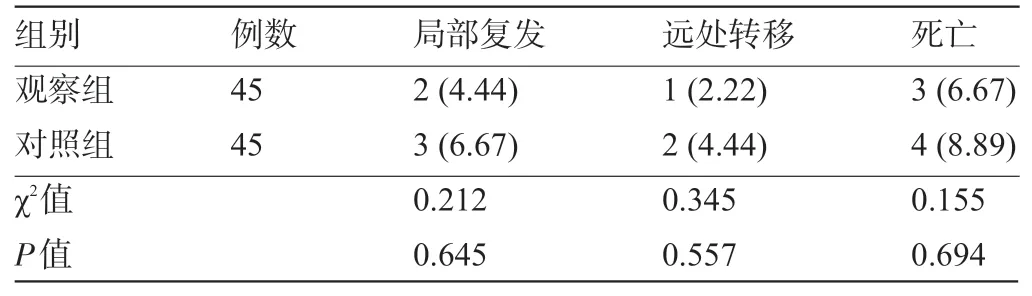
表5 两组患者预后情况比较[例(%)]
3 讨论
我国结直肠癌近30年来的患病率每年上升程度为3%~4%,在城市和农村地区的发病率分别占所有恶性肿瘤的第3位和第5位,且发病有逐渐年轻化的趋势,早期的直肠癌患者通常无明显的临床症状,随着疾病的进展,患者可逐渐出现排便习惯改变、大便性状改变、腹部不适等症状,对生活质量和生命安全均有着重要影响[6-7]。
TME手术理念是在1982年所提出,该方式可降低骶前间隙中残留于直肠系膜中散在肿瘤组织的机率,并减少远期局部复发率,随后逐渐成为直肠癌患者治疗的“金标准”术式[8-9]。随着近年来微创手术的不断发展,经肛门路径的微创手术也在逐渐兴起,其中具有代表性的则是TaTME术式[10]。该术式是在TME手术的基础上发展而来,手术经由肛门入路进入盆底,可克服腹式手术过程中的视线障碍问题,减少盆底分离难度,便于游离和切除低位直肠和系膜,且可保留直肠尾部系膜的完整,有助于提高手术质量[11-12]。在TaTME经腹操作过程中,乙状结肠的系膜裁剪是其中关键的环节,目前TaTME术式的经腹操作过程中,多是以中间、头侧中间和外侧进行入路,最后一步才是乙状结肠的系膜裁剪。但有研究发现,这样的步骤存在一定的弊端,主要包括以下几点:①切断直肠上动脉之后,乙状结肠的系膜扇形的牵拉会丧失张力,无法平展;②在乙状结肠系膜存在严重黏连、肥厚的患者中,难以准确的辨认各支血管和边缘的血管弓,延长系膜过程困难,可能会出现边缘血管损伤,甚至增加吻合口瘘并发症发生风险,影响预后;③当结肠长度拖出不够时,容易出现近端肠管切除过短,对手术效果产生影响[13-14]。
为克服上述弊端,本研究提出经结肠系膜入路TaTME用于直肠癌患者的治疗。本研究结果显示,两组患者在术中出血量、淋巴结清扫数量、肿瘤标本至远端切缘长度、环周切缘阳性情况方面比较差异均无统计学意义(P>0.05)。但使用结肠系膜入路TaTME的患者经腹游离时间、手术时间和肿瘤标本至近端切缘长度、尿管留置时间、初次肛门排气时间及住院时间结果均明显更短,且系膜完整率明显更高,体现出更好的应用优势。分析原因如下:①在对乙状结肠进行牵拉后,可使用未切断的肠系膜下血管或者直肠的上动脉部位,形成一种自然的对抗牵拉力量,并在直肠上动脉、乙状结肠和其系膜之间产生一个扇形平面,更容易辨认边缘的血管弓,便于对左结肠的显露及保护;②术中可充分显露乙状结肠血管,在使用电刀标记乙状结肠系膜裁剪显露之后,再进行裁剪处理,可减少对边缘血管弓不必要的损伤,提高手术安全性;③裁剪乙状结肠系膜之前,提前将边缘血管弓切断,并采用自锁式尼龙扎带将肠腔阻断,符合无瘤原则,且该处理也利于后期的游离,缩短经腹游离时间和总体手术时间[15];④裁剪乙状结肠之前对肿瘤近端的长度进行量化,可进一步确保肿瘤标本至近端肠管切缘的长度,保证系膜完整性;⑤在减少手术时间及术中损伤的同时,也有助于促进术后恢复,缩短尿管留置时间、初次肛门排气时间及住院时间。此外,本研究还显示,在术后并发症和2年的复发、远处转移及死亡情况的比较中,两组患者差异均无统计学意义(P>0.05),经结肠系膜入路TaTME未体现出更好的远期优势,但直肠癌患者的术后随访是一个漫长的过程,针对更远期的情况方面仍需持续探讨。
综上所述,经结肠系膜入路TaTME治疗直肠癌疗效明显,可明显减少经腹游离时间、手术时间,保证肿瘤标本至近端切缘长度和系膜完整性,且可促进术后恢复,值得推广应用。
