ChiCGB方案对非霍奇金淋巴瘤行自体造血干细胞移植的预处理效果
2021-04-01陈莉王凌云郭彩玲熊际群罗梦
陈莉 王凌云 郭彩玲 熊际群 罗梦
(四川大学华西医院 1.血液内科;2.风湿免疫科,四川 成都 610041)
淋巴瘤为源自淋巴组织或者淋巴结的恶性肿瘤,依据病灶组织细胞特点可以分为非霍奇金淋巴瘤(Non-Hodgkin's lymphoma,NHL)以及霍奇金淋巴瘤[1]。淋巴瘤患者中有近90%为NHL;我国NHL发病率高于国外,同时其发病率有逐渐上升趋势[2]。造血干细胞移植是治疗血液恶性疾病主要方式,在进行大剂量化疗之后行自体造血干细胞或者异体造血干细胞支持,使患者免疫功能以及造血功能可以有效恢复并达到重建,在患者安全情况下,应尽量杀灭肿瘤细胞,改善治疗效果[3]。造血干细胞移植预处理为影响患者移植效果重要环节,其处理目的为尽量杀灭肿瘤细胞,应用毒性低以及效果优异的预处理方案可以有效改善NHL治疗效果[4]。目前临床上应用较多预处理方案有BuCy、BEAm、CBV以及TBI方案[5-6]。本研究选择西达本胺+克拉屈滨+吉西他滨+白消安(ChiCGB)方案进行NHL患者自体造血干细胞移植前预处理,并观察治疗效果以及安全性,为后期该方案大量应用提供参考。
1 资料与方法
1.1 一般资料 收集我院2015年3月~2019年7月收治的66例NHL患者相关资料。纳入标准:①NHL病情经由病理检测以及免疫组织化学证实。②肿瘤分类依据WTO造血以及淋巴瘤分类要求[7]。③接受自体造血干细胞移植治疗,且治疗前以ChiCGB方案进行预处理。④所有资料完整。排除标准:①身体器官如心脏、颅脑等功能异常。②采用非自体造血干细胞移植方式进行治疗。③采用非ChiCGB方案预处理。④治疗资料,随访资料等不全者。66例患者中男性37例,女性29例;年龄16~63岁,平均(39.48±12.13)岁;疾病类型:B细胞NHL和T细胞NHL分别41例和25例;肿瘤分期Ⅰ~Ⅱ型和Ⅲ~Ⅳ型分别19例和47例。
1.2 方法
1.2.1 移植前治疗 66例患者在治疗前病情完全缓解、部分缓解以及病情进展患者分别43例、16例以及7例。患者接受移植前均接受4个周期化疗治疗,化疗方案包括BEACOP、CHOP、R-CHOP以及CHEP等。
1.2.2 自体造血干细胞动员与收集 采用粒细胞集落刺激因子(G-CSF)联合化疗作为患者造血干细胞动员方案,化疗方案应用患者移植前治疗有效化疗方案,按照情况适量上调化疗剂量。采用化疗方案治疗后待白细胞水平下降到最低后开始上升时皮下注射浓度为7 μg/(kg*d)G-CSF(齐鲁制药厂,国药准字Sl9990049,规格:100 μg:0.6 mL),注射时间2~12 d以达到动员患者造血干细胞目的。采用Baxter CS3000型号血细胞分离仪对含有CD34+细胞外周单核细胞进行分离。分离完成后对细胞悬液进行CD34+细胞以及单核细胞进行计数,应用RPMI1640培养液(内含10%DMSO)予以稀释,将其冻存于液氮中。
1.2.3 ChiGCB预处理 患者分别在移植前7 d、4 d、移植当天以及移植后第3 d早餐后30 min口服西达本胺片(深圳微芯生物科技有限责任公司,国药准字H2014012,规格:5 mg*24 s)30 mg;在移植前2~6 d静脉注射10 mg克拉屈滨(海正辉瑞制药有限公司,国药准字H20052240,规格:10 mL:克拉屈滨10 mg与氯化钠90 mg);移植前6、前2 d静脉注射吉西他滨(江苏豪森药业集团有限公司,国药准字H20030104,规格:0.2 g),注射浓度为2500 mg/m2,在克拉屈滨注射完成后4 h静脉注射;在移植前3~6 d静脉注射浓度为3.2 mg/kg白消安(Ben Venue Laboratories Inc,注册证号BH20040642,规格:10 mL:60 mg),此期间同时注射5 mg地塞米松磷酸钠注射液(上海现代哈森(商丘)药业有限公司,国药准字H41021924,规格:1 mL:5 mg)。
1.2.4 自体造血干细胞输注 患者进行单核细胞以及CD34+细胞输注,移植完成后5 d进行7 μg/(kg·d)浓度G-CSF皮下注射,至患者白细胞计数超过4×109/L后停药。
1.2.5 支持治疗 移植前患者需要分别应用阿昔/更昔洛韦、复方磺胺甲恶唑片以及氟康唑预防病毒、卡氏肺孢子虫以及真菌感染,同时还需用药避免出血性膀胱炎以及改善患者肠胃道反应。
1.2.6 随访 患者移植治疗出院后通过住院复查、病历资料查询、门诊复查以及电话随访等形式进行随访,随访截止时间为2020年4月30日,随访时间6~51个月,中位随访时间为20个月。
1.3 观察指标 分析自体造血干细胞采集情况、移植完成后造血重建情况、预处理毒性、患者疗效以及生存情况。
1.4 评价标准 造血重建标准:粒细胞植入为G-CSF注射后中性粒细胞超过0.5×109/L,且超过时间达到连续3 d以上的第1 d,血小板植入为未进行血小板输注血小板水平即超过20×109/L,且超过时间达到连续3 d以上的第1 d。不良反应:在患者进行预处理当天开始评估患者治疗毒性,标准依据美国国立癌症研究所常规毒性评定标准[8]予以评估。疗效标准:按照国际淋巴瘤工作组制定标准[9]在患者移植完成后3个月评估治疗效果,将患者治疗效果分为完全缓解、部分缓解、病情稳定以及进展。移植后总反应率为患者完全缓解率以及部分缓解率之和,结局指标主要指总生存率以及无进展生存率。总生存时间(OS)为患者进行造血干细胞输注时间到随访截止或者死亡时间。无进展生存时间(PFS)为造血干细胞移植后患者病情获得完全缓解到病情复发、死亡或者随访截止时间。

2 结果
2.1 自体造血干细胞采集情况分析 患者每次进行采集循环血量为7000~11000 mL,进行了2~3次血量采集,单核细胞及CD34+细胞数量分别为(6.83~20.5)×108/kg和(1.39~28.53)×108/kg,中位数分别为11.36×108/kg和13.68×106/kg。所有采集造血干细胞均置于液氮中保存,采集完成后1~3个月行细胞输注。
2.2 移植完成后造血重建分析 66例患者均顺利完成造血重建,粒细胞植入时间为7~16 d,平均(10.32±3.14) d;血小板置入时间为8~21 d,平均(12.28±5.06) d。
2.3 预处理毒性分析 预处理所致毒性主要包含发热、恶心呕吐、感染以及腹泻等,见表1。66例患者移植期间有37例(56.06%)患者出现感染,病原学检测显示患者肺部、肠道以及尿路感染分别9例(13.64%)、3例(4.55%)以及1例(1.52%),粒细胞缺乏并感染20例(30.30%),败血症4例(6.06%)。
2.4 患者疗效分析 66例患者移植完成后3个月达到完全缓解和部分缓解患者分别为46例和17例,而病情稳定及进展分别为3例和0例。患者移植后总反应率为95.45%。
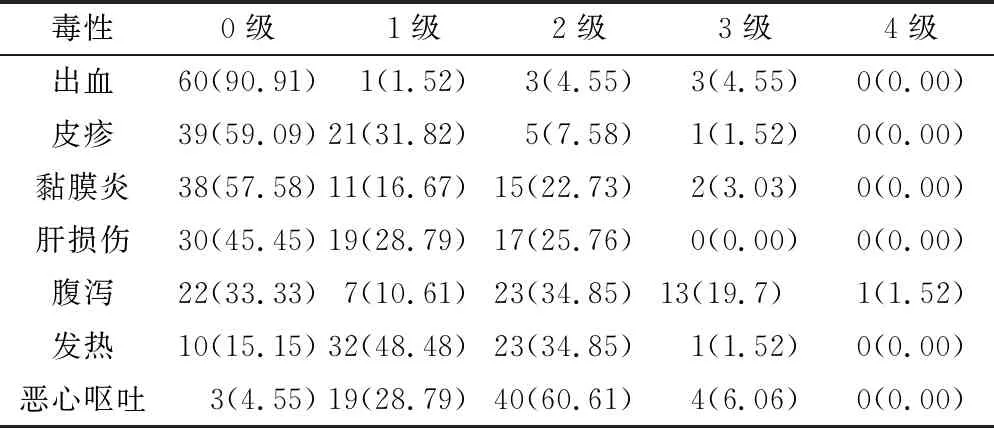
表1 预处理其他毒性[n(×10-2)]
2.5 生存分析
2.5.1 移植后患者生存情况 66例患者随访时间6~51个月,中位随访时间为26个月,在随访期间29例患者病情进展,19例患者死亡,其中16例因为病情进展而死亡,剩余3例死亡原因分别为脓毒症、肝功能衰竭以及心律失常。至随访结束时间,患者1年OS率和PFS率分别为84.85%和71.21%,3年OS率和PFS率分别为72.73%和60.61%,见图1。
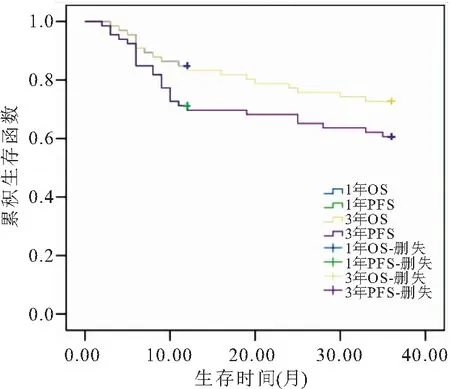
图1 1年和3年OS和PFS率
2.5.2 患者3年OS和PFS率单因素分析 单因素分析结果显示,疾病分期、难治性或者复发性疾病与患者3年OS率有关(P<0.05),与年龄、疾病分类、病情确诊至移植时间、移植前治疗效果、IPI评分与患者3年OS率无关(P>0.05);疾病分类、疾病分期、IPI评分与患者3年PFS率有关(P<0.05),与年龄、病情确诊至移植时间、移植前治疗效果、难治性或者复发性疾病与患者3年PFS率无关(P>0.05),见表2。
2.5.3 患者3年OS和PFS率多因素分析 COX回归分析结果显示,疾病分期、难治性或者复发性疾病为影响患者3年OS率的独立危险因素(P<0.05);疾病分期是影响患者3年PFS率的独立危险因素(P<0.05),疾病分类、IPI评分不是影响患者3年PFS率独立危险因素(P>0.05),见表3。
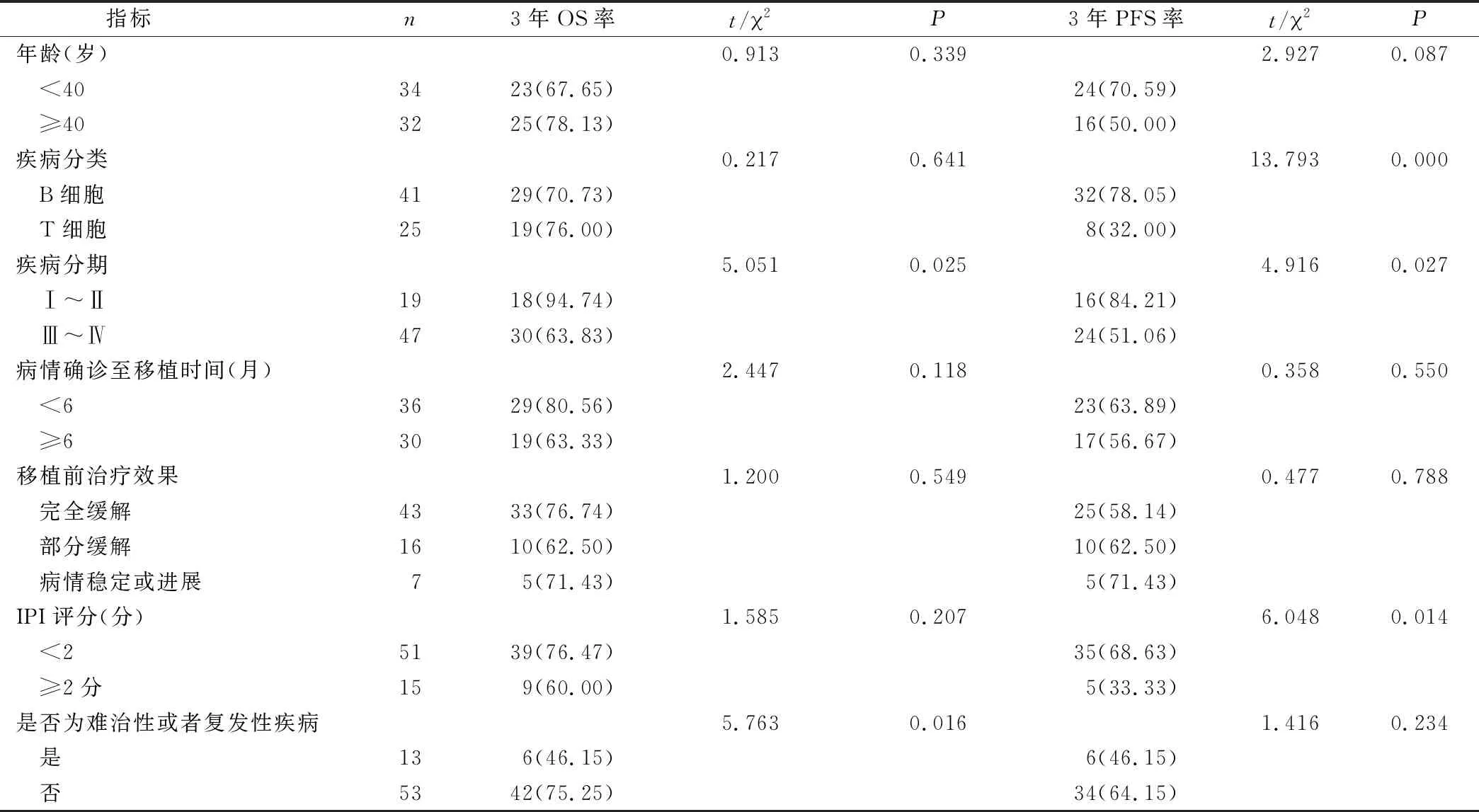
表2 影响患者3年OS和PFS单因素分析
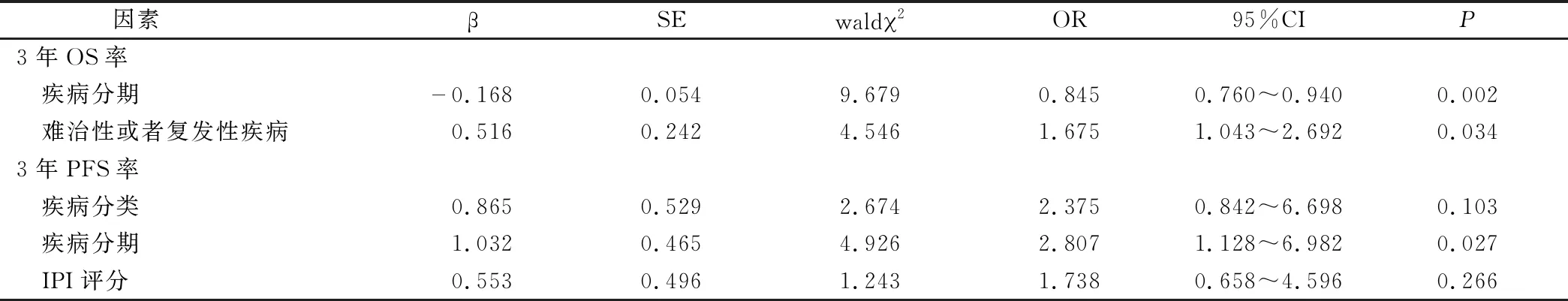
表3 患者3年OS和PFS率多因素分析
3 讨论
NHL患者治疗后病情复发导致治疗效果不佳,而造血干细胞移植可有效改善高危NHL患者预后,是恶性血液疾病治疗新方式[10]。造血干细胞移植中干细胞可以来源于自体以及异基因,接受异基因来源造血干细胞移植患者虽然移植完成后复发率低,但是患者移植后并发症相关死亡率较高,同时治疗费用昂贵,其治疗存在一定局限性[11]。自体造血干细胞不会受到干细胞供者影响,植入后不会出现免疫排斥反应,同时移植相关并发症发生率低,该方式治疗安全经济,治疗适宜人群广[12]。移植前预处理是自体造血干细胞移植治疗中重要环节,同时也是自体造血干细胞移植研究难点与热点。
史幼梧等[13]研究显示,在霍奇金淋巴瘤自体造血干细胞移植应用CBV、BEAM以及BEAC预处理方案患者治疗后5年PFS率分别为69.2%、46.9%以及54.5%,5年OS率分别为100%、100%以及90.9%。另有研究[14]显示,复发难治性淋巴瘤进行异基因造血干细胞移植之前采用BEAM、Cy/TBI、Bu/Cy以及改良Bu/cy预处理方案患者2年OS率为46.1%。本研究中患者1年OS率和PFS率分别为84.85%和71.21%,3年OS率和PFS率分别为72.73%和60.61%,提示自体造血干细胞移植前行ChiCGB方案预处理是安全可行的,治疗NHL疗效肯定。对于患者生存情况影响因素分析结果显示,疾病分期、难治性或者复发性疾病为影响患者3年OS率独立危险因素,疾病分期是影响患者3年PFS率独立危险因素。王希等[15]研究认为淋巴瘤患者病情分期可有效反映患者病情严重程度,分期高患者出现远处以及淋巴结转移风险更大,患者预后不佳可能性高。韩婷婷等[16]研究同样认为临床分期与青少年非霍奇金淋巴瘤患者OS率关系密切,Ⅰ~Ⅱ期和Ⅲ~Ⅳ期患者3年OS率分别为100%和60.4%。江梦天等[17]研究发现复发难治性淋巴瘤治疗采用化疗联合自体造血干细胞移植治疗前疗效不能导致完全缓解,患者在移植前进行PET/CT检查时显示患者阴性率较低,患者预后情况不佳。
克拉屈滨、阿糖胞苷以及白消安可以有效改善肿瘤细胞对化疗治疗敏感性,经由消耗DNA甲基转移酶导致患者体内白血病细胞凋亡,尽可能杀灭患者体内存在肿瘤细胞,有效避免白血病患者治疗后病情复发[18-19]。本研究中预处理方案选择西达本胺+克拉屈滨+吉西他滨+白消安联合用药,其中吉西他滨作为相同嘧啶类抗癌药物,作用机制与阿糖胞苷相似。在此方案中加入组蛋白去乙酰化酶抑制剂(HDACi)西达本胺,可以进一步增强了CGB肿瘤细胞杀灭能力[20-22]。另有研究[23]证实了克拉屈滨诱导持久缓解淋巴瘤治疗潜力。国外研究者应用西达本胺治疗淋巴瘤疗效及安全性较好[24]。Chen等[25]研究显示白消安在NHL自体干细胞移植中的疗效。
杨懿春等[26]研究认为造血重建是自体造血干细胞移植成功关键,重建时间越短患者生存率越佳,移植所致死亡率明显下降。本研究中所有患者均顺利完成造血重建,粒细胞植入平均时间为(10.32±3.14)d,血小板平均植入时间为(12.28±5.06)d,低于张建华等[27]研究中患者造血重建时间。粒细胞植入时间以及血小板植入时间短有效保证了患者其后治疗效果。本研究中患者移植后3个月总反应率为95.45%,即患者移植后3个月完全缓解以及部分缓解效果较好。本研究中自体造血干细胞移植患者较高的预处理相关并发症有感染、腹泻、发热、恶心呕吐,采用积极对症治疗后大部分患者对毒性相关耐受性,不良反应发生率与陈颖莹等[28]研究中淋巴瘤自体造血干细胞移植采用CEAC预处理不良反应结果相似。本研究为回顾性研究,纳入病例较少,未对不同预处理方案患者治疗效果进行分析,其后可进行多中心、大样本前瞻性随机研究进一步评估ChiCGB预处理方案与其他预处理方案之间的优劣,以期筛选出最合适预处理方案。
4 结论
NHL患者行自体造血干细胞移植前采用ChiCGB方案预处理无不可接受预处理毒性,同时患者预后较好,是自体造血干细胞移植患者安全有效的预处理方案。
