VmaH和PMA在指状青霉中的表达及其作为潜在杀菌作用靶点的可能性
2021-03-31彭丽桃杨书珍
范 明,彭丽桃,闫 等,范 刚,杨书珍,李 杰
(华中农业大学食品科技学院,湖北 武汉 430070)
由指状青霉(Penicillium digitatum)侵染导致的柑橘绿霉病是引起采后柑橘腐败变质的重要原因。据统计,约有90%的腐烂柑橘果实是由于被指状青霉侵染所致,经济损失巨大[1]。目前,化学杀菌剂处理仍是控制柑橘采后贮运病害的重要手段,但化学杀菌剂的长期大量使用使得病原真菌的抗药性日益增强,杀菌剂的使用周期显著缩短[2-4]。因此,研究与开发具有新型药物作用靶点的杀菌剂对柑橘采后安全生产具有十分重要的意义。
酸碱平衡是维持细胞内环境稳定、保证细胞正常代谢与功能的前提[5]。为了适应更多极端的生长和侵染环境,真菌细胞较其他真核生物具有更强大的pH值调控和H+转运机制[6]。其中V型ATP酶质子泵(vacuolar H+-ATPase,V-ATPase)和P型质子泵(plasma membrane H+-ATPase,P-ATPase)在保持细胞内的pH值动态平衡和建立细胞膜内外的质子梯度中起着关键作用[7-9]。在球孢白僵菌的研究中发现V-ATPase功能的缺失导致细胞内pH值和钙离子的失衡,从而影响了真菌细胞骨架的维持[6]。对白色念珠菌的研究表明[10],编码V-ATPase亚基的基因缺失会导致菌株毒力降低。Billack等[11]研究也发现P-ATPase在白色念珠菌致病力上具有重要作用。因此,V-ATPase和P-ATPase在真菌细胞生命活动和对寄主的侵染过程中发挥着重要作用。
VmaH(vacuolar ATP synthase subunit H)基因所编码的蛋白是V-ATPase的一个关键亚基,它不但调控复合体V1和V0的组装,而且还通过调控ATP(水解ATP)活性而调控H+跨膜运输[12]。Rizzo等[13]研究表明VmaH基因表达水平的差异会影响V-ATPase的组装。VmaH基因的缺失会导致害虫的死亡和真菌侵染毒力的下降[14-15]。PMA1(plasma membrane ATPase 1)是编码P-ATPase的主要基因,位于细胞质膜上,主要是产生电化学梯度,把细胞内的H+泵出膜外,驱动一定数量的次级跨膜转运系统,促进离子和代谢物的吸收;同时P-ATPase有助于保持细胞内pH值的调节,维持细胞内pH值的相对稳定,从而保证各种生命活动的正常运行[16]。Morsomme等[17]研究表明,PMA缺陷型真菌突变体的许多生理活动不能正常进行,生长几乎停止。但目前有关VmaH和PMA的研究主要集中在植物[18-19]、酵母菌[6,14]和其他少量真菌上,对于植物病原真菌尤其是柑橘绿霉病菌中VmaH和PMA基因的研究尚鲜见报道。本研究在利用生物信息学分析VmaH和PMA基因的基础上,采用实时聚合酶链式反应(real-time polymerase chain reaction,real-time PCR)技术分析VmaH和PMA在柑橘绿霉病菌中的表达规律,进一步探讨VmaH和PMA作为抑制柑橘绿霉病的药物作用靶点的可行性,以期为研发适合柑橘采后病害控制的新型、安全、高效的柑橘采后杀菌剂提供参考。
1 材料与方法
1.1 材料与试剂
指状青霉菌株(菌株编号:DSM62840),购自德国微生物菌种保藏中心。
马铃薯蔗糖琼脂(potato saccharose agar,PSA)培养基:马铃薯200 g,加入1 L蒸馏水,煮沸后取滤液加入蔗糖10 g,琼脂20 g。马铃薯蔗糖肉汤(potato saccharose broth,PSB)培养基:马铃薯200 g,加入1 L蒸馏水,煮沸后取滤液加入蔗糖10 g。
柱式真菌总RNA抽提纯化试剂盒、柱式植物总RNA抽提纯化试剂盒 生工生物工程(上海)股份有限公司;HiScript®II Q RT SuperMix for qPCR(+gDNA wiper)反转录试剂盒、荧光定量试剂盒 南京诺唯赞生物科技有限公司;松属素、香芹酚、辛烯醛阿拉丁试剂(上海)有限公司。
1.2 仪器与设备
qTOWER2.2实时定量PCR仪 德国耶拿分析仪器股份有限公司;Gel Doc XR+凝胶成像仪 美国Bio-Rad公司;SPX-150BIII生化培养箱 北京鑫润科诺仪器仪表有限公司;SHZ-82A气浴恒温振荡箱 金坛市宏华仪器厂;YXQ-LS-18SI手提式压力蒸汽灭菌器 上海博讯实业有限公司;LGJ-10冷冻干燥机 北京松源华兴科技发展有限公司。
1.3 方法
1.3.1VmaH和PMA基因生物信息学分析
在NCBI网站上下载指状青霉VmaH(GenBank:AKCT01000068.1)和PMA(GenBank:JH993691.1)氨基酸和蛋白序列。利用BLAST程序与GenBank数据库中的基因序列进行同源性比对。利用Pfam在线预测软件(http://pfam.janelia.org/search)对指状青霉VmaH和PMA结构域进行分析。蛋白质多序列比对采用DNAMAN 8.0程序。系统进化分析利用MEGA程序(版本号5.02)中的邻接法构建系统进化树。
1.3.2 引物设计
参照NCBI上已发布的指状青霉VmaH和PMA基因的mRNA保守区序列设计real-time PCR引物,所涉及引物均由天一辉远有限公司合成(表1)。

表 1 PCR扩增所用引物序列Table 1 Primer sequences used for PCR amplification
1.3.3VmaH和PMA基因表达规律分析
1.3.3.1 菌龄对指状青霉生长过程中VmaH和PMA基因表达的影响
取在PSA培养基上26 ℃培养3 d的指状青霉孢子,制成1×106CFU/mL孢子菌悬液,取200 μL涂布于含玻璃纸的PSA培养基上,于26 ℃培养,分别取培养2、3、4、5、6、7、8 d和14 d的菌丝,液氮速冻后-80 ℃备用。
1.3.3.2 指状青霉侵染脐橙过程中VmaH和PMA的基因表达
新鲜脐橙在0.2%(体积分数)次氯酸钠溶液中浸泡2 min,用蒸馏水冲洗2 次并晾干。使用接种针在果实腰部造伤,深度约3 mm。将长势一致的指状青霉菌丝饼反贴至果实伤口处。将果实放置于26 ℃环境下,分别于第5、6、7、8、9、15天收集病健部组织,液氮速冻后-80 ℃保存备用。
1.3.3.3 酸碱处理对指状青霉菌丝抑制率和VmaH、PMA基因表达的影响
取在PSA培养基上26 ℃培养3 d的指状青霉孢子,制成1×106CFU/mL孢子菌悬液,取200 μL于PSB培养基中,于 26 ℃恒温摇床中120 r/min培养2 d,纱布过滤,无菌水冲洗3 次。称取1.60 g湿菌丝,移至pH值分别为2、4、6、8、10、12的PSB培养基中胁迫24 h。用1 mol/L NaOH和HCl溶液调节PSB培养基pH值至2、4、6、8、10、12,以pH 6 PSB培养基培养的菌丝作空白对照。处理过程结束后,用于RNA提取的样品收集菌丝液氮速冻后-80 ℃保存备用,用于测定菌丝抑制率的样品冷冻干燥48 h后称量干质量,并按下式计算各处理组的菌丝抑制率:

1.3.3.4 葡萄糖饥饿和回补对指状青霉VmaH和PMA基因表达的影响
取在PSA培养基上26 ℃培养3 d的指状青霉孢子,制成1×106CFU/mL孢子菌悬液,取200 μL于PSB培养基中,于26 ℃恒温摇床中120 r/min培养2 d,纱布过滤,无菌水冲洗3 次。取8.00 g湿菌丝于500 mL锥形瓶中,加入300 mL 50 mmol/L KCl溶液,4 ℃饥饿24 h,收集菌丝液氮速冻后-80 ℃保存备用。取饥饿24 h的菌体过滤,无菌水冲洗3 次,取1.00 g湿菌丝重悬于20 mL 10 g/100 mL葡萄糖溶液中,处理10、20、30、40、50 min及60 min。处理过程结束后,收集菌丝液氮速冻后-80 ℃保存备用。
1.3.3.5 不同杀菌物质和氧化还原剂对指状青霉菌丝抑制率和VmaH、PMA基因表达的影响
取在PSA培养基上26 ℃培养3 d的指状青霉孢子,制成1×106CFU/mL孢子菌悬液,取200 μL于PSB培养基中,于26 ℃恒温摇床中120 r/min培养2 d,纱布过滤,无菌水冲洗3 次。称取1.60 g湿菌丝,分别加入50 mL PSB培养基、50 mL含200 μL乙醇的PSB培养基、50 mL含37.5 μL乙醇的PSB培养基、50 mL含20 μL DMSO的PSB培养基和50 mL含不同浓度松属素、联苯苄唑、香芹酚、辛烯醛、H2O2、Na2SO3的PSB培养基中胁迫处理24 h,处理过程结束后,用于RNA提取的样品液氮速冻后-80 ℃保存备用,用于测定菌丝抑制率的样品冷冻干燥48 h后称量干质量,计算各处理组的菌丝抑制率。其中50 mL PSB培养基培养的菌丝作为空白对照(CK1),50 mL含200 μL乙醇、37.5 μL乙醇、20 μL DMSO的PSB培养基培养的菌丝作为溶剂对照组(CK2)。松属素、香芹酚、辛烯醛用乙醇分别配成20%松属素、105μL/L香芹酚、辛烯醛的母液,联苯苄唑用DMSO配成0.032 g/mL母液。
以指状青霉肌动蛋白基因(β-actin)作为内参基因,检测在不同条件下VmaH和PMA在转录水平上的相对表达量。
提取总RNA,反转录后通过real-time PCR检测VmaH和PMA的表达水平。real-time PCR体系为:SYBR Green PCR Master Mix 5 μL,不同样本的cDNA 1 μL,10 μmoL/L上下游引物(β-actin引物:actin-F/R;VmaH引物:Q-VmaH-F/R,PMA引物:Q-PMA-F/R,序列见表1)1 μL,双蒸水补足体积至10 μL。反应程序为:95 ℃预变性30 s;95 ℃变性5 s,60 ℃延伸30 s,40 个循环收集荧光信号。每个样品3 次重复,采用2-∆∆Ct公式进行计算。
1.4 数据统计分析
用Excel 2007软件进行平均值、标准差计算和图形绘制,所有数据均为3 次重复所得,采用SPSS 22软件对实验数据进行单因素方差分析,应用最小显著差数法检验差异显著性(P<0.05,差异显著)。
2 结果与分析
2.1 VmaH和PMA结构域、同源性和系统进化分析

图 1 指状青霉与其他物种VmaH的多序列比对Fig. 1 Multiple sequence alignment of VmaH from P. digitatum and other species
通过Pfam在线预测软件对指状青霉VmaH和PMA的结构域进行分析,发现VmaH具有2 个非常保守的结构域,分别为N端的结构域和C端结构域,N端的结构域位于第7~356个氨基酸之间,C端结构域位于第357~475个氨基酸之间;PMA具有3 个非常保守的结构域,分别为位于N端的结构域、E1-E2 ATPase结构域和水解酶结构域,N端的结构域位于第84~141个氨基酸之间,E1-E2 ATPase结构域位于第182~406个氨基酸之间,水解酶结构域位于第422~689个氨基酸之间。有研究表明,酵母中VmaH的N末端域是激活ATP水解所必需的,而C末端域是适当的能量耦合所必需的[20]。PMA中N末端在膜内侧构成H+入口,水解酶结构域控制ATP的水解,E1-E2 ATPase结构域通过构象循环变化实现离子运输,E1对输出的离子有很高亲和力,E2对输入的离子有很高亲和力[21]。

图 2 指状青霉与其他物种PMA的多序列比对Fig. 2 Multiple sequence alignment of PMA from P. digitatum and other species
将氨基酸序列进行BLASTp比对分析,用DNAMAN 8.0软件对指状青霉VmaH和PMA与其他物种的VmaH和PMA进行同源性比对,结果如图1、2所示,对比结果发现,指状青霉VmaH与扩展青霉、曲霉、大观贝氏菌、酵母菌的VmaH同源性较高,其相似度达到79%以上,指状青霉PMA(JH993691.1)与扩展青霉、曲霉、黄萎病菌等真菌PMA1的相似度达到80%以上,表明VmaH和PMA在真菌物种中较为保守。
用MEGA 5.0软件采用邻位相接法(Neighbor Joining)构建指状青霉VmaH和PMA的系统发育树(图3、4)。结果表明,指状青霉VmaH与青霉属、大观贝氏菌序列具有最高的同源性,与曲霉属的VmaH蛋白高度同源;指状青霉PMA与日本曲霉、稻瘟病菌(Magnaporthe oryzae)序列具有最高的同源性,与青霉属、木霉属、小麦酵母等的PMA蛋白高度同源。表明VmaH和PMA基因的氨基酸序列在真菌中具有较高的保守性,亲缘关系较近。

图 3 指状青霉与其他物种VmaH的系统进化树Fig. 3 Phylogenetic tree of VmaH from P. digitatum and other species

图 4 指状青霉与其他物种PMA的系统进化树Fig. 4 Phylogenetic tree of PMA from P. digitatum and other species
2.2 指状青霉生长和侵染过程中VmaH和PMA基因表达
如图5所示,与PMA相比,VmaH相对表达量在指状青霉菌丝生长和侵染脐橙果实的整个过程中变化较为平缓,仅在生长和侵染后期表达量有一定程度的升高。而PMA在菌丝生长和侵染脐橙前期稳定表达,中期开始表达量显著下调。推测在指状青霉生长和侵染脐橙前期,VmaH和PMA共同维持指状青霉生长所需的胞内外pH值,而在中后期主要是由VmaH维持指状青霉生长所需的酸性平衡。

图 5 VmaH和PMA在指状青霉生长(A)和侵染(B)过程中定量表达分析Fig. 5 Quantitative expression analysis of VmaH and PMA during the growth (A) and infection (B) of P. digitatum
2.3 不同酸碱处理对指状青霉菌丝生长和VmaH、PMA表达的影响

图 6 VmaH和PMA在不同pH值下定量表达和抑菌率分析Fig. 6 Quantitative expression and antibacterial rate analysis of VmaH and PMA under different pH conditions
如图6所示,弱酸和弱碱条件下PMA在调节胞内外pH值上发挥着主要作用;而在强酸强碱条件下VmaH和PMA的功能均受到抑制,尤其在极碱条件下VmaH和PMA调控胞内外pH值的能力减弱,菌丝无法正常生长。
2.4 葡萄糖饥饿以及回补条件对指状青霉VmaH和PMA表达的影响
如图7所示,葡萄糖饥饿会使VmaH和PMA基因的表达量显著下调,葡萄糖回补可以恢复VmaH和PMA基因的表达,且VmaH在回补状态下基因表达量显著高于PMA基因的表达量。
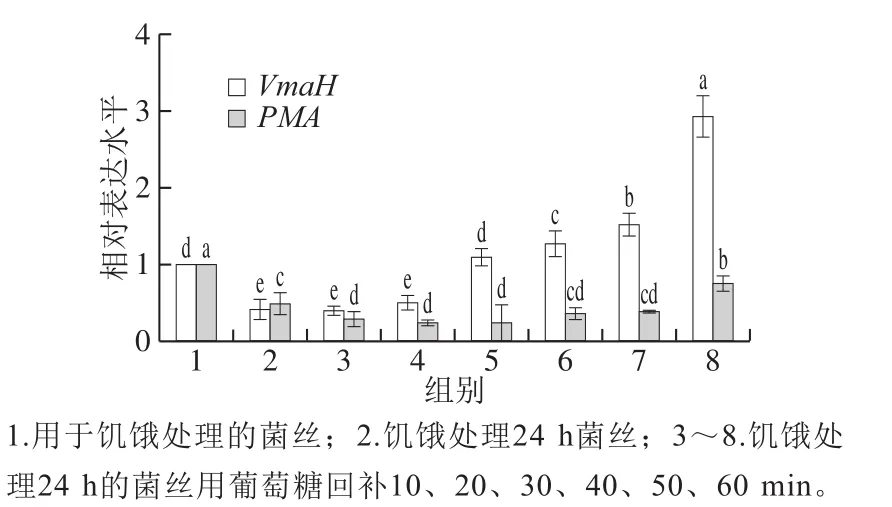
图 7 VmaH和PMA在葡萄糖饥饿和回补中定量表达分析Fig. 7 Quantitative expression analysis of VSH and PMA under glucose starvation and supplementation
2.5 氧化还原剂对指状青霉菌丝抑制率和VmaH、PMA表达的影响
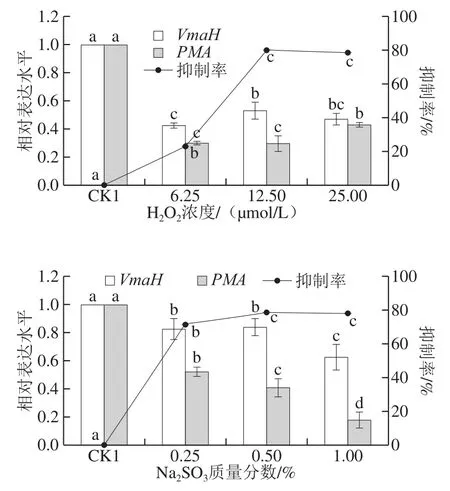
图 8 VmaH和PMA在H2O2和Na2SO3胁迫下定量表达和抑菌率分析Fig. 8 Quantitative expression and antibacterial rate analysis of VmaH and PMA under the stress of H2O2 and Na2SO3
如图8所示,H2O2和Na2SO3处理显著降低了指状青霉VmaH和PMA的表达量,且与VmaH相比,PMA对H2O2和Na2SO3处理更敏感。可以看出,随着VmaH和PMA的表达的显著下调,菌丝体的生长受到明显抑制。
2.6 杀菌剂处理对指状青霉菌丝抑制率和VmaH、PMA基因表达的影响
如图9所示,经黄酮类化合物松属素处理后,指状青霉菌丝生长均被显著抑制,PMA表达量在各个用量下均显著下调,而VmaH在高浓度时才会显著下调。经细胞膜抑制剂联苯苄唑处理后,指状青霉菌丝生长量和PMA表达量均被显著抑制,且抑制程度随其质量浓度增加而增强,而对VmaH的表达量影响不显著。经植物香精油香芹酚和辛烯醛处理后,VmaH和PMA相对表达量均显著下调,且下调程度随其用量增加而增强。VmaH经低用量辛烯醛处理后相对表达量下调了48%,而经低用量香芹酚处理后相对表达量仅下调了13%,表明相较于香芹酚,VmaH对辛烯醛响应更敏感。在高用量辛烯醛和香芹酚处理下,VmaH相对表达量分别下调了53%、49%,PMA相对表达量均下调了98%,表明相比于VmaH,PMA对香芹酚和辛烯醛处理更为敏感。
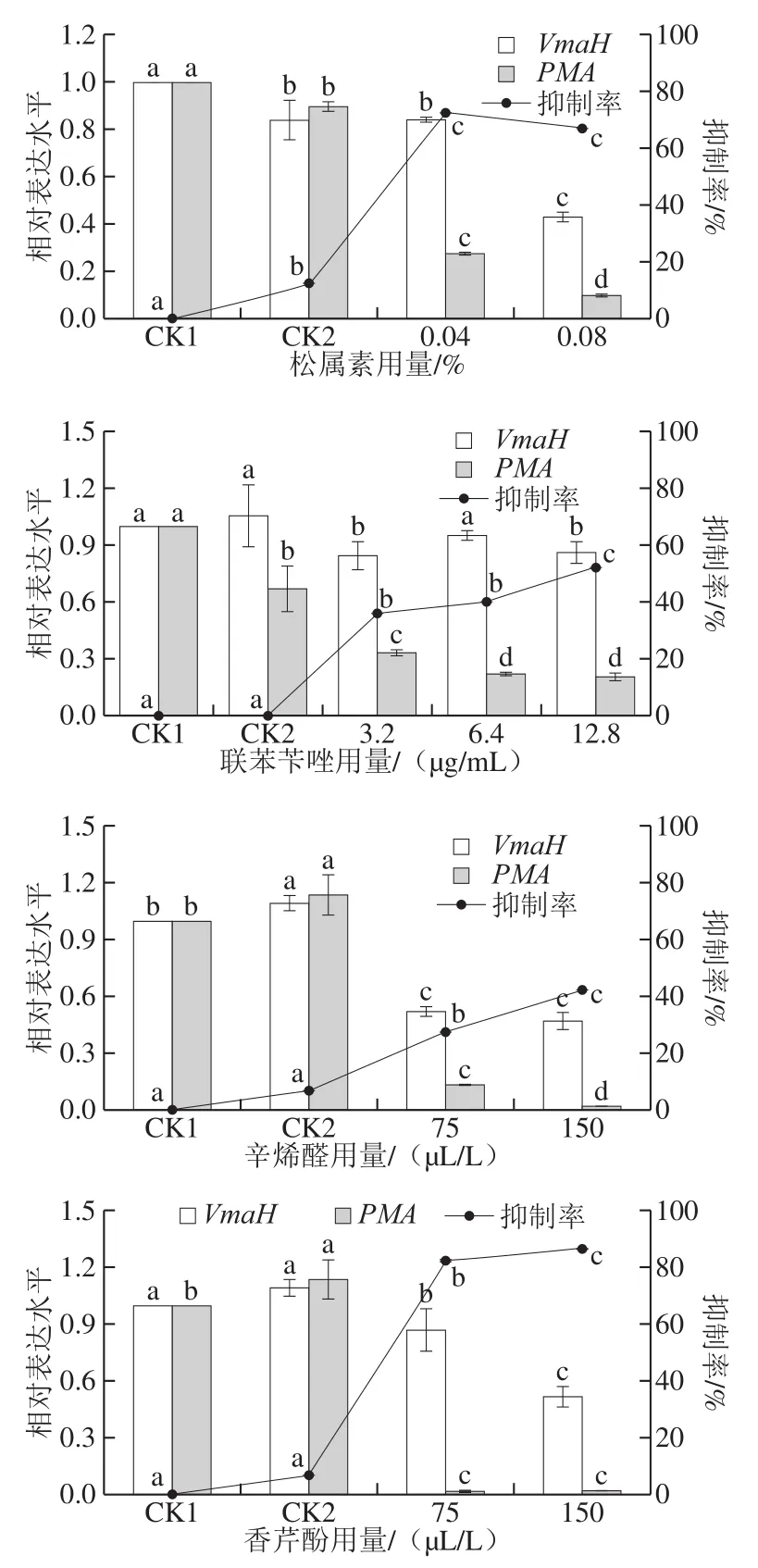
图 9 VmaH和PMA在不同类型杀菌剂胁迫下定量表达和抑菌率分析Fig. 9 Quantitative expression and antibacterial rate analysis of VSH and PMA under the stress of different types of fungicides
3 讨论与结论
本研究通过结构域分析发现指状青霉中的VmaH具有2 个非常保守的结构域,分别为N端结构域和C端结构域,与酵母VmaH[20]有相同的结构域;PMA具有3 个非常保守的结构域,分别为位于N端的结构域、E1-E2 ATPase结构域和水解酶结构域,与大多数真菌[21]PMA结构域相同。表明指状青霉中的VmaH和PMA与其他真菌中的VmaH和PMA发挥着同样的功能。同源性和系统进化分析发现指状青霉中的VmaH和PMA基因所编码的蛋白和青霉属、曲霉属、酵母等其他种属具有相同结构域和高度同源性,而与其他植物细胞和哺乳类动物细胞同源性较低,尤其是PMA编码的蛋白是真菌特有蛋白,与哺乳动物无同源性,表明VmaH和PMA适合作为药物作用靶点。因此,从生物信息学方面,VmaH和PMA所编码的蛋白可以作为真菌特异性药物作用靶点进一步对其功能特性进行深入研究。
研究发现,VmaH功能缺失后会导致球孢白僵菌侵染毒力下降[6]、酿酒酵母生长状态受到影响[14]、东方粘虫中毒或死亡[12]、东亚飞蝗个体出现死亡和显著的蜕皮缺陷表型[15]。进一步研究发现[6],VmaH主要通过影响液泡pH值,从而调节细胞内外pH值环境,以致改变其侵染能力。此外,Petrov[22]的研究同样发现PMA缺失和PMA定点突变的酿酒酵母突变体泵H+和ATP水解功能均受到抑制,从而导致酿酒酵母生长状态受到影响。本研究也发现VmaH和PMA在指状青霉菌丝生长和侵染橙子前期均维持较高表达水平;而在中后期仅VmaH维持较高表达水平,PMA显著下调。表明VmaH和PMA在指状青霉生长和侵染寄主的前期发挥着重要作用,尤其VmaH在指状青霉生长和侵染后期发挥着重要作用。酸碱平衡与真菌的生长和侵染能力密切相关,VmaH和PMA在调控真菌细胞内外pH值平衡上具有重要作用。因此,从指状青霉生长和侵染方面,VmaH和PMA可作为指状青霉药物作用靶点进一步研究。
在外界环境胁迫下,不同基因编码的蛋白在维持细胞内环境稳定的过程中发挥着不同作用。本实验通过研究在酸碱、葡萄糖以及各种杀菌物质的环境胁迫下VmaH和PMA在指状青霉中的表达情况,分析VmaH和PMA作为指状青霉酸代谢、碳代谢、氧化还原等方面药物靶点的可能性。胞外pH值和葡萄糖会影响V-ATPase和P-ATPase的活性[23],进而影响真菌酸碱平衡。研究表明,酵母菌P-ATPase的表达对酸胁迫敏感,在pH值为2.5时,PMA1的mRNA水平和酶活性显著下降[24],而弱酸条件可增加真菌P-ATPase的活性[25]。本实验也发现在弱酸弱碱环境中,指状青霉生长所需的胞内外pH值主要是由PMA发挥作用,而在极酸极碱条件下VmaH和PMA的活性均受到损伤,从而导致指状青霉无法正常生长,表明其在指状青霉的酸碱平衡中发挥着重要的调控作用。Kane[26]研究发现,葡萄糖信号传导途径可能介导V-ATPase的拆卸和重新组装,进而影响V-ATPase的活性。在含葡萄糖的培养基中,V-ATPase有55%~70%的V0区段与V1组装在一起,但在葡萄糖饥饿后,只有15%~20%的V0区段与V1结合,经葡萄糖回补后,组装水平再次为55%~70%。另有研究表明,在葡萄糖饥饿条件下可能导致PMA1和其他ATP驱动的过程直接失活[27],而向酵母细胞中添加葡萄糖可激活P-ATPase介导的质子外排[28]。本研究同样发现,葡萄糖饥饿显著降低了VmaH和PMA基因表达水平,葡萄糖回补可以恢复两个基因的表达水平,尤其是VmaH相对表达量显著上调,表明VmaH和PMA在指状青霉糖代谢过程中发挥着重要的调控作用。因此,VmaH和PMA可作为酸代谢、碳代谢方面可能性药物靶点进一步研究。
本实验发现在氧化还原剂以及各种杀菌物质胁迫条件下,PMA在各种药物胁迫下均受到抑制,而VmaH仅在部分药物胁迫下才会受到抑制,表明VmaH和PMA是响应不同种类药物的重要作用靶点,可以影响氧化还原等方面,对生命活动至关重要,是重要的药物作用靶点,值得深入探讨。丁俐文等[29]研究也发现V-ATPase可作为粘虫的药物作用靶点,通过苦皮藤素V产生杀虫效果。过表达Put VHA-c的转基因酵母具有更高的耐盐性,表明V-ATPase在逆境胁迫中发挥重要作用[30]。在铜胁迫下酿酒酵母的质膜组织受到破坏从而使P-ATPase的活性降低[31]。Billack等[11]的研究同样发现PMA可作为白色念珠菌的药物作用靶点,通过抑制剂如依布硒对真菌生长产生强烈抑制作用。因此,从VmaH和PMA对不同药物的响应方面,VmaH和PMA有作为指状青霉药物作用靶点的可能性。
综上所述,VmaH和PMA所编码的蛋白真菌特异性强,参与了指状青霉生长和侵染寄主的过程,在指状青霉的酸代谢、糖代谢过程中发挥着重要作用,对于不同的胁迫环境响应差异显著,其中PMA对外界环境胁迫反应更为明显,VmaH在胁迫条件下对细胞pH值平衡发挥的作用更显著。因此,VmaH和PMA作为潜在的抗指状青霉药物靶点,值得进行深入研究和探讨。同时,本实验为接下来通过基因过表达、沉默、敲除等手段进一步研究VmaH和PMA作为指状青霉药物靶点的可能性提供了理论支持。
