肺表面活性物质联合布地奈德治疗重症呼吸窘迫综合征早产儿的临床效果
2021-03-27姜小华申薇祺
陈 静 姜小华 申薇祺
1.重庆市合川区人民医院新生儿科,重庆 401520;2.重庆医科大学附属涪陵中心医院新生儿科,重庆 408000
呼吸窘迫综合征(RDS)是指肺内、外严重疾病导致的以进行性呼吸困难、发绀、呻吟等为主要临床症状,以弥漫性损伤、肺毛细血管通透性增强为基础,以肺水肿、透明膜形成、肺不张等为主要病理变化的一类呼吸衰竭综合征[1-2]。RDS 好发于早产儿,其发病机制极其复杂,主要是因为缺乏肺泡表面活性物质(PS)导致的肺功能障碍[3]。临床治疗多通过补充PS 以提高机体肺功能,阻止疾病进展。但近年来临床实践证实[4],单纯的PS 治疗难以改善宫内感染导致的炎症,难以达到理想预期的治疗效果。以布地奈德为代表的糖皮质激素可有效抑制炎症反应,既往常采用雾化吸入的方式用于治疗支气管哮喘、刺激性咳嗽、急性喉炎等疾病[5]。现临床有关PS 联合布地奈德治疗重症RDS 早产儿的相关报道尚不多见,就此展开分析。
1 资料与方法
1.1 一般资料
纳入标准:①诊断标准参考《实用新生儿学》[6];②新生儿血流动力学稳定,胸片证实为病情Ⅲ~Ⅳ级;③监护人签署知情同意书;④胎龄为28~36 周。排除标准:①严重遗传代谢性疾病、先天畸形、神经系统异常;②多胎妊娠;③伴有严重感染性疾病;④中途因其他原因退出治疗;⑤出生时已经出现严重呼吸困难的症状;⑥产妇产前接受过糖皮质激素治疗。
本研究经重庆市合川区人民医院医学伦理委员会批准。选取2016 年7 月—2019 年12 月重庆市合川区人民医院收治的168 例重症RDS 早产儿为研究对象,根据随机数字表法将其分为对照组、研究组,每组84 例。两组一般资料比较,差异无统计学意义(P >0.05),具有可比性。见表1。
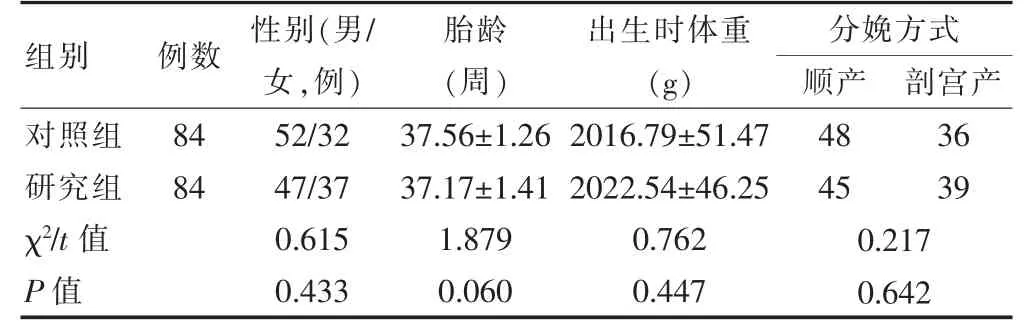
表1 两组一般资料比较
1.2 方法
两组给予吸氧、纠正低血糖、机械通气、保温、纠正酸碱平衡、吸痰和营养支持等治疗。在此基础上,对照组给予PS(Chiesi Farmaceutici S.p.A.,生产批号:H20151202,规格3 mL:0.24 g)治疗,100 mg/kg 气管内给药,每8~12 小时给药1 次,每次给药时间控制在10 min 内,最多给药4 次。研究组则在对照组的基础上联合布地奈德(鲁南贝特制药有限公司,生产批号:20160317,规格:每瓶含布地奈德20 mg,每瓶200 揿,每揿含布地奈德0.1 mg)治疗,0.25 mg/kg 雾化吸入治疗,每8~12 小时给药1 次。两组均治疗72 h。
1.3 观察指标
①比较两组治疗72 h 后(治疗后)临床疗效及并发症发生情况。②于治疗前后抽取患儿2 mL 桡动脉血,参考武汉华美生物科技有限公司试剂盒说明书(生产批号:20160217、20160124)进行,采用酶联免疫吸附试验检测炎症因子指标:白细胞介素-6(IL-6)、肿瘤坏死因子-α(TNF-α)。采用丹麦雷度公司生产的血气分析仪检测氧合指数(OI)、动脉二氧化碳分压(Pa-CO2)、动脉血氧分压(PaO2)。
1.4 疗效判定标准
疗效判定标准参考《实用新生儿学》[6],治疗后发绀、进行性呼吸困难、呻吟等临床症状未见改善甚至加重为无效;治疗后状态较治疗前安静,上述临床症状有所改善,呼吸仍稍有急促为有效;治疗后患儿安静,上述临床症状消失,面色红润为显效。总有效率=(显效+有效)例数/总例数×100%。
1.5 统计学方法
采用SPSS 25.0 统计学软件进行数据分析,计量资料用均数±标准差()表示,两组间比较采用t 检验;计数资料用例数或百分率表示,组间比较采用χ2检验。以P<0.05 为差异有统计学意义。
2 结果
2.1 两组血气分析指标比较
治疗前,两组血气分析指标比较,差异无统计学意义(P<0.05)。治疗后两组PaO2、OI 高于治疗前,且研究组高于对照组(均P<0.05);两组PaCO2低于治疗前,且研究组低于对照组(均P<0.05)。见表2。
2.2 两组临床疗效比较
治疗后研究组总有效率高于对照组(P<0.05)。见表3。
2.3 两组炎症因子水平比较
治疗前两组炎症因子水平比较,差异无统计学意义(P<0.05)。治疗后两组血清IL-6、TNF-α 水平低于治疗前,且研究组低于对照组(均P<0.05)。见表4。
表2 两组血气分析指标比较()
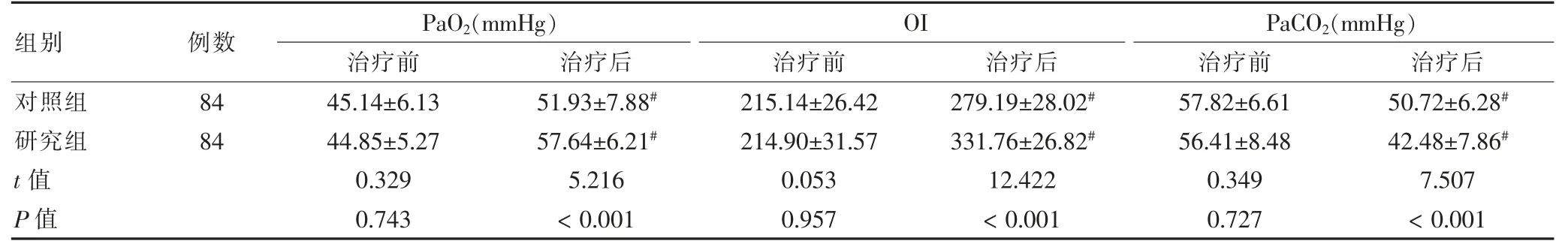
表2 两组血气分析指标比较()
注:与本组治疗前比较,#P <0.05。PaO2:动脉血氧分压;OI:氧合指数;PaCO2:动脉二氧化碳分压。1 mmHg=0.133 kPa
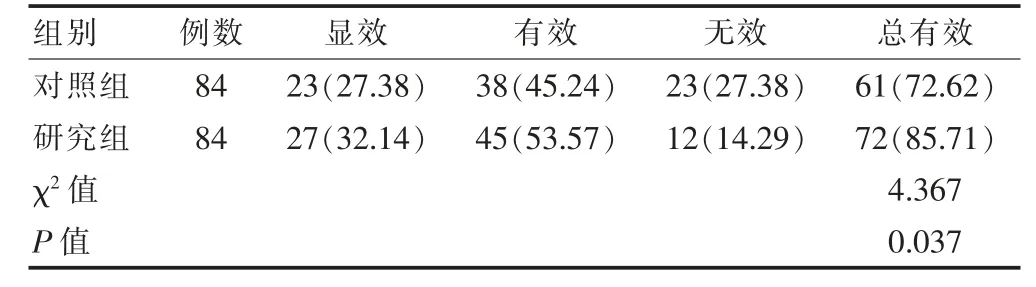
表3 两组临床疗效比较[例(%)]
表4 两组炎症因子水平比较(pg/mL,)
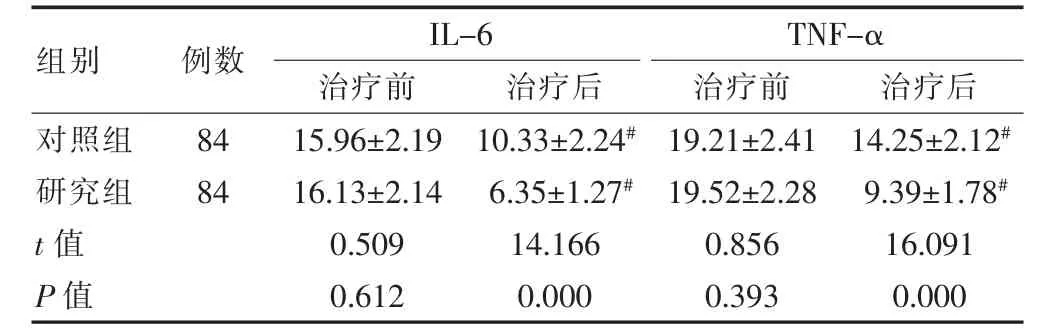
表4 两组炎症因子水平比较(pg/mL,)
注:与本组治疗前比较,#P <0.05。IL-6:白细胞介素-6;TNF-α:肿瘤坏死因子-α
2.4 两组并发症发生情况
两组并发症总发生率比较,差异无统计学意义(P>0.05)。见表5。

表5 两组并发症发生情况比较[例(%)]
3 讨论
重症RDS 好发于早产儿,且胎龄越小发病率越高,病情越危重。该病主要是由肺泡Ⅱ型上皮细胞分泌PS 过少,进而导致呼吸末肺泡发育不全,发生呼吸窘迫、低氧,甚至引起死亡[6-8]。早产儿由于肺泡细胞发育不成熟,PS 无法顺利合成,进而发病;此外,随着“二孩”政策的开放,高龄产妇不断增加,不少产妇选择剖宫产进行分娩,致使胎儿在娩出过程中肺部未能得到有效挤压,肺泡内液体残留增加,亦成为PS 无法合成的主要原因,故临床重症RDS 患儿亦并不少见[9-11]。现临床针对重症RDS 的治疗尚无统一方案,多以机械通气和药物进行治疗,药物治疗主要以补充外源性PS 为主,PS 具有增加肺泡顺应性、减少肺泡表面张力、防治肺泡发生萎陷等作用[12-13]。但单用PS 在纠正早产儿缺氧状态时无法做到迅速起效,疗效不太理想[14]。同时机械通气也可增加支气管肺发育不良的发生风险,对患儿的影响较大,影响患儿预后。布地奈德具有作用迅速、使用剂量小、作用部位准确的优势,可明显减轻肺部水肿,抑制机体炎症,近年来已逐渐应用于RDS 的治疗中[15-16]。
本研究结果显示,治疗后研究组总有效率高于对照组(P<0.05),提示PS 联合布地奈德治疗重症RDS 患儿,可进一步提高治疗效果。分析其原因,PS 的主要成分为特异性蛋白、磷脂酰胆碱,除了可扩张肺泡外,还可刺激内源性PS 分泌,从内外促进肺的发育[17]。布地奈德对全身代谢影响非常小,半衰期短,适用于早产儿治疗,它可通过促进PS 和肺抗氧化酶的生成,显著改善肺功能。与PS 联合应用,发挥协同作用,共同促进治疗效果的提升[18-19]。既往研究结果显示[20-21],炎症反应是导致重症RDS 患儿发病的中心环节,表现为细胞因子大量释放,触发炎症介质的瀑布样级联反应,促进RDS 患儿的疾病进展。IL-6、TNF-α 均是临床常见的炎症介质,可反映机体炎症严重程度,IL-6经缺氧、内毒素刺激后,可由肺泡巨噬细胞、气道上皮细胞等合成,损伤组织,使组织纤维化[19,22-24]。本研究结果显示,治疗后研究组IL-6、TNF-α 水平低于对照组(均P<0.05),这可能与布地奈德的以下作用机制有关[25-27]:布地奈德能通过增加平滑肌细胞、内皮细胞和溶酶体膜的稳定性减少组织胺、IL-6 等炎症因子的释放。布地奈德与PS 联合治疗可以加速激素扩散溶解,提高其抗炎作用,减轻肺损伤。本研究结果显示,治疗后研究组PaO2、OI 高于对照组,PaCO2低于对照组(均P<0.05)。血气分析常用于反映机体的呼吸功能以及代谢功能。布地奈德与PS 联合治疗后,可减轻肺毛细血管渗透压,降低其通透性,提高肺的顺应性,萎陷肺泡逐渐充气,通气和换气功能得以改善,引起OI、PaO2升高,PaCO2下降,缓解机体缺氧状态,避免酸中毒现象的发生,纠正机体呼吸性酸中毒[28]。另外,两组并发症总发生率比较,差异无统计学意义(P >0.05)。可见PS 联合布地奈德治疗安全性较好。
综上所述,PS 联合布地奈德治疗重症RDS 早产儿,可有效降低炎症因子水平,改善患儿血气分析,安全有效。
