乳腺X射线摄影非立体定位在乳腺微钙化灶活检中的临床应用*
2021-03-26洪强莫春生李娟娟梁丽春孔之华潘成熙陈徐生
洪强,莫春生,李娟娟,梁丽春,孔之华,潘成熙,陈徐生
(广东省中西医结合医院 胸外乳腺科,广东 佛山528200)
乳腺的多形性和微钙化具有很高的恶性概率,簇状微钙化灶可能是乳腺癌的早期征兆[1-2]。在乳腺影像报告数据系统中(BI-RADS 分级)被归类为BI-RADS 4 级的患者一般都需要组织学活检[3]。然而,即使是BI-RADS 3 级的钙化灶,也应进行短时间间隔随访或组织学确认[4-5]。超声难以识别微钙化灶,因为病变的区域包含腺体组织的回声[6]。而乳腺X 射线摄影是一种用于检测微钙化灶的非常敏感的检查方法。采用乳腺X 射线摄影或立体定向设备引导的细针定位以切除微钙化灶是必要且可行的。然而,立体定位设备比较昂贵,并且要培养具有特定经验和技能的放射科医师。真空辅助乳房活检系统(vacuum-assisted breast biopsy, VABB)于1996年首次用于良性乳腺结节活检[7-8],随后被开发用于良性乳腺病变的治疗。VABB 不仅使操作者获得足够数量的标本,而且可以完全去除小而临床难于触及的良性病变,其适应证包括可触及或不可触及的乳腺病变(nonpalpable breast lesion,NPBL)[9]。
临床实践表明,乳腺微钙化灶的定位比较困难,国内外大量采用的先进方法又因种种原因至今难以在我国基层医院推广。为此,笔者设计了一种基于传统乳房X 射线检查的手动立体定位(非立体定位)方法,即采用乳腺X 射线摄影手动定位乳腺微钙化灶,其所需设备已经在基层医院普遍使用。现报道如下。
1 资料与方法
1.1 研究对象
选取2015年1月—2019年1月广东省中西医结合医院常规乳腺X 射线摄影中发现有病灶的患者84 例,采用随机数字表法分为实验组和对照组,每组42 例。纳入标准:患者乳腺X 射线摄影检查有簇状、弥漫性或散在微钙化,并且均为BI-RADS 3 或4a 级。排除标准:同侧乳腺癌或既往曾行乳腺手术。该研究获得医院伦理委员会批准,所有患者均签署知情同意书。
1.2 方法
肿瘤定位由2 位放射科医师和1 位乳腺外科医师完成,外科手术由2 位乳腺外科医生完成。实验组患者手动定位,在乳腺X 射线摄影的颅尾(craniocaudal, CC)和中外侧斜(mediolateral oblique,MLO)视图上检测到微钙化灶。在乳腺X 射线片的CC 视图上,使用电子直尺测量CC 位病灶到乳头所在矢状面的垂直距离d1,并检查微钙化是位于外部还是内部。以同样的方式,在乳腺X 射线片的MLO 视图上测量MLO 位病灶到乳头所在矢状面的垂直距离d2。在行乳腺X 射线摄影检查时嘱患者将双手举起至同一位置。医生绘制一条从颅侧到尾侧的与Y 轴距离d1 且与其平行的直线a1,以及一条60°从内侧到侧面与a 或者b 距离d2 且与其平行的直线b1。两条直线在微钙化灶所在的位置相交(见图1,两条红线所示)。如有必要,可以采用乳腺X 射线摄影的真实侧视图。在确定好病灶的体表投影后,通过测量乳腺X 射线片中病灶到皮肤表面的距离,钩针在乳房体表定位处垂直插入。再次拍正、负24°角X 射线片,观察钩针位置。
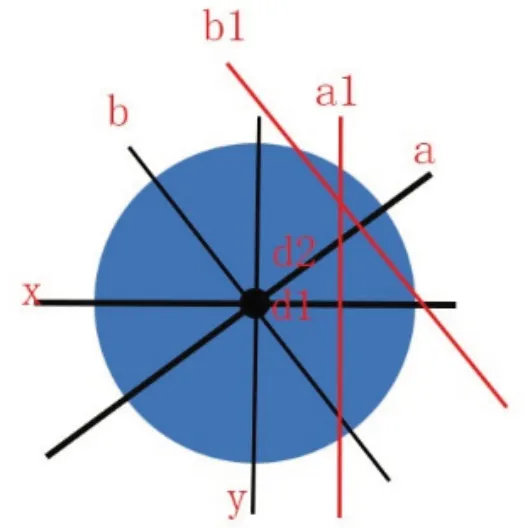
图1 实验组画线方法
对照组患者同样行CC 和MLO 影像,按病灶位置进行测量,测量方法为传统方法,CC 位以过乳头垂直胸壁为轴线(X 轴),测量病灶到轴线的垂直距离d1,在定位图上画出过此距离点与此坐标轴的垂线a1,MLO 位以过乳头垂直胸壁为Y 轴,测量病灶到轴线的垂直距离d2,在定位图上画出过此距离点与此坐标轴的垂线b1。两垂线的交点为病灶的位置,在确定好病灶的体表投影后,通过测量乳腺X 射线片中病灶到皮肤表面的距离,钩针在乳房体表定位处垂直插入。再次拍正、负24°角X 射线片,观察钩针位置。见图2。
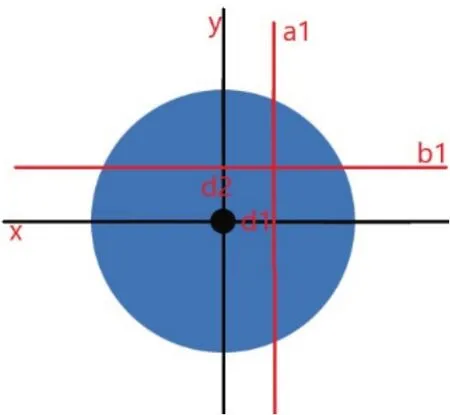
图2 对照组画线方法
两组患者均采用常规手术方法切除钩针定位处标本,对标本进行乳腺X 射线摄影以验证微钙化灶。如果标本乳腺X 射线片显示有足够量的微钙化,则完成该过程,否则考虑进一步扩大切除。采集所有标本乳腺X 射线片,测量钩针与最近钙化点的距离进行统计学分析。
1.3 统计学方法
数据分析采用SPSS20.0 统计软件,计量资料以均数±标准差(±s)表示,比较采用t检验,计数资料以率(%)表示,比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组患者年龄、X 射线摄影次数、钩针与最近钙化灶的距离比较
两组患者的年龄比较,经t检验,差异无统计学意义(P>0.05);两组患者行乳腺X 射线摄影次数、钩针与最近钙化灶的距离比较,经t检验,差异有统计学意义(P<0.05);实验组定位中无出血、定位导丝折断等并发症发生。见表1。
表1 两组患者年龄、X射线摄影次数、钩针与最近钙化灶的距离比较 (±s)
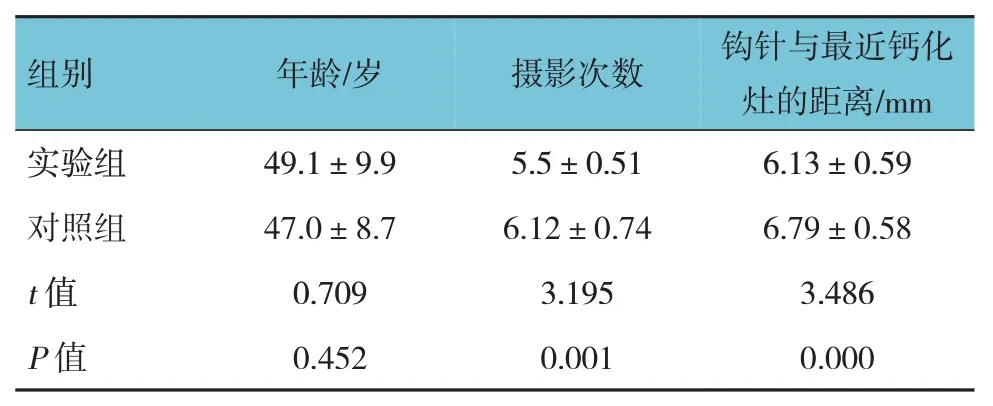
表1 两组患者年龄、X射线摄影次数、钩针与最近钙化灶的距离比较 (±s)
组别年龄/岁摄影次数钩针与最近钙化灶的距离/mm实验组对照组t 值P 值49.1±9.9 47.0±8.7 0.709 0.452 5.5±0.51 6.12±0.74 3.195 0.001 6.13±0.59 6.79±0.58 3.486 0.000
2.2 两组患者活检手术后病理结果比较
实验组活检患者中恶性9 例(均为导管内癌),纤维囊性改变17 例(40.5%),纤维腺瘤8 例(19.0%),硬化性腺病2 例(4.8%),常见乳腺增生4 例(9.5%),非典型导管增生2 例(4.8%),恶性检出率为7.1%。对照组活检患者中恶性8 例(均为导管内癌),纤维囊性改变15 例(35.7%),纤维腺瘤9例(21.4%),硬化性腺病3 例(7.1%),常见乳腺增生6 例(14.3%),非典型导管增生1 例(2.4%),恶性检出率为4.8%。两组恶性检出率比较,差异无统计学意义(χ2=0.322,P=0.644)。
2.3 两种活检手术的敏感性和特异性比较
实验组1 例恶性标本在切除后看不到显著的微钙化,进一步扩大切除最后病理确诊为恶性,敏感 性 为88.9%[95% CI:(0.565,0.980)],特异性为100.0%[95% CI:(0.896,1.000)],见表2和图3。对照组5 例标本在切除后看不到显著的微钙化,进一步扩大切除最后病理确诊1 例恶性,敏感性为87.5%[95% CI:(0.529,0.978)],特异性为88.2%[95% CI:(0.734,0.953)],见表2和图4。两组敏感性比较差异有统计学意义(χ2=8.571,P=0.014),两组特异性比较差异无统计学意义(χ2=2.299,P=0.129)。

表2 两组敏感性和特异性比较

图3 实验组ROC曲线
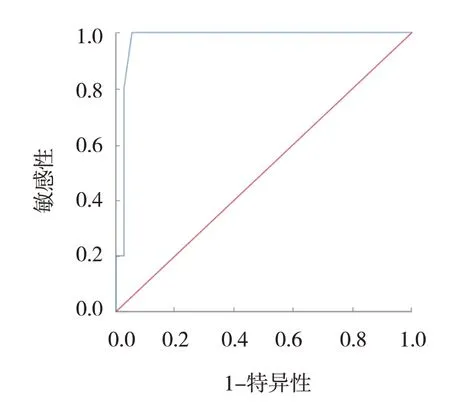
图4 对照组ROC曲线
3 讨论
乳腺癌是最常见的癌症,也是我国女性死亡的第2 大原因。在乳腺癌筛查中,每1 000 例女性就有5 例检测为浸润性癌,其中2.7 例患者的乳腺癌直径<15 mm[2]。有研究表明[10],超过1/3 的已切除乳腺病变具有临床隐匿性,且大约2%~4%的女性存在NPBL,其中2%~3%为乳腺癌。NPBL 的X射线征象包括:①孤立小结节状肿块;②放射状毛刺火星芒状影;③成簇细小钙化影不伴肿块;④局限性致密影;⑤局部结构紊乱。细小钙化影因为不伴肿块,在超声检查时难以发现,而X 射线摄影立体定位活检已用于验证这些可疑的微钙化[1]。立体定向活检定位准确,比大范围切除活检创伤小,术后瘢痕更小,恢复时间短[11-15]。然而,立体定位装置很昂贵并且只能由熟练的放射科医师使用。如果乳腺X 射线摄影检测到NPBL,医生可以估计乳腺病变的位置,这被称为非立体定位或手动立体定位。临床可以通过乳腺X 射线摄影的CC 和MLO 视图来测量病变的大致位置。在乳腺X射线摄影的CC 视图中,基于来自乳头的垂直线确定位置是外部还是内部;在MLO 视图中,基于乳头的垂直线确定为上部外部或下部内部。微钙化灶位于两条直线相交处。侧向乳腺X 射线摄影片有时也有助于准确定位微钙化灶[16]。对于NPBL,钩针定位是最常用的方法[17-18],该方法使用钩形或J形线来定位NPBL,用于活检或乳腺肿瘤切除术。尽管钩针定位通常在超声引导下进行,但超声难以识别微钙化灶,而乳腺X 射线摄影可以很好地识别微钙化灶,可以在乳腺X 射线摄影引导下对NPBL 进行立体定位。乳腺X 射线摄影引导立体定位有几个缺点:①辐射暴露的剂量高于超声引导;②NPBL 的钩针定位和切除通常分别由不同的医生(例如放射科医师和外科医生)执行,放射科医师和外科医生应在手术前充分讨论分析,以获得良好的结果;③立体定位设备比较昂贵。
本研究采用乳腺X 射线摄影非立体定位的方法指导手术切除乳腺微钙化灶组织,结果表明该方法在准确的定位下可取得比传统定位更好的定位效果。实验组在保证病灶完整切除的同时,减少了患者的摄影次数,定位中无出血、定位导丝折断等并发症发生。乳腺科医生应该充分熟悉乳房X射线检查结果和具备钩针定位的技能,且应该与影像科医生在定位现场进行充分的沟通,才能达到减少创伤和精准切除的目的。
当立体定位方法无法使用或失败时,本方法在某些情况下会有所帮助。综上所述,乳腺X 射线摄影手动定位乳腺微钙化灶简单、易行,精确度高,具有令人满意的定位效果。这将是这类乳腺病变的有效诊断技术。
