基于计算机辅助药物设计探究扶正避瘟方预防新型冠状病毒感染的物质基础及分子机制
2021-03-21靳晓杰王菲毛建军王燕如关瑞宁刘东玲魏本君李亚玲张利英张志明刘永琦
靳晓杰 ,王菲,毛建军,王燕如,关瑞宁,刘东玲,魏本君,李亚玲,张利英,张志明,刘永琦,4
1.甘肃中医药大学药学院,甘肃 兰州 730000;2.甘肃中医药大学甘肃省高校重大疾病分子医学与中医药防治研究重点实验室,甘肃 兰州 730000;3.甘肃中医药大学附属医院,甘肃 兰州 730000;4.甘肃中医药大学敦煌医学与转化教育部重点实验室,甘肃 兰州 730000
新型冠状病毒(SARS-CoV-2)引起的传染性疾病对人类健康构成严重威胁[1-4]。中医药在该病毒引起的疾病预防、治疗和康复的全过程中发挥了举足轻重的作用[5-8]。甘肃省注重发挥中医优势,坚持“一患一方”“湿邪贯穿全程”“慎用苦寒”“早用中医,截断病势”“立足肺脾、祛湿为先”等理念,积极采用中医全程参与防治。甘肃省专家组总结经验,形成了“甘肃方剂”系列方,涵盖预防、治疗、康复各阶段。其中,具有益气固表、扶正辟瘟功效的扶正避瘟方推荐用于普通人群、医务人员、监测点工作人员和密切接触者的预防用药[9-11]。《全国各省区中医药治疗新型冠状病毒肺炎(COVID-19)的诊疗方案分析》显示,方中苍术、防风、黄芪、连翘用药频次高[12]。
计算机辅助药物设计(computer aided drug design,CADD)中的同源模建、分子对接、结合模式分析等技术可以从相关靶点结构或基因序列出发,在得到相应靶点和结合位点特征的基础上,对中药化合物与靶点之间的相互作用方式及亲和力进行基于力场或知识的预测,从而虚拟筛选得到潜在活性成分。研究表明,SARS-CoV-2 利用高度糖基化的同源三聚体S 蛋白与人血管紧张素转换酶2(ACE2)结合进入宿主细胞[13-14]。该蛋白是介导病毒进入宿主细胞的关键靶点,在与ACE2 发生结合前处于不可达状态的预融状态[15]。预防方的作用期是病毒进入人体之前,ACE2 和SARS-CoV-2 S 蛋白均处于各自的稳定构象,故本研究选择SARS-CoV-2 S 蛋白预融状态的受体结合区域(receptor binding region,RBD)及其受体ACE2 的结构作为目标靶点,采用同源模建、分子对接方法探寻扶正避瘟方对病毒起直接阻断作用的物质基础及相互作用模式。在此基础上,为分析阻断活性化合物是否会影响ACE2 的正常功能而产生不良反应,本研究对潜在阻断成分与ACE2 的活性位点进行分子对接和深入的相互作用模式分析,并通过靶点预测-KEGG 通路分析-分子对接验证的系统研究方法分析方中非阻断药味通过调节机体间接抵御病毒的分子机制,为该方的进一步优化及开发提供依据。
1 资料与方法
1.1 虚拟筛选
1.1.1 配体准备
通过中药系统药理学数据库与分析平台(TCMSP)[16]、ETCM[17]和TCMID[18]数据库,以“苍术”“白术”“防风”“荷叶”“黄芪”“连翘”“生姜”为关键词检索扶正避瘟方化学成分结构,共收集到化合物871 个。
1.1.2 晶体结构选择及同源模建
SARS-CoV-2 S 蛋白和SARS-CoV S 蛋白序列比对结果(见图1)显示,二者一致性为76.47%,符合同源模建的条件。以SARS-CoV S 蛋白为模板(PDB ID:6ACD)[19]在Swissmodel 平台[20]完成同源模建,获得 SARS-CoV-2 的 RBD 结构,该结构和SARS-CoV-2 S 蛋白与ACE2 结构复合物晶体结构中SARS-CoV-2 RBD 结构[13]高度相似(Pymol 中RMSD计算值为1.235 Å)。
1.1.3 分子对接
使用Glide 的标准精度方法(standard precision,SP)进行分子对接。下载蛋白结构并对其进行预处理,SARS-CoV-2 结合位点的确定是基于同源模建后的结构与复合物晶体结构(PDB ID:2AJF)[17]在Pymol中叠合得到,对SARS-CoV S(PDB ID:6ACD)选择与复合物晶体结构(PDB ID:2AJF)叠合后S 蛋白结合区域周围4 Å 以内的残基作为活性位点产生Grid 文件,对ACE2(PDB ID:1R42)[15]蛋白选择其结合S 蛋白的活性位点产生Grid 文件。对“1.1.1”项下收集的小分子结构用LigPrep2.3 进行处理,运用MMFFs 力场得到相应的低能构象。Epik2.0 以pH=7.0±2.0 为条件分配电离状态并进行对接计算。
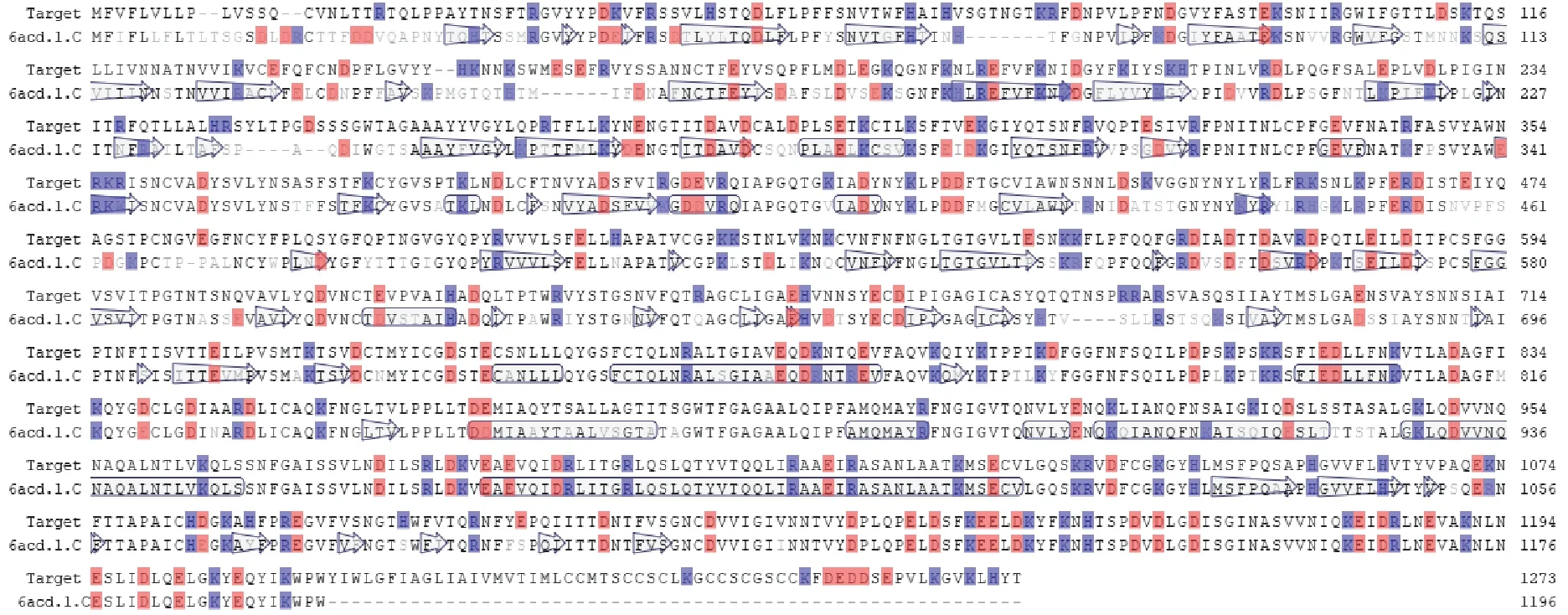
图1 SARS-CoV-2 S 蛋白与SARS-CoV S 蛋白序列比对
1.2 中药化合物靶点反向预测
中药化合物与特定靶点结合,通过调节靶点相应的生物学功能,使药物发挥治疗作用。依据分子相似性原理对化合物的作用靶点进行预测。本研究采用SwissTargetPrediction 在线分析工具(http://www.swisstargetprediction.ch),预测扶正避瘟方中非直接阻断药味的作用靶点,并将概率值≥0.5 的生物大分子作为该成分的潜在有效靶点。先将符合Lipinski 规则的中药化合物转化为标准的SMILES 格式,再将SMILES 格式文件导入SwissTargetPrediction,设置属性为“Homo sapiens”。
1.3 生物功能和通路富集分析
生物学信息注释数据库DAVID(https://www.omicshare.com/tools/)为大规模基因或蛋白富集工具,提供系统综合的生物功能注释信息,能够找出最显著富集的生物学注释[21]。将白术预测作用靶点导入DAVID 数据库,Select identifier 设置为official gene symbol,List type 设置为gene list,限定物种为homo sapiens,阈值为P<0.05,进行KEGG 通路分析。利用Image GP(http://www.ehbio.com/ImageGP/)工具在线绘制气泡图。
2 结果
2.1 靶点阻断成分筛选结果
通常打分值≤-5 的化合物被认为与靶点具有较强的相互作用,多靶点对接结果(见表1)显示,扶正避瘟方中对SARS-CoV-2 蛋白与ACE2 的结合具有潜在阻断作用的成分数量较多的药味是连翘、生姜、荷叶和黄芪,表明方中这4 味药对SARS-CoV-2 感染具有针对性的阻断作用,其中连翘、荷叶中的连翘脂苷A、(-)-儿茶素、熊竹素等单体成分具有现代药物研究基础,可作为单一成分用于预防SARS-CoV-2 感染的研究与开发,而白术对病毒感染不具有针对性的阻断作用。该结果与相应药味的药性及作用较为相符:连翘疏风散热,防止邪犯卫表;荷叶性凉,清凉解热可利湿;生姜入肺经,解表散寒、温肺止咳,阻止毒气入里;黄芪常用于补气升阳、增强正气以提高自身免疫力。本研究发现黄芪中某些成分也具有直接阻断病毒的作用。该结果初步阐明了扶正避瘟方的“避瘟”物质基础。白术为补气药,功效健脾益气,推测其主要通过调节机体免疫功能发挥“扶正”作用。
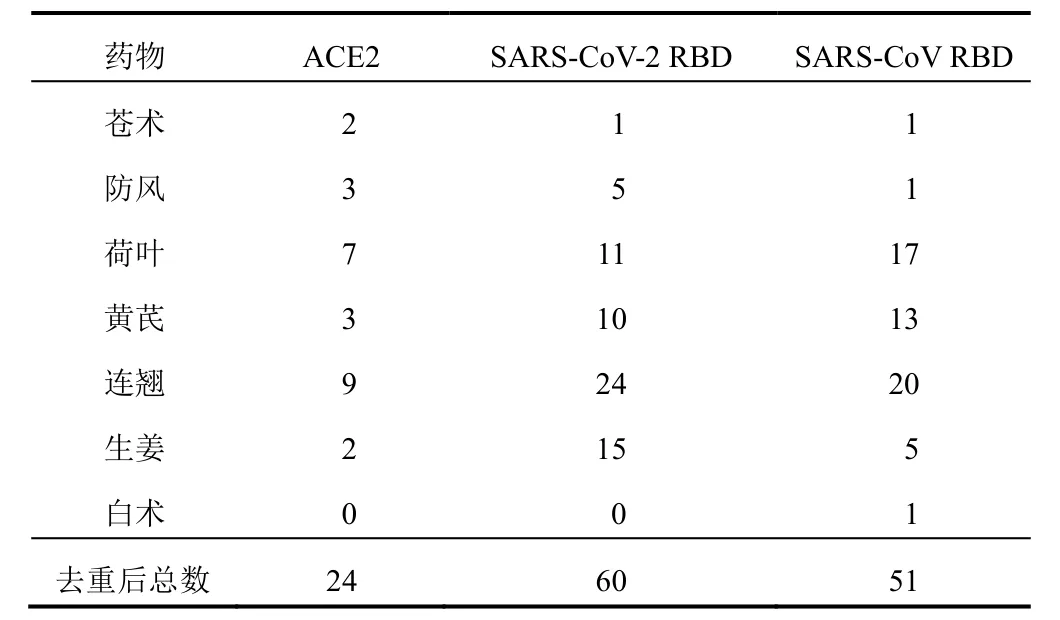
表1 扶正避瘟方中药成分对接数量(打分值≤-5)
2.2 各药味对多靶点的选择性分析
由分子对接结果可知,扶正避瘟方各药味对不同靶点具有一定的选择性。整体而言,方中诸药对S 蛋白阻断力更强,且对不同冠状病毒均有作用。连翘、荷叶显示了较强的双向阻断能力,而黄芪、生姜对S蛋白的选择性更突出。结构比对表明,SARS-CoV-2和SARS-CoV的RBD结构高度相似,但分子对接结果显示扶正避瘟方中不同药味对二者具有选择性,这为中药药味的精准选择提供了依据(见图2)。由图2可知,扶正避瘟方整体对2种病毒的阻断作用差异不大,而方中不同药味对不同病毒有一定的选择性,该结果在荷叶和生姜之间尤为突出。荷叶20个潜在阻断成分中,13个对SARS-CoV 有针对性阻断作用,7个对SARS-CoV-2有作用。生姜打分值高的12个成分中,11个对SARS-CoV-2有针对性阻断作用,而对SARS-CoV 有作用的只有1个。这一结果表明,荷叶对SARS-CoV 的选择性高于SARS-CoV-2,生姜对SARS-CoV-2的选择性高于SARS-CoV。
2.3 各靶点阻断成分作用机制分析
ACE2对接结果显示其潜在阻断化合物的结合位点分为内外两区域,外侧(图3A)是结合化合物比较多的区域,该位点共有16个化合物结合,占66.67%。以打分值≤-5和口服生物利用度(OB)>30%为依据从与2个位点结合的化合物中分别挑选出MOL007214(白矢车菊苷元)、MOL000239(熊竹素)用于ACE2 阻断成分结合模式分析(见图3A、图3B)。MOL003331(连翘脂苷A)、MOL000239(熊竹素)、MOL000096((-)-儿茶素)与SARS-CoV-2、SARS-CoV结合模式图见图3C~图3F。
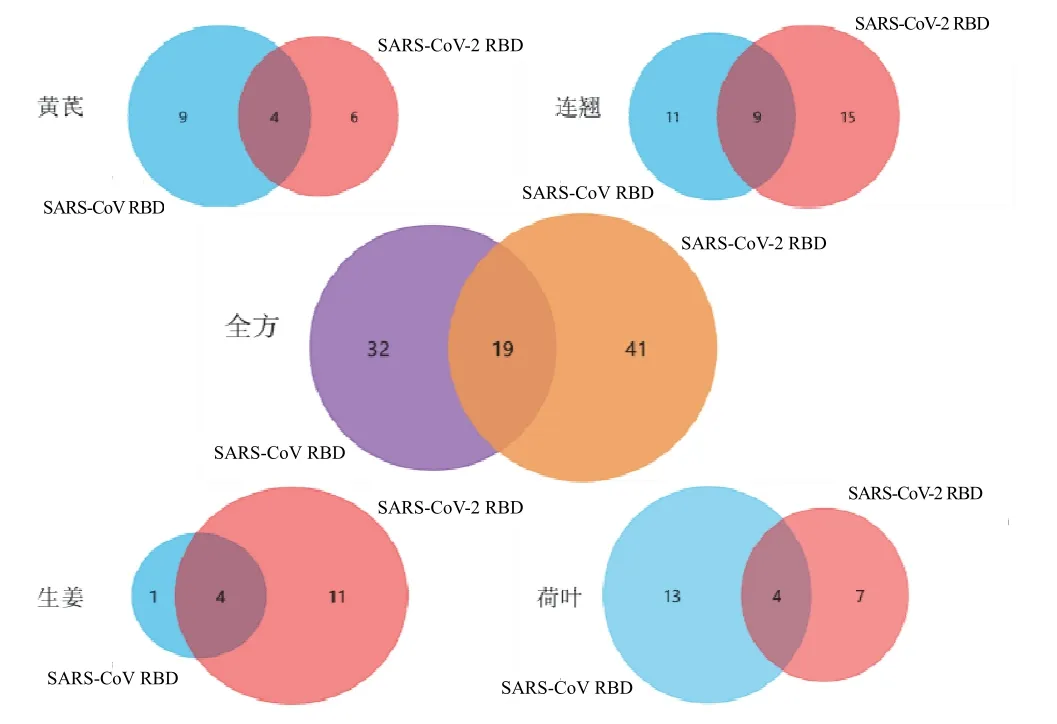
图2 扶正避瘟方各药味与SARS-CoV-2和SARS-CoV 靶向作用(打分值≤-5)成分对比分析
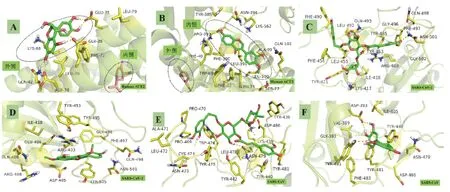
图3 代表化合物与ACE2、SARS-CoV-2、SARS-CoV 结合模式图
白矢车菊苷元结合在ACE2的外侧(见图3A),其母核为黄烷-3,4-二醇类结构,A 环7位的羟基与Asp38形成氢键相互作用,A 环5位羟基、C环4位羟基同时与残基Glu 35形成氢键相互作用,同时B环上3、4位的羟基也与Glu 75存在氢键相互作用,残基Phe72、Leu 39以疏水作用力作用在化合物上,这些作用力使化合物稳定结合于ACE2蛋白。
熊竹素垂直嵌入ACE2 的疏水空腔内(见图3B),与Tyr 385、Phe40、Phe 390、Trp 69等残基形成疏水相互作用。该化合物母核结构为黄酮类,其A 环上的6位羟基与Arg 393形成氢键相互作用,周围的极性残基和离子型残基也进一步稳定了化合物的结合。
生姜活性成分(+)-顺式香芹酚与ACE2结合时其活性位点位于蛋白内侧空腔,而ACE2与S蛋白的预融构象的结合位点则位于外侧。S蛋白亚稳定状态预融构象为了与宿主细胞ACE2 受体结合,S1 亚基RBD会经历铰链式的构象变化,这些变化能够诱导ACE2暴露受体结合位点。ACE2 与S 蛋白的结合主要发生在外侧残基,而复合物的对接结果[22]显示,中药成分的结合均在外侧。本研究对ACE2 单体结构进行对接结果显示,有部分打分较好的化合物其作用区域并不在外侧,表明中药(如生姜)的成分在ACE2 与病毒S蛋白结合前后的作用位点不同。部分化合物与ACE2单体结合时,其位点处于内侧,导致阻断能力下降,但对ACE2 与S 蛋白形成的复合物,这些成分可能因与S 蛋白形成复合物而暴露的ACE2 外侧的结合位点发生结合,产生阻断活性。
连翘中连翘脂苷A 与2 种S 蛋白的结合模式相似,主要集中在RBD 与ACE2 的结合界面上[13]。由图3C可知,连翘脂苷A苯环上的羟基与残基Phe 490、Asn 501、Tyr 495 形成氢键相互作用,2 个六元环上羟基分别与Tyr 453、Lys 417 形成氢键相互作用,化合物支链的醚氧原子与Tyr 453 亦形成氢键相互作用,周围的Leu 492、Tyr 490、Phe 497、Leu 455 等残基表现为疏水性质,周围的极性残基和离子型残基进一步稳定了化合物-蛋白结构。熊竹素苯环(A 环)与SARS-CoV-2 上的Tyr 505 产生π-π 堆积作用,且环上4 位的羟基与残基Gly 496 形成氢键相互作用,另一个环与残基Arg 403 表现为阳离子-π 作用,残基Ile 418、Tyr 453、Tyr 496、Phe 497 通过疏水作用稳定了化合物与蛋白的结合(见图3D)。连翘脂苷A 与SARS-CoV 蛋白间的主要作用力是氢键和疏水作用力(见图3E)。(-)-儿茶素与SARS-CoV 结合时,其A环上7 位羟基、B 环3,4 位羟基及C 环3 位羟基分别与残基Tyr 491、Asp 393、Tyr 440 形成氢键相互作用(见图3F)。
通过结合模式分析可知,在化合物结合区域SARS-CoV-2 与SARS-CoV 具有很多相同的热点残基,包括Tyr 453、Leu 492、Tyr 495、Phe 497、Tyr 505等,但SARS-CoV-2 中有部分热点氨基酸(Leu 455、Phe 490、Gln 493、Glu 406)发生了突变,这些突变可能是中药成分对2 种病毒S 蛋白产生选择性作用的主要原因。
2.4 潜在活性化合物对肾素-血管紧张素-醛固醇系统的影响评估
ACE2 广泛存在于人体各部位,主要分布在肾、心、肺、肝、肠等器官[23],通过肾素-血管紧张素-醛固醇系统起到平衡局部肾脏稳态[24],保护血管内皮细胞[25]、减轻动脉粥样硬化[25]、预防肺血管收缩和肺纤维化等作用[1]。因此,对ACE2 正常功能的影响将导致潜在的危险。为探讨潜在阻断成分是否会干扰ACE2 的正常功能,本研究对将潜在阻断化合物与ACE2 抑制剂的结合位点进行分子对接,发现只有2个化合物的打分值比ACE2 抑制剂MLN1706 的打分值高,分别为汉黄芩苷(MOL013068)和连翘苷G(MOL003338)。与该位点结合强的化合物进入人体后可能占据ACE2 活性位点,从而影响ACE2 的催化功能。但有研究表明,中药起效时体内各化学成分实际血药浓度可能比化学药的最小有效血药浓度更低,单一中药成分进入体内激动相关靶点并引起相应药理效应的可能性较小,通常需要多种化学成分叠加作用于相同靶点才能产生相应作用[26]。且汉黄芩苷和连翘苷G 均为苷类化合物,OB 值分别为7.07%、3.32%[16],均较低,不会直接影响ACE2 在体内的正常功能,对正常人和患有基础性疾病人群尤其高血压患者较为安全[1,27]。
2.5 非阻断药味机体调控的分子机制
分子对接结果显示,白术缺乏阻断病毒S 蛋白与ACE2 的物质基础,表明其直接阻断病毒的能力不足。本研究通过反向靶点预测方法预测白术化合物作用靶点并对其进行生物过程和通路富集分析,利用分子对接验证白术化合物与潜在靶点的亲和力。
依据Lipinski 规则筛选得到白术化合物41 个,对其进行靶点预测,保留概率值≥0.5 的24 个靶点。将24 个靶点基因名称导入DAVID 数据库,进行生物过程和通路富集分析[28]。生物过程富集结果(P<0.05)见图4,白术成分可能通过one-carbon metabolic process(一碳代谢过程)、G-protein coupled glutamate receptor signaling pathway(代谢性G 蛋白-偶联谷氨酸受体调控)等生物过程参与机体功能调节。通路富集结果(P<0.05)见图5,白术化合物靶点参与的通路包括Retrograde endocannabinoid signaling(逆行性内源性大麻素信号)、Neuroactive ligand-receptor interaction(神经活性配体-受体相互作用通路)、Glutamatergic synapse(谷氨酸能突触)等。
药物成功上市的靶点在成药性和机体调控中的关键地位是经过大量实践证实的,本研究预测靶点中有对应上市药物且临床试验成功的靶点共7 个,经查询有4 个可获得晶体结构,分别为大麻素受体2(cannabinoid receptor 2,CB2)、碳酸酐酶12(carbonic anhydrase Ⅻ,CA12)、离子型谷氨酸受体蛋白(红藻氨酸盐型)1(glutamate receptor ionotropic kainate 1,GRIK1)、α 过氧化物酶体增殖物活化受体(proliferator-activated receptor alpha,PPARA)。将这4个个靶点与白术术41 个化合物进行分子对对接(PDBID分别为CB2:6PT0[29]、CCA12:1JDOO[30]、GRIK11:4MMF3[31]、PPARRA:4IC4[32]),结果CB2、CA12、GRIKK1、PPPAARA 与各自自靶点有相互互作用的比例例分别为8/133、4/99、3/10、9/116,总比例为为24/48。
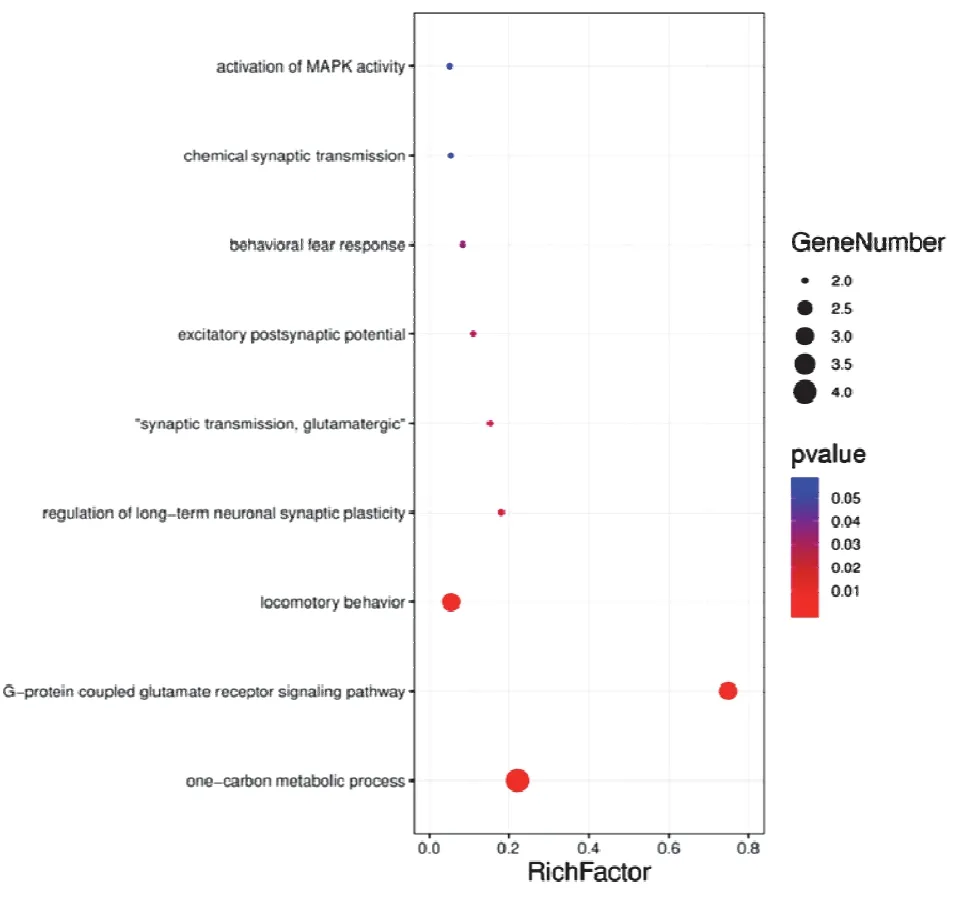
图4 白术成分靶靶点GO 富集分析析
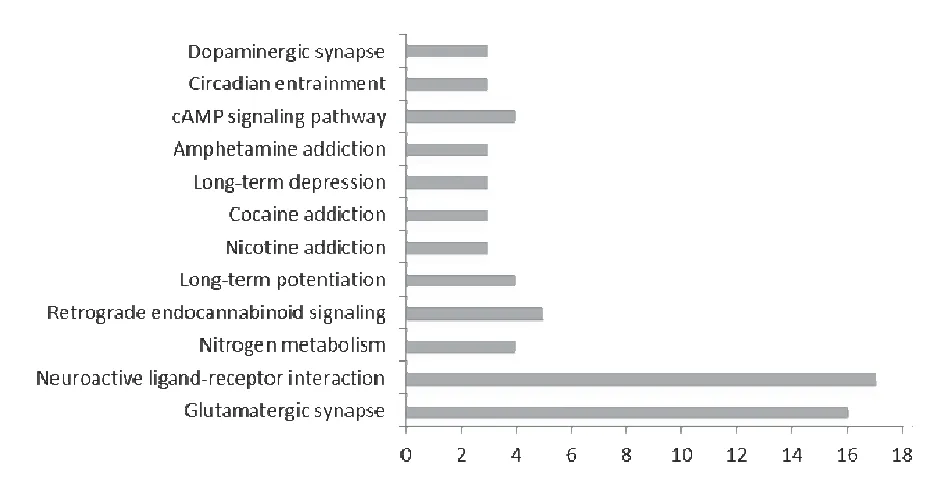
图5 白术成分靶点KEGG 通路富集分析
分子对接结结果显示,白白术与CB2打分值<-5的成分有30 个,其中打分值值<-8 的有3 个,分别别为白术内酯Ⅲ(OOB:68.11%%)、苍术酮(OB:41.10%%)和茅茅苍术醇(OOB:38.59%%),表明这33 种化合物与与免疫靶靶点CB2有有较强的潜在结结合能力。CCB2 显著表达达于免疫疫系统如B淋淋巴细胞,具具有关键的免疫疫调控功能[333]。其主要通过丝裂原活化蛋蛋白激酶(miitogen activaated prootein kinase,MAPK)信信号通路中的的3 个主要亚亚族发挥挥调控作用,,包括细胞外外调节蛋白酶酶(extracelluular siggnal-regulatedd kinase,ERRK)、c-Jun氨基末端激激酶(cc-Jun N-termminal kinase,JNK)和p338。研究表明明,CBB2 活化后,通通过激活Gii/o 释放其β、、γ 亚单位,激活MAPK 通路路,促进细胞胞内Ca2+浓度度升高,促进进β-内啡肽释放,从从而产生消炎炎镇痛作用[344];CB2 激活活后亦可可通过激活Rap1 逆转作作用,抑制炎炎症反应[34],对细胞间间黏附分子和和p-选择素的的表达进行抑抑制,进而减减少巨噬噬细胞的黏附附和浸润[33]。动物实验表明,激活活CB2可可降低白细胞胞内皮细胞相相互作用,以以进一步防止止败血症症中的炎症损损伤[35]。本研研究对白术靶靶向CB2成成分的结结合模式分析析发现,其中中具有与CBB2 激动剂相相似的结结合模式[29],,表明白术可可能通过作用用于CB2激激活其免免疫调节功能能,从而间接接抵御病毒入入体。PPARAA可参与与胰高血糖素素(glucagonn signaling paathway)、环环磷酸腺腺苷(cAMPP)、脂肪细胞胞因子(adippocytokine)、非酒精性脂肪肝肝(non-alcohholic fatty lliver diseasee(NAAFLD)等信号通路的调节[36],是高脂血症[36]、高脂蛋蛋白血症[36]、、高胆固醇和和二型糖尿病病[37]等基础性性疾病的的治疗靶点。基础疾病患患者对SARS-CoV-2 更加加易感,,白术中有228 个成分与PPARA 打分分值<-5,具具有潜在在的结合作用用,表明白术术成分具有通通过PPARAA调节基基础性相关代代谢通路的作作用,从而对对上述基础性性疾病产产生药理活性性,扶正避温温方在预防病病毒的同时也也可兼顾顾相应的基础础性疾病。
3 讨讨论
本本研究基于病病毒感染过程程的分子机制制,通过对病病毒和人人体的靶点进进行阻断成分分的筛选,初初步得到扶正正避瘟方方“避瘟”的的分子依据,并对方中药药物对不同冠冠状病毒毒发挥作用的的成分差异进进行了深入分分析,可为抗抗病毒中中药的差异化化、精准化使使用提供物质质基础和方法法学参考考。
本本研究对靶点点晶体结构选选择时进行了了充分考虑,SARSS-CoV-2 高度度糖基化的同同源三聚体S蛋白以亚稳稳定状态态的预融合构构象存在,该该结构发生构构象重排后与与宿主细细胞膜融合。由于S1亚亚基与宿主细细胞受体的结结合破坏坏了融合前三三聚体的稳定定性,导致S1 亚基脱落,S2亚亚基过渡到高度度稳定的融合合后构象。为为了与宿主细细胞受体体结合,S1 RRBD 经历了类类似于铰链的的构象运动,这些运运动可暂时隐隐藏或暴露受受体结合位点点。这2 种状状态被称称为“下”构构象和“上”构象,其中中“下”对应应于受体体的结合属于于不可达状态态,“上”对对应于受体可可达状态态,而受体可可达状态被认认为是不稳定定的。该蛋白是在与与ACE2 结合合发生结合之之前,处于不不可达状态的的预融状状态。因此,本研究选择择SARS-CoVV-2 S 蛋白预预融合构构象(“下”构构象)用于预防防方阻断成分分的筛选[38]。同样,,由于发生感感染前ACE22 尚未与S 蛋蛋白结合,故故对ACCE2 阻断成分分筛选时,选选择ACE2 单单体结构。为为探讨中中药是否对高高度相似的病病毒蛋白具有有选择性,本本研究设设计了SARSS-CoV S 蛋白白结构的虚拟拟筛选,用于于对比分分析。
本研究结果基本符合相关药味在方中的作用和相应药性,连翘、生姜、荷叶、黄芪对SARS-CoV-2感染具有针对性阻断作用,分别有24、15、11、10个阻断成分,而白术缺乏直接阻断成分。选择性分析显示不同药味对不同靶点具有针对性,荷叶对SARS-CoV 的选择性高于 SARS-CoV-2,生姜对SARS-CoV-2 的选择性高于SARS-CoV,而黄芪和连翘对2 种病毒的针对性成分数量差异不大。《证治准绳.疡医》有“连翘黄芪汤”,连翘解毒凉血、散结消肿,黄芪益气生血、托疮生肌,二者配伍有解毒消肿、托疮排脓之效。本研究表明,连翘、黄芪分别对ACE2、冠状病毒S 蛋白具有较强针对性作用,可配合使用,增强抵御冠状病毒疗效。依据《既是食品又是药品的物品名单》(卫法监发[2002]51 号),荷叶、黄芪、生姜均为药食同源中药,其中荷叶、生姜既是食品又是药品,黄芪属于保健食品类别。民间有“黄芪生姜汤”“荷叶老姜茶”等,《医学衷中参西录》记载了黄芪与荷叶相配的用法,表明这些药味配伍具有一定的应用基础和合理性。根据研究结果,荷叶、生姜、黄芪配伍值得作为防治冠状病毒感染的保健品或食疗方进一步研发。通过对白术中非直接阻断成分的作用靶点进行反向预测及通路分析可知,其主要通过逆行性内源性大麻素信号等通路发生抑制炎症作用,从而帮助机体抵御病毒。
扶正避瘟方中对SARS-CoV-2 具有潜在阻断活性成分84 个,而分子对接结果显示其中只有2 个化合物对ACE2 的催化位点具有潜在结合能力。中药体内单一化学成分激动相关靶点并引起相应药理效应的可能性较小,加之这2 个化合物口服生物利用度较低,表明该方在阻断病毒同时不会扰乱由ACE2 参与调控的肾素-血管紧张素-醛固醇系统而造成相应副作用。
本研究通过计算机辅助药物设计验证了扶正避瘟方的有效性和安全性,并对非直接阻断药味白术进行了系统性的预测,结果表明白术成分可能会激活CB2 等免疫靶点,间接调节机体免疫功能,从而起到“扶正”作用。
