注射用重组人TNK 组织型纤溶酶原激活剂对急性缺血性脑卒中的有效性及安全性研究
2021-03-13刘仕武卢展宏陈翠云
刘仕武 卢展宏 陈翠云
急性缺血性脑卒中具有高复发率、高致残率、高死亡率等特点,严重影响着人民群众的身体健康,给社会带来沉重的负担。静脉溶栓仍是治疗急性脑卒中的主要治疗手段,阿替普酶治疗急性缺血性脑卒中的有效性及安全性已得到公认,但其血管再通率并不理想,且存在一定的出血风险。本院采用第三代溶栓药物——注射用重组人TNK 组织型纤溶酶原激活剂进行静脉溶栓,取得一定成果,现报告如下。
1 资料与方法
1.1 一般资料 选取2019 年本院收治的31 例使用注射用重组人TNK 组织型纤溶酶原激活剂静脉溶栓的急性缺血性脑卒中患者作为观察组,另选取2017~2018 年本院收治的35 例使用阿替普酶静脉溶栓的急性缺血性脑卒中患者作为对照组。观察组中男20 例,女11 例;年龄48~95 岁,平均年龄(69.9±11.8)岁。对照组中男22 例,女13 例;年龄47~86 岁,平均年龄(69.4±11.3)岁。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。纳入标准:有缺血性脑卒中导致的神经功能缺损,症状出现<4.5 h;年龄≥18 岁;患者或家属签署知情同意书,且通过医院伦理委员会的批准。排除标准:有明确的溶栓禁忌证;NIHSS 评分>20 分的重度卒中患者;溶栓后行介入治疗患者。
1.2 方法 对照组采用阿替普酶进行静脉溶栓治疗,用量为0.9 mg/kg,选择10%进行静脉注射,其余90%的药量采用静脉滴注,持续1 h。观察组采用注射用重组人TNK 组织型纤溶酶原激活剂进行静脉溶栓治疗,用量为16 mg,一次性静脉注射。
1.3 观察指标及判定标准 比较两组患者溶栓前后NIHSS 评分、溶栓后不同时间临床疗效以及不良反应发生率、死亡率、痊愈率。采用NIHSS 评分评估两组患者溶栓前后神经功能缺损状况,记录溶栓前以及溶栓后1 h、3 h、6 h、24 h、72 h、7 d 的NIHSS 评分,评价其临床疗效,治愈:NIHSS 评分降低≥91%;显效:NIHSS 评分降低46%~90%;有效:NIHSS 评分降低19%~45%;无效:NIHSS 评分降低≤18%,甚至增加。总有效率=(治愈+显效+有效)/总例数×100%[1]。观察颅内出血、过敏反应等不良反应发生情况。比较两组患者溶栓30 d 及90 d 的痊愈情况,利用改良 Rankin量表(mRS)评定生活质量,0~1 分为痊愈,2~5 分为预后不良[2]。
1.4 统计学方法 采用SPSS13.0 统计学软件处理数据。计量资料以均数±标准差()表示,采用t检验;计数资料以率(%)表示,采用χ2检验。P<0.05 表示差异有统计学意义。
2 结果
2.1 两组患者溶栓前后NIHSS 评分比较 观察组溶栓后1 h、3 h、6 h、24 h、72 h、7 d 的NIHSS 评分均低于溶栓前,差异均具有统计学意义(P<0.05)。对照组溶栓后NIHSS 评分总体上呈下降趋势,溶栓后24 h 有一过性增高,溶栓后1 h、3 h、6 h、24 h、72 h、7 d 的NIHSS 评分与溶栓前比较,差异无统计学意义(P>0.05)。见表1。
2.2 两组患者溶栓后不同时间临床疗效比较 观察组溶栓后1、3 h 总有效率分别为71.0%、77.4%,均高于对照组的14.3%、51.4%,差异均具有统计学意义(P<0.05)。两组患者溶栓后6 h、24 h、72 h、7 d 总有效率比较,差异均无统计学意义(P>0.05)。见表2。
表1 两组患者溶栓前后NIHSS 评分比较(,分)

表1 两组患者溶栓前后NIHSS 评分比较(,分)
注:与本组溶栓前组比较,aP<0.05
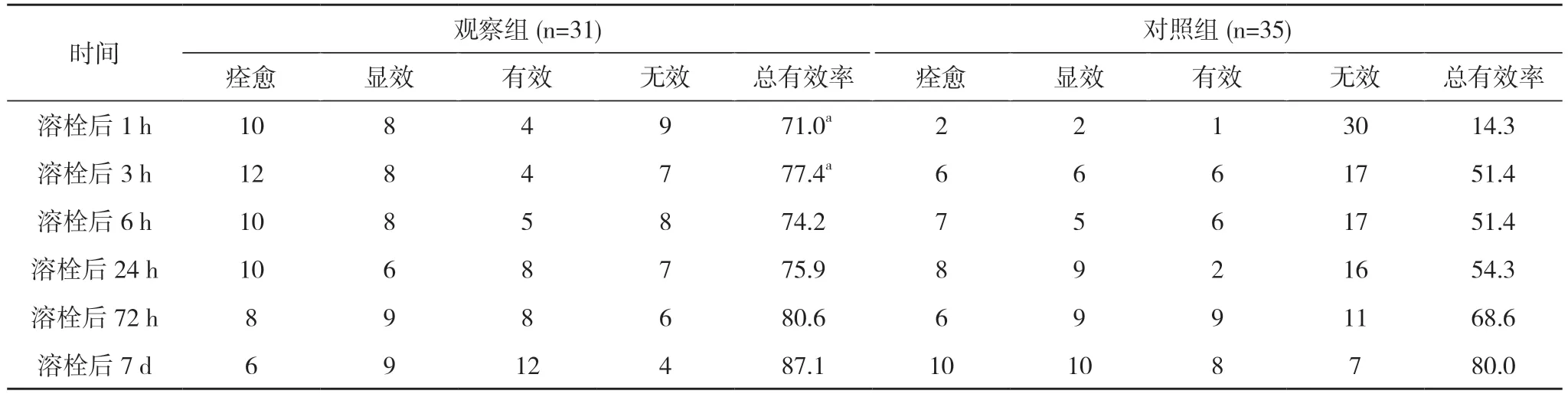
表2 两组患者溶栓后不同时间的临床疗效比较(n,%)
2.3 两组患者不良反应发生率比较 对照组颅内出血发生率为11.4%(4/35),过敏反应发生率为0,不良反应发生率为11.4%;观察组颅内出血发生率为3.2%(1/31),过敏反应发生率为6.5%(2/31),不良反应发生率为9.7%。两组患者不良反应发生率比较,差异无统计学意义(P>0.05)。
2.4 两组患者死亡率比较 对照组死亡0 例,观察组死亡1 例(3.2%),两组死亡率比较差异无统计学意义(P>0.05)。
2.5 两组患者溶栓后30、90 d 痊愈率比较 观察组溶栓后30 d 的痊愈率71.0%(22/31)与对照组的54.3%(19/35)比较,差异无统计学意义(χ2=1.944,P=0.163>0.05);观察组溶栓后90 d 的痊愈率83.9%(26/31)高于对照组的57.1%(20/35),差异具有统计学意义(χ2=5.561,P=0.018<0.05)。
3 讨论
阿替普酶是第二代溶栓药物,具有纤维蛋白选择活性,理论上不增加全身纤溶亢进,较第一代溶栓药的出血转化风险低,但体内半衰期短,为3~5 min,需短期内大量给药,引起潜在颅内出血风险[3]。第三代溶栓药物——注射用重组人TNK 组织型纤溶酶原激活剂是组织型纤溶酶原激活剂的多点变异体,其较阿替普酶半衰期延长,为18~22 min,纤维蛋白特异性和抗纤溶酶原激活物抑制剂-1(PAI-1)活性增强,血管再通更迅速,对较久的血栓溶解更强,可单次静脉推注使用,促进了溶栓治疗的快速进行,可显著提高急性缺血性脑卒中患者的早期神经功能改善率,改善患者的预后,并且不增加不良事件的发生率[4]。本次研究提示注射用重组人TNK 组织型纤溶酶原激活剂有可能减少进展性脑梗死的发生率,能够有效促进超早期患者的神经功能的恢复,改善患者的远期预后。
综上所述,注射用重组人TNK 组织型纤溶酶原激活剂可显著提高急性缺血性卒中患者的早期神经功能改善率,改善预后,并且不增加不良事件的发生率,值得在临床上推广应用。
