金属离子掺杂TiO2光催化剂及其表征技术的研究进展*
2021-03-08欧玉静石俊青
欧玉静,石俊青,赵 丹,郑 毅
(兰州理工大学 石油化工学院,兰州 730050)
0 引 言
近年来,光催化技术凭借绿色环保,无二次污染,氧化性强[1]等特点成为解决环境保护问题最有效手段之一。目前半导体光催化剂中TiO2是研究最多并且有应用的,并且TiO2在多种反应中显示出作为理想和强效光催化剂的巨大潜力[2]。TiO2的导带边支配着光激发电子的还原性,价带边支配着氧化性。然而,由于TiO2具有较宽的带隙能和较短的电子空穴对时间,因此其应用仅限于紫外活化。尽管为解决这些问题作出了许多努力,但取得的成功非常有限。提高光生载流子的分离效率,减小带隙是二氧化钛光催化剂研究核心问题。
对于半导体光催化剂,提高半导体光催化剂的光谱响应范围的手段包括贵金属沉积[3],金属离子掺杂[4],染料敏化[5]等。其中,金属掺杂方法简单,易于产业化,被认为是在可见光范围内收获的一个有吸引力的策略。金属掺杂是一种通过在带隙中创建缺陷态来延迟电荷的快速重组和使可见光吸收的方法。将价带空穴或导带电子困在缺陷部位,抑制了光致空穴与电子的复合,改善了界面电荷转移。本文将从污染物降解方面以及对金属掺杂TiO2的常用表征方法综述金属掺杂TiO2的国内外研究进展,并对其未来发展趋势进行展望。
1 TiO2的光催化降解机理
当光照射到TiO2时,价带上的电子会吸收光子(hv>Eg)进而被激发至导带,在价带上留下空穴。本征TiO2的氧化还原电位在3.0 eV附近,具有很强的氧化能力。对于位于价带上的光生空穴,通过氧化羟基(1.99 eV)或者水分子(2.18 eV),生成具有强氧化能力的羟基自由基,发生氧化还原反应。在TiO2导带附近(-0.2 eV),具有还原能力的光生电子会与溶氧发生反应生成超氧自由基,超氧自由基与氢离子反应生成过氧羟基自由基,过氧羟基自由基与光生电子结合生成羟基自由基。过程中生成的超氧自由基,过氧羟基自由基,羟基自由基攻击有机分子,发生氧化还原反应,达到降解目的。因此,在光催化过程中,采取一定的措施将光生载流子分离或消耗是提高TiO2光催化性能的重要手段。具体过程如下:
TiO2+Light→e-+h+
TiO2(h+)+H2O→TiO2+·OH+H+
2HO2·→H2O2+O2
H2O2+TiO2(e-)→TiO2+·OH+OH-
TiO2(h+)+OH-→·OH
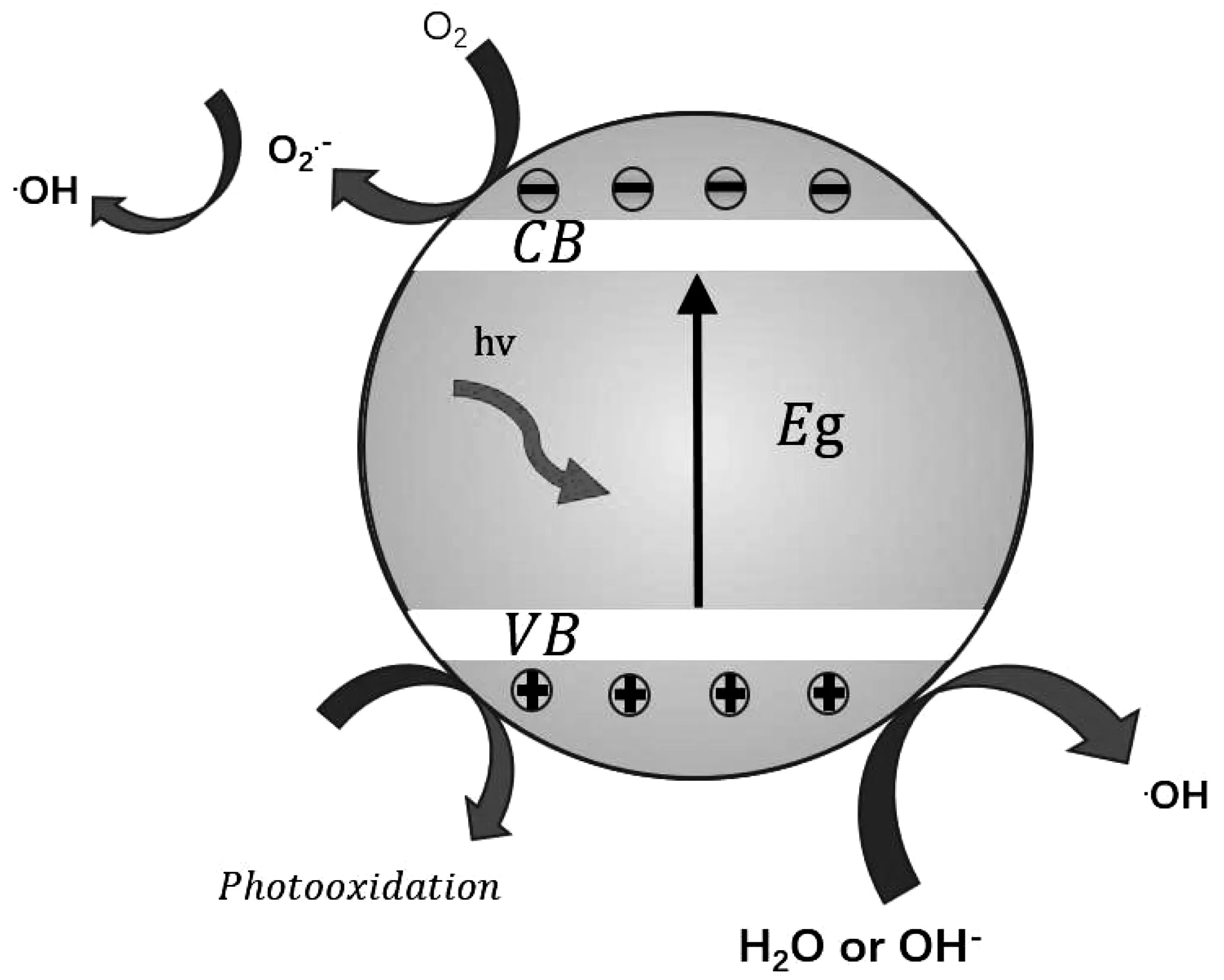
图1 光催化过程
2 金属离子掺杂
2.1 过渡金属离子掺杂
过渡金属是最早被用作掺杂剂的元素,常用的掺杂剂包括第一过渡系的铬、锰、铁、钴、镍、铜;第二过渡系的钇、锆、铌、钼、钌;第三过渡系的钽、钨等。当过渡金属离子掺杂TiO2时,在半导体的价带和导带之间会产生出现掺杂能级,从而改变能带间隙并将吸收边缘移到可见光区域[6]。L.Gomathi等人将钒,钼掺杂到TiO2在可见光下降解毒死蜱。实验结果发现所有掺杂的光催化剂都产生明显的红移,移动的程度取决于金属离子的性质和浓度,当掺杂浓度从0.02%增加到0.06%时,所有掺杂物的红移都增加,超过这个掺杂浓度吸收显示轻微蓝移。研究者分析得出当TiO2掺杂V5+,Mo6+等过渡金属时可能出现n型行为,掺杂物(V5+,Mo6+)的3d和4d轨道会在导带以下形成中间带隙,导致红移的产生[7]。近年来,Sena Yang等人研究了铬、锰、铁、钴和镍掺杂的TiO2纳米粒子光催化氧化2-ATP。实验结果显示过渡金属掺杂的TiO2(TM-TiO2)的最大价带值相对于费米能级从3.1 eV降低到1.81 eV(Cr-TiO2,2.56 eV;Mn-TiO2,2.52 eV;Fe-TiO2,2.07 eV;Co-TiO2,1.81 eV;Ni-TiO2,2.61 eV),由于掺杂过渡金属使TiO2缺陷结构增强,对于过渡金属掺杂的TiO2,由于氧原子处于钛原子和过渡金属原子之间的桥接结构,但未配对的电子会向掺杂的d轨道移动,因此,带内间隙被填满,费米能级向导带移动,从而使带隙变窄[8-9]。
一般认为在过渡金属的掺杂中,会有新相的出现,主要从两个方面产生新相。首先对于最大掺杂浓度比较低的金属来说,当掺杂浓度大于最大掺杂浓度时,掺杂金属会在TiO2表面积聚,TiO2向无定型结构转变,从而产生新相[10]。L.Gomathi Devi等人将Fe3+,Mn2+掺入TiO2,光降解靛蓝。实验发现Fe3+掺杂浓度在0.06%时,光催化剂相组成比锐钛矿:金红石比为90∶10,而在较高掺杂浓度0.1%时,相组成比为52∶48。当掺杂浓度升高时,TiO2晶格中的掺杂带来的氧空位也会随之增加,从而增大了TiO2晶格离子的重排空间,并且减少减少了应变能,使TiO2更容易相变[11-12]。最近,Wang等人合成了Sn掺杂锐钛矿型TiO2,研究发现随着掺杂浓度的增加出现了金红石相。说明掺杂浓度的提高使锐钛矿型TiO2向金红石型TiO2转变[13]。
另一方面是比Ti4+离子半径大的离子在低浓度掺杂时,TiO2的表面可能会析出氧化物,使TiO2发生相变,对光催化性能产生影响。Xinhua Gao等人研究了Mn2+、Al3+、Ni2+对TiO2的掺杂。Mn2+和Ni2+的离子半径分别为67和69 pm,明显大于Ti4+(60.5 pm),进入晶格有困难,因此在TiO2纳米管上产生了MnO和NiO,阻碍了光生电子空穴对的分离,光催化活性受到限制。而Al3+的离子半径为53.5 pm,离子很容易在晶格中被取代,两个掺杂离子取代了两个Ti4+,出现氧空位,晶体结构发生改变,产生新相,同时促进电子空穴对的产生[14]。
一般来说当过渡金属离子Mn+(n≠4)掺杂TiO2时,在TiO2中一定会存在一些缺陷来满足电荷平衡,即电荷补偿[15]。Shamsa Munir等人制备了Cu2+,Ni2+掺杂的TiO2纳米粒子。实验中通过XPS检测将TiO22p精细谱与铜,镍掺杂样品进行比较,发现在铜、镍掺杂样品中在低结合能处出现Ti3+特征峰。分析原因发现由于Cu2+,Ni2+的化合价小于Ti4+,在TiO2晶格中引入氧空位,减少了晶体系统的负电荷,该负电荷由Ti4+转化为Ti3+来平衡,发生电荷补偿[16]。
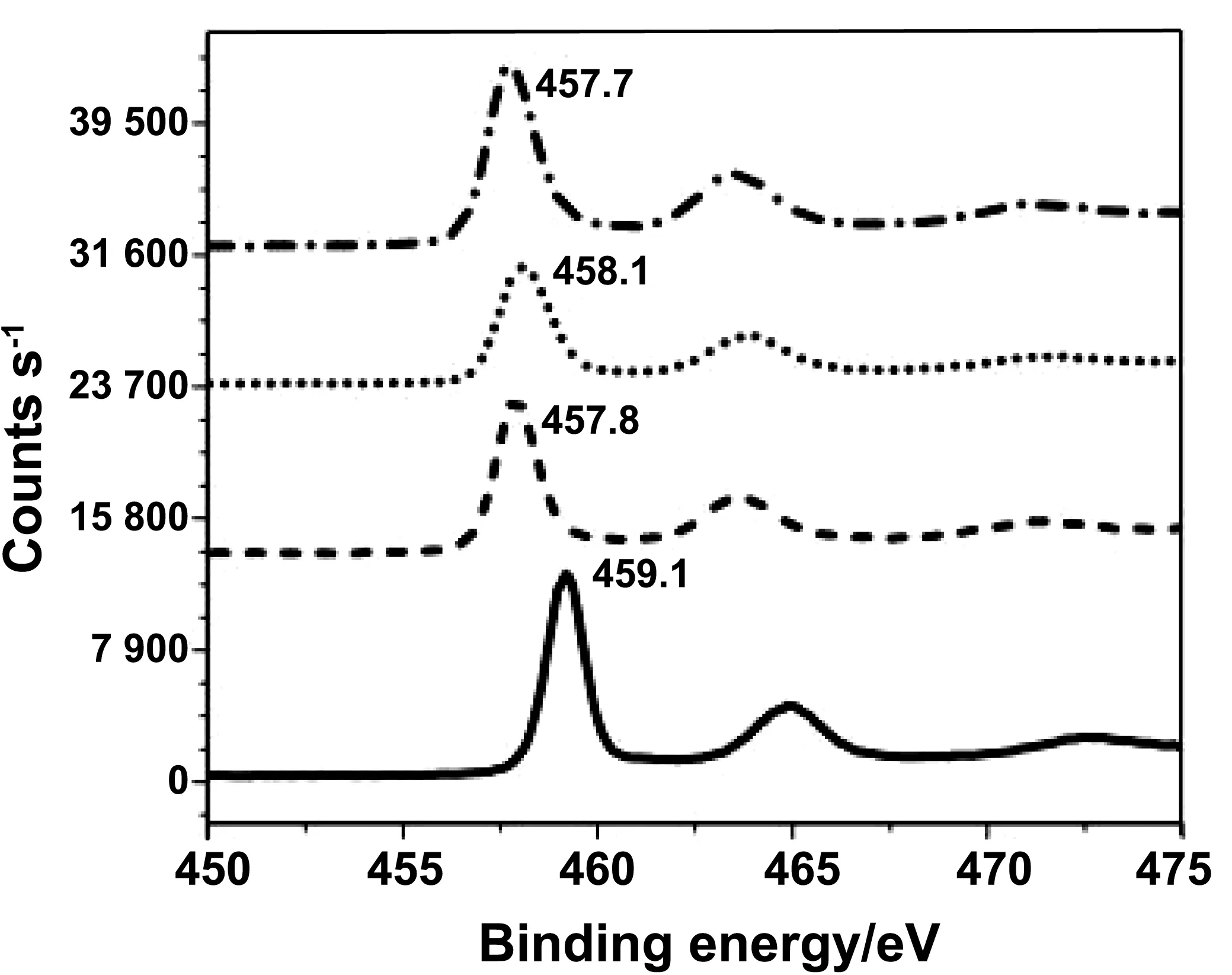
图2 TiO2(实线)XPS光谱4% Cu-TiO2、4% Ni-TiO2和2% Cr-TiO2
2.2 镧系稀土金属掺杂
在金属离子掺杂中,镧系稀土元素拥有独特的电子结构,在元素周期表处于相对特殊的位置,受到研究者们的青睐。对于镧系元素,它的电子组态为[Xe]4fn5dm6s2(n=0~14,m=0和1),有未充满的4f轨道和空的5d轨道(除镧、铈、钆、镥的5d有一个电子),使稀土离子的4f电子可以在f-f或f-d组态之间跃迁[17]。近年来,研究表明将这种电子结构特殊的元素掺杂到TiO2中,可以显著增强TiO2的光催化活性。
稀土金属离子进入TiO2晶格中,通常会形成Ti3+和氧缺陷,而氧缺陷和Ti3+有助于光生电子空穴对的分离[18]。镧系稀土金属掺杂同样可以抑制TiO2的相变。Zeinhom M.El-Bahy等人制备了镧,钐,钕,铕,钆和镱掺杂的TiO2,研究发现稀土金属离子(La3+,Sm3+,Nd3+,Eu3+,Gd3+,Yb3+离子半径分别为0.1032,0.0958,0.0983,0.0947,0.0938,0.0868 nm)半径大于Ti4+(0.068 nm),不能掺入TiO2基体中,因此,稀土金属离子Re3+会在-Ti-O-Ti-O-网络结构周围与非桥氧离子结合,形成Re2O3,而Ti4+会取代镧系稀有金属氧化物中的Re3+,从而导致Ti4+被还原成Ti3+或四面体钛位点的形成,不同四面体钛原子之间的相互作用抑制了TiO2的相变[19]。
在镧系稀土元素掺杂的研究中,普遍认为稀土元素的掺杂使TiO2表面Lewis碱性位数量增加,增强吸附能力[20]。Lin Cheng等人制备了Yb3+掺杂TiO2单晶空心纳米颗粒光催化降解橙黄Ⅱ,结果表明光照160 min后Yb3+掺杂浓度为0.5%的TiO2NHPs降解了86%的橙黄Ⅱ,是未掺杂的两倍,这是由于Ti4+以Ti3+取代稀土金属氧化物中的Yb3+,导致电荷不平衡,更多氢氧根离子被吸附在表面,氢氧根离子与光生空穴反应生成羟基自由基,从而氧化被吸附的橙黄Ⅱ分子,有效抑制了光生电子空穴对的复合[21]。
镧系稀土金属掺杂可以增大TiO2的比表面积,抑制TiO2纳米粒子在高温下的团聚。Mohamed等4种镧系稀土金属(La,Nd,Sm和Gd)制备了稀土元素掺杂TiO2-SiO2复合材料,实验现象表明材料比表面积与所掺杂的元素有关,Gd掺杂的TiO2比表面积最大,达到495 m2/g(TiO2-SiO2比表面积为320 m2/g)[22]。类似的,Liang Song等人两步法制备了镧系稀土金属(镧,铈,镨,钐,铕,铽,铒)掺杂TiO2纳米棒,通过对甲基橙和木质素的降解来测定其光催化效率。研究表明镧系稀土金属掺杂可以有效减少TiO2纳米粒子的团聚,抑制了锐钛矿型TiO2的相转变,其中Eu3+掺杂光催化活性最高[23]。
2.3 共掺杂
单一元素掺杂可以在一定程度上提高TiO2某一方面的性能,但是掺杂元素本身在掺杂过程中会成为复合中心,从而降低了单元素掺杂TiO2的电荷分离,增加了光生电子空穴对的复合速率。而多元素共掺杂可以利用多种离子之间互补,使光响应范围更宽,量子效率更高,提高光催化活性。对于多金属离子共掺杂,大致分为两种情况,一种情况是两种离子分别做光生电子捕获陷阱和光生空穴捕获陷阱,降低光生电子空穴的复合率;另一种情况是一种离子拓宽TiO2的光吸收至可见光,另一种离子作为光生电子空穴对的捕获陷阱[24]。Imen Tbessi等人合成了掺杂锰和铈的TiO2,对双氯芬酸进行了降解。研究结果表明锰和铈在改善半导体光生电子空穴对分离中起不同的作用,锰作为光生空穴捕获陷阱,铈作为光生电子捕获陷阱,降低了光生载流子的复合几率[25]。Sanitnon, P等人溶胶凝胶法制备了Zr,Ag共掺杂的TiO2纳米粒子,光催化降解亚甲基蓝。该样品展现出优异的光催化性能,紫外可见分光光度计测定了合成的光催化剂的波长吸光度,显示掺杂Ag的TiO2在荧光灯下的吸光度明显向长波长转移,吸光度明显增加。这可能归因于表面等离子体共振,这是Ag纳米粒子与光相互作用时的一种独特的光学性质,掺杂Zr4+的TiO2光谱出现了明显的光吸收边蓝移和窄带隙,这是由于TiO2晶格中Zr4+被替换所致对其分析原因发现Zr和Ag之间存在协同作用,Ag通过减小能带间隙提高了TiO2在可见光下的吸收能力,而Zr则捕获电子,阻碍电子/空穴对的复合[26]。
相对于单元素掺杂,多元素掺杂可以增大TiO2的光吸收红移程度,多种元素之间的协同效应更加显著的抑制光生电子空穴对的复合,增强光催化性能[27]。Tianping Lv采制备了钒和钴共掺杂TiO2光催化剂,对甲基橙进行降解,研究者发现发现钒钴共掺杂TiO2的孔径更窄,易于捕集甲基橙分子,有利于提高对甲基橙的吸附性能,从而提高光催化降解效率。并且共掺杂样品比钒掺杂和钴掺杂的样品红移更明显,从405 nm移向475 nm,在钒离子和钴离子共掺杂后,引起TiO2晶格畸变,内部偶极矩增大,光生电子空穴复合速率进一步降低[28]。
3 金属掺杂TiO2的表征研究
3.1 XRD
自1912年W.H.Bragg和V.L.Bragg使用XRD表征NaCl晶体的结构特性以来[29],该技术已成为识别晶体原子和分子结构的流行工具。XRD测量基于晶体原子使入射X射线束衍射到许多特定方向的方式。研究者通过XRD研究了掺杂剂对TiO2结晶度和相变的影响,因为掺杂物(如Nb[30], ce[31],Li[32])的存在降低了结晶度,如果掺杂物优先出现在其中一个相中,也会诱导相转变。Kityakarn, S等研究发现在金红石TiO2中掺杂Ce会迅速降低金红石相特征峰的强度[31],如图3,而同时出现了与板钛矿(121)晶面相对应的新峰,这表明少量的掺杂剂对TiO2的光催化性能影响很大。El Mragui, A等人制备了铁和钴共掺杂的TiO2,与未掺杂的TiO2NPs相比,所有样品(主要是共掺杂的TiO2NPs)的锐钛矿峰强度均降低。此外,仔细分析了锐钛矿的主峰(101)。对于Fe掺杂的TiO2和 Co掺杂的TiO2纳米颗粒,向较高角度的一侧略有偏移。通过比较Co2 +(0.074 nm),Co3 +(0.061 nm),Fe2 +(0.076 nm)和Fe3 +(0.065 nm)与Ti4 +(0.068 nm)的阳离子半径值[25,28,30,32],研究者推测二氧化钛的结构中掺入了一些掺杂元素,并取代了钛离子,引起了锐钛矿晶体结构的扰动。导致结晶度降低并且峰位置移动[33]。同样,XRD技术可以确定金属掺杂TiO2后的结构信息,例如微晶尺寸[34],尺寸分布[35],形貌[36],晶体结构[37]等。
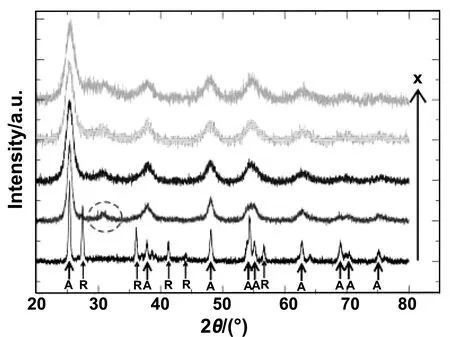
图3 Ti1-xCexO2的衍射数据
3.2 拉曼光谱法
3.3 电感耦合等离子体-原子发射光谱(ICP-AES)
ICP-AES可以基于每种元素特有的发射光谱对物质进行表征,每种元素对应不同的特征谱线。Zhao, Y研究了以过氧金属络合物制备了Sn4+掺杂的TiO2,通过ICP-AES分析得出Sn4+成功掺杂,理论上说过氧钛配合物是由两个过氧化物配体配位的Ti4+离子双核。这个双核的过氧钛络合物慢慢凝聚成多核阴离子。这种情况下的基本结构是[M(OH)2TiO5Ti]0。溶剂热处理后,过氧基分解,形成单体[M(OH)4(OH2)2]0(M: Ti或Sn)生长单元。ICP-AES分析发现大部分Sn4+离子存在于TiO2颗粒表面以上。虽然Sn4+含量高,能形成更多金红石核。但八面体[M(OH)4(OH2)2]0单位(M = Ti或Sn)与溶剂的反应性不同,阻碍了金红石相的形成[41]。

图4 TiO2拉曼光谱
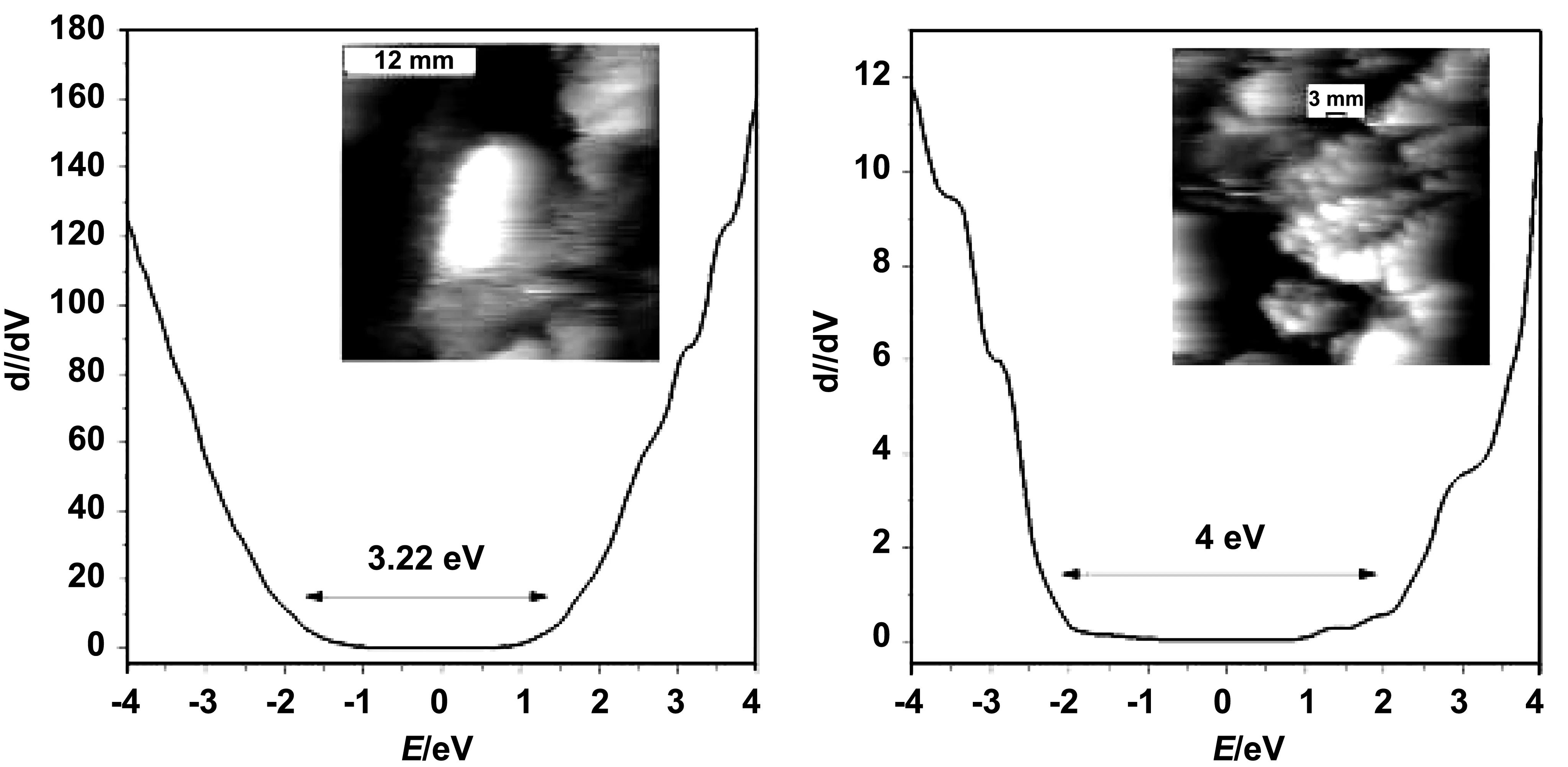
图5 STM图像
3.4 扫描隧道显微术(STM)
STM被用来研究样品电子特性。它可以探测费米能级上的电荷密度。当尖端与样品之间施加的偏置电压(Vbias)为正时,电子从尖端进入试样,然后探测试样的最低未占据状态[42]。当施加负Vbias时,电子从试样进入尖端,并探测试样的最高占据状态。由于尖端尖锐,STM图像可以显示原子分辨率。近年来,对金属掺杂TiO2的电子性质进行了理论和实验研究[43]。隧穿光谱是通过将尖端放置在不同的孤立的TiO2纳米粒子上并测量其Ⅰ-Ⅴ特性来实现的。对Ⅰ-Ⅴ特性的测量总是重复几次,信号最终被平均100次运行。通过对测得的Ⅰ-Ⅴ曲线进行数值微分,得到了与态的特征密度相对应的dⅠ/dⅤ对Ⅴ的特性。Grujic-Brojcin, M研究了镧掺杂对溶胶-凝胶法制备的TiO2纳米粉体结构和形貌的影响。研究者通过STM测试,对比了掺杂与未掺杂La的TiO2粒子的dI/dV对V的特性,发现在La掺杂后表面带隙从3.2 eV提升到了4 eV[44]。
3.5 其他
除上述技术外,还包括扫描电子显微镜(SEM),HRTEM,X射线电子能谱(XPS)等。SEM通常用于研究金属掺杂TiO2的形态,并且通过EDX能谱和EDX mapping观察组分与元素分布[45]。HRTEM是基于金属掺杂TiO2某一特定区域确定其元素组成和物相结构的最常用技术[46]。XPS用于研究物质表面化学状态和化学组成通过结合能和化学位移来分析掺杂金属离子在TiO2中的化学价态和存在形式[47]。
4 结 语
综上所述,国内外研究者对过渡金属离子掺杂,镧系稀土金属离子掺杂以及多种金属离子共掺杂TiO2的催化活性进行了研究。通过不同金属离子的掺杂,主要从三个方面来提高TiO2材料的性能。一是通过金属离子掺入在TiO2晶格中引入缺陷,尤其是氧缺陷,来增加材料的表面活性位点,增强光催化性能;二是金属离子掺杂可以抑制锐钛矿型TiO2的相转变;三是金属离子掺杂会引入新的杂质能级,调控TiO2价带和导带的位置,扩大光吸收范围。但是,在金属离子掺杂TiO2的理论和应用方面仍然存在一些问题。(1)在单元素掺杂中,金属离子的掺入会作为光生空穴电子对的复合中心,导致光催化性能降低,因此在以后研究中需要恰当的选择一种掺杂金属和合适的掺杂浓度范围;(2)使用单元素金属离子掺杂虽然可以提高TiO2的光催化性能,但是提高是有限的,而多种元素之间共掺杂可以发挥元素之间的协同作用,获得比单掺杂更好的效果。特别是镧系稀土金属之间的共掺杂具有很大的发展潜力,会是今后TiO2掺杂的主要研究方向;(3)在TiO2中掺入金属离子可以提高光催化性能,但掺入的物质可能会造成环境污染,比如重金属离子。因此,探究一种经济无害的物质掺杂TiO2也是今后一个研究重点和难题。在表征金属掺杂TiO2方面,先进的表征技术可以描述物理化学性质和光催化过程,也可以用来评价光催化剂的性能。这些先进的表征技术的发展不仅将扩大对光催化基础研究的贡献,而且将促进具有高太阳能转换效率的新型钛基光催化剂的设计。
致谢!兰州理工大学红柳一流学科建设项目!
