隐丹参酮纳米混悬剂的制备及其抗肿瘤活性
2021-03-07李晓婷决利利郝海军王世广
李晓婷,决利利,郝海军,王世广
(1.郑州工业应用技术学院医学院,河南郑州 451150;2.中国医药工业研究院,上海 201203)
隐丹参酮是从唇形科植物丹参Salvia miltiorrhizaBge.中提取得到的主要脂溶性活性成分之一[1],对胃癌、宫颈癌、肺癌等多种肿瘤细胞具有明显抑制作用[2],也对心肌梗死、扩张冠状动脉、活血化瘀等心血管疾病有着较好的治疗作用,但它属于难溶性成分[2],从而大大限制了其药效发挥[3],成为相关临床应用的瓶颈。虽然磷脂复合物、自微乳、脂质体等技术解决了一些难溶性药物药效较低的问题,但均存在一定局限性,如稳定性差、制备工艺复杂、大量使用表面活性剂等。
纳米混悬剂是通过加入稳定剂后采用某种制剂技术而制备得到的一种亚微米胶体给药体系[4-5],它无需载体材料,可有效避免共溶剂的不良反应,并可显著提高药物溶解度和疗效。因此,本实验将隐丹参酮制成纳米混悬剂,对其粒径、Zeta 电位、形态、稳定性、体外释药进行考察,并采用四甲基偶氮唑盐(MTT)法研究它对人胃癌细胞SGC-7901 的抑制作用,以期为进一步相关研究提供参考。
1 材料
QUINTX224-1CM 型电子天平(德国Sartorius公司);Agilent 1260 型高效液相色谱仪(美国Agilent 公司);JY92-III 型超声仪(浙江大天科学仪器有限公司);SZCL-H 型温控磁力搅拌器(郑州宇华仪器有限公司);Master-sizer 型粒度分析仪(英国马尔文仪器有限公司);FD10-QX 型真空冻干机(上海天赐科学仪器公司);Kylin-Bell 型漩涡混合器(海门其林贝尔仪器制造有限公司);MR-96T 型酶标仪(南京贝登医疗股份有限公司);HNA-122DTABA I 型CO2恒温培养箱(日本三洋公司)。
隐丹参酮原料药(批号Y-034-181217,纯度>98%,上海源叶生物科技有限公司);隐丹参酮对照品(批号110852-201702,纯度99.5%,中国食品药品检定研究院)。大豆卵磷脂(批号PC-95,上海辅必成医药科技有限公司);泊洛沙姆188(批号WPEE578,德国巴斯夫公司);胰蛋白酶(美国HyClone 公司);RPMI-1640 培养基(美国Gibco 公司);二甲基亚砜(DMSO)、四甲基偶氮唑盐(MTT,批号1524B37,美国Amresco 公司)。人胃癌SGC-7901 细胞,购自上海研域生物工程有限公司。
2 方法与结果
2.1 色谱条件 Agilent Zorbax C18色谱柱(4.6 mm×250 mm,5 μm);流动相乙腈-0.5% 甲酸(72∶28);体积流量1.0 mL/min;柱温30 ℃;检测波长272 nm;进样量20 μL。
2.2 隐丹参酮纳米混悬剂制备 取大豆卵磷脂、泊洛沙姆188 各200 mg,超声溶解于100 mL 蒸馏水中,作为溶液A;取隐丹参酮100 mg,超声溶解于10 mL 无水乙醇中,作为溶液B。设置磁力搅拌器温度为70 ℃,转速为800 r/min,将溶液B 逐滴加到溶液A 中,同一温度下真空浓缩除去乙醇,设置均质压力为80 MPa,循环10 次后补加蒸馏水至100 mL,即得。
2.3 隐丹参酮纳米混悬剂理化性质研究
2.3.1 粒径、Zeta 电位测定 取3 批隐丹参酮纳米混悬剂,蒸馏水按照1∶6 比例稀释后置于粒度分析仪上,测定粒径、Zeta 电位,结果见图1~2。由此可知,纳米混悬剂粒径分布在50~200 nm 之间,平均粒径为104.15 nm,PDI 为0.014,Zeta电位为-36.3 mV。

图1 隐丹参酮纳米混悬剂粒径分布Fig.1 Particle size distribution of cryptotanshinone nanosuspensions

图2 隐丹参酮纳米混悬剂Zeta 电位Fig.2 Zeta potential of cryptotanshinone nanosuspensions
2.3.2 形态 取隐丹参酮纳米混悬剂、空白纳米混悬剂各100 μL,加入4 mL 蒸馏水,摇匀后滴至铜网上,自然晾干,滴加1.0% 钨酸钠溶液染色,静置10 min,滤纸吸干后置于透射电镜(TEM)下观察形态,结果见图3~4。由此可知,隐丹参酮纳米混悬剂中纳米粒之间无粘连现象,基本呈球形;空白纳米混悬剂中纳米粒形态类似囊泡结构,可能是由于其中的表面活性剂(磷脂)未吸附于纳米粒表面,而是分散在水相中形成该类结构。

图3 隐丹参酮纳米混悬剂TEM 图Fig.3 TEM image for cryptotanshinone nanosuspensions
2.4 隐丹参酮纳米混悬剂稳定性研究

图4 空白纳米混悬剂TEM 图Fig.4 TEM image for blank nanosuspensions
2.4.1 室温下 取隐丹参酮纳米混悬剂(蒸馏水将其质量浓度稀释至0.5 mg/mL),室温下于0、1、3、5、7、15、21、30 d 测定粒径,结果见图5。由此可知,15 d 后粒径增大了约10 nm,而30 d后增大了约21 nm,但肉眼未发现沉淀或聚集现象。

图5 室温下隐丹参酮纳米混悬剂粒径Fig.5 Particle size of cryptotanshinone nanosuspensions at room temperature
2.4.2 空白血浆、1.8%氯化钠溶液中 将隐丹参酮纳米混悬剂与空白血浆按1∶4 比例混合,或与1.8%氯化钠溶液按1∶1 比例混合(质量浓度为0.5 mg/mL)后,置于37 ℃水浴中,于0、1、2、4、6、8、10、12 h 测定粒径,结果见图6。由此可知,加入空白血浆、1.8%氯化钠溶液后,与加入前(104.15 nm)相比0 h 粒径分别增加约42、36 nm,随着时间延长均逐渐升高,在12 h 后仍均小于162 nm,而且在1.8%氯化钠溶液中的变化程度更小,故可考虑将其作为注射分散介质。
2.5 隐丹参酮纳米混悬剂冻干粉制备
2.5.1 冷冻干燥工艺 将隐丹参酮纳米混悬剂分成若干份,每份3 mL,置于西林瓶中,加入冻干保护剂,混匀,置于真空冻干机中(初始温度-55 ℃),按照图7 程序进行冷冻干燥,并在25 ℃下保持4 h,即得浅红色疏松的冻干粉,其色泽均匀,外形饱满,再分散性良好。

图6 空白血浆、1.8%氯化钠溶液中隐丹参酮纳米混悬剂粒径Fig.6 Particle sizes of cryptotanshinone nanosuspensions in blank plasma and 1.8% sodium chloride solution
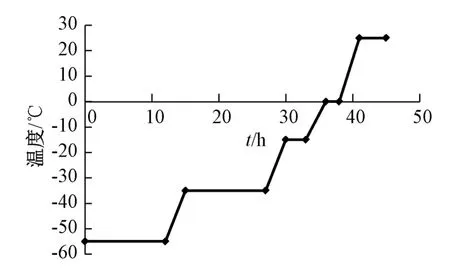
图7 冷冻干燥程序Fig.7 Lyophilization procedure
2.5.2 冻干保护剂种类及用量 取不同质量分数甘露醇、乳糖、蔗糖,加入到隐丹参酮纳米混悬剂中,冷冻干燥后取适量冻干粉,加入蒸馏水复溶后测定粒径、Zeta 电位,结果见表1。由此可知,加入3%甘露醇后冻干粉粒径、Zeta 电位与冷冻干燥前(104.15 nm、-36.3 mV)相比变化最小,故选择其作为冻干保护剂。

表1 冻干保护剂种类及用量对粒径、Zeta 电位的影响(n=3)Tab.1 Effects of lyoprotectant kind and consumption on particle size and Zeta potential(n=3)
2.6 隐丹参酮纳米混悬剂体外释药研究 用2 mL 1.5%十二烷基硫酸钠溶液分别制备隐丹参酮及其纳米混悬剂冻干粉的混悬液(含10.0 mg 隐丹参酮),置于透析袋中(截留分子量8 000~14 000 Da),两端扎紧。以900 mL 1.5%十二烷基硫酸钠溶液为释放介质,设定温度为(37 ± 1)℃,转速为100 r/min[6-7],于0、0.5、1、1.5、2、3、4、6、8、12、24、48 h 各取样3 mL 后,立即补加3 mL空白溶出介质以保持总体积不变,取样液过0.45 μm微孔滤膜,在“2.1”项色谱条件下进样测定,体外释放曲线见图8,可知原料药在24 h 内累积释放度仅为23.17%,之后几乎没有释放,这与其溶解度差、颗粒大等因素有关;纳米混悬剂在前12 h 释放相对较快,累积释放度达到64.28%,之后呈明显缓释特征;释药过程最符合Higuchi 模型,见表2。
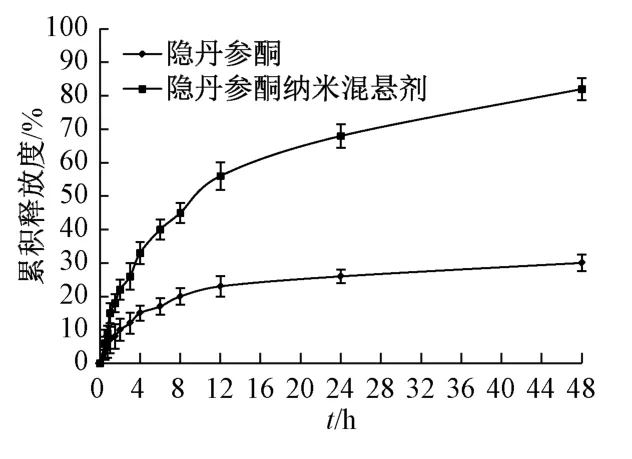
图8 隐丹参酮体外释放曲线Fig.8 In vitro release curves for cryptotanshinone

表2 药物释放拟合结果Tab.2 Results of drug release fitting
2.7 隐丹参酮纳米混悬剂对SGC-7901 细胞的抑制作用
2.7.1 药液制备 将30.0 mg 隐丹参酮溶于100 mL DMSO 中,得到300 μg/mL 母液,用含10%FBS 的RPMI-1640 培养液将其依次稀释至30、24、18、12、6 μg/mL;取隐丹参酮纳米混悬剂冻干粉,用含10% FBS 的RPMI-1640 培养液将其依次稀释至30、24、18、12、6 μg/mL(以隐丹参酮计),即得。
2.7.2 分组与给药 采用MTT 法。取对数生长期的SGC-7901 细胞,0.25%胰蛋白酶消化并吹打成单细胞悬液,细胞培养液调整其浓度为5×105/mL,取100 μL 接种于96 孔板中,置于37 ℃、5%CO2细胞培养箱中培养12 h,弃去培养液,设置空白对照组(细胞加培养液)、隐丹参酮组(30、24、18、12、6 μg/mL)、隐丹参酮纳米混悬剂组(30、24、18、12、6 μg/mL),每个质量浓度3 个复孔。继续培养6、12、24、48 h 后,每孔加入20 μL 0.5%MTT 溶液,继续孵育4 h 后甩板,每孔加入150 μL DMSO,固定于摇床上振荡1.0 h 以充分溶解蓝紫色结晶物,在参比波长630 nm、主波长570 nm 的酶标仪中测定吸光度(A),计算抑制率,公式为抑制率= {1 -[(A空白对照组-A给药组)/A空白对照组]} ×100%,通过GraphPad Prism 5 软件计算IC50,SPSS 22.0 软件进行统计学分析。
2.7.3 结果分析 表3 显示,随着药物质量浓度增加,隐丹参酮及其纳米混悬剂对SGC-7901 细胞的抑制作用均更明显,并且在药物质量浓度相同的情况下随着作用时间延长,该活性也逐渐增强,即呈浓度、时间依赖性;在药物质量浓度相同的情况下,纳米混悬剂抑制作用均强于原料药,而且后者作用48 h 后各质量浓度下抑制率与前者比较,差异均有统计学意义(P<0.05,P<0.01);IC50分别为24.72、11.76 μg/mL,两者比较,差异也有统计学意义(P<0.01)。
表3 隐丹参酮纳米混悬剂对SGC-7901 细胞的抑制率(, n=3)Tab.3 Inhibitory rates of cryptotanshinone nanosuspensions on SGC-7901 cells(, n=3)

表3 隐丹参酮纳米混悬剂对SGC-7901 细胞的抑制率(, n=3)Tab.3 Inhibitory rates of cryptotanshinone nanosuspensions on SGC-7901 cells(, n=3)
注:与隐丹参酮组比较,∗P<0.05,∗∗P<0.01。
3 讨论
纳米混悬剂中的表面活性剂可吸附于纳米粒表面,提供立体位阻作用,防止粒子之间发生聚集现象,从而提高制剂稳定性,但表面活性剂对纳米粒粒径、Zeta 电位的影响较大。前期预实验对不同表面活性剂进行筛选,发现粒径大小由低到高依次为大豆卵磷脂、泊洛沙姆188、聚乙烯醇、聚山梨酯80。研究表明,几种表面活性剂联合应用有助于提高制剂长期稳定性[6],故本实验最终采用采用大豆卵磷脂、泊洛沙姆188(比例1∶1)作为表面活性剂。
体外抗肿瘤实验结果显示,在相同用药剂量下隐丹参酮纳米混悬剂对SGC-7901 细胞的抑制作用强于原料药,其原因一方面可能是由于纳米粒能通过非特异性内吞作用或吞噬作用内化入胞,从而增强药效[8-13];另一方面,纳米混悬剂稀释后隐丹参酮处于溶解状态,处方中大豆磷脂有助于促进药物进入细胞[7],而泊洛沙姆188 会影响肿瘤细胞转运蛋白作用[14],降低肿瘤细胞对胞内药物的外排,从而增加药物胞内蓄积。前期研究表明,泊洛沙姆188 具有逆转耐药、增加药物药效等作用[14-16]。因此,纳米混悬剂不仅有助于解决隐丹参酮溶解度差的问题,而且可提高其药效。
