定量血流分数评价左心室舒张功能不全患者心肌缺血的价值△
2021-03-07黄美萍黄育铭丘庆华谈文开
席 悦,黄美萍,,黄育铭,丘庆华,谈文开
[1.华南理工大学医学院,广州 510006;2.广东省心血管病研究所介入导管室广东省人民医院(广东省医学科学院),广州 510080]
左心室舒张功能不全(left ventricular diastolic dysfunction,LVDD)是射血分数保留型心力衰竭(heart failure with preserved ejection fraction,HF⁃pEF)发生的重要基础[1]。冠状动脉粥样硬化性心脏病(冠心病)患者的心肌舒张功能先于收缩功能出现障碍,是提示早期心肌缺血的重要标志。早期诊断心肌缺血相关LVDD 并及时治疗可以延缓、阻止患者心功能不全的进展,改善预后,提高生存率[2]。传统的定量冠状动脉造影(quantitative coronary angiography,QCA)可从解剖学角度评估冠状动脉狭窄,但该技术是在二维平面进行测量,受血管解剖因素和图像角度影响很大,易漏诊或误诊。血流储备分数(fractional flow reserve,FFR)可通过测量病变压力改变,从功能学角度评估心肌缺血。但FFR 测定需要使用压力导丝等特殊器械,且价格昂贵。目前,FFR 多用于临界病变、中度狭窄病变、分叉病变等的评估[3]。而LVDD 患者较多,无法普遍使用FFR 评估有无合并心肌缺血。近年来,我国原创的基于冠状动脉造影的定量血流分数(quantitative flow ratio,QFR)可通过血管三维重建与流体力学分析快速获得血流储备分数(fractional flow reserve,FFR),是一种新颖且快速地评估冠状动脉功能学狭窄的分析方法,并且不需要压力导丝等昂贵及特殊的耗材[3-5]。本文将结合冠状动脉造影及FFR 探讨QFR 在早期识别心肌缺血相关的LVDD 中的作用。
1 资料和方法
1.1 一般资料
选择2017 年1 月至2018 年12 月间因胸闷等不适至广东省人民医院就诊,超声诊断为LVDD并在本院进行冠状动脉造影检查及完成FFR 测量的患者110 例。排除标准:左心室收缩功能障碍[左心室射血分数(left ventricular ejection fraction,LVEF)<50%]、FFR 测量禁忌、因图像质量问题无法完成QFR 及QCA 检测。本研究通过广东省人民医院伦理委员会审核,所有患者均签署知情同意书。
1.2 数据收集
收集研究患者的临床及影像学相关资料:(1)患者临床基线资料[年龄,性别,并发症情况(糖尿病、高血压、高脂血症),超声心动图数据,既往史,个人史及家族史];(2)患者冠状动脉造影资料;(3)FFR 测量结果。
1.3 分组方法
以FFR 测量结果作为诊断心肌缺血的“金标准”,根据FFR 值分为心肌缺血组(FFR≤0.80,n=52),男40 例,女12 例;对照组(FFR>0.80,n=58),男36 例,女22 例。分别用QCA 和QFR 两种工具对两组患者既往的造影图像处理分析并进行比较。
1.4 定量冠状动脉造影分析方法
本研究使用QCA 工作软件(北京思创科技有限公司)进行分析,图像选择对比剂充盈良好的静态图,以6 F 的导管作为参考值校正像素,获得病变血管的直径狭窄率等数据。在每次分析之前,研究者需告知技术员测量血管的位置,由两名熟练的具有中级职称的技术员分析血管的QCA 数值,且由一名高级技术员核实准确性。
1.5 定量血流分数分析方法
将患者造影图像传送到QFR 分析系统(Angio Plus,搏动医疗影像技术上海有限公司,中国上海)。选择两幅造影角度相差>25°的图像,优先使用血管轮廓自动描绘法识别病变血管的轮廓,如果自动法出现误差,允许手动校正血管的轮廓,使用数帧法来模拟血流压力,最终计算血管QFR 数值。在每次分析之前,研究者需告知技术员测量血管的位置,由两名熟练的具有中级职称的技术员分析血管的QFR 数值,且由一名高级技术员核实准确性(图1)。
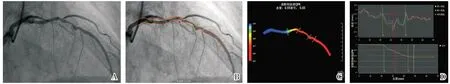
图1 QFR 测量过程图[A:冠状动脉造影显示前降支狭窄;B:血管轮廓识别;C:冠状动脉三维重建后计算得出前降支QFR 为0.55;D:QFR 分析数据]
1.6 统计学分析
应用SPSS 17.0 和MedCalc 19.0 软件进行统计学分析。计量资料用()表示,采用t检验。计数资料以[n(%)]表示,采用卡方分析或者Fisher检验。根据既往研究结果及指南建议[3],以QFR≤0.80 及QCA≥50%作为诊断界点,并计算其敏感度、特异度、阳性预测值、阴性预测值、阳性似然比、阴性似然比,绘制受试者工作曲线(receiver operat⁃ing characteristic curve,ROC)比较QFR 与QCA 的诊断效能。以P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者的基线资料比较
两组患者在性别、年龄、糖尿病(糖化血红蛋白浓度)、原发性高血压(高血压)及分级、血脂浓度、吸烟史、冠心病家族史、胸痛表现、特殊用药(他汀类药物和β受体阻断药及硝酸酯类)、左心房内径、左心室舒张末期直径、LVEF等临床资料比较,差异均无明显统计学意义(P>0.05),详见表1和表2。
2.2 QFR 与QCA 对心肌缺血相关LVDD 诊断效能比较
首先比较QFR 与FFR 结果一致性,以0.8 为QFR 与FFR 诊断界值,计算本研究中QFR 与FFR的Cohen′s kappa 值为0.616,其与0 差异具有统计学意义(P<0.001),提示QFR 与FFR 具有较强的一致性。以FFR 作为参考标准,QFR 的诊断效能均明显高于QCA,其中准确度、敏感度、特异度、阳性预测值及阴性预测值比较,差异均有统计学意义(P<0.01),见表3。QFR 与QCA 的阳性似然比分别为8.721vs.1.577(n=100),阴性似然比分别为0.274vs.0.761(n=100)。QFR 与QCA 诊断心肌缺血的ROC 的曲线下面积分别为0.94(95%CI:0.88~0.98)和0.67(95%CI:0.58~0.76)(Z=5.167,P<0.0001),见图1。
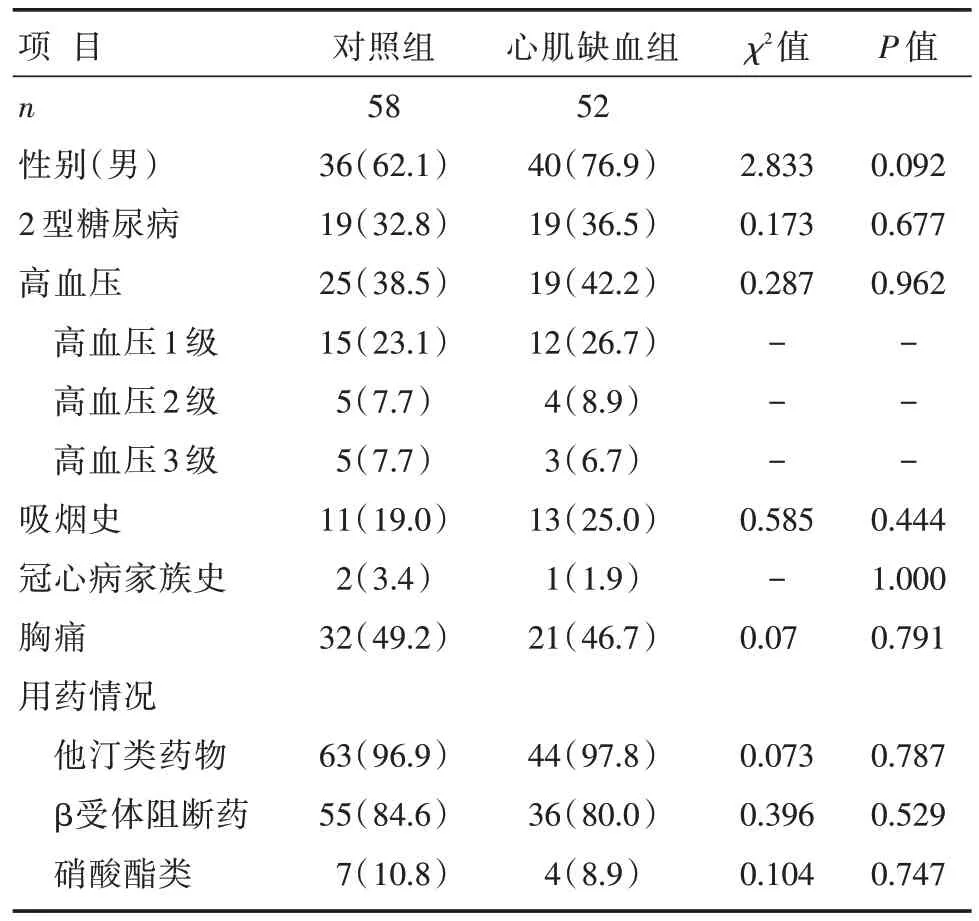
表1 两组患者的计数基线资料比较 [n(%)]
表2 两组患者的计量基线资料比较 []
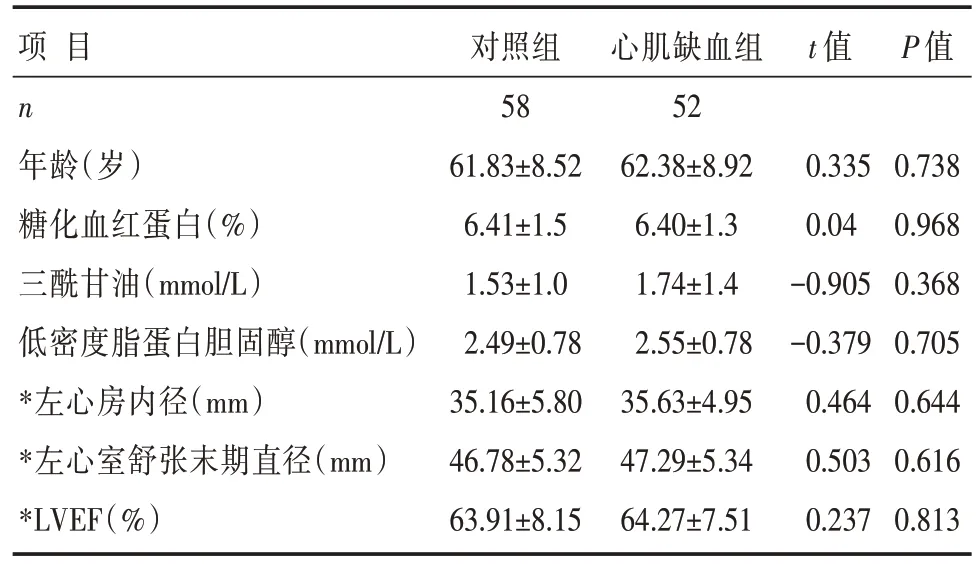
表2 两组患者的计量基线资料比较 []
注:* 数据来自冠状动脉造影术同期超声心动图资料
3 讨论
LVDD是临床工作中十分常见但容易被忽视的疾病,在成年人人群中的患病率为20%~30%[6]。研究显示,即使在控制了年龄、性别、射血分数、并发症因素之后,LVDD 仍与HFpEF 发生有很大关系,且对全因死亡有独立预测价值[7]。年龄、冠心病、心血管并发症及糖尿病是LVDD 发生的独立危险因素。研究显示,微循环障碍、冠状动脉钙化是LVDD 发生的重要机制[8-9]。Ren 等[10]观察了693 例心脏收缩功能正常的冠心病患者,34%的患者有不同程度的LVDD,且中度到重度LVDD 与心力衰竭住院事件和心脏病死亡有很强的相关性。因此,LVDD 是提示早期心肌缺血的重要标志,而改善心肌血运是治疗LVDD、延缓心功能不全进展的重要手段。临床中针对LVDD 患者往往只处理高血压、糖尿病等明确的危险因素,而由于诊断工具能力有限,无法早期识别心肌缺血相关性LVDD 并及时启动冠心病二级预防治疗。

表3 QFR≤0.8 和QCA 直径狭窄≥50%与FFR≤0.8 的诊断性能比较
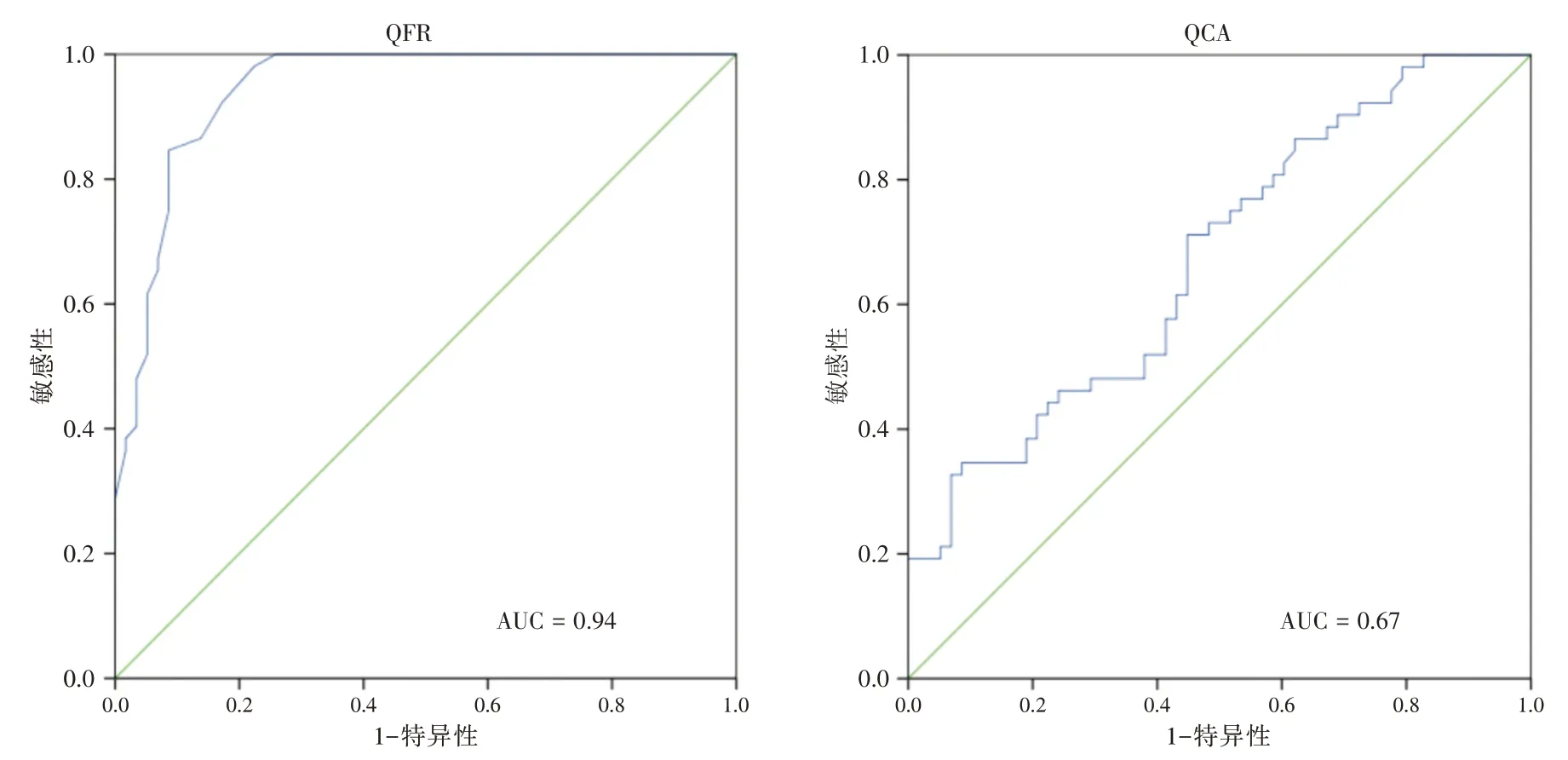
图2 QFR 及QCA 的ROC 图(以FFR 作为参考标准,FFR≤0.80、QFR≤0.80 以及QCA 直径狭窄率≥50%诊断为心肌缺血;QFR 与QCA诊断心肌缺血的ROC 曲线下面积分别是0.94 和0.67,P<0.0001)
冠状动脉造影能清晰显示冠状动脉树,是目前评估冠状动脉解剖学狭窄程度的“金标准”,除目测法以外,QCA 分析是目前常用的客观评估冠状动脉解剖狭窄程度的指标。但是越来越多的研究表明,冠状动脉解剖学狭窄程度与功能学狭窄程度并不一致,其功能学评估更能敏感地反映心肌缺血的程度,FFR 能通过压力导丝测定病变两端压力的变化反映缺血程度,是当前评估冠状动脉功能学狭窄及指导血运重建的“金标准”[11-13]。QFR 是近年来我国研发的基于3D-QCA 的无导丝FFR 技术,通过两幅血管造影图像及对比度流速计算“FFR”值,与FFR 比较,QFR 无需导丝及血管扩张药物、时间成本低、价廉、操作方便,且其准确性得到了大规模临床研究的验证,是目前有望替代FFR 的新技术[14-15]。
对于怀疑冠心病的LVDD 患者,及时确诊并进行血运重建等治疗与患者的预后密切相关[16-18]。本研究证实患者行冠状动脉造影检查后,传统的QCA 分析诊断心肌缺血的敏感度仅有46.2%,特异度为70.7%,对于LVDD 患者是否合并心肌缺血诊断能力有限,容易漏诊、误诊,延误诊疗。QFR操作简单、花费低、时间成本低,且不需压力导丝及血管扩张药物,其敏感度能达到76.4%,特异度高达91.4%,在临床上可以较QCA 更为准确、及时地诊断心肌缺血相关LVDD,以便指导临床更早进行干预,从而降低心肌缺血相关LVDD 患者发生心肌梗死、HFpEF 等危险心脏事件的发生风险,改善患者预后[19-20]。
本研究对QFR 用于评估心肌缺血相关LVDD的可行性进行了分析,由于入选样本量偏少,混杂因素较多、病变数目相对单一,且为回顾性分析研究,期待大规模样本的随机双盲对照研究进一步明确。
