急性下消化道出血的临床特征及严重LGIB 的危险因素
2021-03-05张琼侠张雯甘惠中
张琼侠,张雯,甘惠中
(安徽医科大学第三附属医院(合肥市第一人民医院消化内科),安徽 合肥 230022)
0 引言
急性下消化道出血Acute lower gastrointestinal bleeding (LGIB)是一种临床常见疾病,发病率逐年增加[1]。LGIB 与上消化道出血不同,因为虽然LGIB 通常具有自限性,80-85%的患者可自愈[2],但病情危重时可出现不同程度的发热、贫血、低血容量休克甚至死亡[3,4]。因此,早期筛选出危重患者并进行及时有效的治疗对患者预后非常重要。日本相关研究通过基于8 个因素开发并验证了严重LGIB 风险评分系统,有助于临床早期干预和决策[5]。国内的指南中尚未制定急性下消化道出血进行危险分级评估标准。本文通过回顾性分析我院收治的195 例急性LGIB 病例,分析其病因并筛选出与疾病严重程度相关性较高的危险因素并指导临床诊治。
1 材料与方法
1.1 一般资料及纳入标准
一般资料:选取2016 年1 月至2020 年6 月合肥市第一人民医院195 例急性下消化道出血患者作为研究对象。所有患者均接受了结肠镜检查确诊为下消化道出血。
纳入标准:病史≤3 天,主诉便血,临床表现为鲜红色血便、黑便、暗红色血便、脓血便、便后滴血;经结肠镜确诊为急性下消化道出血;年龄≥18 岁。排除标准:有呕血等,胃镜检查提示上消化道出血。
严重下消化道出血标准:按照Strate[6]对严重LGIB 的定义进行筛选,其中符合以下任意一项的即是严重的LGIB:(1) 24小时内持续出血;(2)至少需要输血2 个单位的红细胞;(3)在病情稳定24 小时后血细胞比容降低至少20%或再发出血;(4)出院1 周内再次出血入院。
我们按照上述定义,将研究对象分为两组:轻症出血组与严重出血组。其中轻度出血组154 例,严重出血组41 例。
1.2 观察指标
1.2.1 观察统计195 例急性下消化道出血患者年龄,性别,服药史,发病时间,晕厥史,发热,腹痛,排便习惯,体重变化,生命体征(血压,心率,体温和呼吸频率)等临床资料。比较分析上述因素与发生LGIB 的相关性;同时比较轻症组与严重组之间的上述指标差异。
1.2.2 通过直肠指检、结肠镜、实验室检查明确发病原因及明确治疗后病灶的恢复状况。
1.3 统计学方法
使用卡方检验进行分类变量分析,并使用t 检验分析连续变量。使用二元逻辑回归评估每个风险因子与严重LGIB之间的关系作为结果。将具有P<0.1 的单变量显性的风险因子纳入多变量分析。
2 结果
2.1 患者的基本资料
我院2016 年1 月至2020 年6 月住院共195 名患者诊断急性LGIB 被纳入研究。其中男性110 例(56.41%),女性85例(43.59%),非老年组62 例(31.79%),老年组133 例(68.21%),轻度出血组154 例(78.97%),严重出血组例41(21.03%)。患者的基本信息在(表1)中列举。
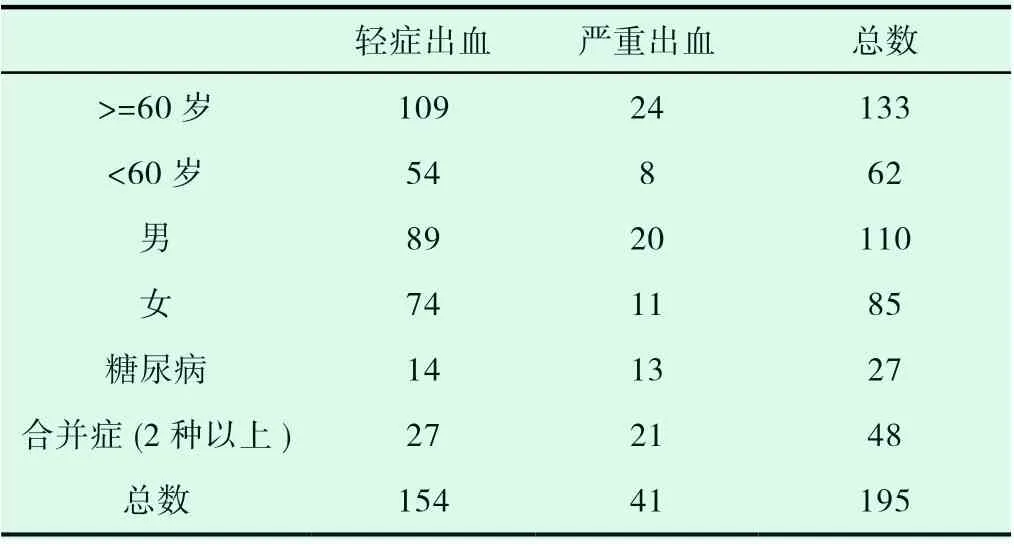
表1 患者的基本资料
2.2 出血病因
轻症出血以缺血性肠炎、肿瘤和痔疮多见,分别占轻症出血患者的38.31%、11.04%、4.88%;严重出血常见于肿瘤病人,约占严重出血患者的70.73%,其次为憩室出血,约占7.32%。具体见表2。
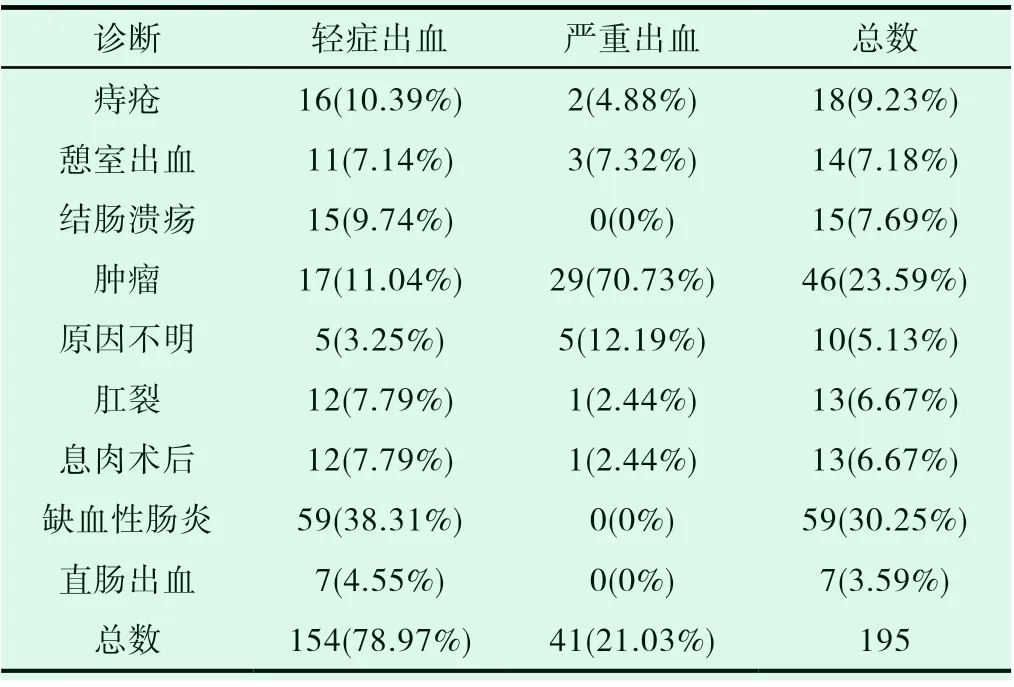
表2 下消化道出血的原因[n(%)]
2.3 严重下消化道出血的危险因素分析
纳入严重LGIB 组的共41 名患者。26 例患者持续出血,22 例血细胞比容降低至少20%,29 例患者至少输2 单位血细胞。6 名患者有再次出血。严重LGIB 患者的平均住院时间11.2 天,而轻症LGIB 的时间为5.3 天。单因素分析(表3)显示严重出血的患者高危因素包括年龄超过60 岁、有2 种以上的合并症、长期服用阿司匹林病史。严重LGIB 的患者通常有血液动力学不稳定,其临床表现通常为晕厥。严重LGIB 组的平均血红蛋白(Hb)和白蛋白显着低于普通组(P<0.01)。我们通过二元逻辑回归分析(表5)确定了严重LGIB 的四个独立因素。这些包括服用阿司匹林病史,晕厥病史,血红蛋白低于100 mg / dl 和白蛋白低于38 g / l。
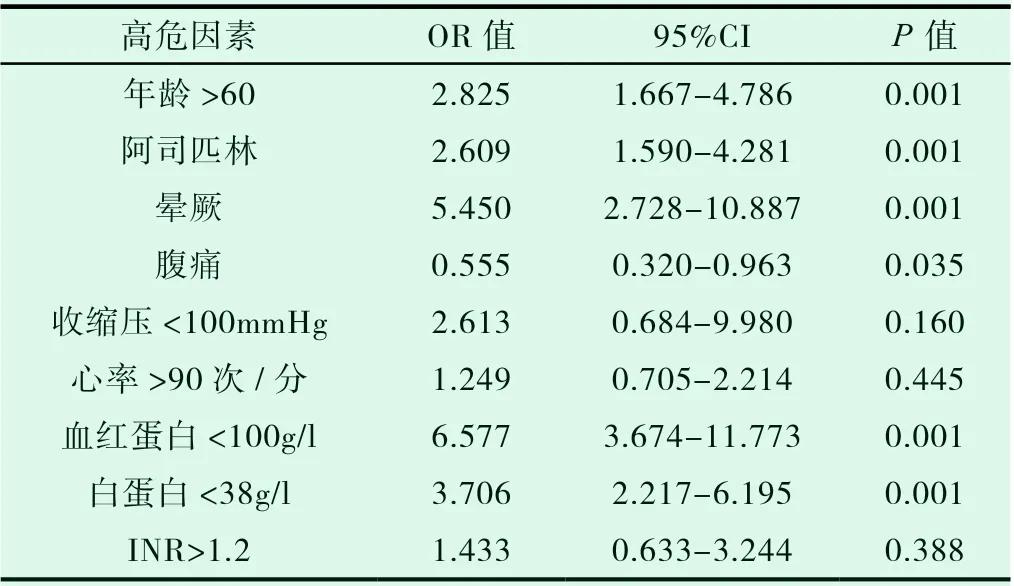
表3 单因素分析严重下消化道出血的危险因素
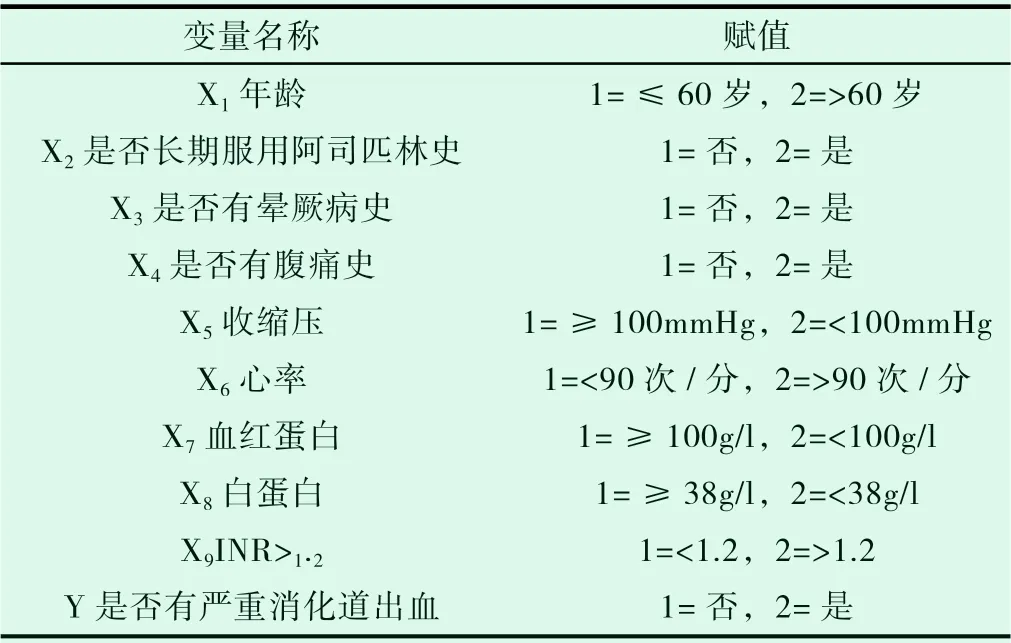
表4 变量赋值表
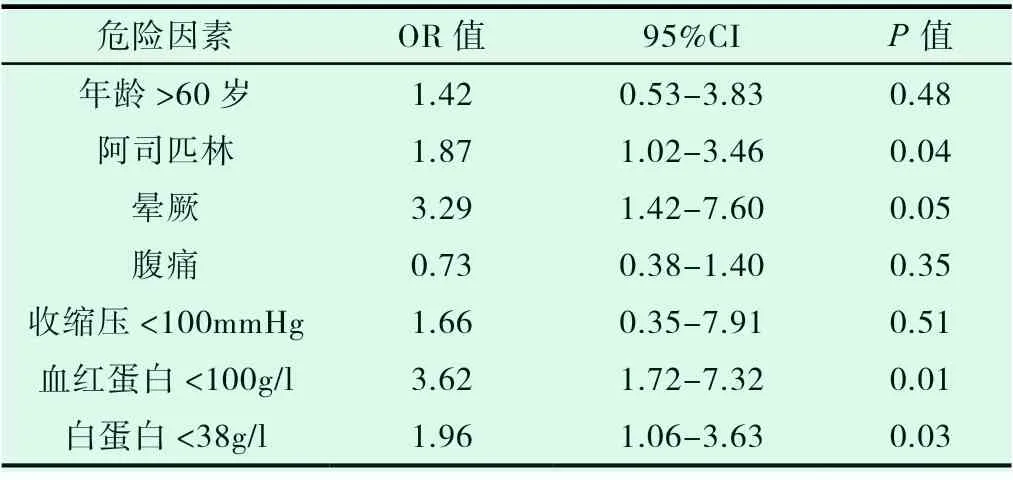
表5 多元分析严重下消化道出血的危险因素
3 讨论
急性下消化道出血系消化内科常见的急症,短期出血量可达800 mL 以上,严重LGIB 可危及患者生命,老年人的发病率甚至会超过上消化道出,因下消化道与上消化道相比其部位更长,其出血则临床表现可能有滞后性,增加诊治难度[7]。许多研究试图分析胃肠出血的危险因素,但大部分研究内容结果各异。如何认定严重LGIB 并未有公认的明确标准,目前大部分研究选择Strate[6]对严重LGIB 的定义标准。另外,Kollef 开发的“BLEED”标准认为再出血是病情不稳定的标志,是转入ICU 的指征[8]。BLEED 标准包括:1)活动性出血;2)低收缩压;3)凝血酶原时间延长;4)神志改变;5)严重的合并症。也有国外相关研究提出LGIB 的危险因素包括:男性,伴有合并症,结肠憩室病和动脉血管畸形的病史,直立性低血压,鲜红色的直肠出血,收缩压<100mmHg,红细胞压积偏低(<30%)和高肌酐(> 130 mmol / L)[9]。
本研究通过回顾性分析我院严重LGIB 患者的临床特征,初步筛选了严重LGIB 的四个独立危险因素,即服用阿司匹林,晕厥病史,血红蛋白低于100mg/dl 和白蛋白低于38g/l。 血流动力学不稳定提示出血严重,而血流动力学不稳定的临床表现之一晕厥,可能是严重LGIB 的更好的临床预测因素。研究表明使用干扰凝血药物将增加严重LGIB 风险[10]。有学者[10,11]认为抗血小板药物会增加胃肠道出血的风险;其中下消化道出血的风险大约是上消化道出血的三倍。一项对于消化道出血患者的短期回顾性研究显示,患者出血后持续服用阿司匹林,5 年内胃肠道再出血的发生率明显升高(18.9%vs6.9%),但严重心血管事件发生率和死亡率偏低[12]。我们的资料中长期服用阿司匹林的出血患者风险比普通人高2.6 倍。白蛋白是全身炎症反应的常见标志物。一项大规模前瞻性研究表明低白蛋白水平与住院患者的死亡风险相关[13]。我们的结果显示低蛋白血症是下消化道出血的危险因素。总之,我们的研究结果与上述研究的危险因素具有一定一致性。
我们的研究发现,轻症出血患者以缺血性肠炎、肿瘤和痔疮多见,分别占轻症出血患者的38.31%、11.04%、4.88%;重症出血常见于肿瘤病人,约占重症出血患者的70.73%,其次为憩室出血。在西方国家,急性LGIB 的原因:憩室出血占30%-65%,缺血性结肠炎5%-20%,痔疮5%-20%,结直肠息肉/肿瘤2%-15%,此外还有息肉切除后出血、炎症性肠病、感染性结肠炎、直肠溃疡、结直肠静脉曲张、放疗性直肠炎等原因;而在热带国家,结肠息肉/肿瘤(29%-53%)和结肠炎(23%-38%)是常见病因,憩室出血较少见(4%-19%)[9]。
本研究中患者均行结肠镜检查。对于结肠镜检查时机选择,相关研究建议在出血后24 小时内使用4-6 L 聚乙二醇快速结肠清洗后进行,以优化出血源的检测和处理。尽管多项研究数据混杂,但早期结肠镜检查与更高的出血灶检测和治疗干预有关[14]。结肠镜检查提供了诊断和治疗的潜力,但其对肠道准备要求较高。有学者[15]认为肠道清洁度对于急诊肠镜的诊断率影响显著,一定程度限制了在危重LGIB 患者中的应用。选择合适的时机行结肠镜检查显得尤为重要,Jensen[16]等人证实,患者入院后12 小时内接受急诊结肠镜检查可降低再出血率和手术率,但如果结肠镜检查后持续出血则需要手术治疗。在LGIB 的一项随机对照试验中,Green[17]证实,LGIB 患者在再次出血率,输血率,死亡率或住院时间上,急诊肠镜检查组(12 小时内结肠镜检查)与普通组(74 小时内结肠镜检查)相比无明显差异。同样,另一项随机对照试验发现12 小时内结肠镜检查与36 至60 小时内结肠镜检查结果无差异[18]。此外,美国放射学会建议如果有时间进行肠道准备结肠镜检查应作为血流动力学稳定患者的初选。血管动力学不稳定伴大量出血的患者初选血管造影[9,19]。血管造影检查可以对任何消化道出血部位进行诊断和治疗,适用于因循环不稳定无法性结肠镜检查的活动性出血患者。但其诊断依赖持续快速的活动性出血点,通常风险要高于结肠镜检查,而且诊断通常须通过结肠镜检查确认。因此我们认为,结肠镜检查虽为必须,但具体时机选择则需视临床具体情况而定。
综上所述,本研究通过分析急性LGIB 患者临床特征并筛选重症患者危险因素,以期协助临床早期筛选出重症出血患者,制定合理的治疗方案,但由于单中心回顾性研究样本量少,存在一定局限性,故需通过大样本、多中心的前瞻性研究,予以证实。
