阿帕替尼治疗复发性和进展性韧带样纤维瘤的疗效与安全性分析*
2021-03-02方建国王一天郑传禧闵理罗翼周勇段宏屠重棋
方建国 王一天 郑传禧 闵理 罗翼 周勇 段宏 屠重棋
韧带样纤维瘤(desmoid fibromatosis,DF)是一种罕见的、起源于肌肉、筋膜或腱膜组织的纤维母细胞肿瘤,以浸润性生长和局部复发率高为特征,但无转移倾向[1]。DF发生部位广泛,主要分布于腹壁、腹腔肠系膜和四肢[2]。四肢部位的DF 更易局部复发,其治疗对于外科医生来说是一个挑战[3]。
美国国家综合癌症网络(NCCN)指南提出,对于无症状的患者可采取观察的手段,而对于有症状或进展的患者,手术切除仍然是主要的治疗方法,而放疗或全身药物治疗则为辅助治疗[4-5]。手术治疗时,边缘切除常难以达到镜下的阴性切缘,而广泛切除又对肢体造成不同程度的损害,多个中心报道的DF术后复发率为20%~80%[6-9]。对于不可切除、手术切缘阳性以及手术复发的患者,放疗可作为一种治疗手段[10-12]。虽然联合术后放疗可降低术后的局部复发率,但放疗易造成局部切口愈合不良、放疗后肿瘤恶变和周边脏器组织相关的并发症[10]。
对于局部治疗无效或无法局部治疗的有症状或进展的DF 患者,需考虑全身治疗。全身治疗包括非甾体抗炎药物[13]、化疗(阿霉素、甲氨蝶呤、长春花碱)[14]、抗雌激素药物(他莫昔芬、托瑞米芬)[15-17]、生物制剂(低剂量干扰素)[18]及靶向治疗等[19-23]。抗雌激素药物治疗报道病例较少,仅有部分患者达到临床症状的缓解,而无影像学改变[15-17,24]。传统的阿霉素、甲氨蝶呤以及长春花碱等药物的联合化疗有一定疗效,但各中心的化疗效果差异较大,且化疗对于育龄期女性有累积的心脏毒性,潜在影响患者生育功能[25-27]。
酪氨酸激酶抑制剂(tyrosine kinase inhibitor,TKI)作为一种常用的多靶点靶向药物,包括伊马替尼、索拉非尼及帕唑帕尼,目前已应用于不可切除、进展或复发性DF 的治疗中[3,21-23]。阿帕替尼是中国自主研发的多靶点小分子抗血管生成靶向药物,作用靶点有血管内皮细胞生长因子受体2(vascular en⁃dothelial growth factor receptor 2,VEGFR-2)、血小板衍生生长因子受体(platelet-derived growth factor re⁃ceptor β,PDGFRβ)、SRC、c-KIT 和RET,但高度选择性抑制VEGFR-2激酶活性,阻断肿瘤血管生长,从而抑制肿瘤生长[28]。有报道阿帕替尼治疗肢体软组织肉瘤获得一定疗效[29-30]。本研究对服用阿帕替尼的DF患者进行随访,评估其疗效和不良反应。
1 资料与方法
1.1 一般资料
收集2017年10月至2020年9月四川大学华西医院收治的37例DF患者临床资料,其中男性9例,女性28 例,年龄9~62 岁,中位年龄30.1 岁。8 例为初次治疗,29 例为既往接受治疗后发生肿瘤复发或进展。发生部位均位于四肢、肢带或臀部。本组所有患者均经活检病理证实为DF。
纳入标准:1)病理切片于本院病理科确诊为DF;2)肿瘤位于四肢、肢带、臀部或盆腔;3)多次治疗后复发或进展的患者或未接受治疗发生进展;4)瘤体包绕神经血管不可切除,或者无法接受功能严重受损者;5)肝肾功、血常规、甲状腺、血脂基本正常;6)临床资料完整者。
排除标准:1)病理诊断未明确;2)无法耐受药物不良反应;3)无法按规律服药;4)临床资料不完整;5)失访。
本研究经本院伦理委员会批准,所有患者在签署知情同意书之前了解阿帕替尼药物治疗的不良反应。
1.2 方法
1.2.1 治疗方法 所有患者阿帕替尼的起始剂量均为250 mg/d,4 周为1 个疗程。连续服用直至疾病快速进展或出现不可耐受的不良反应。若不良反应达到3 级及以上时暂停用药,予以相关对症治疗,待恢复至2级以下后,下调剂量(由250 mg/d调至125 mg/d)继续给药;若2周后仍未恢复,则永久停药。
1.2.2 肿瘤学评价 患者自服药后每3 个月进行患侧肢体的MRI 检查,依据实体瘤疗效评价标准(RE⁃CIST 1.1)[31]评估患者的近期疗效:完全缓解(com⁃plete response,CR)为所有目标病灶消失;部分缓解(partial response,PR)为基线病灶最大径总和缩小≥30%;疾病进展(progressive disease,PD)为基线病灶最大径总和增加≥20%或出现新病灶;病情稳定(sta⁃ble disease,SD)为基线病灶最大径总和有缩小但未PR 或有增加但未达PD。客观有效率(objective re⁃sponse rate,ORR)=(CR+PR)例数/总例数×100%,疾病控制率(disease control rate,DCR)=(CR+PR+SD)例数/总例数×100%。无进展生存期(progression-free survival,PFS)为确诊日期至疾病进展日期或最后一次随访日期的时间,总生存期(overall survival,OS)为确诊日期至死亡或失访的时间。
1.2.3 功能评价 通常情况肢体部位的DF均会影响邻近关节的活动度。研究记录患者受累关节治疗前后的关节活动度(rang of motion,ROM)。采用视觉模拟评分(visual analog scale,VAS)法评估患者治疗前后的疼痛程度,分值区间为0~10分,分值越低,代表疼痛程度越轻。
使用上肢功能评定表(disabilities of the arm,shoulder and hand,DASH)[32]评估上肢功能,评估得分从0(无症状,功能全面)至100(最严重的残疾)。采用髋关节Harris 评分评价患者治疗前后的髋关节功能,通过疼痛、功能、畸形和关节活动4 个方面评价,满分100分,≥90分为优,80~89分为良,70~79分为尚可,<70 分为差。使用美国特种外科医院(HSS)评分[33]评价患者的膝关节功能,总分为100 分,通过疼痛、功能、活动度、肌力、屈曲畸形5 个方面评价膝关节功能,分值越高表明膝关节功能越好。
1.2.4 安全性评价标准 观察并记录患者用药过程中出现的不良反应,根据国立癌症研究所通用不良事件通用术语标准(NCICTC)4.0 版本将药物不良反应分为1~4级。
1.3 统计学分析
采用SPSS 26.0 软件进行统计学分析,计量资料以x±s表示,采用Kaplan-Meier法绘制PFS和OS生存曲线。所有患者治疗前后受累关节的关节活动度(包括屈、伸、外展、内收、外旋、内旋等方面各自进行比较)及功能评分比较采用配对t检验(正态分布资料)或Wilcoxon 符号秩和检验(非正态分布资料),以P<0.05为差异具有统计学意义。
2 结果
2.1 一般情况
37例DF患者平均年龄为30.2岁。原发部位:腋窝2例,肩部2例,肩胛区3例,上臂3例,前臂4例,肘部1例,手指2例,大腿8例,小腿1例,足部1例,腘窝1例,髋部3例,臀部5例,盆腔1例。29例患者(78.4%)有手术史;5例(13.5%)既往接受甲氨蝶呤、长春花碱、阿霉素等化疗,2例患者曾接受放疗(5.4%)。经评估肿瘤可切除25例(67.6%),其中既往治疗后复发20例(54.1%),既往未接受治疗发生进展5例(13.5%);肿瘤不可切除的患者有12 例(32.4%),其中既往治疗后复发9 例(24.3%),既往未接受治疗发生进展3例(8.1%),见表1。
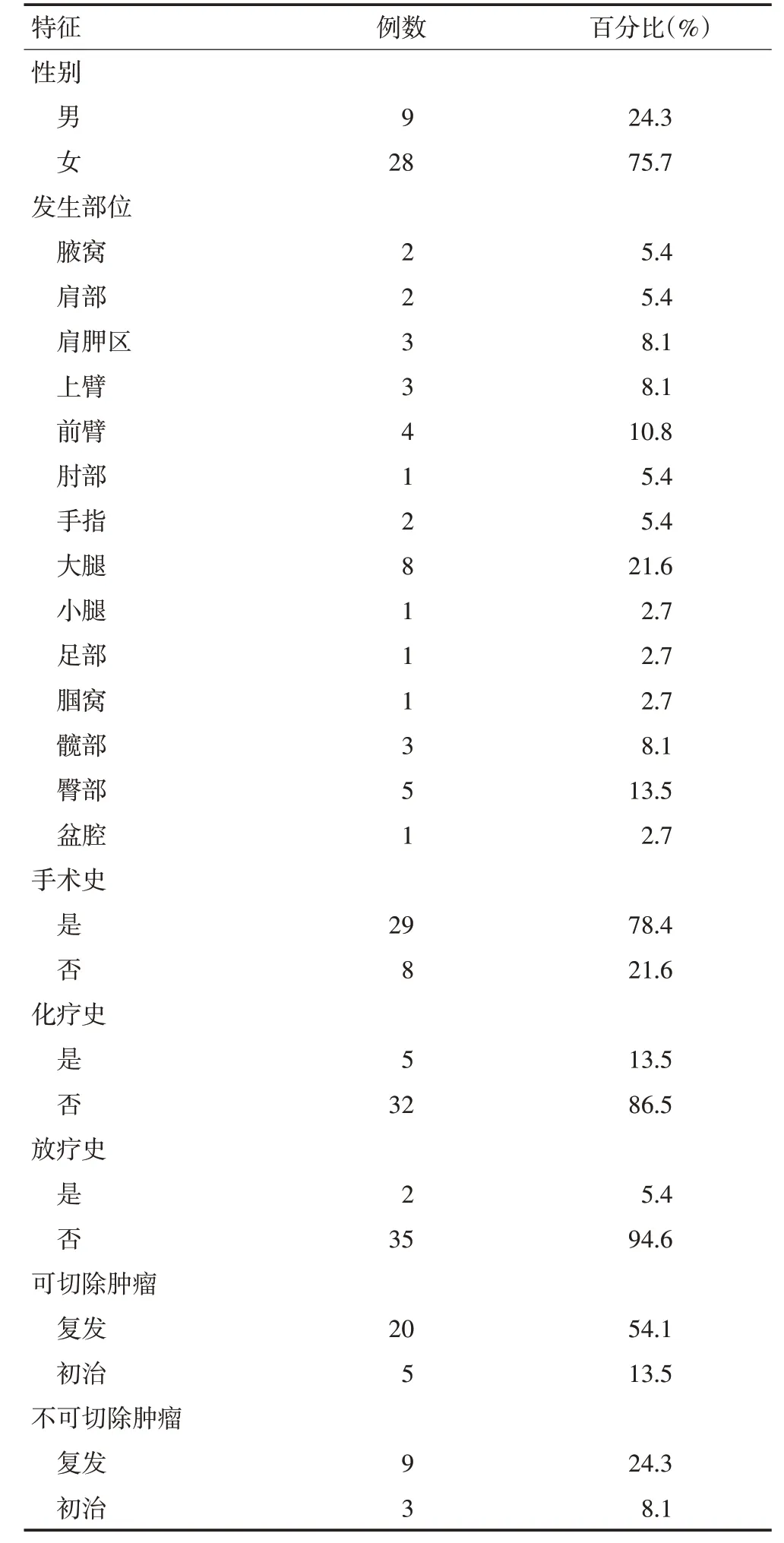
表1 患者基线资料
2.2 肿瘤学疗效
截至2020年8月,所有患者的平均服药时间为(18.7±10.3)个月。37 例患者中无CR,17 例PR(45.9%),18 例SD(48.6%),2 例PD(5.4%),ORR 为45.9%,DCR为94.6%。1年PFS率为94.6%,中位PFS和OS均未达到(图1,2)。2例PD患者接受了安罗替尼(8 mg,qd)靶向治疗,目前仍在随访中。
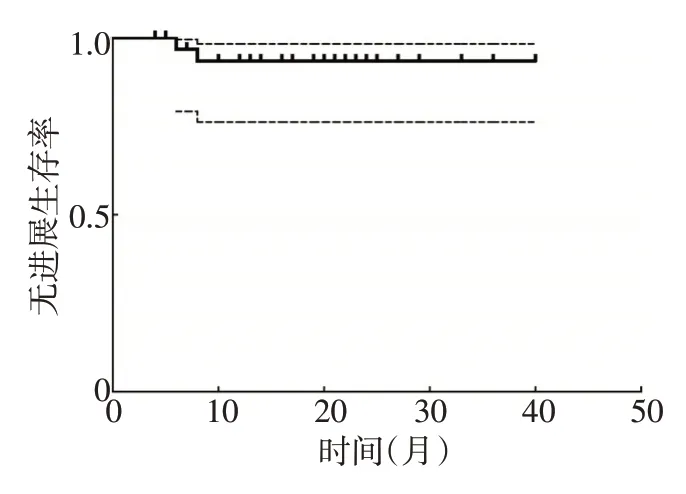
图1 患者的无进展生存曲线
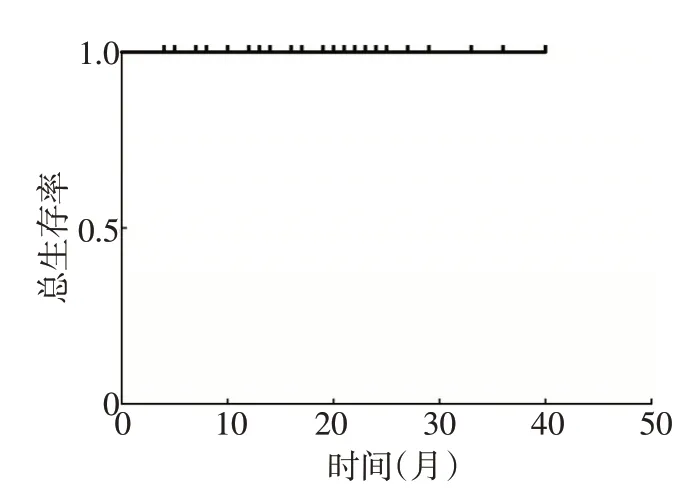
图2 患者的总生存曲线
2.3 功能结果分析
除2 例PD 患者之外,所有患者在治疗后各个关节活动度较治疗前有改善,差异有统计学意义(P<0.05,表2)。对于所有发生在上肢的DF患者,治疗后上肢各个关节屈曲度数为87.5°±28.2°,后伸度数为65.3°±40.7°,外展度数为53.3°±20.5°,内收度数为40.0°±20.8°,外旋度数为45.0°±13.9°,内旋度数为56.7°±17.0°,较治疗前均有统计学差异(均P<0.05)。另外,上肢DF 的VAS 评分为2.3±1.4,疼痛症状明显缓解,差异有统计学意义(P<0.05)。上肢DF 治疗后的DASH评分为21.8±12.3,较治疗前差异有统计学意义(P<0.05)。对于DF发生于髋部和大腿的患者治疗后的屈髋度数为111.3°±16.2°,后伸度数为11.9°±4.3°,外展度数为33.1°±8.5°,内收度数为27.9°±4.3°,较治疗前均具有统计学意义(均P<0.05)。所有髋关节DF患者治疗后VAS评分为2.0±1.6,较治疗前差异有统计学意义(P<0.05)。对于本研究纳入的2 例膝关节受累DF,治疗后膝关节的屈伸度数分别为120°(治疗前为80°)和100°(治疗前为70°),VAS 评分分别为3 分(治疗前为5 分)和2 分(治疗前为7 分)。HSS分别为68分(治疗前为44分)和57分(治疗前为38分),见表3。
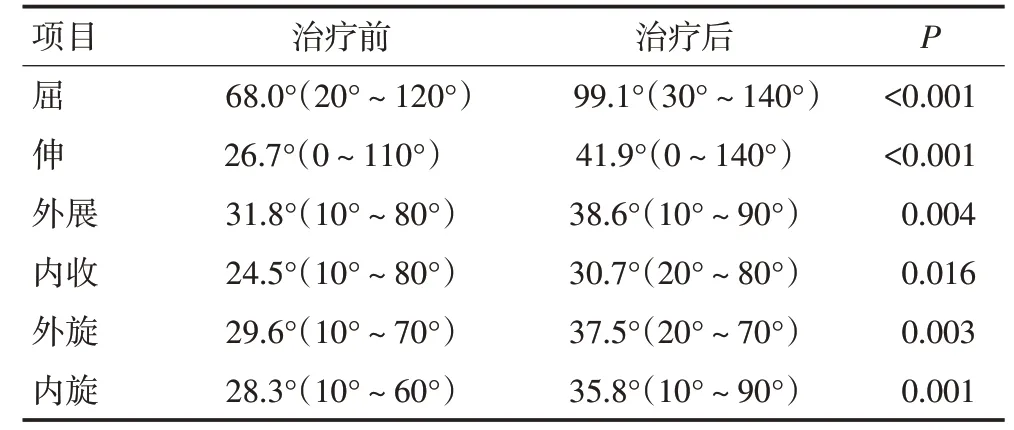
表2 治疗前后的关节活动度对比
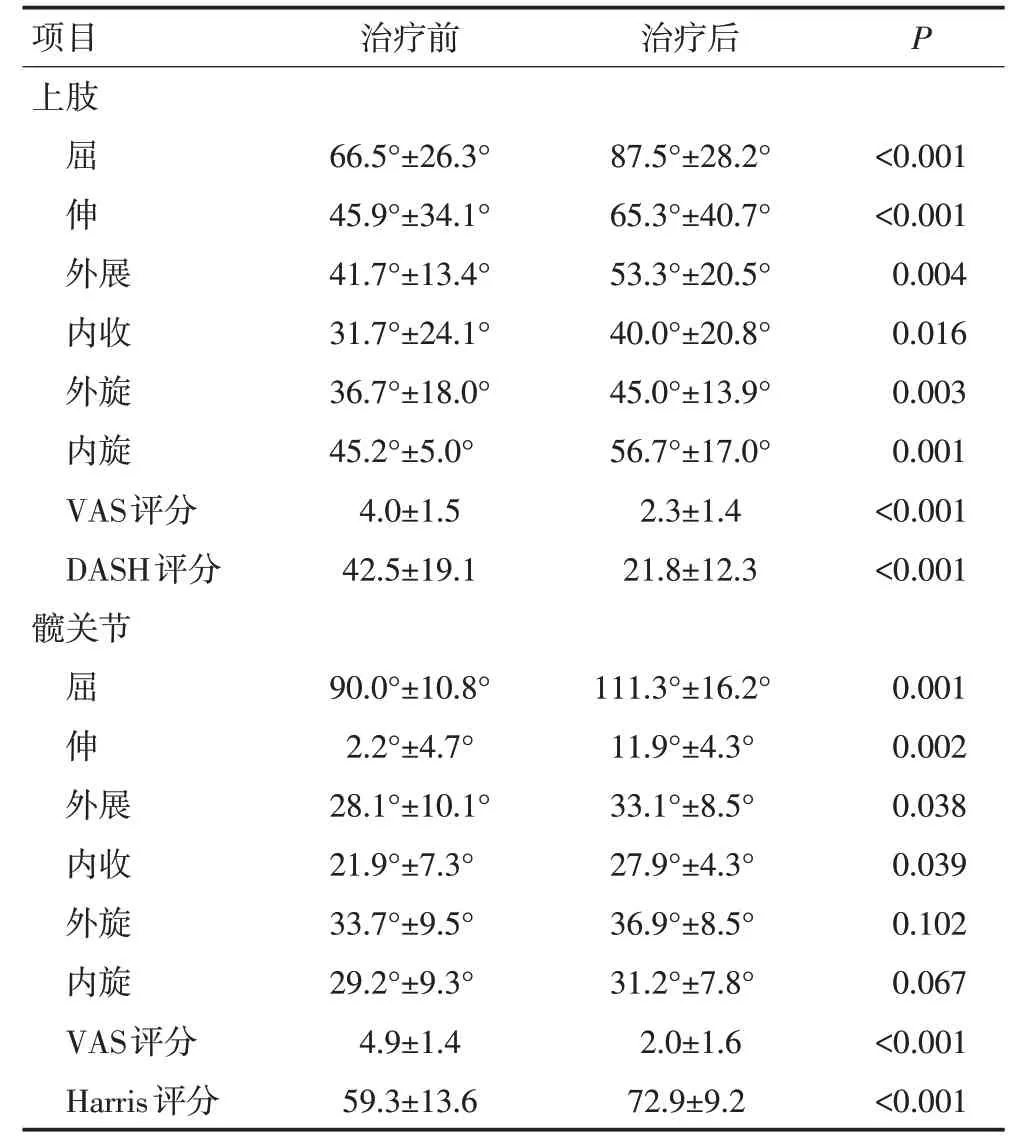
表3 治疗前后四肢功能的对比
2.4 不良反应
最常见的不良反应为手足综合征14例(37.8%),其中1 级9 例(24.3%),2 级5 例(13.5%),3~4 级2 例(5.4%)。2 例3~4 级患者因足部皮肤蜕皮严重影响行走,经药物减量(减至125 mg/d)及对症治疗后症状明显缓解。其次为胃肠道反应11 例(29.7%),1 级8例(21.6%),2级3例(8.1%)。月经紊乱8例(21.6%),1 级7 例(18.9%),2 级1 例(2.7%)。口腔溃疡7 例(18.9%),1级5例(13.5%),2级1例(2.7%),3~4级1例(2.7%)。此例3~4级患者因严重口腔溃疡无法进食,最终因无法耐受而终止治疗。乏力6例(16.2%),均为1 级。其他不良反应包括腹泻、伤口愈合不良、蛋白尿、高血压及白细胞减少等,均为1级或2级,经服用益生菌、反复清洁换药、口服降压药等对症处理均得到有效控制,无需调整剂量(表4)。
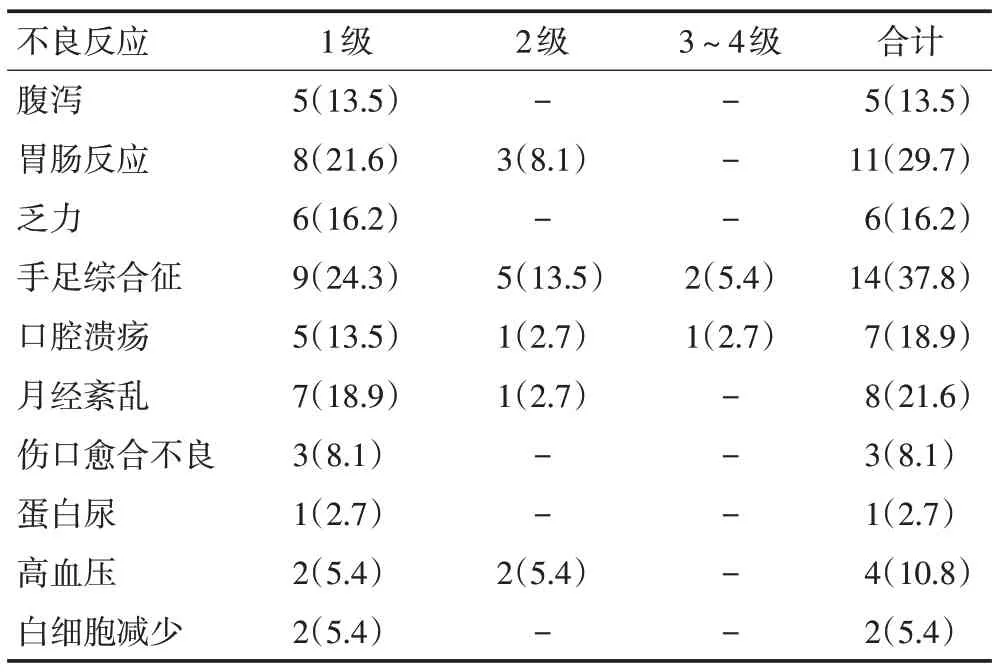
表4 阿帕替尼治疗后的不良反应 例(%)
3 讨论
DF是一种罕见的、局部侵袭性强、易发生复发的交界性肿瘤。目前对于复发性和进展性DF,国内尚无标准的治疗方案。近年来,随着对DF 发病机制的深入研究,越多越多的靶向药物被应用于DF,并显示出一定的疗效。阿帕替尼的主要作用机制是高度选择性地抑制VEGFR-2 酪氨酸激酶活性,竞争性结合该受体胞内酪氨酸ATP结合位点,阻断VEGF结合后的信号转导,从而发挥抗肿瘤效应[28]。
Penel 等[20]报道一项伊马替尼的Ⅱ期临床试验,通过CT/MRI检查盲法评估35例进展或复发性DF中的疗效,结果为1例(2.8%)CR,28例(80.0%)SD,3例(8.6%)PR 和3 例(8.6%)PD。中位PFS 为25 个月,ORR和DCR分别为11.4%和91.4%。Chugh等[19]的研究表明,51 例DF 患者中,伊马替尼获得了43 例SD(84%),5 例PD(9.8%),其中3 例患者未评估。Gounder等[22]进行一项双盲Ⅲ期临床试验,评估了87例进展、有症状或复发性DF 患者接受索拉非尼(50例)或安慰剂(37例)的疗效。在索拉非尼组中,CR 1例,PR 15 例。ORR 和DCR 分别为33%和91.4%。本研究结果显示37例DF患者的ORR为45.9%,DCR为94.6%,1年PFS率为94.6%,与Gounder等[22]的报道基本相符,提示阿帕替尼在DF 治疗中有着确切的疗效。伊马替尼相关分子实验表明,伊马替尼很可能通过抑制PDGFRβ 受体发挥疗效[19,34]。而阿帕替尼的作用靶点中不仅包含PDGFRβ受体,其作用靶点较伊马替尼更为广泛[28]。因此,本研究推测此为采用阿帕替尼治疗较伊马替尼PR患者更多、ORR更高的原因。
本研究首次提出将患者的肢体功能评价纳入DF的整体疗效评价中,一方面对受累关节治疗前后的ROM以及VAS评分进行统计学对比,另一方面是分别对上肢关节(肩关节、肘关节及腕关节)、髋关节和膝关节的功能进行量化评分[35-36]。研究发现上肢DF治疗后的DASH评分明显优于治疗前(21.8vs.42.5,P<0.05)。大腿及髋部DF治疗后的Harris评分也从差转变为尚可(72.9vs.59.3)。上述结果分别与治疗前后上肢(4.0vs.2.25)以及大腿、髋部(4.9vs.2.0)的VAS评分改变趋势一致,提示患肢症状的改善与疼痛的缓解是相关的。本研究中,9例上肢关节受累的患者中有6例DASH评分有明显改善,7例髋关节受累的患者中有5例Harris评分等级由差提高至尚可,推测是由于DF周围分布着大量的胶原基质,而阿帕替尼主要作用于肿瘤实质细胞,虽然瘤体大小无明显变化,但肿瘤质地变软,因此改善了相应的肢体功能[37]。
在安全性方面,由于DF为交界性肿瘤,用药的目前主要是缓解患者临床症状和防止肿瘤进展,因此不同于其他恶性肿瘤,本研究将阿帕替尼的初始剂量定为250 mg/d,在尽量减少不良反应的同时保证疗效[38-39]。阿帕替尼相较于其他TKI 药物具有更短的半衰期(<10 h),因此不良反应发生率更低[28]。本研究中主要的不良反应为手足综合征,尽管其中2 例(5.4%)患者达3级不良反应,但通过暂时的停药和停药后减量均达到有效的控制。仅有1 例(2.7%)患者因口腔溃疡4 级无法耐受而停药。其他不良反应包括胃肠道反应、月经紊乱、口腔溃疡、腹泻、高血压、蛋白尿等。而在Penel等[20]开展的伊马替尼研究中,5例(12.5%)患者因伴有肌痛和肌溶解的瘙痒性皮炎、转氨酶升高等不良反应终止治疗。在先前索拉非尼的报道中,与索拉非尼相关的4级事件包括血小板减少症(2%)和贫血(2%),并且1 例患者死于与疾病相关的肠穿孔[22]。而在Szucs 等[23]的报道中,帕唑帕尼治疗中有1 例患者出现无法控制的不良反应(3 级高血压),导致早期治疗中断。上述研究表明阿帕替尼的不良反应较轻,患者可耐受,安全性良好,相对于其他TKI药物更易接受。
本研究尚存在着以下局限性:1)由于病例数量的限制,缺少对照研究;2)单中心研究,需进一步联合多中心临床试验;3)平均随访时间较短;4)阿帕替尼作为多靶点TKI,作用于DF 的具体机制需进一步探明。
综上所述,阿帕替尼对于进展性和复发DF 有一定的疗效,且不良反应较轻,多可耐受或通过药物控制,但由于本研究样本量小,尚需进一步大样本的随机对照研究进行验证。
