正交实验法探究乙醛与氢氧化铜演示实验的最适条件
2021-02-21周怡刘晓玲
周怡 刘晓玲
摘要:采用正交实验法探究乙醛与氢氧化铜演示实验的最适条件,对影响实验的氢氧化钠的量、硫酸铜的量、乙醛的量、水浴温度4个因素进行系统探究,確定了乙醛与氢氧化铜演示实验的最适条件。
关键词:正交试验;乙醛的检验;最适条件
文章编号:1008-0546( 2021)01-0085-03
中图分类号:G632.41
文献标识码:B
doi: 10.3969/j .issn.1008-0546.2021.01.024
一、研究背景
“人教版”普通高中课程标准实验教科书(选修5)《有机化学基础》中介绍了乙醛与氢氧化铜反应的实验“在试管中加入10%的氢氧化钠溶液2mL,滴人2%的硫酸铜溶液4-6滴,得到新制的氢氧化铜,振荡后加入乙醛溶液0.5mL加热,观察并记录实验现象。反应中产生砖红色氧化亚铜沉淀是判断该反应是否发生的重要现象,但在反应过程如果控制不好量的关系,就难以观察到红色的沉淀生长,甚至看不到红色沉淀。该反应在加热的过程中,溶液往往出现黄色的聚合物会干扰氧化亚铜的颜色观察。
教材中乙醛的体积给的是0.5mL,在乙醛的质量分数不确定的情况下,给出的氢氧化钠和硫酸铜的量的关系以及乙醛的量是否还有意义,有待商榷。大多数研究者[1-5]使用控制变量法探究乙醛、氢氧化钠、硫酸铜的最佳质量分数。却鲜有研究者通过正交实验法系统地探究乙醛与氢氧化钠、硫酸铜溶液反应的最佳反应条件。基于此,本实验利用正交实验法探究检验乙醛的最适条件,从而为一线教师在课堂演示实验时提高课堂教学效率提供最佳实验方案。
二、用正交实验法进行研究
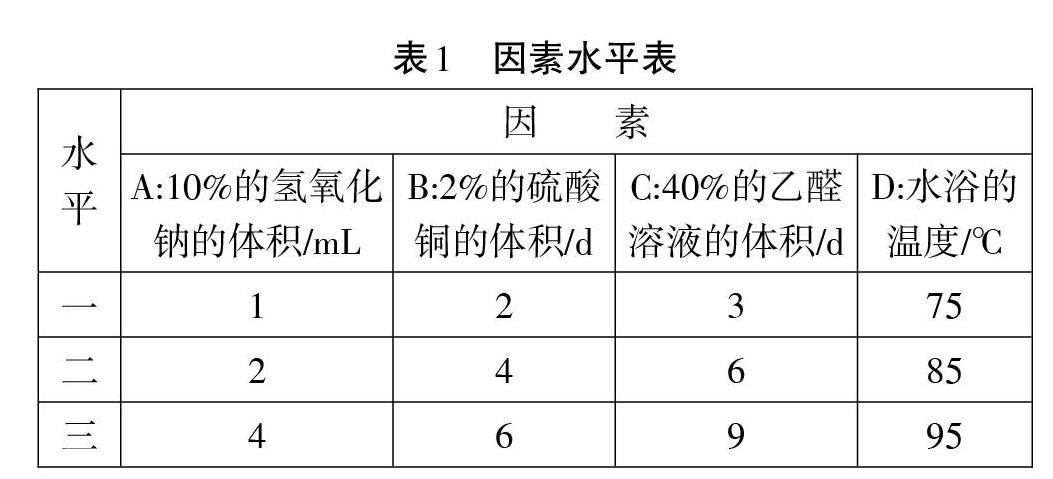
1.因素、水平的选取
根据实验反应原理,确定本实验的主要影响因素是乙醛的量、硫酸铜的量、氢氧化钠的量和反应条件。有研究者[6]将氢氧化钠溶液与硫酸铜溶液的体积保持不变,探究氢氧化钠和硫酸铜的最佳浓度。郭彦青[7]等用控制变量法,得出当氢氧化钠溶液与硫酸铜溶液的浓度过大或过小时,只要滴加合适的体积量,也可产生效果较好的砖红色沉淀,给了笔者启示:将氢氧化钠和硫酸铜的质量分数保持不变,即采用教材上质量分数为10%的氢氧化钠和2%的硫酸铜,改变二者的体积,这样省去了配制各种质量分数的溶液的繁琐过程。教材中给出的氢氧化钠的体积为2mL,为了节约药品、教师演示方便,以及实验效果明显。通过预实验,最终确定氢氧化钠的体积水平采用1mL、2mL、3mL;硫酸铜的体积水平分别为4滴、5滴、6滴;现行不同版本教材中加入乙醛的体积都为0.5mL,但却并没有指明乙醛的质量分数,通过查阅资料发现市售的乙醛的质量分数多为40%,按照教材的量进行实验发现即使乙醛的体积减少,也能观察到砖红色的沉淀,通过大量的预实验,发现用40%的乙醛进行实验,几滴就可以观察到砖红色的沉淀。最终确定40%的乙醛的滴数为3滴(d)、6滴(d)、9滴(d);通过查阅文献发现酒精灯直接加热,乙醛易挥发,乙醛量不足会导致高温下生成的Cu2O被空气氧化成CuO。部分Cu(OH)2受热分解产生黑色Cu0,最后溶液呈黑色或褐色[8]。陈伟霞,丁伟[9]研究了乙醛与氢氧化铜反应的加热条件,得出70℃是出现砖红色沉淀的临界点,温度越高,砖红色沉淀出现得越快,反应采用水浴加热的方式并控制温度在85℃-90℃范围内,能达到较好的实验效果。综合分析后,确定本实验的加热方式采用水浴加热,温度水平分别为75℃,85℃,95℃。根据以上分析确定因素与水平,如表1所示。
2.实验步骤:
(1)配制10%的氢氧化钠溶液、2%的硫酸铜溶液备用,准备干净的小试管,并贴好标签。
(2)按照实验方案,往对应的试管中加入10%的氢氧化钠溶液,再滴人2%的硫酸铜溶液,振荡后,再加入40%乙醛溶液,将试管放于相应温度的恒温水浴锅中加热。
(3)观察实验过程中的颜色变化,记录开始产生沉淀的时间。从产生沉淀时开始计时,反应五分钟后将试管取出。待其冷却后,转移至离心管中,用50%的乙醇洗涤沉淀,再放人离心机中离心,倒掉上层清液。重复三次后,观察沉淀的颜色和沉淀的相对量,并做好记录。
3.实验指标和评分标准的确定
对于该反应,在水浴加热过程中,能看到反应体系的一系列颜色变化:蓝色悬浊液→黄绿色浊液→亮黄色浊液→橙黄色浊液。最终希望在课堂演示时,学生能够在较短时间内观察到试管底部有较多的砖红色的沉淀生成。因此确定从水浴加热开始到肉眼能够观察到红色沉淀的时间以及从开始产生红色沉淀之后的五分钟之内产生沉淀的量的相对多少为指标。指标1-“产生沉淀所需的时间”,指标2一“产生砖红色沉淀的量的相对多少”权重各为50%。采用2指标综合评分法进行评分,根据实验现象,评分标准确定如下:指标1-“产生砖红色沉淀所需的时间”:根据现象出现的时间进行评分,满分为50分,60s出现红色沉淀评为50分,时间每多20s减5分。看不到红色沉淀,得分为零。指标2一“产生砖红色沉淀的量的相对多少”:根据生成生成砖红色沉淀的量的相对多少进行评分,生成沉淀的量越多,分数越高。分为四个等级:①50-40分,较多;②40-30分,多;③30-20,少;④20-10分较少;⑤10-0很少,几乎看不到红色沉淀物或者沉淀为其他颜色,得分为零。
4.1 正交表的选取与处理
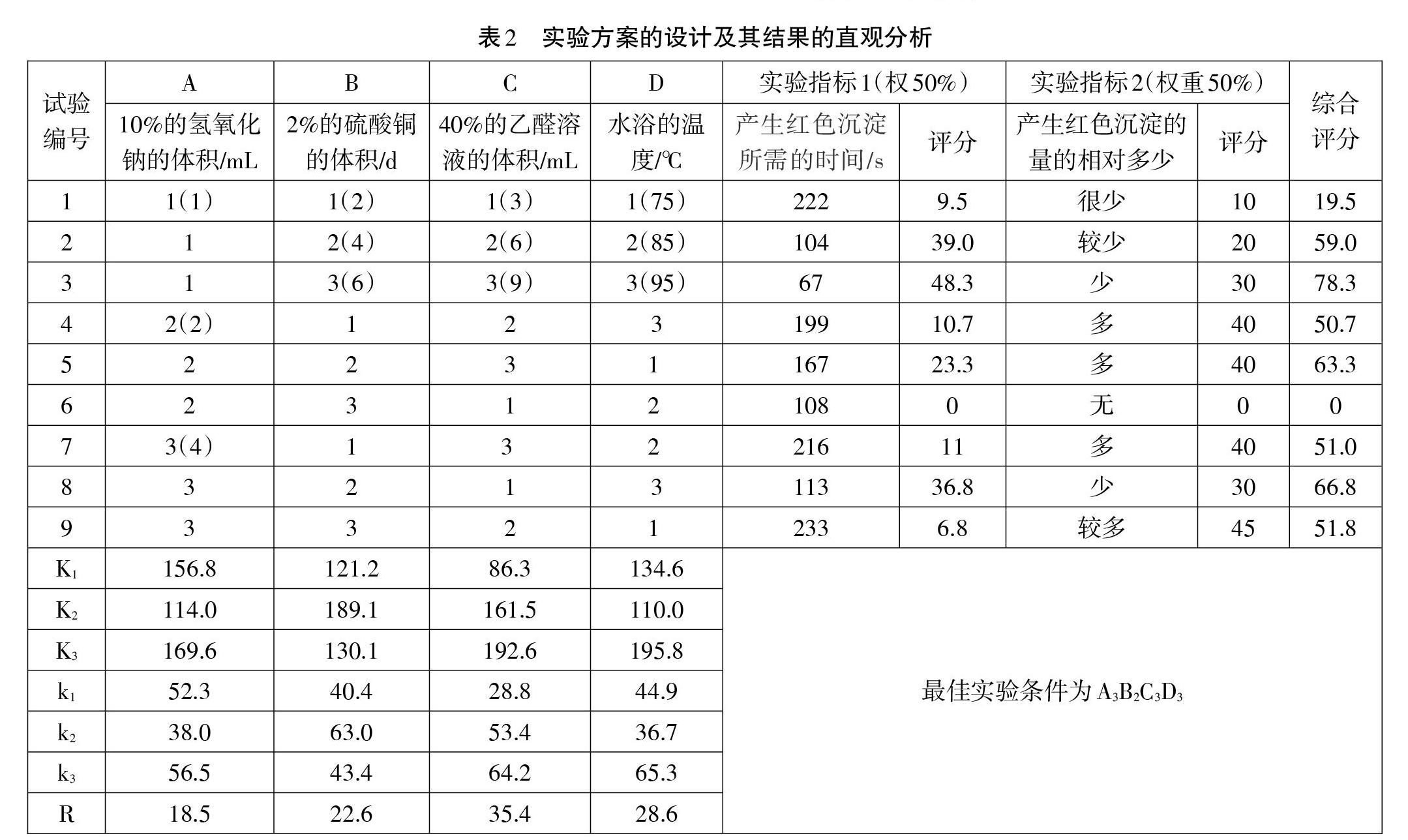
本实验设计为三水平四因素的正交实验,选用三水平四因素L9( 34)正交表来安排实验。为了排除偶然因素的干扰,共进行了3次平行实验。各数据的记录是平行实验数据的平均值。实验数据整理如表2所示。
5.实验结果分析
k值越大,实验效果越好,根据k值的大小,可以判断在所选定的因素水平范围内的最佳实验条件为A3B2C3D3,但其在本次实验安排中并未出现,做验证性实验:在试管中加入10%的氢氧化钠4mL,2%的硫酸铜的体积4滴,40%的乙醛溶液9滴,95℃水浴加热,实验结果为在92秒开始产生沉淀,用酒精洗涤离心后产生较多沉淀。按照评分标准进行评分,最终分数为42+40=82分,证明其为最佳实验条件。说明验证试验结果与正交试验结果相一致,表明优选出的条件达到了预期效果。
三、研究结论
按照教材上的操作进行实验,教师在不知道乙醛的质量分数的情况下加入0.5mL的乙醛,具有盲目性,采用市售的40%的乙醛进行实验,按照本研究探究出的最佳条件进行实验,只需要92秒即可看到较多的砖红色沉淀,实验现象明显,实验效果显著,节省时间,能够较好地满足教师演示实验的教学效果。
参考文献
[1] 张应红.新制氢氧化铜与乙醛反应的再研究[J].化学教育,2007(8):51-52
[2]刘湘强.乙醛2个特征反应实验应注意的问题[J].化学教育,2009,30(3):63-64
[3]丁云香地谈乙醛还原Cu(OH):实验[J].化学教育,2002 (10):47-48
[4][7]郭彦青,庞云,乔金锁.氢氧化铜检验醛基最佳条件的探究[J].化学教学,2019(6):79-82
[5] 陆燕海,吴文中.乙醛与氢氧化铜反应需强碱性条件的主因[J].化学教育(中英文),2017,38(15):75-78
[6] 张小林,戴兴德.氢氧化铜系列氧化剂氧化性实验研究[J].化学教育,2007(10):48-49
[8] 尹静,丁伟.对乙醛还原氢氧化铜实验的探讨[J].教学仪器与实验,2013,29(9):28-29
[9] 陈伟霞,丁伟.CH3CHO与Cu(OH)2反应加热条件的探究[J].化学教学,2011(7):51
