锌铜原电池实验的改进
2021-02-21林红剑
林红剑
摘要:通过分析教材中“锌一铜一硫酸”原电池实验现象产生的原因,从双液电池的构造和析氢超电势两个角度对电极进行改造或替换,使得该实验进一步优化。
关键词:锌铜原电池;析氢超电势;电极改造
文章编号:1008-0546(2021)01-0097-01
中图分类号:G632.41
文献标识码:B
doi: 10.3969/j .issn.1008-0546.2021.01.028
一、问题提出
人教版化学《必修2》在化学能与电能这一节中安排了“锌一铜一硫酸”原电池的实验。学生在实验中观察到的现象是锌片上有大量气泡,而铜片上几乎看不到气泡。这样的现象不利于学生深刻认识原电池的原理。
二、问题分析
锌片上之所以会产生气泡,其一是因为锌片与稀硫酸直接接触,若使用带有盐桥的双液电池则可以解决问题,但是双液电池增加了学生的理解难度,必修课程中不宜采用。
其二是因为锌片不纯,氢气在不同的金属上析出的超电势不同,粗锌中的一些杂质使得析氢超电势降低,导致氢气在锌片上析出。
三、问题解决
方法一:模仿双液电池的构造,将盐桥隐形化处理。具体措施如下:
1.配制氯化锌饱和溶液;
2.在氯化锌饱和溶液中加入淀粉,将溶液加热,使之呈糊状;
3.将淀粉糊均匀涂抹在锌片表面。
如此处理后的锌片不能与硫酸直接接触,既起到了双液电池的效果,又避免了装置的复杂化。在演示实验时,可以观察到锌片上无气泡,而铜片上有大量的气泡产生。
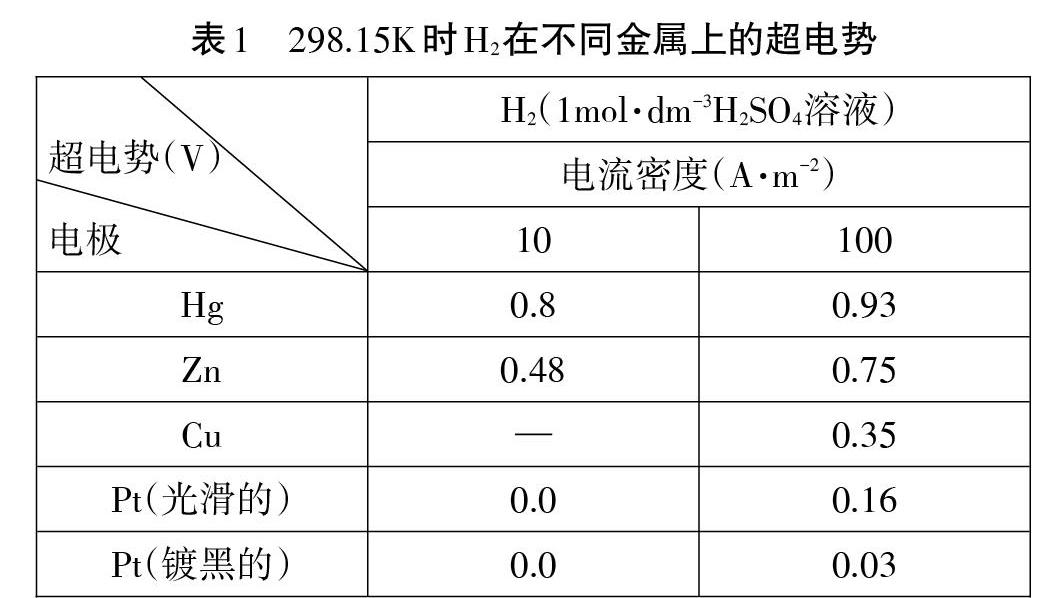
方法二:运用析氢超电势对电极进行改造,加大负极金属的析氢超电势,同时减小正极材料的析氢超电势。一些金属的析氢超电势如表1所示。
由表中数据可知,Hg的析氢超电势较大,因此用锌汞齐代替锌片作负极可以减少氢气在负极上析出。用Pt代替铜作正极可以极大地降低正极的析氢超电势,有利于氢气生成;或者用锉刀将铜片的表面处理成凹凸不平状,增大铜和硫酸的接触面积,加快了氢离子在铜表面的吸附速率,因而降低铜的析氢超电势[1]。
四、实验改进说明
原电池的原理是一个难点,需要通过电流表指针的偏转和铜片上的气泡,来认识电路中有电子的转移以及电子的流动方向。原来的实验看不到铜片上的气泡,学生难以借助这样的宏观现象来认识原电池的微观原理。在原有装置的基础上,对电极进行改造,既不增加装置的复杂性,又能使实验现象更明显。
参考文献
[1]傅献彩等.物理化學[M].北京:高等教育出版社,1990:668-672
