Ag2S/rGO纳米复合材料的细菌还原制备及光电性能研究
2021-02-13谈碧玉石先阳
谈碧玉,石先阳
(安徽大学 资源与环境工程学院,合肥 230000)
在环境污染和能源危机的压力下,迫切需要光催化技术来解决环境污染等问题,确保人类社会的可持续发展[1-2]。开发活性高、光生载流子分离效率快的催化材料是光催化技术的关键[3]。太阳能具有可再生、零污染等特性,被认为是化石燃料最有希望的替代品之一,因此,制备能充分利用太阳能的高效光催化剂至关重要[4]。
氧化石墨烯(GO)作为典型的二维材料,具有超高的比表面积(2600 m2/g)、优异的载流子迁移率、良好的导电性等特点,是一种非常理想的光催化材料[5-6]。然而,GO 的零带隙结构,限制了其在光电化学领域的发展。在半导体纳米材料中,金属硫化物以其独特的光学特性,在催化、光吸收、电化学等领域有着广阔的应用前景[7],可考虑将其引入而制备一种高效的石墨烯基光催化材料[8]。其中,纳米Ag2S 作为一种窄能隙半导体材料,由于其表面效应和量子尺寸效应,而具有很高的化学稳定性和良好的光学特性[9-12]。
目前,已经有许多制备纳米Ag2S 的方法被开发出来[13],包括电化学法、溶胶-凝胶法、牺牲模板法等。然而,传统合成方法存在有毒化学试剂、反应时间较长或反应温度较高等不足,容易造成环境污染并且有害于人体的健康。因此,寻找绿色简单、经济便捷、反应条件温和的制备方法,对于大规模生产Ag2S 纳米材料具有重要意义。微生物法可以在温和的条件下合成纳米粒子,是一种绿色环保的有效途径。Shewanella oneidensisMR-1(S. oneidensisMR-1)是一种兼性厌氧菌,在自然界中大量存在,并且具有较强的还原能力,这种革兰氏阴性菌已被应用于金属[14-15]和金属硫化物[16]的还原。
本文以S. oneidensisMR-1 为还原剂,将S2O32-离子还原为S2-,同时将氧化石墨烯(GO)变为还原氧化石墨烯(rGO),在rGO 纳米片上负载纳米Ag2S,制备Ag2S/rGO 复合催化剂。对其进行结构和性能表征,并对Ag2S/rGO 制备的纳米材料光电极进行循环伏安扫描(CV)、线性伏安特性扫描(LSV)、电流-时间(I-t)等光电化学测试,研究其光电性能。
1 实验
1.1 试剂
GO 购自拉丁(上海)生化科技股份有限公司;十二烷基苯磺酸钠(SDBS)由上海其福青材料科技有限公司生产;AgNO3、Na2S2O3·5H2O、聚乙烯吡咯烷酮(PVP)等均为市售分析纯试剂,实验用水为超纯水。
微量元素储备液:称取1.5 g 次氮基三乙酸,用超纯水定容500 mL,使用KOH将pH调节至6.5,加入MgSO4·7H2O 3.0 g,CaCl2·2H2O 1.0 g,NaCl 1.0 g,ZnSO4·7H2O 0.18 g,CoSO4·7H2O 0.18 g,MnCl2·2H2O 0.5 g,FeSO4·7H2O 0.1 g,NiCl2·6H2O 0.025 g,KAl (SO4)2·12H2O 0.02 g,CuSO4·5H2O 0.01 g , H3BO30.01 g , Na2MoO4·2H2O 0.01 g ,Na2SeO4·5H2O 0.3 mg,待全部溶解混合均匀后定容1000 mL 备用。
1.2 细菌还原制备纳米材料
1.2.1 培养基的配制
Luria-Bertani (LB)培养基:在2 L 纯水中溶解20 g NaCl、20 g 蛋白陈和10 g 酵母粉制备得到。
厌氧培养基配方为0.048 g MgSO4·7H2O、9.532 g 4-羟乙基哌嗪乙磺酸(HEPES)、0.51 g (NH4)2SO4、4.484 g 乳酸钠、0.93 g NaCl 和10 mL 微量元素储备液,将其溶解于2 L 纯水中,搅拌均匀后在每个血清瓶中分装50 mL 厌氧培养基,充N215 min,在121℃下灭菌20 min 备用。
1.2.2S. oneidensisMR-1 的培养
S.oneidensisMR-1 被接种于LB 培养基后,在30℃、150 r/min 的恒温震荡培养箱中培养24 h 后,得到的菌液在6000 r/min 离心5 min,并用厌氧培养基洗涤3 次。
1.2.3 Ag2S/rGO 复合材料的制备
用厌氧培养基配制25 mL 1%的SDBS,加入15 mL 1 mg/mL 的GO 分散液超声处理,将200 mg PVP、0.5308 g AgNO3和0.7756 g Na2S2O3依次加到混合溶液中,常温下继续搅拌4 h。用无菌注射器取上述混合液2 mL 加入到装有厌氧培养基溶液的血清瓶中,同时加入一定体积洗涤后的S. oneidensisMR-1 溶液,使血清瓶中菌的初始浓度OD600= 0.5 (约为5×106CFU/mL)。将血清瓶在恒温震荡培养箱中于150 r/min,30℃避光培养48 h。反应结束后,将混合溶液在6000 r/min 下离心10 min,再以9000 r/min离心8 min,将收集到的产物用纯水洗涤3次,最后于60℃的烘箱中干燥12 h。得到Ag2S/rGO 复合材料,用于分析表征和电极制备。rGO 以GO 分散液为原料和S. oneidensisMR-1 在厌氧培养基中共同培养。将PVP、AgNO3和Na2S2O3依次加到混合溶液中,在相同的条件下利用S. oneidensisMR-1介导合成Ag2S 纳米粒子。
1.3 样品分析表征
1) 形貌和结构表征。
用电子透射显微镜(TEM,日本JEOL 公司JEM-2100 型)表征样品的形貌,并对其进行元素分析和面元素分布的检测。测试方法是将样品在乙醇溶液中均匀分散,在铜网上滴入两滴悬浮溶液进行干燥处理。加速电压为200 kV,最大放大倍数为1500 k。
X 射线晶体衍射仪(XRD,日本Rigaku 公司Smart Lab 型)分析材料的晶体结构。检测条件Cu-Kα 为辐射源,扫描范围(2θ) 10°~80°。
用孔隙度分析仪(ASAP 2460)进行N2吸附测试。实验参数:将液氮在180℃的温度下脱气处理12 h,得到其比表面(BET)特征。
2) 化学图谱表征
用X 射线光电子能谱仪(美国Thermo Fisher 公司ESCALAB 250Xi 型XPS)测试样品的元素化学形态。以Al-Kα为X 射线辐射源,以表面污染碳的C 1s (B.E. = 284.8 eV)为基准校正其他元素的结合能。
用紫外可见分光光度计(UV-Vis)扫描样品的吸收光谱。取定量粉末分散在载台中,以硫酸钡作为参比。
Nexus870 型傅里叶变换红外光谱仪(FT-IR,美国Nicolet 公司,Vertex80+Hyperion2000 型)对粉末样品进行红外光谱扫描测试。
荧光分光光度计(PL,Horiba Fluoro max plus 型)测试材料的荧光光谱,激发光源为He-Cd 灯。
1.4 光电化学测试
将40 mg 样品,5 mg 聚偏二氟乙烯(PVDF)粘合剂和5 mg 的乙炔黑混合用打浆机制备成电极浆料。将浆料均匀涂覆在面积为1 cm×1 cm 的FTO 玻璃上制成玻璃电极。
测试三电极系统由铂网、涂上样品的FTO 玻璃和饱和甘汞电极构成,并用1 mol/L 的硫酸钠(Na2SO4)溶液作为电解液,以300 W 氙灯做光源,用电化学工作站(上海辰华仪器有限公司CHI600E型)对制备材料的光电化学性能进行评价。
2 结果与讨论
2.1 实验材料及仪器
微生物法合成Ag2S/rGO 复合材料的可能机理如图1 所示。首先,SDBS 作为连接剂将Ag+粘附在比表面积较大的GO 上,S2O32-和S. oneidensisMR-1 共同在厌氧培养基中培养。S. oneidensisMR-1 作为一种典型的还原菌,Psr 系统和Sir 系统是它的电子通道,PsrA 和SirA 起着终端还原酶的作用。S2O32-进入到S. oneidensisMR-1 的细胞周质内,接受细胞内源呼吸产生的电子,电子从PsrC 传递到PsrA,S2O32-被还原成SO32-,生成的SO32-被Sir 系统进一步还原[24]。SirA 从MQ 获得电子将SO32-还原为S2-,随后S2-扩散到细胞外与GO 上的Ag+结合生成Ag2S。同时由于GO 良好的导电能力,电子也可以由S. oneidensisMR-1 直接传递到GO 上,GO 被还原为rGO,最后合成的Ag2S 被吸附在rGO上形成Ag2S/rGO 纳米复合材料。
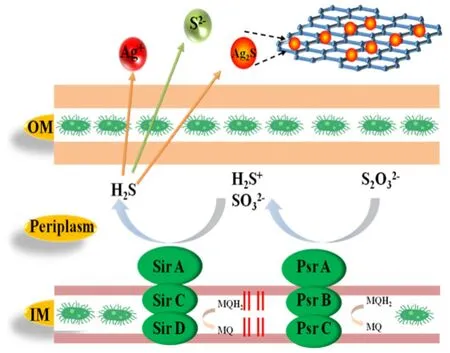
图1 S. oneidensis MR-1 合成Ag2S/rGO 的机理示意图Fig.1 Mechanism diagram of Ag2S/rGO synthesis by S. oneidensis MR-1
2.2 形貌和结构表征
2.2.1 形貌和元素分析
图2 为采用透射电镜对Ag2S/rGO 粉末样品进行表征的结果。由图2(a)~(c)可以看出,微生物法一步合成的Ag2S 较为均匀地分布在rGO 的表面上,其粒径大小在10 nm 左右。比表面积较大的rGO 能够为其提供较多的活性位点和有效地阻止Ag2S 纳米颗粒的团聚。由图2(d)的高分辨率透射电镜(HRTEM)图像可以清晰地观察到Ag2S 的晶格条纹,说明其具有较高的结晶度。Ag2S 主要有两种晶型:单斜晶体(α-Ag2S)和面心立方体(β-Ag2S)。HR-TEM 晶格间距测量结果显示晶面间距d= 0.21 nm,对应α-Ag2S 的(103)晶面。图2(e)能量色散光谱(EDX)证实Ag2S/rGO 纳米复合材料中存在着C、Ag 和S 三种元素。图2(f)的元素选区面扫描图,进一步证实了C、Ag 和S 的分布状态,可以看出Ag2S NPs 被成功负载地在rGO 纳米片上。
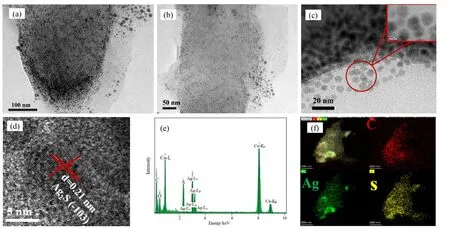
图2 Ag2S/rGO 的形貌表征 Fig.2 Morphology characterization of Ag2S/rGO
2.2.2 比表面(BET)测定

图3 Ag2S 和Ag2S/rGO 的比表面测试N2 吸附-脱附曲线(a)和孔径分布图(b)Fig.3 N2 adsorption-desorption curve (a) and pore size distribution diagram (b) of Ag2S and Ag2S/rGO BET test
2.2.3 XRD 分析
Ag2S、rGO 和Ag2S/rGO 样品的XRD 图谱如图4 所示。Ag2S/rGO 纳米复合材料在2θ为28.97°、31.52°、34.39°、36.56°、37.72°、40.74°、43.41°、45.42°和53.28°处的特征衍射峰,分别归因于α-Ag2S(JCPDS No.14-0072)的(-111)、(111)、(-112)、(-121)、(121)、(-103)、(031)、(200)和(-213)晶面,表明Ag2S 已成功合成。而在2θ= 20.7°的位置上的特征峰,这是rGO 的特征衍射峰,说明S. oneidensisMR-1 将GO 还原。
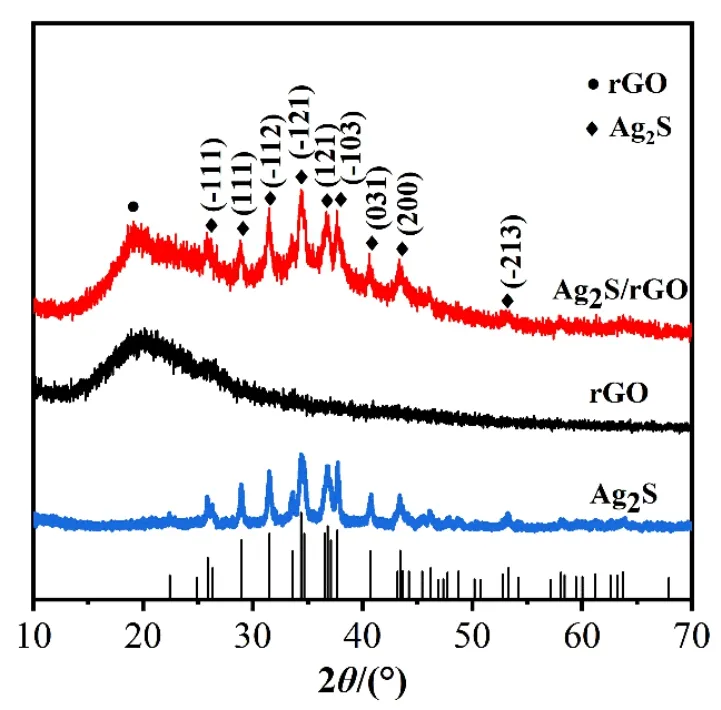
图4 Ag2S、rGO 和Ag2S/rGO 的X 射线晶体衍射图谱Fig.4 X-ray crystal diffraction pattern of Ag2S, rGO, Ag2S/rGO
2.3 化学图谱表征
2.3.1 FT-IR 分析
FT-IR 光谱如图5 所示,GO 的光谱在1630 cm-1 和1392 cm-1处出现了两个特征振动峰,分别归因于C=O 和O-H 的伸缩振动峰,在1085 cm-1处的振动峰证明了C-O 键的存在[17-18]。观察Ag2S/rGO 纳米复合材料的光谱,上述特征峰的强度明显降低,大量的含氧基团的明显减少,表明GO 被还原为rGO。
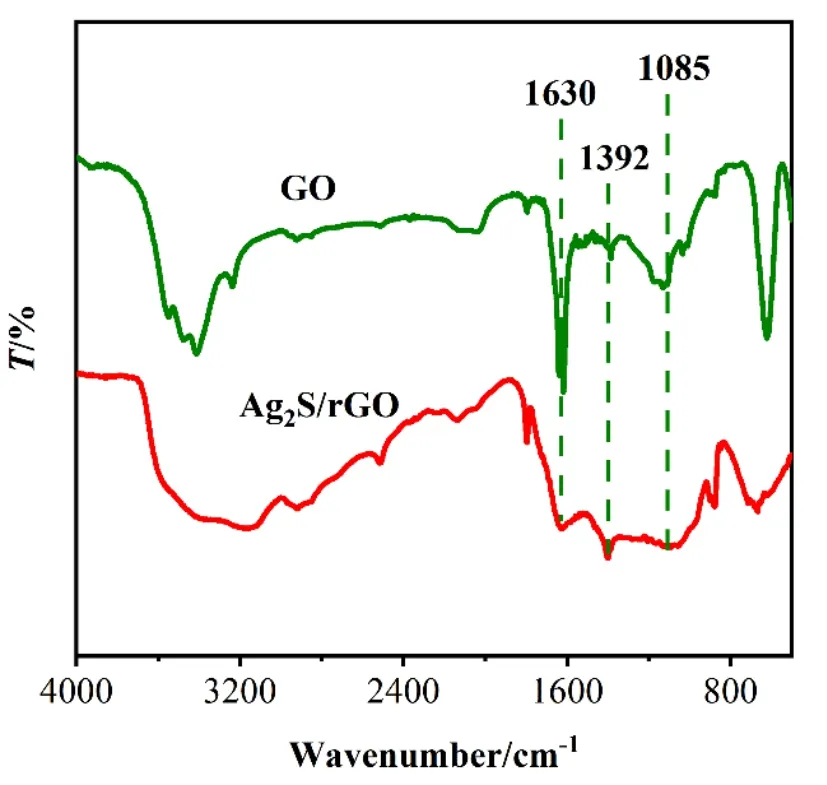
图5 GO 和Ag2S/rGO 的红外光谱图Fig.5 FT-IR spectrum of GO and Ag2S/rGO
2.3.2 XPS 分析
XPS 可以提供原子的价态信息,用于研究纳米材料中的元素组成。Ag2S/rGO 样品的XPS 测定结果如图6 所示。
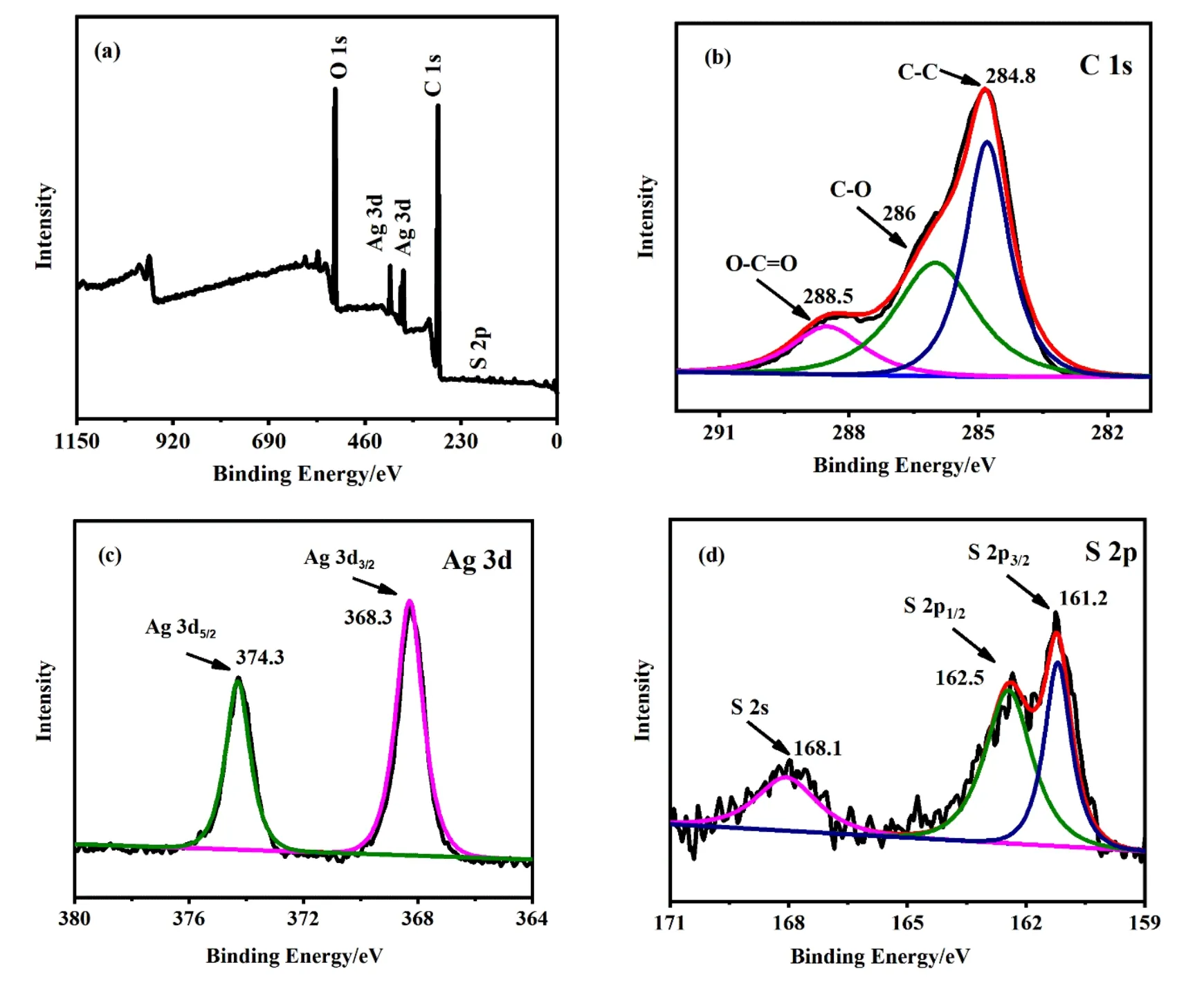
图6 Ag2S/rGO 的XPS 能谱图Fig.6 The XPS spectrum of Ag2S/rGO
图6(a)为Ag2S/rGO 复合材料的全谱图,从中可以看到有Ag、O、S 和C 四种元素及其对应的特征峰。在图6(b)中,Ag2S/rGO 的C 1s 谱图显示出3个峰,位于284.8、286 和288.5 eV,分别对应于CC、C-O 和O-C=O 官能团,含氧官能团在XPS 中明显减少,结果与FT-IR 光谱一致,表明GO 被成功还原[19]。图6(c)为Ag 3d 的高分辨谱,在368.3 eV和374.3 eV 的峰对应于Ag 3d5/2和Ag 3d3/2轨道,表明Ag 是以Ag+的形式存在的[20-21]。图6(d)中S 2p的XPS 谱图,在161.2 eV 和162.5 eV 处的峰对应于S 2p3/2和S 2p1/2轨道的结合能,表明复合材料中的S 是以S2-形式出现。
2.3.3 荧光光谱(PL)分析
为了研究光生电子-空穴对的复合情况,对Ag2S 和Ag2S/rGO 纳米复合材料进行PL 测试,结果如图7 所示。由图7 可见,在379 nm 的激发波长下,分析480 nm 处强特征峰的变化程度,结果如图7。纳米Ag2S 由于光生电子和空穴的迅速复合而表现出强烈的发射峰,而随着 rGO 的引入,Ag2S/rGO 纳米复合材料表现出明显的荧光淬灭,证明rGO 和Ag2S 的协同作用提高了光生载流子分离效率。

图7 Ag2S 和Ag2S/rGO 的荧光光谱图Fig.7 Fluorescence spectra of Ag2S and Ag2S/rGO
2.3.4 吸收光谱(UV-Vis)分析
图8 为紫外可见吸收光谱图。

图8 (a)rGO、Ag2S 和Ag2S/rGO 的紫外可见漫反射光谱;(b) rGO、Ag2S 和Ag2S/rGO 的(Ahv)2-hv 曲线Fig.8 (a) UV-Vis diffuse reflectance spectra of rGO, Ag2S and Ag2S/rGO; (b) (Ahv)2 vs. hv curves of rGO, Ag2S and Ag2S/rGO
图8(a)表明,与Ag2S 相比,Ag2S/rGO 复合材料对可见光的吸收性能明显增强,在500~800 nm 处的吸收增强幅度较大,改善了rGO 和Ag2S 纳米材料对于可见光的吸收效果。在可见光区域,Ag2S/rGO 纳米复合材料吸收光的响应强度在不断增加,可以充分利用太阳光中的可见光。导体材料的禁带宽度与其光学和电学性能密切相关,根据禁带宽度的计算公式[22]:

式中,A为吸收系数,h 为普朗克常数,v为光的频率,K 为吸收常数,Eg为禁带宽度。
计算结果如图8(b)所示,与Ag2S 的禁带宽度1.94 eV 相比,本研究制备的Ag2S/rGO 纳米复合材料的禁带宽度减小到1.67 eV。表明由于rGO 的掺入,Ag2S/rGO 纳米复合材料的禁带宽度变窄,使得光响应范围拓宽到可见光区域,增强了纳米材料对可见光的利用效率,提高了光催化剂在可见光下的催化活性。
2.4 材料的光电性能
2.4.1 测试结果
用电化学工作站三电极系统进行 Ag2S 和Ag2S/rGO 两种纳米材料所制作电极的光电化学测试,结果如图9 所示。
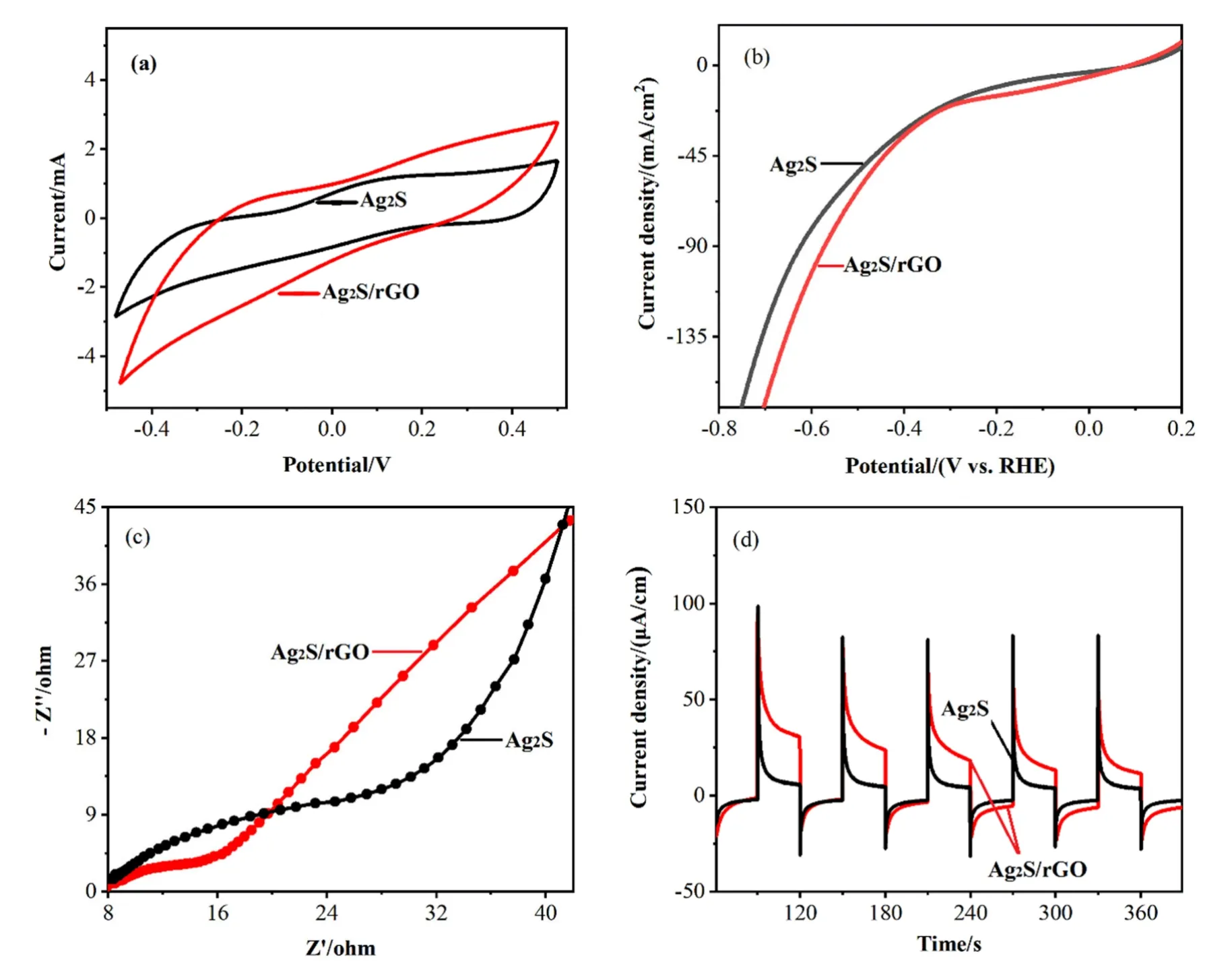
图9 Ag2S/rGO 和Ag2S 纳米材料电极的电化学性能测试曲线Fig.9 Electrochemical performance test curves of Ag2S/rGO and Ag2S nanomaterial electrode
图9(a)为两种电极的CV 曲线。由图可见,Ag2S的电导率和电活性相对较弱,所以它的CV 电流较低;Ag2S/rGO 纳米复合材料的CV 电流远远高于Ag2S 纳米材料。在相同的条件下,用Ag2S 和Ag2S/rGO 分别作为光电极进行LSV 测试,以观察其光电特性,结果如图9(b)所示,Ag2S/rGO 纳米复合材料的起始电位小于纳米Ag2S,从而更容易进行 催化反应。通过电化学阻抗谱(EIS)测试Ag2S 和Ag2S/rGO 纳米复合材料中载流子的产生和迁移能力。一般而言,电化学阻抗半圆的直径越小,电荷在移动的过程中的电阻就越小,从而显示出更大的表面电极响应[23]。如图9(c)所示,Ag2S/rGO 纳米复合材料的圆弧半径小于Ag2S,说明Ag2S/rGO 复合材料具有更好的导电性,证实rGO 的加入增强了复合材料的电导率和电荷分离能力。综合LSV 与EIS曲线可以得出,Ag2S/rGO 纳米复合材料中光生电子-空穴对复合的几率大大地降低,因此,它的光催化活性更高。I-t的测试是在相等的时间间隔内,保持暗电流与光电流之间的来回切换,观察光电流响应的变化程度。图9(d)展示了Ag2S 和Ag2S/rGO 纳米复合材料的瞬态光电流测量结果,Ag2S/rGO 纳米复合材料的光电流强度出现了显著的增强,最高可以达到40 µA/cm2,并且Ag2S/rGO 纳米复合材料的光电流密度约为Ag2S 纳米材料(13 µA/cm2)的3 倍,表明复合材料中光生电子-空穴对的分离效率更高。
这可能是由于Ag2S和rGO纳米片之间的相互作用,从而延长了电子-空穴对的寿命。
2.4.2 Ag2S/rGO 的光电性能机理分析
基于本文的实验结果,针对Ag2S/rGO 纳米复合材料提出了一种促进电子-空穴对分离的可能机制,如图10 所示。
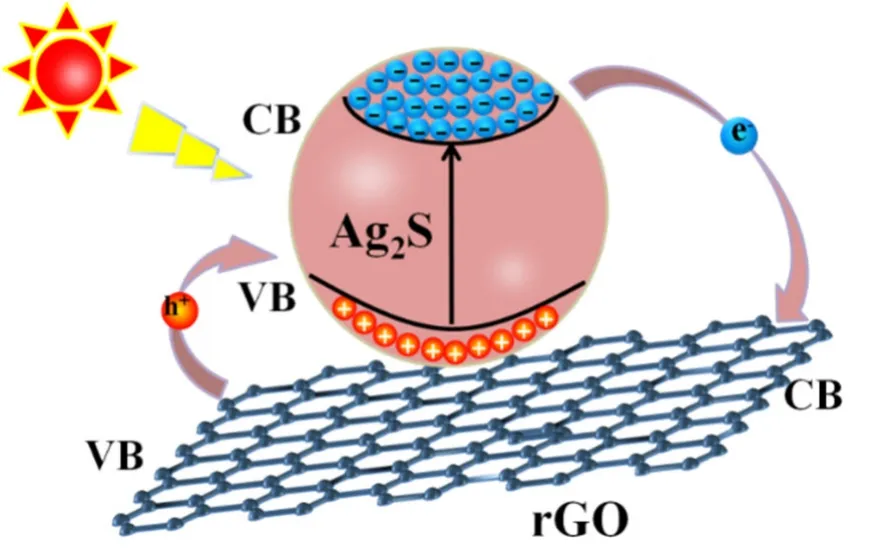
图10 Ag2S/rGO 纳米复合材料中电子迁移的示意图Fig.10 Schematic diagram of electron migration in Ag2S/rGO nanocomposites
在可见光的照射下,Ag2S 与rGO 中的电子从价带(VB)被激发到导带(CB),从而在CB 中产生电子,在VB 中留下空穴。由于rGO 具有优异的载流子迁移率,Ag2S CB 中的电子会被转移到rGO 的CB 上[11,25],rGO VB 上的一部分空穴又会转移至Ag2S 的VB 中,从而有效地促进电子-空穴对的分离[26]。因此,Ag2S/rGO 纳米复合材料的构建可以大大提升载流子的分离效率,从而提升纳米材料光电极的光电化学响应。
3 结论
1) 利用S. oneidensisMR-1 的介导原位合成Ag2S/rGO 纳米复合材料。S.oneidensisMR-1 作为还原剂,不仅可以同时还原GO 和S2O32-,合成的纳米材料具有良好的生物相容性和优异的光学性能。
2) 表征测试结果表明,生物合成法将GO 成功还原为rGO,粒径大小在10 nm 左右的Ag2S NPs 较均匀地分布在rGO 的表面,rGO 巨大的比表面积有效地阻止Ag2S 纳米颗粒的团聚。
3) 在相同条件下,Ag2S/rGO 的光电流密度(40 µA/cm2)明显大于Ag2S (13 µA/cm2)。Ag2S/rGO 纳米复合材料有效地提高了光生电子-空穴对的分离效率,从而获得更加优异的光电化学响应。
