短脉宽Er:YAG 激光处理对牙本质表层性质及粘接界面的影响
2021-02-12郑蒲珏黄文燕曾素娟杨雪超
郑蒲珏,黄文燕,曾素娟,杨雪超
(1.广州医科大学附属口腔医院儿童口腔科,广东 广州510182;2.广州医科大学附属口腔医院牙体牙髓科,广东省口腔组织修复与重建工程技术研究中心,广州市口腔再生医学基础与应用研究重点实验室,广东 广州510182)
掺铒钇铝石榴石(Er:YAG,简称“铒”)激光波长为2 940 nm,在水及羟基磷灰石OH-的吸收峰附近[1-2]。Er:YAG 激光消融硬组织是建立在光热机械作用的基础上,因此在使用Er:YAG 激光时,不应忽视牙体硬组织热损伤的风险。热分析研究结果显示,有机成分、水分子和碳酸盐在100 ℃以上即可发生热改性[3]。无机和有机成分的变化可影响牙体硬组织的硬度、渗透性、溶解性或粘附性[4]。粘接是保持修复体远期成功的重要因素。树脂基修复材料与牙本质的粘接原理为粘接剂渗透至胶原纤维网形成混合层和渗透至牙本质小管内形成树脂突。
牙本质的表面结构、力学性能和化学组分是牙本质修复治疗的重要影响因素。与以往大部分研究激光处理后牙本质表面变化的报道不同,本研究将探索Er:YAG 处理后涂布自酸蚀粘接系统及全酸蚀粘接系统后牙本质的表面形貌,同时研究激光处理对牙本质表面下层化学组分及显微硬度的影响。临床上最重要的激光参数之一是脉冲持续时间(即脉宽),其与激光的切削能力和牙体组织的热沉积密切相关[5]。激光脉冲越快,切削能力越强,热量传导到邻近组织的时间越短,组织残留热量越低,热损伤越低。到目前为止,临床激光装置可设置的最短脉宽为50 μs。本研究拟采用短脉冲模式(50 μs 脉宽)及300 μs 脉宽铒激光处理牙本质,得出更有利于粘接的激光参数结合扫描电镜(scanning electron microscopy,SEM)、能量色散X 射线光谱(energy dispersive X-ray spectroscopy,EDX)、显微硬度仪定性及定量评估牙本质表面及下层性状的变化。
1 材料与方法
1.1 处理样本
本项目已通过广州医科大学附属口腔医院伦理委员会审查(伦理审批编号:KY2019002)。本实验样品为因阻生拔除的完整人类第三磨牙,离体牙纳入的标准为无龋坏、无氟斑、无釉质发育不全和非四环素牙。拔牙后用手工洁治器刮除牙体上的软组织、色素,置于1%氯胺T 溶液中4 ℃保存。使用高速涡轮机金刚砂车针在水喷雾下去除冠部釉质层,暴露中层牙本质,作为牙本质圆盘表面。将每颗牙从釉牙骨质界下2 mm 处切断牙根,去除牙髓,大致按照半径约5 mm、厚度3 mm 的规格初步制备牙本质圆盘。#320、800、1 200、3 000 目砂纸在流水下于磨片机(EXAKT,E400CS,北京共赢联盟国际科技有限公司,德国)上抛光1 min,在30 倍体视显微镜(Leica,EZ4 W,徕卡,德国)下观察确保无釉质残留,弃去表层有裂纹的牙块,超声波振荡清洗20 min,得到最终牙本质圆盘,置于0.9%生理盐水中4 ℃保存,1 周内用于实验。
1.2 牙本质表面切削
球钻组:采用金刚砂球钻处理,高速涡轮机上金刚砂球钻在水冷却下去除一薄层牙本质,每5 次预备后更换新的球钻。
Er:YAG 激光处理组:实验光源为Er:YAG 激光(Fotona 欧洲之星,M021-5AF/1,Fotona d.d.,斯洛文尼亚),脉冲频率0~50 Hz 可调,激光光束通过关节臂传输后经透镜直接聚焦于组织样品上,光斑直径为1.3 mm。激光消融参数:能量100 mJ,频率20 Hz,脉冲宽度分别为50 μs 或300 μs。在连续喷水喷雾下,在距靶点1 mm 的非直接接触模式下,用R14 型手持设备进行激光传输,移动激光手具,使其通过牙块的全长度形成一个线状的隧道样照射区[6]。
1.3 粘接处理
本研究使用金刚砂球钻、参数为100 mJ 及50 μs的Er:YAG 激光、参数为100 mJ 及300 μs Er:YAG 激光切削牙本质表面,每组6 个样本,分别进行以下处理:(1)按说明书涂布自酸蚀粘接剂;(2)不进行酸蚀处理,仅涂布全酸蚀粘接剂;(3)37%磷酸蚀刻15 s 后,涂布全酸蚀粘接剂;(4)37%磷酸蚀刻30 s 后,涂布全酸蚀粘接剂。本研究使用的自酸蚀粘接剂为一步法弱酸型粘接系统(iBond,贺利氏,德国),涂布牙面后静置10 s,用强压空气除去挥发成分后使用光固化灯(3M ESPE,Elipar TM S10,3M Deutschland Gmbh,美国)照射10 s;全酸蚀粘接剂为以丙酮为溶剂的Prime Bond NT(Dentsply,德国),用37%磷酸酸蚀15 s,水气加压冲洗15 s,再涂布粘接剂,保持湿润20 s,气枪吹5 s,光固灯照射10 s。涂布粘接剂并光固化后进行扫描电子显微镜检测。
1.4 显微硬度检测
采用投硬币法在经金刚砂球钻或参数为100 mJ 及50 μs 的Er:YAG 激光中各随机抽取5 个样本,表面处理后的样品中心沿颊舌方向纵切分成两部分,一部分进行显微硬度检测,另一部分进行扫描电子显微镜-能谱仪检测。将纵切后的牙块侧面依次在#320、800、1 200、3 000 目砂纸流水下抛光,形成光滑的表面,超声波振荡清洗20 min,环氧树脂将牙块固定在圆柱形板中。采用平行度计,确保表面与水平面保持平行,在距离表面30 μm 深度的管间牙本质加压,压痕的加载力为1 gf,重复测量6 次,记录显微硬度值。
1.5 扫描电镜及X 射线能量色散谱检测
EDX 借助于分析样品发出的元素特征X 射线的波长和强度实现的,根据波长测定元素组成,根据强度测定元素的相对含量[7]。样品经常规固定、干燥、喷金,用SEM(日立,S-3400N II,Hitachii,日本)分析牙本质组织微结构变化,放大倍数为1 000、3 000,加速电压为15 kV。用安装在SEM 上的EDX(550i,IXRF Sytems,Austin TX,美国)检测消融牙本质元素的组成,每个样本随机选取3~4 个激光照射区域和正常骨组织区域,测定钙(Ca)、磷(P)元素的含量(Atomic %),并计算钙/磷比例。
1.6 统计学方法
应用SPSS 23.0 统计学软件进行分析,符合正态分布的计量资料以表示,采用Wilcoxon 秩和检验、t检验和Kruskal Wallis H 检验,组间两两比较采用Bonferroni 检验,P<0.05 为差异有统计学意义。
2 结果
2.1 牙本质表面形貌分析
SEM 结果如图1 显示,球钻组牙本质表面有一玷污层,牙本质小管封闭;Er:YAG 激光组牙本质表面呈鳞片状不规则形态,无玷污层,牙本质小管开放,呈袖口状突出。涂布自酸蚀粘接剂后,球钻组表面见少量不规则、粗糙的多层突起物,100 mJ 及50 μs的Er:YAG 激光组表面可见大量不规则、粗糙的多层突起物,100 mJ 及300 μs 的Er:YAG 激光组表面覆盖一层粗糙的粘接层,可见大量散在孔隙,未见多层突起物。未酸蚀而直接涂布全酸蚀粘接剂后,3 组牙本质表面均覆盖一层均匀的粘接层,其中球钻组表面见少量粗糙的突起物。磷酸蚀刻15 s及涂布全酸蚀粘接剂后,球钻组牙本质表面覆盖一层薄而均匀的粘接层,有少量散在孔隙,100 mJ 及50 μs 的Er:YAG 激光组表面可见粗糙的粘接层,可见较多散在孔隙,100 mJ 及300 μs 的Er:YAG 激光组表面可见均匀的粘接层,可见大量散在孔隙。磷酸蚀刻30 s 及涂布全酸蚀粘接剂后,球钻组牙本质表面覆盖一层薄而均匀的粘接层,有大量散在孔隙,100 mJ 及50 μs 的Er:YAG 激光组表面可见粗糙的粘接层,可见少量散在孔隙,100 mJ 及300 μs 的Er:YAG 激光组表面可见均匀的粘接层,可见较多散在孔隙。

图1 扫描电镜下牙本质表面形貌图(2 000×,标尺20 μm)
球钻组及Er:YAG 激光组分别进行自酸蚀粘接、全酸蚀粘接、酸蚀15 s+粘接、酸蚀30 s+粘接处理后,球钻组表面玷污层,涂布粘接后牙本质表面形貌分别为少量不规则多层突起物、少量粗糙突起物、薄而均粘接层、薄而均粘接层有大量孔隙;激光组表面呈鳞片状,涂布粘接后牙本质形貌显示,100 mJ及50 μs 组有大量不规则多层突起物、均匀粘接层、粗糙粘接层及较多孔隙、粗糙粘接层及少量孔隙;100 mJ 及300 μs 组有大量孔隙的粗糙粘接层、均匀粘接层、大量孔隙的均匀粘接层、较多散在孔隙的均匀粘接层。
2.2 牙本质表面钙磷比例分析
EDX 结果如图2 显示,球钻组牙本质表面钙磷比例为0.86±0.06,Er:YAG 激光组牙本质表面钙磷比例为0.85 ±0.02,两组间钙磷比例差异无统计学意义(t=0.416,P=0.685)。
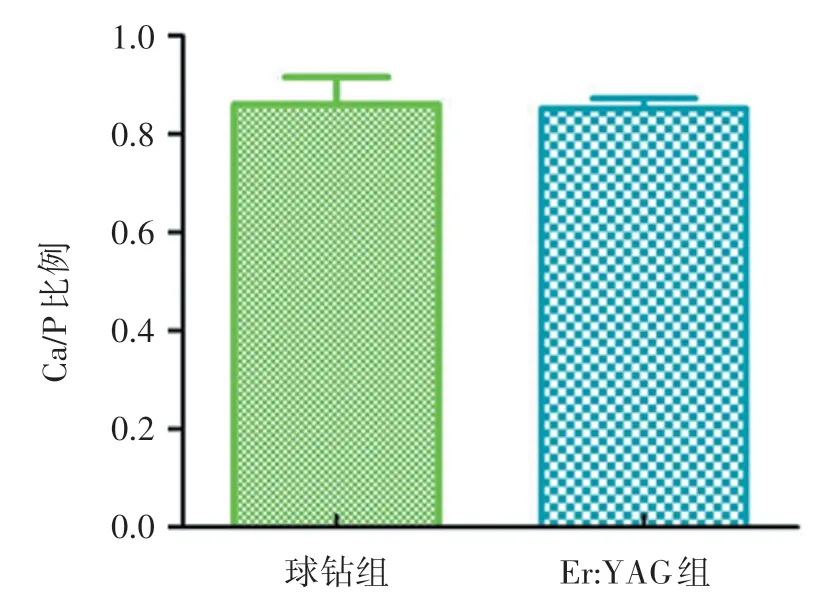
图2 两组牙本质表面钙磷比例
2.3 牙本质下层不同深度钙磷比例分析
EDX 结果如图3 显示,Er:YAG 激光及球钻处理后,牙本质下层5~30 μm 处钙磷比例与表层间比较,差异无统计学意义(P球钻=0.15;在激光组,与表层组相比,P5μm=0.1,P10μm=0.7,P15μm=0.4,P20μm=1.0,P25μmμm=0.1,P30μm=0.1)。Er:YAG 激光组与球钻组在牙本质表面及下层不同深度处的钙磷比例比较,差异无统计学意义(P表层=1.0P5μm=0.7,P10μm=1.0,P15μm=0.7,P20μm=0.7,P25μm=0.4,P30μm=0.4>0.05)。
2.4 显微硬度分析
显微硬度测量结果如图4 显示,Er:YAG 激光处理后牙本质下层30 μm 处显微硬度值为71.9 ±4.44,球钻处理后牙本质下层30 μm 处显微硬度值为66.84 ± 3.73,两组比较,差异有统计学意义(t=4.337,P=0.000)。
3 讨论
临床上常使用全酸蚀技术处理牙本质表面,由于牙本质结构间含水量的差异,酸蚀优先去除管周牙本质,形成扩大的漏斗状开口的小管;酸蚀还可暴露多微孔、脱矿的胶原纤维网,便于树脂基粘接剂渗透形成混合层。本研究结果显示,Er:YAG 激光处理后,牙本质表面呈鳞片状不规则形态,无玷污层,牙本质小管开放,呈袖口状突出。利用涡轮手机磨削牙齿后,会在牙体表面留下一玷污层,使牙本质小管封闭。这说明铒激光对牙本质的作用不同于酸蚀,激光更多地选择性消融管间牙本质,形成袖口状突出的小管,且激光处理没有暴露形成混合层所必需的胶原纤维网,这与以前的研究结果是一致的[8-9]。
牙本质由有机组分和无机组分组成,其中无机组分主要是羟基磷灰石晶体中的钙和磷。当有机组分与无机组分发生变化时,钙磷比值发生变化,可能影响硬组织的渗透性、溶解性和粘附性[4]。激光照射后生物组织的化学改变很大程度上取决于其成分的性质。与以往大部分研究不同,本研究对牙本质不同深度处的钙磷比例进行检测,结果表明,参数为100 mJ 及50 μs 的Er:YAG 激光组与球钻组间牙本质下层0~30 μm 范围内钙磷比例无显著性差异。Katirci 等[10]研究表明,激光处理后牙本质表面钙磷比例与球钻组间无显著性差异(P>0.05)。不同深度的牙本质钙磷含量、小管密度不同,推测表面与深层间钙磷比例的差异可能与牙本质的部位及深度有关,与激光照射无显著相关性。
显微硬度检测结果显示参数为100 mJ 及50 μs的激光组的显微硬度高于球钻组(P<0.05),这与Moosavi 等[11]研究结果一致,该团队研究发现相对于传统高速手机,Er:YAG 激光处理提高牙本质下层基质30 μm 处的显微硬度及钙含量,推测可能是因为水和有机组分蒸发使基质中矿物质含量相对增加,从而提高牙本质硬度。而He 等[6]发现激光处理后牙本质显微硬度、弹性模量在10 μm 以内下降约40%,15~50 μm 范围内与正常牙本质无明显区别。在不同的照射条件下,Er:YAG 激光可引起不同的组织改性结果。Chinelatti 等[12]使用不同能量水平(160、200、260、300、360 mJ)的Er:YAG 激光分别处理浅层、深层牙本质,最低能量水平(160 mJ)增加浅层牙本质表面(20 μm 范围内)的显微硬度,160、200 mJ 的能量未影响深层牙本质表面(20 μm范围内)的显微硬度,而更高的能量水平均使浅层及深层牙本质的显微硬度降低,160 mJ 能量组的牙本质硬度最高,360 mJ 能量组硬度最低。高能量Er:YAG 激光所引起的硬度改变可能与牙本质有机基质的变性后其抵抗局部变形能力降低有关。
Er:YAG 激光消融硬组织是建立在光热机械作用的基础上的,照射过程中产生的过量热量可引起牙齿硬组织的超微结构和成分的变化。Er:YAG 激光的能量主要被水吸收,水介导的爆炸式组织去除法已被证明是最有效去除硬组织的方法,水爆破的同时可转移热量,使传递到邻近牙体组织的热量降低。热效应的强度取决于激光参数,包括能量、频率、波长、脉宽等及组织的光学特性。本研究实验得到的更有利于粘接的激光参数为50 μs 脉宽,很多研究认为50 μs 脉宽是临床上适合有效的牙体硬组织消融参数,伴随外部水喷雾时,可有效地消融牙体硬组织,减少热损伤。Trevelin 等[13]研究发现,50 μs 脉冲宽度的Er:YAG 激光预处理牙本质是保持胶原纤维结构完整的最佳方案,300、600 μs 组则可见牙本质表面熔融、碳化,胶原纤维融合区消失,纤维间隙消失。Cersosimo 等[14]使用50 μs 脉宽Er:YAG 激光分别处理正常、脱矿牙本质,相对于未使用激光的球钻组,微剪切强度提高,认为使用短脉冲激光有利于改善牙本质的粘接性能。在临床中,必须优化激光参数来减少热效应,以避免对后续粘接产生负面影响。本研究在铒激光处理牙本质后,进行常规粘接处理,扫描电镜显示,不论是自酸蚀粘接处理或是全酸蚀粘接处理,100 mJ 及300 μs 的Er:YAG 激光组的牙本质表面均较100 mJ 及50 μs 的Er:YAG 激光组有很多的散在孔隙,这可能会影响混合层的粘接强度。由此推测,100 mJ 及50 μs 激光处理后的牙本质较100 mJ 及300 μs 激光处理组更利于粘接层形成。
本研究不仅探索Er:YAG 激光处理对牙本质表面下层化学组分及显微硬度的影响,同时研究涂布自酸蚀粘接系统及全酸蚀粘接系统后激光处理牙本质的表面形貌,更直观地探讨Er:YAG 激光蚀刻及球钻处理后哪种粘接系统效果更优。对使用不同粘接系统后形成的粘接界面进行电镜扫描的结果显示,涂布自酸蚀粘接系统后50 μs 激光组的牙本质表面可见粗糙的粘接界面,球钻组表面见少量粗糙的突起物,直接涂布全酸蚀粘接系统后所有组表面均见均匀的粘接界面,而在自酸蚀粘接系统或磷酸蚀刻后涂布粘接剂时,相对于磷酸蚀刻后涂布全酸蚀粘接系统,自酸蚀粘接系统或直接涂布全酸蚀粘接系统在与铒激光处理后牙本质结合中提供了更好的粘接性能。牙本质粘接的基础是形成混合层并产生微机械固位力。Ramos 等[9]得到全酸蚀粘接组粘接强度明显低于自酸蚀组,推测可能是由于铒激光处理后牙本质胶原纤维变性融合,间隙缩小,影响磷酸接触牙本质,阻碍粘接剂渗透至脱矿全层。Oliveira 等[15]得到两种自酸蚀粘接剂(clearfil protect bond,clearfil tri-s bond)粘接强度均高于全酸蚀粘接剂(single bond plus),且水保存6 个月后,粘接强度未降低,推测可能是由于两种自酸蚀粘接剂均含有10-甲基丙烯酰氧基磷酸二氢(10-MDP),其与羟基磷灰石发生化学反应,形成稳定持久的粘接。
Er:YAG 激光作为一种龋病治疗的微创手段,有着良好的发展前景,但目前仍不能完全替代传统牙科手机[16],然而可以考虑作为现今牙本质表面处理方式的替代,以往研究总体上都证实牙本质表面粘接性能的提升可以由Er:YAG 激光辐照来实现[17]。本研究证实,经参数为100 mJ 及50 μs的Er:YAG 激光处理后,牙本质表面结构发生改变,更有利于粘接,这种改变与钙磷比例无显著相关。深入研究Er:YAG 激光照射后牙本质的结构特性,本质是为了探索适用于激光处理后牙本质的粘接方法,进而提高牙本质修复效率。本研究仅仅对激光照射牙本质表层性状进行了初步的研究,显微硬度的提高是否更有利于粘接、牙本质深层结构的热损伤机制以及其对后续粘接修复的影响还需进一步探索。
