微流控液滴模板法可控构建功能微颗粒材料
2021-01-30苏瑶瑶李平凡汪伟巨晓洁谢锐刘壮褚良银
苏瑶瑶,李平凡,汪伟,2,巨晓洁,2,谢锐,2,刘壮,2,褚良银,2
(1 四川大学化学工程学院,四川成都610065; 2 四川大学高分子材料工程国家重点实验室,四川成都610065)
引 言
以功能材料为主导的新材料产业,被公认为是全球最重要、发展最快的高新技术产业之一。其中,功能微颗粒材料由于具有微型化、多功能化等诸多优点,而被广泛用于化工、医药、生物、电子等领域,应用前景非常广阔。微颗粒材料的微观空间结构和材料化学组成对其功能特性具有至关重要的作用。例如,具有多孔结构的微颗粒可以提供多孔限域空间用于药物或相变材料包埋[1-2]以及细胞黏附和增殖[3],亦可以提供大的功能比表面积用于物质的吸附[4-5],因而其在药物递送、相变储能、吸附分离等领域具有广泛应用。而具有腔室结构的微颗粒则可以提供封闭的腔室空间用于活性物质(如药物、酶等)的封装保护,并通过囊壁中功能组分的物化性质变化来实现封装物的可控释放[6-7],因而其在物质封装、控制释放、固定化酶反应等领域具有重要作用。除了微观结构和组成外,微颗粒的功能特性亦取决于微颗粒的尺寸、形状和均一性。例如,均一的尺寸和形状对于微颗粒的组装和堆积特性、微颗粒中物质的封装量及其释放动力学等具有重要影响[8-11],且有利于使得每个微颗粒均具有相同的结构特征和功能特性。由此可见,可控构建具有特定尺寸、结构、组成和形状的微颗粒材料对于其功能特性的调控强化以及新功能特性的设计具有重要意义。然而,传统的微颗粒制备技术如沉淀聚合、喷雾干燥、层层自组装等,通常难以实现对具有均一可控尺寸,以及多样化结构、组成和形状的功能微颗粒的可控构建。相比于上述制备方法,自20世纪90 年代迅猛发展起来的微流控技术由于具有优良的流体界面操控能力,可在微尺度空间精确操控多相流体的流动和分散,从而可控构建多样化的微尺度乳液液滴体系[12-14];通过独立精巧设计乳液液滴体系中的多个液相和界面的结构和组成,可在乳液液滴微空间内精确调控其微观结构和组成,进而理性设计和可控构建多样化的新型功能微颗粒材料[6,15-17]。因此,微流控技术作为一种崭新的材料制备技术平台,已在基于乳液液滴体系来创新设计和可控构建功能微颗粒材料方面展现出传统技术无法比拟的创造性和优越性。
鉴于微流控技术在功能微颗粒材料设计构建方面展现出的独特优势,本文主要介绍了近年来基于微流控液滴模板法来可控构建功能微颗粒材料的研究新进展。文中主要关注于面向化工、医药、储能、环境等领域的多样化功能微颗粒材料;重点介绍了如何基于微流控乳液液滴模板的结构组分设计来理性设计和可控构建多孔结构球形微颗粒、腔室结构球形微颗粒以及多样化结构非球形微颗粒等功能材料;详细探讨了微颗粒的结构组成与其功能之间的构效关系;展望了微流控技术在创新设计和可控构建功能微颗粒材料方面的未来发展趋势,以期为具有特定功能的新型微颗粒材料的理性设计和可控构建提供科学指导。
1 微流控可控制备乳液液滴
1.1 微流控可控制备单乳液滴
微流控技术是在数十至数百微米的微小通道中处理或操纵微量体积(10-9~10-18L)流体的技术[18]。由于微流控技术可以在微尺度条件下精确操控多相流体的流动、分散、界面、传质、传热和反应等,因而在材料制备、分析检测、分离纯化等多个领域具有广阔的应用前景。特别在材料制备领域,微流控技术可控产生的具有多样化结构和组成的乳液液滴体系为设计和构建新型功能微颗粒材料提供了优良的模板。通常来说,微流控装置中乳液液滴的产生主要是利用不相溶液体间的剪切作用来实现。常见的用于制备乳液液滴的微流控装置主要包括具有3D微通道结构的微流控装置和2D微通道结构的微流控装置,其用于产生液滴的微通道结构主要有同轴共流动型结构(co-flow)、十字流动型结构(cross-junction)和T形流动型结构(T-junction)等[15]。
典型的具有3D 微通道结构的微流控装置主要由圆形玻璃毛细管和方形玻璃毛细管组装而成[13]。其中,圆形毛细管一端经加工后形成锥口,并插入方形毛细管内进行同轴组装。圆形玻璃毛细管的外径和方形玻璃毛细管的内径相匹配,从而保证了所组装的玻璃毛细管的共轴性。如图1(a)所示为具有同轴共流动型结构的玻璃毛细管微流控装置。当该装置用于乳液制备时,将作为分散相的一种液体由圆形毛细管中注入,而将作为连续相的另一种液体由方形毛细管与圆形毛细管之间的间隙处注入;当这两种互不相溶的液体同向流动至圆形毛细管的锥口处时,从锥口处流出的分散相液体将在连续相液体的剪切作用下断裂形成液滴。而典型的具有2D 微通道结构的微流控装置主要利用聚二甲基硅氧烷(PDMS)[19]、聚甲基丙烯酸甲酯(PMMA)、玻片[20-21]等作为基材,通过软光刻、精密铣削加工等技术在基材上构建微通道结构。如图1(b)所示为具有十字流动型结构的2D 微通道微流控装置;其中,分散相液体由微通道A 流入,而连续相液体则由微通道B 和C 流入;当这两种互不相溶的液体在十字形交汇处相遇时,分散相液体将在聚焦流动的连续相液体的剪切作用下断裂形成单分散的乳液液滴。如图1(c)所示为具有T字形流动型结构的2D微通道微流控装置;相似地,在该装置中由微通道B 流入的分散相液体将在T 字形交汇处受到微通道A 中的连续相液体的剪切作用,从而形成单分散的乳液液滴。由于乳液体系是热力学不稳定体系,为了提高其稳定性,通常需要在连续相液体中加入两亲性的表面活性剂或者纳米颗粒,使其排布于液相界面上起到降低界面张力、稳定液滴界面的作用。此外,在具有3D 微通道结构的玻璃毛细管微流控装置中,分散相液体从锥口流出后,其四周均被连续相液体环绕,不会接触到微通道壁面,因而一般不需要对玻璃毛细管微流控装置的微通道壁面进行亲疏水改性,即可方便地将其用于不同类型(如W/O 和O/W 型)乳液液滴的制备。而在具有2D 微通道结构的微流控装置中,分散相和连续相液体均会与微通道壁面相接触,为了更稳定地形成乳液液滴,需要根据所形成的乳液液滴类型(如W/O 或O/W 型)分别对微通道的不同部位进行选择性的亲疏水改性。
相比于传统的搅拌制乳法或者膜乳化法同时生成大量液滴的过程,在该微流控乳化过程中一次仅形成一个液滴,因而通过恒流泵或恒压泵分别调控连续相和分散相液体的流速,可以在微流控装置中形成尺寸可控的均一乳液液滴。通常使用偏差系数(CV 值)来描述液滴尺寸的单分散性,并将直径的CV 值小于5%的液滴认为是高度单分散的。利用微流控技术,能可控地产生尺寸从毫米尺度到亚微米尺度的单分散乳液液滴。而通过改变各液相流速或者玻璃毛细管中微通道的尺寸,还可以在保证单分散性的前提下,灵活调控液滴的尺寸。在微流控制备乳液液滴的过程中,各液相的物理性质、微通道的尺寸和几何结构以及工艺参数等均对液滴形成过程具有重要影响。比如,在同轴共流动型结构中,连续相液体的黏度(ηc)和流速(uc)、分散相液体的密度(ρd)和流速(ud)以及圆形玻璃毛细管的锥口尺寸(dtip)、连续相和分散相液体之间的界面张力(γ)等都是影响液滴尺寸及尺寸分布的重要因素。通常来说,随着微通道尺寸的减小以及连续相液体流速的增大,液滴的尺寸将逐渐减小;而随着分散相液体流速的增大,则液滴的尺寸将逐渐增大。同时,黏度和界面张力也是影响液滴形成的两个重要参数,因为微通道中液滴的形成涉及液滴上界面张力和剪切应力的平衡。通常,上述影响因素可以归结为两个典型的无量纲量,即毛细管数(Cc=ηcuc/γ)和Weber 数(Wd=ρddtipud2/γ);研究发现,这两个无量纲量影响了液滴形成过程中液滴流和喷射流两种乳液形成模式之间的转变[22-23]。在喷射流模式中,所形成的乳液液滴尺寸更小,但尺寸分布更宽、CV 值更大;而液滴流模式虽会形成较大的乳液液滴,但其尺寸分布更窄、CV值更小,单分散性更好[23]。
1.2 微流控可控制备多重乳液液滴
微流控技术在制备乳液液滴方面具有高度的可控性和可升级拓展特性。通过将用于产生液滴的同轴共流动型结构、十字流动型结构和T 形流动型结构等微通道结构进行组合连接,则可以操控更多种液相的流动和分散,从而制备具有液滴嵌套液滴结构的多重乳液液滴[12-13,21]。
如图1(d)所示为具有两个串联的同轴共流动型结构的两级玻璃毛细管微流控装置[13]。在该装置的第一级同轴共流动型微通道结构中,内相液体首先被中间相液体剪切形成单分散乳液液滴;该内相液滴随着中间相液体一同流入下一级同轴共流动型结构的圆形玻璃毛细管中,同时,携带内相液滴的中间相液体将在锥口处进一步被外相液体剪切形成液滴。此时,内相液滴将被封装入所形成的中间相液滴中,形成液滴包含液滴的双重乳液。类似地,当串联两个十字流动型结构时,所得到两级微流控装置亦能通过两步乳化过程制备双重乳液[图1(e)][21]。所制得的双重乳液中,内、外液滴的尺寸可分别通过调控各液相的流速来进行调控;同时,通过调控各液相流速来调节两级微通道结构中的液滴产生频率,可以精确控制双重乳液液滴所含的内部液滴数目。例如,当单位时间内产生的内相液滴的数目是中间相液滴数目的两倍时,所形成的每个双重乳液液滴中都将包含有两个内相液滴。
除了上述串联连接方式外,通过将用于液滴产生的微通道结构并联连接,再将该并联结构与另一个用于液滴产生的微通道结构串联连接,则可以组装构建得到用于制备内含不同组分液滴的双重乳液的模块化微流控装置。如图1(f)所示为将三个同轴共流动型结构作为液滴产生单元模块,通过其并联和串联组装构建的模块化微流控装置[12]。其中,通过Y字形微通道并联连接的两个同轴共流动型结构可用于并行产生两种不同组分的内相液滴;当这两种内相液滴经Y字形微通道汇流到下一级串联的同轴共流动型结构中时,其进一步被封装到所形成的中间相液滴中,从而制备得到内含两种不同内相液滴的多组分双重乳液。同样地,基于两级十字流动型结构微流控装置,通过利用第一级十字流动型结构的微通道A 和微通道B分别交替产生两种不同的内相液滴,再将其在第二级十字流动型结构中封装入中间相液滴中,亦可制备得到内含两种不同液滴的多组分双重乳液[图1(g)][21]。在上述多组分双重乳液中,通过调控各液相流速以及微通道尺寸,可以灵活调节双重乳液中不同种类液滴的数目、比例和尺寸。同时注意到,在图1(f)所示的微流控装置中,两个并联的液滴产生单元模块中产生的液滴分别是由该液滴产生单元模块中的中间相液体独立剪切而成的;而在图1(g)所示的微流控装置中,第一级十字形结构中两种液滴的形成则是由同一微通道中的同一种中间相液体剪切而成的。由于并联的液滴产生单元模块具有很好的独立性,因而可独立、灵活地调控并联的液滴产生单元模块中微通道的尺寸以及各液相的流速,来分别对其液滴产生过程进行调控。因此,相比于图1(g)所示的微流控装置,图1(f)所示的模块化微流控装置在调控双重乳液内部两种不同液滴的尺寸、数目和比例方面具有更大的独立性和灵活性。此外,通过在模块化微流控装置中进一步利用Y字形微通道并联更多的液滴产生单元模块,还可以在双重乳液中引入更多种的液滴,实现多样化多组分双重乳液的灵活可控制备[12]。进一步地,通过串、并联更多的微流控装置结构,还可以可控制备结构更为复杂的三重乳液、四重乳液、五重乳液等[12-13,19,24],因而微流控技术在乳液液滴可控构建方面展现出了传统乳液制备技术所无法比拟的独特性和创造性。
2 微流控液滴模板法可控构建多孔结构球形微颗粒
2.1 单一多孔结构球形微颗粒
多孔微颗粒在吸附、催化、控释、储能等诸多领域具有广泛应用。比如,在吸附分离方面,微颗粒的多孔结构可为目标分子与微颗粒之间的相互作用提供大的功能比表面积;在相变储能方面,微颗粒的多孔结构可用于相变材料的限域分隔封装,以有效抑制相分离和过冷度;在药物控释方面,微颗粒的多孔结构可有效调控微颗粒中所装载药物分子的释放传质速率;在催化反应方面,微颗粒的多孔结构可为催化剂的负载以及反应物与催化剂之间的接触提供大的功能比表面积等。通常来说,通过将用于构建微颗粒的材料溶解或分散到液相中,由微流控技术制得均一乳液液滴,则可作为合成功能微颗粒的模板。由于微流控技术可以灵活操控水溶液和不同油相溶液(如有机溶剂等)等多种液相来制备均一乳液液滴,因而大部分的水溶性或油溶性材料可溶解于液相中来制备乳液液滴模板。而对于不能溶解于液相的材料(如无机功能纳米颗粒),则可以通过基于超声处理、表面活性剂修饰、表面电荷修饰等方法将其有效分散于液相中用于制备乳液液滴模板。由于基于微流控技术制备的乳液液滴在微空间上具有可控的相分离结构,因此其在作为微颗粒的合成模板时,可通过分隔的油相、水相以及两相间的界面来实现不同功能材料在液滴中的精确分布,从而可控构建不同结构、组成和功能的微颗粒材料[15-17]。一般来说,图1中所示的几种不同结构的微流控装置均可用于制备乳液液滴模板,但是在此过程中还应考虑微流控装置材料对所用液相或材料(如有机溶液)的耐受性。比如,基于PDMS 的微流控装置容易被乙醇、二氯甲烷等有机溶剂溶胀甚至溶解;而玻璃毛细管微流控装置则对有机溶剂具有较好的耐受性。当选用合适的微流控装置制得乳液液滴模板后,可进一步通过基于界面传质过程的交联反应、基于紫外光照或者热引发的自由基聚合反应以及基于溶剂交换或溶剂挥发的高分子沉积过程等多样化的物理化学过程来将乳液液滴转化为功能微颗粒,实现功能微颗粒的可控模板合成[15-17]。对于快速的液滴固化过程(如仅需数秒或者几分钟),可以通过调控连续流动的液滴在微通道中的停留时间来在线合成得到功能微颗粒;而对于较慢的液滴固化过程(如需几十分钟甚至数小时),则可通过将微流控装置产生的乳液液滴收集到容器中后,再经缓慢的固化过程制得功能微颗粒。
在制备功能微颗粒的基础上,通过将自组装的表面活性剂胶束或嵌段高分子[25-27]、胶体颗粒[28]、液滴[5,29]、气泡[30]、细菌[31]、微球[32]等作为致孔模板加入到液相中来制备乳液液滴,则可以构建得到具有纳米尺度或微米尺度孔径的多孔结构的功能微颗粒。比如,通过微流控技术将含有致孔模板(如两亲分子组装形成的胶束、纳米颗粒或者液滴、微米颗粒或液滴等)的液相乳化为单分散乳液液滴,再经乳液液滴固化为微颗粒后,则可构建得到孔径与致孔模板相近的多孔结构功能微颗粒。Mou 等[29]以内含均质乳化的微小油滴的(O/W)/O 乳液液滴作为模板,通过将乳液液滴收集至容器中后,再由紫外光照引发乳液液滴内N-异丙基丙烯酰胺(NIPAM)单体发生自由基聚合反应,首先构建了含有大量微小油滴的聚N-异丙基丙烯酰胺(PNIPAM)微颗粒;然后,利用PNIPAM 微颗粒的温敏体积相变特性,通过升温使其PNIPAM 高分子网络发生收缩以挤出内部包载的微小油滴,从而制得了具有类似海绵的开放式多孔结构微颗粒[图2(a)]。在构建(O/W)/O 乳液液滴模板的过程中,为了稳定乳液内部大量的微小油滴的界面,在油滴相和水相中分别加入了表面活性剂聚甘油蓖麻醇酸酯和Pluronic F127,从而使得微小油滴不易合并,以便用于构建微颗粒内的多孔结构。相比于不具备多孔结构的PNIPAM 微颗粒,由于多孔结构为微颗粒体积相变过程中水分子在PNIPAM 高分子网络中的传递提供了快速传质通道,因此上述多孔结构PNIPAM 微颗粒均可展现出更快的体积收缩/溶胀行为,实现了对功能微颗粒响应速率的强化。
Li 等[1]基于微流控技术产生的单分散W/O 乳液液滴,通过利用液滴中自组装的两亲分子作为致孔模板,经界面水解/缩合反应可控构建了封装有Na2SO4·10H2O的相变储能多孔结构SiO2微颗粒[图2(b)]。该微颗粒的介孔结构可有效用于Na2SO4·10H2O 相变材料的限域分隔封装;同时,结合介孔结构内封装的少量成核剂硼砂和晶习改变剂六偏磷酸钠,该微颗粒可有效抑制Na2SO4·10H2O 相变过程中的过冷度大和相分离的问题,从而实现温和温度下的重复储能和释放。进一步地,Li 等[33]基于上述微流控制备策略,先利用内含磁性Fe3O4纳米颗粒的W/O 乳液液滴构建磁性介孔SiO2微颗粒,再利用多巴胺的黏附性和还原性在微颗粒底部涂覆多巴胺并还原得到Ag纳米颗粒,从而制得了自驱动型多孔SiO2微颗粒[图2(c)]。该微颗粒底部的Ag 纳米颗粒可以分解水中的H2O2产生O2气泡,从而推动微颗粒向反方向快速运动,促进水中的混合传质;同时,微颗粒多孔结构中的Fe3O4可催化H2O2分解产生具有强氧化性的·OH 自由基,并通过Fenton 反应实现对水中有机污染物罗丹明B的快速有效降解。

图2 微流控制备单一多孔结构球形微颗粒。具有海绵状开放式多孔结构的PNIPAM微颗粒(a)[29];封装Na2SO4·10H2O的介孔SiO2微颗粒(b)[1];用于水中污染物催化降解的自驱动型磁性介孔SiO2微颗粒(c)[33]Fig.2 Microfluidic fabrication of porous spherical microparticles.PNIPAM microparticles with sponge-like open-celled porous structures(a)[29].Mesoporous SiO2 microparticles encapsulated with Na2SO4·10H2O(b)[1].Self-propelled mesoporous SiO2 microparticles for catalytic degradation of pollutants in water(c)[33]
2.2 分级式多孔结构球形微颗粒
相对于采用单一致孔模板来构建单一多孔结构微颗粒,通过在微颗粒制备过程中耦合两种不同的致孔模板,则可以构建得到具有不同尺度孔结构的分级式多孔结构微颗粒。相比于仅具有单一尺度孔结构的多孔微颗粒来说,具有分级式多孔结构的微颗粒有望有效耦合不同尺度孔结构的特点来实现性能强化。比如,纳米级尺度的孔结构可为微颗粒与物质分子之间的相互作用提供大的功能表面积,而微米级尺度的孔结构则可为物质分子在多孔结构中的传递提供快速传质通道。通过将纳米级尺度的孔结构与微米级尺度的孔结构结合,可以在增大功能表面积的同时又强化传质过程,从而使得微颗粒获得更好的综合性能。基于微流控液滴制备技术,通过在乳液液滴中采用双重模板致孔策略,可以实现分级式多孔结构功能微颗粒的可控构建。Zhang 等[4]利用均质乳化得到的O1/W 乳液作为分散相,由微流控技术制得(O1/W)/O2乳液液滴作为模板,通过水解/缩合反应构建了尺寸均一的磁性分级式多孔SiO2微颗粒[图3(a)、(b)]。同样地,在该乳液液滴模板的O1相和W 相中分别加入了表面活性剂聚甘油蓖麻醇酸酯和Pluronic F127来稳定微小油滴的界面。同时,在该乳液液滴中,采用了该均质乳化的微小O1液滴和自组装的表面活性剂胶束分别作为致孔模板,用于构筑微颗粒中的大孔结构和介孔结构。该微颗粒中的介孔结构可为水中污染物分子的吸附提供大的功能比表面积,而其孔径为几百纳米的大孔结构则可为污染物分子向多孔结构内部的快速传质提供便利的通道。因此,该分级式多孔结构微颗粒可有效耦合不同尺度多孔结构的特点,展现出比仅具有介孔结构的SiO2微颗粒更快的吸附性能,实现了对水中有机染料(如亚甲基蓝)[图3(c)]和重金属离子(如Pb2+)的有效吸附。
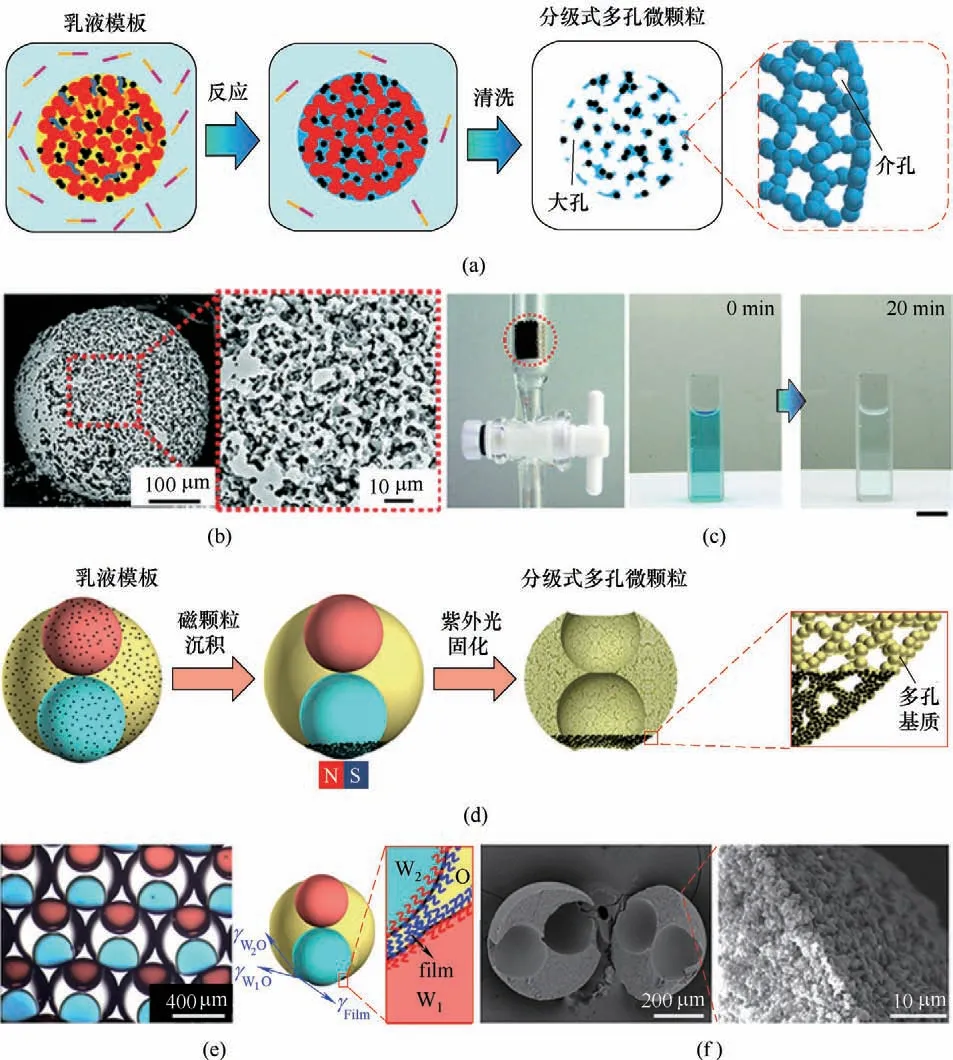
图3 微流控制备分级式多孔结构球形微颗粒。磁性分级多孔SiO2微颗粒[(a),(b)]及其对水中亚甲基蓝染料的吸附(图中标尺为1 cm)(c)[4];以可控演化的双重乳液为模板[(d),(e)]构建的分级式多孔聚合物微颗粒及其断面多孔结构(f)[34]Fig.3 Microfluidic fabrication of hierarchical porous spherical microparticles.Magnetic hierarchical porous SiO2 microparticles[(a),(b)]and their adsorption of methylene blue dyes in water(scale bar is 1 cm)(c)[4].Controllably evolved double emulsions[(d),(e)]for template synthesis of hierarchical porous SiO2 microparticles and the porous structures in their cross-section(f)[34]
Su等[34]以两级微流控装置产生的内含不同液滴的(W1+W2)/O/W1双重乳液为初始模板[图3(d)],通过液相密度差和界面黏附能诱导乳液内部两个微米级水滴垂直排列并发生反浸润[图3(e)],同时使外部水相在油相中过量表面活性剂作用下跨界面传质至油相中形成纳米水滴,最后经磁铁诱导Fe3O4@Ag纳米颗粒沉积至双重乳液底部,从而实现了双重乳液的可控演化。基于该可控演化的双重乳液,通过以微米水滴和纳米水滴分别作为致孔模板,一步连续可控构建了底部结合有Fe3O4@Ag 纳米颗粒的自驱动型分级式多孔聚乙氧基化三羟甲基三丙烯酸酯(PETPTA)微颗粒[图3(f)]。该微颗粒可以利用其底部的Fe3O4@Ag 纳米颗粒分解水中的H2O2产生O2气泡,推动微颗粒向反方向运动,从而通过溶液中的混合传质强化增强微颗粒对水中污染物如有机染料(亚甲基蓝)和重金属离子(Pb2+)的吸附。Chen等[35]以含有磁性Fe3O4@Ag 纳米颗粒和光催化特性ZIF-8@ZnO 纳米颗粒的O/W 乳液液滴作为模板,可控构建了能有效催化降解水中污染物的自驱动型分级式多孔PETPTA微颗粒[图4(a)]。乳液液滴中的ZIF-8@ZnO 纳米颗粒可在界面能驱使下向液滴表面迁移,而Fe3O4@Ag纳米颗粒则可在外加磁场作用下定向沉积至液滴底部;而在乳液液滴中过量表面活性剂作用下,外相水分子可跨界面扩散至乳液内形成纳米水滴作为致孔模板。因此,以此乳液液滴作为模板合成的微颗粒具有分级式多孔结构,其第一级大孔结构主要源自于纳米水滴致孔模板,而第二级微孔结构则源自于ZIF-8@ZnO 纳米颗粒的多孔结构。该微颗粒的表面和底部分别结合有ZIF-8@ZnO和Fe3O4@Ag纳米颗粒,可有效耦合气泡驱动运动的混合传质强化效应[图4(b)]、ZIF-8@ZnO 对污染物分子的吸附富集作用以及ZIF-8@ZnO 和H2O2/UV 的光催化降解性能,实现对水中有机污染物的高效协同降解[图4(c)]。
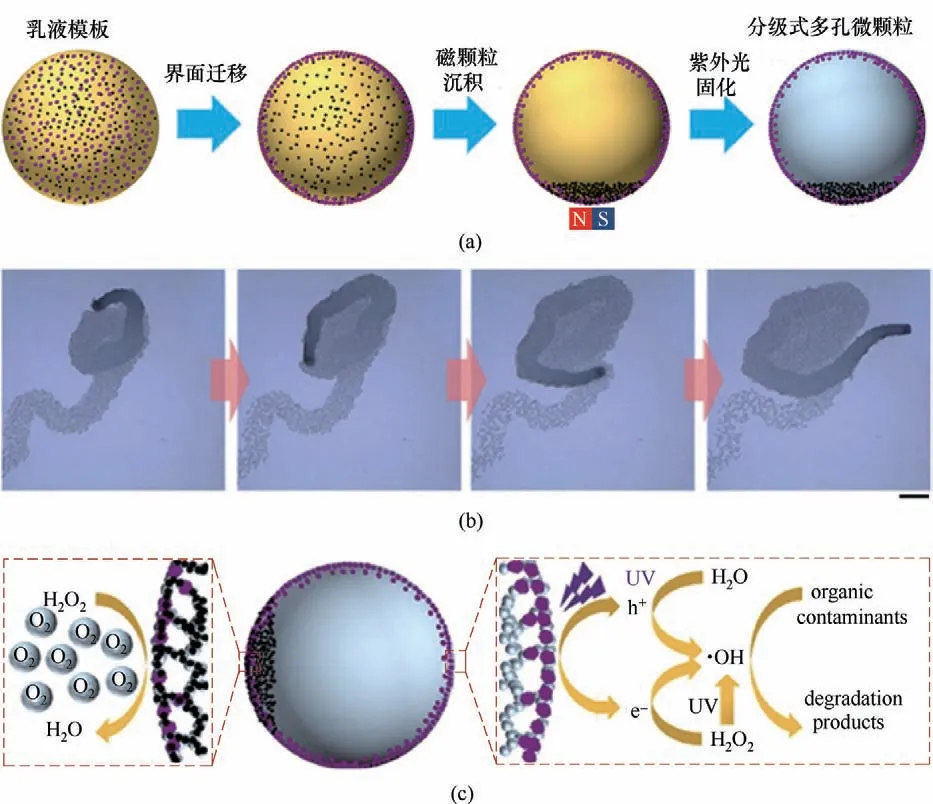
图4 微流控制备自驱动型分级式多孔微颗粒[35]。自驱动型分级式多孔微颗粒的制备过程(a),气泡驱动运动(标尺为1 mm)(b),以及其光催化降解水中污染物(c)Fig.4 Microfluidic fabrication of self-propelled hierarchical porous microparticles[35].Fabrication process(a),and bubble-propelled motion(scale bar is 1 mm)(b)of the hierarchical porous microparticles,and their photocatalytic degradation of pollutants in water(c)
3 微流控液滴模板法可控构建腔室结构球形微颗粒
3.1 单腔室结构球形微颗粒
具有物质封装和释放功能的单腔室结构微颗粒被广泛用于物质封装保护、药物控释、分析检测、微型反应等领域[6,15-17]。在单腔室结构微颗粒中,物质的封装和释放性能主要取决于其腔室结构和囊壁结构及其功能性。通过在微颗粒中构建中空结构或者液核作为腔室,可以实现亲水性或者亲油性物质的封装保护,而通过调控囊壁组成、结构、厚度和功能性,则可以实现对封装物质的可控释放。通常地,腔室结构微颗粒可以通过高分子自组装和相分离以及基于液滴或者颗粒模板的层层组装过程来实现。然而,传统的制备方法往往难以实现对于微颗粒尺寸以及腔室结构的精确调控,且其材料选择范围受到一定限制。微流控技术产生的尺寸、结构和组成精确可控的乳液液滴为腔室结构微颗粒的可控构建提供了优良的模板。比如,通过以尺寸高度单分散的单乳液滴作为模板,可以通过液滴表面的界面反应构建囊壁,从而制备得到均一的中空单腔室结构微颗粒;而基于单分散的双重乳液模板,则可以利用其“液滴包裹液滴”的微相分离结构,通过将外部液滴固化为囊壁、内部液滴作为液核腔室,从而制备得到均一的核壳型单腔室结构微颗粒。由于微流控技术可以灵活操控多种具有不同组成、密度、黏度和界面张力的液相的流动和分散,因此,诸如高分子、有机/无机纳米颗粒、生物活性物质(如蛋白质)等材料均可以用于腔室结构微颗粒的可控构建。同时,通过微流控技术独立、精确地调控液滴的尺寸、结构和组成,还可以实现对于腔室尺寸、封装物含量、囊壁厚度及功能性的灵活调控。
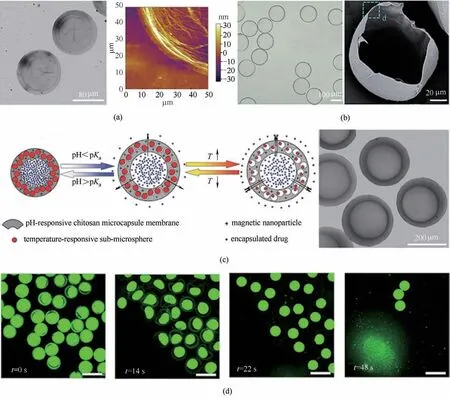
图5 微流控制备单腔室球形微颗粒。具有纳米级囊壁的单腔室壳聚糖微颗粒(a)[36];具有纳米级囊壁的单腔室APSi微颗粒(b)[7];具有多重刺激响应性释药功能的单腔室壳聚糖微颗粒(c)[37];具有梯级次序式释药功能的单腔室壳聚糖微颗粒(标尺为500 μm)(d)[38]Fig.5 Microfluidic fabrication of spherical microparticles with single compartment.Single-compartmental chitosan microparticles with nanometer-sized shell thickness(a)[36].Single-compartmental APSi microparticles with nanometer-sized shell thickness(b)[7].Single-compartmental chitosan microparticles with multi-responsive drug release (c)[37].Single-compartmental chitosan microparticles with sequential drug release(scale bars are 500 μm)(d)[38]
Mu 等[36]以微流控技术产生的单分散O/W 乳液液滴为模板,通过连续水相中的壳聚糖(CS)分子与液滴中的对苯二甲醛在液滴界面处发生交联反应,可控构建了具有超薄囊壁(厚度<10 nm)的单腔室结构壳聚糖微颗粒[图5(a)]。通过调节交联反应时间、反应物浓度和水相黏度,可以在2.8 ~8.0 nm 的范围内灵活调控微颗粒的囊壁厚度。以茶树油作为代表性物质研究该微颗粒的释放性能发现,由于微颗粒的超薄壳聚糖囊壁具有较小的传质阻力,因此其可快速释放内部封装的茶树油分子;并且,通过将囊壁厚度由4.3 nm 减少为3.1 nm 时,其初始释放速率可进一步提升为原来的两倍。Wu 等[7]基于微流控W/O 乳液液滴构建的海藻酸钙微颗粒,通过两步生物硅化过程在微颗粒表面结合鱼精蛋白/二氧化硅壳层,从而可控构建了囊壁厚度约为420 nm 的单腔室海藻酸盐/鱼精蛋白/二氧化硅(APSi)微颗粒[图5(b)]。该微颗粒可以实现对活性物质牛血清白蛋白的高效封装(封装率约为99%)。此外,由于其纳米级壳层的快速传质性能,该微颗粒可高效封装漆酶用于快速酶反应,且可展现出优良的酶储存特性和重复利用性能。
双重乳液具有液滴包封液滴的分层结构,其独特的核壳型微相分离结构为单腔室结构微颗粒的构建提供了良好的模板。典型地,通过将双重乳液中含有功能材料的外层液滴固化为囊壁,则可构建出具有腔室结构的微颗粒。Wei 等[37]通过在O/W/O双重乳液的中间水层中加入壳聚糖分子、PNIPAM亚微米颗粒以及磁性Fe3O4纳米颗粒,并利用界面交联反应将水层中的壳聚糖分子凝胶化,从而可控构建了具有多重刺激响应性药物控释功能的单腔室结构壳聚糖微颗粒[图5(c)]。该微颗粒的壳聚糖囊壁可以响应环境pH 的变化而发生溶胀或收缩,从而改变囊壁渗透性、调控内部封装药物的跨膜传质释放速率;同时,其囊壁内嵌入的PNIPAM 亚微米颗粒可响应环境温度的变化而发生溶胀或者收缩,从而进一步改变囊壁渗透性。结合两种调控机制,可以实现对微颗粒内封装药物分子的控释速率的多样化组合调控。此外,由于微颗粒囊壁中的Fe3O4纳米颗粒具有超顺磁性,通过外加磁场可实现载药微颗粒的靶向运输。Yang 等[38]利用微流控产生的O/W/O 双重乳液作为模板,通过界面交联反应可控构建了具有次序式释药功能的单腔室结构壳聚糖微颗粒。该微颗粒由外层的壳聚糖水凝胶囊壁和内部的油核组成;油核中含有游离的药物分子以及负载有药物的聚乳酸-羟基乙酸共聚物(PLGA)纳米颗粒。该微颗粒的壳聚糖壳层可在酸性条件下溶解,从而在短时间(约60 s)内迅速释放出内部油滴及其包封的游离药物分子和载药型PLGA 纳米颗粒[图5(d)];接着,由于PLGA 纳米颗粒逐渐降解,其内部封装的药物分子在接下来的几天时间内缓慢释放。这种单腔室结构壳聚糖微颗粒不仅可实现不同药物的协同封装,还可实现不同释放模式的耦合,其酸触发的次序式药物控释功能在急性胃炎治疗方面具有良好的应用前景。
3.2 多腔室结构球形微颗粒
多腔室结构微颗粒可以为多种不相容活性物质在单个微颗粒中的独立共封装提供分隔的腔室,从而有效避免交叉污染,因而其在肿瘤治疗[39-40]、组织再生[41]以及限域酶反应[42]等方面具有重要作用。例如,在癌症组合治疗中,通过协同递送两种或更多种能协同作用的药物(如药物和基因[39]),可以获得比每种药物单独给药时的总疗效更好的综合疗效。而在限域酶反应方面,相比于将不同酶混合封装于微载体中,通过将不同的酶分别封装在微载体的分隔腔室中,可获得更好的酶活性和稳定性[42]。在多腔室结构微颗粒中,通过调控其外部囊壁的组成结构和功能性,可以实现封装物质的多样化释放模式;而通过调控其腔室结构、微颗粒尺寸和均一性,可以精确调控物质封装的化学计量比和释放动力学以获得最佳疗效[8,43]。通常来说,具有多腔室结构的微颗粒可以通过基于液滴或者颗粒模板的多步组装过程来制备[44-46],但这些方法往往涉及多个复杂的制备步骤,且其难以精确控制微颗粒的尺寸及其多腔室结构(如内部腔室的数目、尺寸等)。通过微流控技术可控产生内含不同液滴的双重乳液和具有更高级分级结构的多重乳液,可以为具有多样化多腔室结构微颗粒的可控构建提供优良的模板。基于微流控技术对于乳液内部液滴尺寸、数目和组成的精确调节,可以实现对微颗粒内部腔室尺寸、数目和封装物的精确调控,以及对腔室囊壁尺寸、结构和功能的精确调控。Wang 等[12]基于其开发的用于可控制备多组分多重乳液的模块化微流控技术,可控产生了内含不同液滴的O/W/O 双重乳液作为模板,并进一步以该乳液液滴为模板构建了具有可控协同封装和热触发协同释药功能的多腔室微颗粒[图6(a)][47]。该微颗粒利用了双重乳液内部所含的不同组分油滴作为分隔腔室分别封装不同的油溶性物质,同时,这些油滴均由同一层温敏性PNIPAM 水凝胶囊壁包裹。通过利用微流控技术精确调控双重乳液内部不同组分油滴的数目、比例和尺寸,可以精确调控不同组分在同一个微颗粒中的含量,从而优化其封装剂量。而当环境温度升高时,微颗粒的温敏性囊壁发生收缩,从而将内部不同的油核一并释放出来,实现对不同封装物质的协同释放。
除了利用内含不同液滴的双重乳液来构建上述具有平行多腔室结构的微颗粒外,通过利用微流控技术制备结构更为复杂的多重乳液液滴,还可实现具有同心多腔室结构的微颗粒的可控构建。相比于平行多腔室结构微颗粒在单一刺激下的一次性协同释放模式,同心多腔室结构微颗粒可以通过对不同囊壁的功能设计,实现封装物的梯级次序式释放,这种次序式释放模式可在癌症化疗中获得更好的疗效和更低的毒性副作用[48-49]。Mou 等[50]利用多级微流控装置制得了具有多层液滴嵌套结构的(O1/W2)/O3/W4/O5四重乳液,该乳液最内部含有经均质乳化得到的微小O1油滴。以该四重乳液作为模板,通过将其W2相水滴中的壳聚糖和W4相水滴中的N-异丙基丙烯酰胺单体分别由界面交联和紫外光照引发聚合,从而可控构建得到了具有“微囊包裹微球”结构的同心多腔室微颗粒[图6(b)]。该多腔室微颗粒的温敏性PNIPAM 囊壁中包含有O3油滴,而油滴中封装有一个含有多个微小O1油滴的壳聚糖微球。当环境温度升高时,其PNIPAM 囊壁会迅速收缩,并首先将O3油滴以及壳聚糖微球一并释放出来。随后,当环境pH 降低时,壳聚糖微球进一步降解,从而将最内部的多个微小O1油滴释放出来,实现对于不同封装物质的梯级次序释放。进一步地,Mou 等[24]利用微流控可控产生的O1/W2/O3/W4/O5四重乳液为模板,通过将其W2相和W4相水滴中的功能组分分别转化为功能性囊壁,构建得到了具有特洛伊木马式“微囊包裹微囊”结构的同心多腔室微颗粒[图6(c)]。当选择不同的功能材料用于构建其内、外层囊壁时,可以实现不同刺激响应条件下O1相和O3相中封装物的梯级次序释放。如图6(d)所示为具有内、外两层壳聚糖囊壁的壳聚糖@壳聚糖多腔室微颗粒,该微颗粒可以在外界酸刺激下使得外层和内层壳聚糖囊壁先后溶解,从而依次释放其O3相液滴和O1相液滴。如图6(e)所示为具有内层壳聚糖囊壁和外层PNIPAM 囊壁的壳聚糖@PNIPAM多腔室微颗粒,该微颗粒可首先在热刺激下释放内部的O3相液滴和壳聚糖微囊,并进一步在酸刺激下释放最内部的O1相液滴。由此可见,通过巧妙选择功能材料用于构建其内、外囊壁,可以实现多种释放模式在同一微颗粒中的灵活组合。此外,在上述多腔室微颗粒的制备过程中,多重乳液的界面稳定性对于微颗粒多腔室结构的成功构建具有重要影响。由于多重乳液模板中涉及多个界面,且模板合成微颗粒时界面反应和传质等过程会对界面稳定性产生影响,因而需要调控多重乳液各液相中的表面活性剂的种类和含量以及各液相的黏度和密度等物性,从而保证微颗粒制备过程中多重乳液的界面稳定性,以成功合成多腔室微颗粒[24]。
4 微流控液滴模板法可控构建多样化结构非球形微颗粒
4.1 非球形微颗粒
相比于球形微颗粒,非球形微颗粒材料由于其独特的形状而具有独特的新功能,因而在药物递送[51]、组织工程[52]、吸附分离[5]等方面亦展现出了非常重要的作用。例如,由嵌段共聚物自组装得到的圆柱状微颗粒在啮齿动物血液循环中的停留时间比球形微颗粒长10 倍以上[51];而在填充堆积方面,非球形微颗粒可展现出比球形微颗粒更高的堆积密度[53]。在以液滴作为模板来制备微颗粒时,由于界面张力的作用总是使液滴尽可能地维持其球形形状,以使系统处于较低界面能的状态;因此,传统的基于液滴模板的微颗粒制备方法通常难以获得尺寸均一的非球形颗粒。微流控技术由于能精确地操控微尺度流体的流动和分散,并且能精确地调控乳液液滴的尺寸、结构、组成,因而其可以通过调节微通道尺寸形状、液相流动状态、液相界面能量等方式来控制球形乳液液滴的可控形变[54-58]。以可控形变后的液滴作为模板来合成微颗粒,则可以得到具有相应尺寸、结构和形状的非球形微颗粒。此外,由于微流控产生的液滴模板具有均一的尺寸和体积,因而变形后的液滴亦具有相应的均一形状和尺寸,由此可构建得到均一的非球形颗粒。Cai等[55]通过微通道内液相流动调控来改变连续液相对单乳液滴的剪切力,使得液滴变形为心形,从而通过微通道内在线紫外光照聚合得到心形实心微颗粒;而通过减小微通道尺寸来进一步对液滴的形变进行空间限制,则可模板合成得到具有子弹形状的实心聚乙二醇二丙烯酸酯(PEGDA)微颗粒[图7(a)、(b)]。基于该液滴形变调控机制,通过在微通道内产生双重乳液液滴,还能可控制备得到分别具有一个和两个内部腔室结构的子弹形微颗粒[图7(c)]。相比于球形微颗粒,子弹形微颗粒可以展现出更好的微通道阻塞效果,其在栓塞治疗方面具有良好的应用前景。Wang 等[57]利用微流控技术制得内含单体油滴的聚乙烯醇微纤维,再通过对微纤维进行干燥、拉伸等处理来对内部油滴施加挤压作用,实现了单体油滴不同程度的可控形变。以变形后的油滴作为模板,通过紫外光照聚合和聚乙烯醇降解,从而可控构建得到了饼状、棒状等不同形状的非球形实心聚二甲基丙烯酸乙二醇酯(PEGDMA)微颗粒[图7(d)]。
除了利用外部作用力使得乳液液滴发生可控形变外,通过调控双重乳液体系自身的界面能,亦可以实现乳液液滴在界面能驱使下的可控形变。Wang 等[59]基于微流控可控产生的W/O/W 双重乳液模板,提出了一种基于界面黏附能调控来实现双重乳液由球形向橡子形可控演化、进而构建非球形微颗粒的新策略。在该双重乳液体系中,当改变油相中苯甲酸苄酯和丙烯酸酯类光聚合单体的比例时,双重乳液中间油相与内、外水相之间的界面张力发生改变,从而使得双重乳液内、外油/水相界面间的黏附能发生变化。此时,在界面黏附能驱使下,双重乳液内、外液滴的油/水界面将发生黏结,使得内部水滴从中间油滴中凸出来,而双重乳液则由球形可控演化为橡子形[图7(e)]。通过调节界面张力,可以调控内部水滴的凸出程度,从而得到不同橡子形的双重乳液。以可控演化后的双重乳液为模板[图7(f)],经紫外光照引发其油相中的丙烯酸酯类单体聚合,则可以得到具有相应形状的非球形PETPTA 微颗粒[图7(g)]。类似地,Zhang 等[5]通过W/O/W 双重乳液体系的界面能调控,并结合其中间油相与水相间的溶剂交换过程,得到了可控演化的非球形W/O/W 双重乳液。同时,通过在该双重乳液油相中使用过量的表面活性剂,使得水相中水分子跨界面传质至油相中形成纳米液滴作为致孔模板,最终以该演化后的双重乳液为模板构建了具有分级式多孔结构的非球形聚甲基丙烯酸甲酯共聚二甲基丙烯酸乙二醇酯(poly(MMA-co-EGDMA))微颗粒。通过改变内部水滴的大小和数量,可以调控双重乳液演化后的非球形形态,并由此分别构建得到具有相应结构的非球形微颗粒[图7(h)]。这种具有分级式多孔结构的非球形微颗粒,可以展现出比仅具有纳米尺度多孔结构的球形微颗粒更快的蛋白分子吸附性能,其在物质吸附分离方面具有良好的应用前景。
4.2 螺旋形微颗粒
螺旋形微颗粒能在旋转磁场驱动下将其在液体(如水或血液)中的旋转运动转化为前进或后退的定向运动。这种独特的旋转推进运动可以用于微小货物的装载和释放[60]、液体的混合和泵送[61]、pH遥感[62]、组织细胞穿刺[52]以及肿瘤温热治疗[63]等,在生物医学工程领域显示出独特的应用前景。通常来说,螺旋形微颗粒可通过3D 激光直写技术[60]、微流控液相模板合成技术[54,56-57]或者基于牺牲基材上沉积/生长的多层金属的弯曲[64]来构建。其中,微流控液相模板合成技术主要通过微流控技术对液流或者液滴形状结构的精确操控来实现对于螺旋形微颗粒的可控模板合成。Tang等[56]基于微通道内液流的卷绳效应,首先利用微流控技术可控产生卷曲液流模板,制得了内含磁性Fe3O4纳米颗粒的螺旋形海藻酸钙微纤维[图8(a)]。值得注意的是,由于卷曲液流模板主要是利用具有较大黏度差的两种水相来构建,其水/水界面和卷曲结构均难以长时间稳定,因而需要通过快速交联反应来固定住液流模板的卷曲结构,从而构建螺旋形微纤维。接着,通过将该磁性螺旋形微纤维切割成段后,再利用两步生物硅化过程构建得到了具有中空结构的磁性螺旋形APSi微颗粒[图8(a)]。
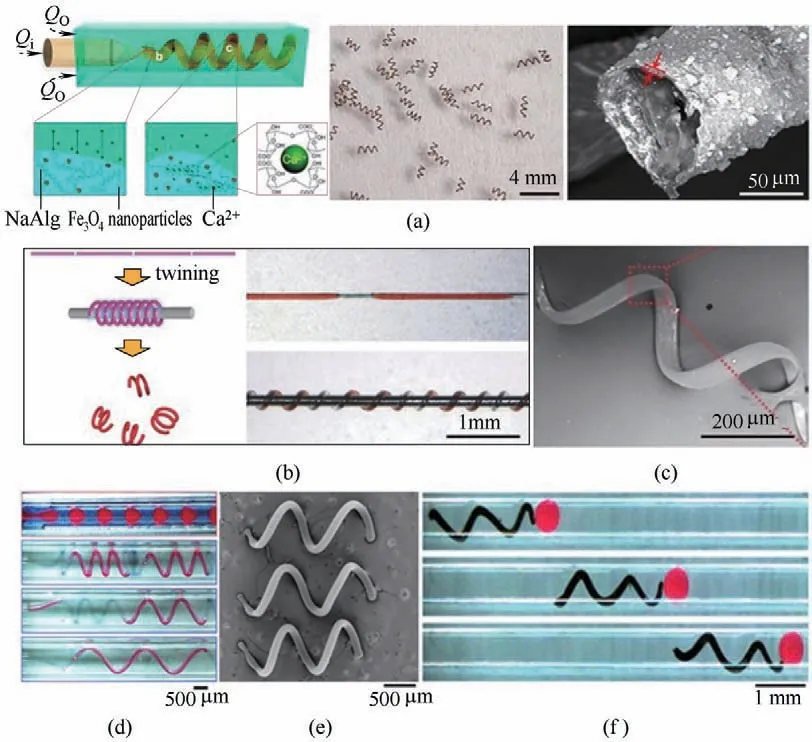
图8 微流控制备螺旋形微颗粒。基于微通道中液流卷曲效应可控构建螺旋形微颗粒(a)[56];基于微纤维中液滴拉伸卷曲变形(b)可控构建螺旋形微颗粒(c)[57];基于微通道中内含液滴的液流的卷曲效应(d)可控构建螺旋形微颗粒(e),及旋转磁场中螺旋形微颗粒对微通道里微球的运输(f)[54]Fig.8 Microfluidic fabrication of helical microparticles.Microflow with coiling effect in microchannel for controllable fabrication of helical microparticles(a)[56].Deformation of droplets upon stretching and coiling in microfiber(b)for controllable fabrication of helical microparticles(c)[57].Droplet-containing microflow with coiling effect in microchannel(d)for controllable fabrication of helical microparticles(e),and their transportation of a microparticle in microchannel under rotated magnetic field (f)[54]
此外,通过巧妙地操控液滴的形变,亦可以基于变形后的液滴来模板合成螺旋形微颗粒。Wang等[57]基于微流控技术构建的内含油相单体液滴的PVA 微纤维,首先通过拉伸PVA 微纤维使得其内部单体液滴变形,再将拉伸后的微纤维缠绕在不锈钢丝上,使得内部液滴随之变为了螺旋形[图8(b)];接着,利用紫外光照聚合该含有磁性Fe3O4纳米颗粒的螺旋形单体液滴,再通过溶解其外部的PVA 微纤维以释放内部微颗粒,从而获得了磁性螺旋形PEGDMA 微颗粒[图8(c)]。进一步地,Cai 等[54]借助微通道内含有海藻酸的液流的卷绳效应来对液流内部的油相单体液滴施加作用力,使得单体液滴随液流一起发生卷曲变形[图8(d)],从而一步连续模板合成了磁性螺旋形PETPTA微颗粒[图8(e)]。在此过程中,由于单体液滴在界面张力作用下会趋于维持球形,因此,为了使单体液滴随液流一起发生稳定的卷曲变形,需将卷曲液流中的海藻酸快速交联,并利用海藻酸钙水凝胶卷曲结构使得单体液滴变形。通过改变液相流速、黏度和界面张力来调控液流的卷曲结构和内部液滴的尺寸,可以实现对磁性螺旋形微颗粒的长度、螺距以及振幅的调控;而通过增加螺旋形微颗粒中的磁性纳米颗粒含量,则可以强化其在旋转磁场驱动下的旋转推进运动速率。这种磁性螺旋形微颗粒在微通道中可受旋转磁场驱动进行快速旋转推进运动,从而有效地运输微通道中的微小物体[图8(f)],以及有效地疏通清除微通道中的堵塞物。这种微流控液相模板合成技术为多种不同材料的螺旋结构微颗粒的可控构建和多样化功能修饰提供了灵活的策略。
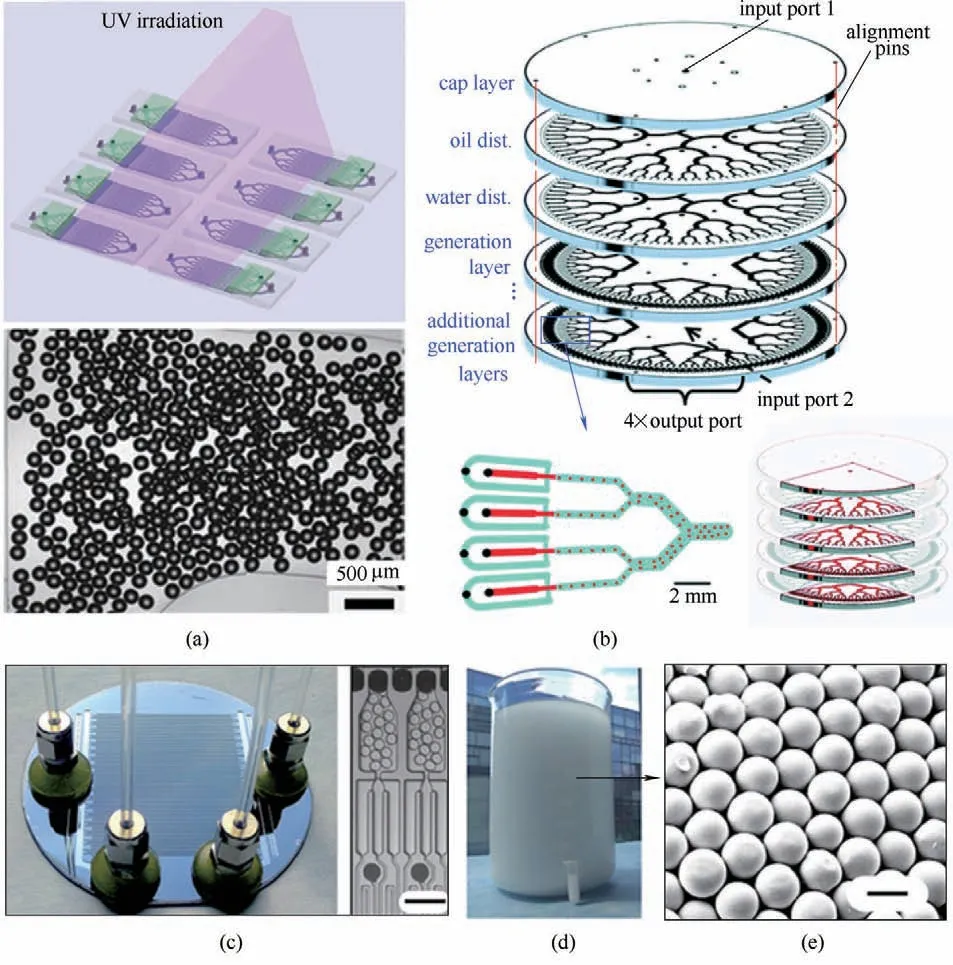
图9 微流控技术批量制备乳液液滴和功能微颗粒。具有8个液滴产生模块的多重模块化PDMS微流控系统用于乳液批量制备(a)[65]。具有层层堆叠结构的圆盘状PMMA微流控装置(b)[66]。具有10260个液滴产生微通道结构的玻璃/硅基材微流控装置(c)用于批量制备乳液(d)和微颗粒(e)[67][(a)、(c)和(e)中标尺分别为500 μm、140 μm和8 μm]Fig.9 Microfluidic techniques for mass production of emulsion droplets and functional microparticles.Multiple modular PDMS microfluidic system with eight droplet-generating modules for mass production of emulsion droplets (a)[65].Disk-like PMMA microfluidic device with stacked-layer structures(b)[66].Silicon and glass based microfluidic device with 10260 droplet-generating microchannels(c)for mass production of emulsion droplets(d)and functional microparticles(e)[67][Scale bars in(a),(c)and(e)are 500 μm,140 μm and 8 μm,respectively]
5 功能微颗粒的微流控批量制备
微流控技术在以乳液液滴为模板可控构建功能微颗粒方面已展现出了独特的优势,但要将微流控技术用于功能微颗粒的批量制备,还需要解决微流控制备技术的放大问题,而其中的关键是要实现乳液液滴的批量生产。目前,微流控技术的放大主要是基于微通道的数量放大,即通过采用更多数量的微通道结构,以在单位时间内产生更多的乳液液滴。图9(a)所示为具有8 个液滴产生模块的多重模块化PDMS 微流控系统,其每个液滴产生模块具有16 个平行的微通道结构用于液滴的生成和聚合[65]。该多重模块化微流控系统每小时可产生总体积为51.2 ml 的微米级液滴,同时,其所制备的微颗粒的产量为每小时约50 g 且CV 值不超过5%,展现出了良好的单分散性。图9(b)所示为具有层层堆叠结构的圆盘状PMMA 微流控装置,其分别由顶层圆盘盖、具有发散树枝状微通道网络结构的流体分布圆盘以及具有128个呈圆环状排列的液滴产生微通道结构的液滴产生圆盘组成[66]。该圆盘状微流控装置具有1个连续相液体进口、1个分散相液体进口以及4 个液滴出口。当制备乳液液滴时,油相和水相液体分别通过第二、三层流体分布圆盘上的微通道网络分配到下层液滴产生圆盘中以并行制备乳液液滴。通过增加所堆叠的液滴产生圆盘的数目(n),则可将更多液滴产生微通道结构(128×n)集成到微流控装置中。该圆盘状微流控装置每小时所产生的微米级液滴的总体积可达到约1 L。图9(c)所示为集成有10260(285×36)个液滴产生微通道结构的玻璃/硅基材微流控装置;该装置仅有1 个连续相液体进口、1 个分散相液体进口以及2 个液滴出口,其通量相比于仅具有一个液滴产生微通道结构的微流控装置提升了10000 倍以上[67]。该高度集成化的微流控装置可以在每小时内产生1万亿个以上的单分散微米级液滴(CV 值<3%),同时,该微流控装置每小时可产生277 g 的单分散聚己内酯微颗粒(CV 值<5%)[图9(d)、(e)]。在多通道微流控装置批量制备乳液液滴和微颗粒的过程中,由于各个液滴产生微通道结构中的连续相和分散相的流速对液滴形成具有重要的影响,因而对于各个微通道中液相的流速调控具有较高要求。这就需要巧妙设计微通道网络结构,使其具有相同的流阻,从而实现液相在多个微通道中的均匀分布,以确保多个平行微通道结构中能精确制备尺寸相同的乳液液滴和微颗粒。上述研究工作展现了微流控技术在面向工业化的功能微颗粒材料批量制备方面的应用前景。
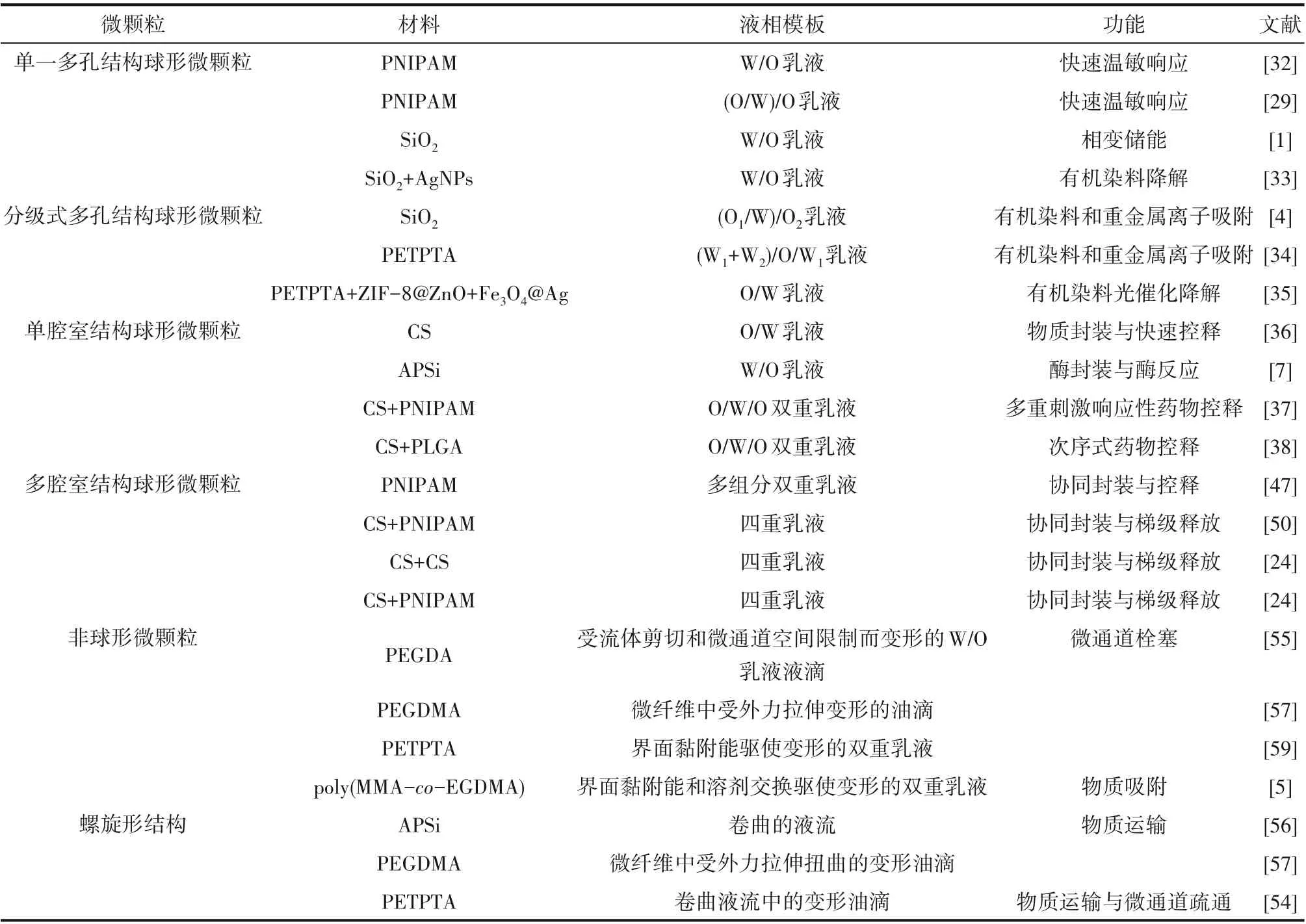
表1 微流控技术构建功能微颗粒的代表性文献总结Table 1 Summary on references for microfluidic fabrication of functional microparticles
6 结 论
综上所述,本文综述了近年来基于微流控液滴模板法来可控构建面向化工、医药、储能、环境等领域的多样化功能微颗粒材料的研究新进展。重点介绍了具有多样化结构和独特功能的微颗粒材料的液滴模板设计思路和制备方法,并探讨了基于微颗粒微观空间结构和化学组成的协同耦合来构筑独特功能特性的设计策略(表1 中对本文所介绍的微流控技术构建功能微颗粒的代表性文献进行了总结)。为了进一步促进微流控技术在功能微颗粒材料创新制备方面的应用,未来的研究工作应充分发挥微流控技术对于材料微观空间结构和化学组成等的精准调控,聚焦于具有高附加值的高度结构化、功能化的微颗粒材料的设计构建;同时,虽然通过微通道的结构设计和数量放大已可高通量制备乳液液滴,但该微流控系统一般仅适于实验室环境制备,且所制得的乳液基本上都是单乳液滴,因而仍需开发经久耐用的微流控设备以及新的多重微通道网络结构来实现单乳液滴以及复杂多重乳液液滴的工业化批量制备;此外,还需系统开展微流控设备的升级放大和系统集成方面的研究,深入探索多重微通道条件下多相流体的分配、流动、传热、传质和反应等物理/化学过程的协同调控机制,为功能微颗粒的产业化规模生产奠定科学基础。
