心率减速力与连续心率减速力对扩张型心肌病患者预后的预测价值△
2021-01-06林晓明杨希立赖玉琼高耀铭刘宇清
林晓明,杨希立,赖玉琼,高耀铭,刘宇清
(佛山市第一人民医院,广东佛山 528000)
扩张型心肌病(dilated cardiomyopathy,DCM)是原因不明心肌病中最常见的一种类型,是以心肌细胞的变性纤维化,进而单侧或双侧心室扩大,而没有其他负荷异常或冠状动脉病变所造成的整体收缩功能损害[1]为特征的严重器质性心脏病。患者常伴恶性心律失常和心力衰竭,是发生心源性猝死的高危人群。因此,寻求有效的预测指标对患者进行危险分层,采取相应的防治措施,对改善DCM 患者预后,提高其生存率有着重要的意义。近年研究表明,心源性猝死的发生与自主神经功能受损密切相关[2]。心率减速力(decelerration capacity of rate,DC)[3]与连续心率减速力(heart rate deceleration runs,DRs)[4]是近年由Georg Schmidt推出的定量检测迷走神经张力新的无创心电指标,但其在DCM 患者中的检测及临床意义的研究尚少。本研究通过对DCM 患者进行DC 和DRs 检测,旨在探讨其对DCM 患者预后的预测价值。
1 资料和方法
1.1 一般资料
选择2017 年1 月至2019 年12 月在佛山市第一人民医院心内科住院的DCM 患者96 例,男63 例,女33 例,年龄(58.3±12.5)岁,均符合2016 年欧洲心脏病学会发布的DCM 指南中的诊断标准[1]:(1)左心室舒张末期容积或直径大于经体表面积与年龄、性别校正的正常图的2 个标准差;(2)左心室射血分数(left ventricular ejection fraction,LVEF)正常;(3)排除先天性心脏病、风湿性心脏病、冠状动脉粥样硬化性心脏病(冠心病)、心肌炎、肺源性心脏病等。在DCM 患者中,根据有无发生心源性猝死将患者分为高危组21 例和低危组75 例。根据心律失常发生情况分为室性心动过速(室速)组(阵发性室速或短阵室速)26 例,室性期前收缩(室早)组(频发室早>100 次/24 h)50 例和无室性心律失常组20 例。按纽约心脏协会(New York Heart Association,NYHA)心功能分级分为Ⅱ级组21 例,Ⅲ~Ⅳ级组75例。选取非器质性心脏病患者100例为对照组,男61 例,女39 例,年龄(56.7±11.2)岁,排除冠心病、高血压性心脏病、肥厚型心肌病、限制型心肌病、肺源性心脏病、心肌炎、心脏瓣膜病、先天性心脏病患者。以上所有患者排除标准:(1)临时或永久起搏器植入、心律转复除颤器植入、心房颤动、心房扑动患者;(2)病窦综合征、窦房传导阻滞、二度和三度房室传导阻滞患者;(3)合并甲状腺功能亢进、急性脑血管意外患者。
1.2 心率减速力与连续心率减速力检测及危险分层
采用深圳博英BI9900 系列动态心电图工作站进行24 h 动态心电图监测,经专门软件脱机分析,用适宜频率对各通道进行采样,通过自动分析计算得出DC 及DRs 值。
DC 是通过24 h 整体趋向性分析和减速能力的测定,定量评估受检查者迷走神经张力的高底,进而筛选和预警猝死高危患者的一种新的无创心电学技术。其检测方法:(1)将24 h 动态心电图经1 200 Hz 数字化自动处理系统转化为以心动周期RR 值为纵坐标的序列图。随后将每一个心动周期的RR 值与前一心动周期进行比较,当较前一个心动周期延长时,称为减速周期。当实测的RR 值比前一个心动周期值延长或缩短超过5%时,该周期则被自动剔除。(2)以每一个减速点为心率段的中心,依次取其两侧的15 个心动周期组成一个心率段,进行不同心率段的有序排列。(3)经位相整序后,分别计算对应周期的平均值X(i),即对应序号的周期进行信号平均(PRSA),再将结果代入公式测定DC 值。计算公式:DC=[X(0)+X(1)-X(-1)-X(-2)]xl/4。X(0)系所有中心点RR 间期的平均值:X(1)系中心点右侧紧邻的第一个心动周期的平均值;X(-1)系中心点左侧相邻的第一个心动周期的平均值;X(-2)系中心点左侧相邻的第二个所有心动周期的平均值。危险分层:DC值>4.5 ms 为低风险值;DC 值2.6~4.5 ms 为中风险值;DC 值≤2.5 ms 为高风险值。
DRs 是指Holter 记录中连续出现心动周期RR间期逐跳延长的现象,是迷走神经对窦性心律在短时间内负性频率的调节结果,能定量评估迷走神经对心率的调控能力是否正常,与DC 技术形成互补。其检测方法:(1)常规记录24 h 动态心电图,测量并标出逐跳的R-R 间期值。(2)确定DC持续的周期值,以R-R 间期为纵坐标,以心动周期的先后序号为横坐标,制成不同DRs 值的顺序图,进而计算出持续周期不同的DC 的各自数值。(3)计算持续周期不同的DC 的数值及相对数量值:先计算持续周期不同(DRl-DRl0)的DC 各自绝对值后,再除以整个记录时间段内窦性心律RR 间期总数值后,则能得到持续不同的DC 周期的相对值。记录DRs 中的DR2、DR4、DR8。DR2 为在连续3 个心动周期中相对第1 个心动周期,后2 个心动周期连续发生心率减速情况;DR4 为在连续5 个心动周期中后4 个心动周期连续发生心率减速情况;DR8 为在连续9 个心动周期中后8 个心动周期连续发生心率减速情况。危险分层:DR4 相对值≤0.05%的患者为高危;DR4>0.05%,且DR2≤5.4%或DR8≤0.005%的患者为中危;DR2>5.4%,且DR4>0.05%,DR8>0.005%的患者为低危。
1.3 超声心动图检查方法
采用Sonos5500 型扇超仪,机械探头3.0 MHz,按照美国超声协会推荐的测量方法测定:左心房内径(left atrial diameter,LAD)、左心室舒张末期内径(left ventricular end diastolic dimension,LVEDD)、左心室收缩末期内径(left ventricular end-systolic dimension,LVESD)、LVEF,其中LVEF 测定采用双平面Simpson法。
1.4 随访方法
对96 例DCM 患者进行住院观察、门诊和电话随访,平均随访36 个月,每6 个月随访1 次,共发生心源性死亡21 例,其中包括心源性猝死6 例,恶性室性心律失常死亡10 例,心力衰竭死亡5 例。观察了解院内和院外地高辛、β-受体阻断药、利尿药、血管紧张素转化酶抑制剂(angiotension converting enzyme inhibitor,ACEI)的使用情况。
1.5 统计学分析
数据处理采用SPSS 11.5软件。计量资料用()表示,3 组间比较采用方差分析,两两比较采用t检验。计数资料以[n(%)]表示,组间比较采用χ2检验。DC、DRs 与心源性猝死、室性心律失常、NYHA分级、LVEF 的相关性采用多重线性回归分析。应用Cox 比例风险回归模型分析影响心源性死亡的发生影响因素。以P<0.05 为差异有统计学意义。
2 结果
2.1 扩张型心肌病组和对照组患者DC、DRs 及基线资料比较
DCM 组患者DC、DR2、DR4、DR8 和LVEF 显著低于对照组,LAD、LVEDD、LVESD 显著高于对照组,差异均有统计学意义(P<0.01);DCM 组和对照组患者年龄、性别及糖尿病、原发性高血压(高血压)、吸烟比较,差异无统计学意义(P>0.05),详见表1 和表2。
表1 DCM 组与对照组患者DC、DRs 及计量基线资料比较 []

表1 DCM 组与对照组患者DC、DRs 及计量基线资料比较 []

表2 DCM组与对照组患者计数基线资料比较 [n(%)]
2.2 扩张型心肌病高危组与低危组患者DC、DRs及基础资料比较
高危组患者与低危组比较,年龄较大(P<0.05),DC、DR2、DR4、DR8、LVEF、ACEI 使用率显著降低(P<0.01),差异有统计学意义;而两组LAD、LVEDD、LVESD、LVEF、性别,糖尿病、高血压和吸烟及地高辛、β-受体阻断药、利尿药使用率比较,差异无统计学意义(P>0.05),详见表3 和表4。
表3 DCM 高危组与低危组患者DC、DRs 及计量基线资料比较 []

表3 DCM 高危组与低危组患者DC、DRs 及计量基线资料比较 []

表4 DCM 高危组与低危组患者计数基线资料比较 [n(%)]
2.3 扩张型心肌病不同心律失常组患者DC、DRs比较
室速组患者DC、DR2、DR4、DR8 显著低于室早组和无室性心律失常组(P<0.01),室早组患者DC、DR2、DR4、DR8 显著低于无室性心律失常组(P<0.01),室速组患者年龄显著高于室早组和无室性心律失常组(P<0.01),差异有统计学意义;而室早组与无室性心律失常组患者年龄比较,差异无统计学意义(P>0.05);室速组、室早组与无室性心律失常组患者性别比较,差异无统计学意义[69.2%(18/26)vs.60.0%(30/50)vs.75.0(15/20),P>0.05],详见表5。
2.4 扩张型心肌病不同NYHA 心功能分级组患者DC、DRs 比较
NYHA 心功能Ⅲ~IV 级组DCM 患者DC、DR2、DR4、DR8 显著低于NYHAⅡ级组(P<0.05),年龄显著高于NYHAⅡ级组(P<0.05),差异有统计学意义,见表6;两组患者性别比较,差异无统计学意义[52.0%(13/21)vs.66.7%(50/75),P>0.05]。
表5 DCM 室速组、室早组与无室性心律失常组患者DC、DRs 比较 []

表5 DCM 室速组、室早组与无室性心律失常组患者DC、DRs 比较 []
注:与室早组比较,*P<0.05,**P<0.01;与无室性心律失常组比较,1)*P<0.05,1)**P<0.01
表6 DCM 不同NYHA 分级组患者年龄及DC、DRs 比较 []

表6 DCM 不同NYHA 分级组患者年龄及DC、DRs 比较 []
2.5 多重线性回归分析结果
多重线性回归分析结果显示,DC 与心源性猝死、室性心律失常、NYHA 分级、LVEF 相关(P<0.05);DR2、DR4、DR8 与心源性猝死、室性心律失常、NYHA 分级、LVEF 相关(P<0.05),详见表7。
2.6 多因素COX 比例风险回归分析结果
以性别(女=1,男=0)、年龄(≥65 岁=1,<65 岁=0)、DC 值(>4.5 ms=0,≤4.5 ms=1)、DR2 值(≤5.4=1,>5.4=0)、DR4 值(≤0.05=1,>0.05=0)、DR8(≤0.005=1>0.005=0),心功能分级(Ⅱ级=1,Ⅲ~IV级=2),LVEF(<35%=1,≥35%=0),高血压(是=1,否=0),糖尿病(是=1,否=0),吸烟(是=1,否=0)为自变量,以是否发生心源性死亡(是=1,否=0)为因变量进行多因素COX 回归分析,结果显示:DC≤4.5 ms、DR2≤5.4%、DR4≤0.05%、DR8≤0.005%是DCM 患者发生心源性死亡的危险因素。
3 讨论
DCM 患者的病因迄今不明,近年认为持续性病毒感染对心肌组织的损伤是导致或诱发的主要原因。DCM 属于严重的器质性心脏病,病理特点为心肌细胞肥大、变性,不同程度的纤维化或纤维瘢痕形成,随着病变进一步发展,患者心腔逐渐扩大,空间构型发生明显异常改变,进而并发不同程度的心力衰竭,当病变累及心脏感受器时可使患者交感神经和迷走神经的传入冲动发生异常,心肌电不稳定性增加,恶性室性心律失常和心源性死亡的发生明显增加。DCM 患者发生恶性室性心律失常的本质是交感-迷走神经失衡,当迷走神经受到极度抑制时,迷走神经对心脏的保护作用减弱,呈现类似“交感风暴”的恶性事件[5],是导致发生恶性室性心律失常和心源性猝死的主要原因。
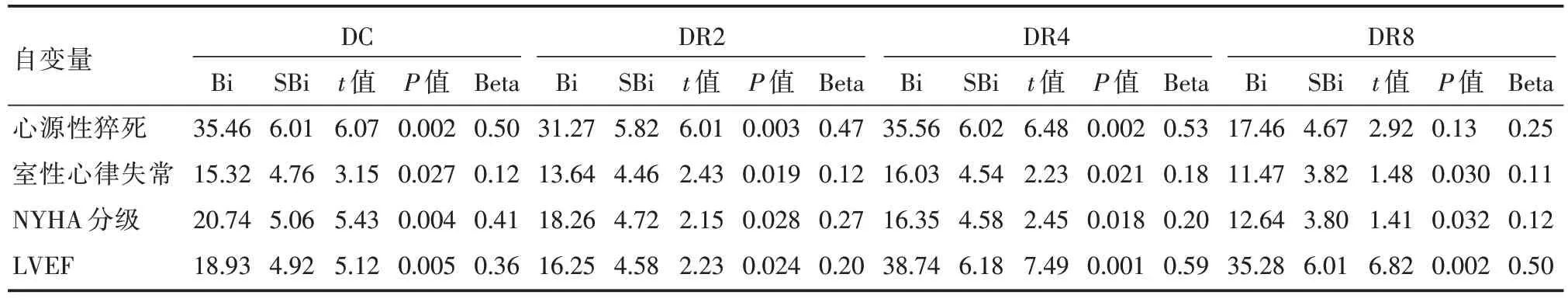
表7 DC、DRs 与心源性猝死、室性心律失常、NYHA 分级、LVEF 的多重线性回归分析结果
DC 是通过24 h 整体趋向性分析和减速能力的测定,定量评估受检查者迷走神经张力的高底,进而筛选和预警猝死高危患者的一种新的无创心电学技术。DRs 是指Holter 记录中连续出现心动周期RR 间期逐跳延长的现象,是迷走神经对窦性心律在短时间内负性频率的调节结果,能定量评估迷走神经对心率的调控能力是否正常,与DC 技术形成互补[6]。以往研究表明,临床上应用心率变异性指标来评价心脏自主神功能,然而很难将交感神经与迷走神经的作用分开计算,使其临床应用有较大的局限性[7],且心率变异性易受外界因素的影响,很难准确反映交感与迷走神经活性,而DC 和DRs 不受外界因素的影响,能相对客观地反映自主神经系统对心率的直接作用,可以对迷走神经的作用做定量分析[8]。本研究结果表明,DCM 组患者DC、DR2、DR4、DR8 明显低于对照组,提示DCM 患者迷走神经调节功能下降,而两组年龄、性别无显著性差异,提示DCM 患者不受年龄、性别影响。DCM 高危组与低危组患者比较,DC、DR2、DR4、DR8 显著降低,说明高危患者迷走神经功能更低,且高危组患者年龄明显高于低危组,提示年龄大心源性死亡的风险更大,可能与神经纤维减少,神经胶质细胞增多导致迷走神经调节功能降低有关[9]。同时本研究结果显示,DCM 患者中发生恶性室性心律失常患者的DC、DR2、DR4、DR8 均明显低于室早组和无室性心律失常组,提示有恶性室性心律失常患者迷走神经调节功能下降,且恶性室性心律失常组患者年龄明显大于室早组和无室性心律失常组,说明年龄越大心肌电越不稳定,迷走神经调节功能越差。本研究结果还显示,NYHA 心功能Ⅲ~IV 级患者DC、DR2、DR4、DR8明显低于Ⅱ级患者,提示DC、DR2、DR4、DR8 与心力衰竭程度相关,且Ⅲ、IV 级患者年龄大于Ⅱ级患者,说年龄越大,心力衰竭的程度越重。
本研究对心源性猝死、室性心律失常,NYHA分级,LVEF 进行了DC 和DRs 的多重线性回归分析,显示DC、DR2、DR4、DR8 与心源性猝死、室性心律失常、NYHA 分级、LVEF 相关,提示DC、DRs可成为预测DCM 患者心源性猝死、恶性室性心律失常、心力衰竭和心功能的重要指标。多因素COX 比例风险回归分析显示,DC、DR2、DR4、DR8降低是DCM 患者发生心源性死亡的危险因素,DCM 患者迷走神经调节功能降低,发生心源性死亡的风险增多。
此外,本研究结果还显示,DCM 组患者的LVEF 显著低于对照组,DCM 高危组患者的LVEF也显著低于低危组,提示DCM 患者和高危患者心功能不全,尤其是高危患者LVEF 更低,心功能更差;而DCM 组与对照组患者年龄、性别、吸烟、糖尿病和高血压发生率比较,差异无统计学意义(P>0.05),提示DCM 患者与年龄、性别、吸烟、是否患糖尿病和高血压无关,DCM 患者风险的高低也与性别、吸烟、是否患糖尿病和高血压无关。
综上所述,DC、DRs 有望成为预测DCM 患者预后的重要指标,是DCM 患者心源性死亡的危险因素。DC、DRs检测简便,快速、安全、价廉,可稳定评估DCM患者迷走神经功能,值得在临床应用推广。
