核因子E2 相关因子2/血红素加氧酶-1 信号轴在心血管疾病中作用的研究进展△
2021-01-06杨贵林赵明一黄劲松
杨贵林,赵明一,吴 敏,黄劲松,朱 平
[1.广东医科大学,广东湛江 524000;2 广东省心血管病研究所广东省人民医院(广东省医学科学院),广州 510080;3.中南大学湘雅三医院儿科,长沙410013]
提要:目前,心血管疾病仍是危害人类健康的最常见的疾病,而导致心血管疾病的主要原因之一是由于细胞的氧化应激。最新研究证明,核因子E2 相关因子2/血红素加氧酶-1(nuclear factor erythroid-2-related actor 2/heme oxygenase 1,Nrf2/HO-1)处在氧化应激的中心位置,激活后能发挥抗炎、抗氧化、减少线粒体损伤、调节细胞凋亡、自噬、焦亡等作用。激活Nrf2/HO-1 信号轴在大多数情况下对心血管疾病具有保护作用,但也可能产生不良作用。本文就Nrf2/HO-1 信号轴在心血管疾病中的最新研究进展进行综述。
目前,心血管疾病仍是威胁人类健康的最常见疾病,其全球发病率和病死率都很高,其中病死人数占全球死亡人数的三分之一[1]。而导致心血管疾病主要原因之一是细胞的氧化应激(oxidative stress,OS)。OS 是指体内氧化与抗氧化作用失衡,促氧化能力超过抗氧化能力,导致活性氧(reactive oxygen species,ROS)的生成增加。ROS,尤其是超氧阴离子和过氧化氢,能诱导促炎基因表达,是心血管细胞中重要的信号分子。最新研究证明:核因子E2 相关因子2/血红素加氧酶-1(nuclear factor erythroid-2-related factor 2/heme oxygenase 1,Nrf2/HO-1)处在氧化应激的中心位置,在激活Nrf2/HO-1 信号轴后,能调控一系列的抗氧化基因和Ⅱ相解毒酶的表达,并增加一系列抗氧化物质的生成,以此发挥抗炎、抗氧化、减少线粒体损伤、调节细胞凋亡、自噬、焦亡等作用。激活Nrf2/HO-1 信号轴在大多数情况下对心肌缺血再灌注损伤、动脉粥样硬化、心律失常、原发性高血压(高血压)、心力衰竭等心血管疾病具有保护作用,但也可能对动脉粥样硬化和心力衰竭产生不良作用。本文就关于Nrf2/HO-1 信号轴对心血管疾病的作用的最新研究进展进行综述,为临床治疗提供分子基础。
1 Nrf2/HO-1 信号轴
Nrf2 属于中文全称(cap‘n’collar-basic leucine zipper,CNC-bZIP)转录激活因子家族成员,包含7 个结构域,分别为Neh1~7;而介导其泛素化降解的Keap1 包含5 个结构域,分别为NTR,BTB,IVR,DGR 和CT 区。在生理状态下,Nrf2 的Neh2 结构域与keap1 的DGR 区结合后位于细胞质中保持惰性,在keap1 功能结构域BTB 和IVR 区参与下经Cul3/Rbx1/E3 泛素化降解以维持浓度稳定。在ROS 和亲电子基团等应激条件下,keap1 中的SH-1 基团构象改变及Nrf2 磷酸化,导致两者解偶联,Nrf2 从keap1 中释放转位入细胞核内。Nrf2 通过Neh1 结构域与Maf 蛋白形成异二聚体后,结合抗氧化反应元件(antioxidant response element,ARE),激活一系列的抗氧化基因和Ⅱ相解毒酶,包括HO-1、铁蛋白、铜锌超氧化物歧化酶、谷胱甘肽过氧化物酶、谷胱甘肽-S-转移酶等[2-3]。HO-1 是分子量为32 kDa的应激蛋白超家族成员,它联合NADPH 及细胞色素P450,通过胆绿素还原酶(biliverdin reductase,BVR),催化血红素分解为胆绿素、二价铁离子和一氧化碳(carbon monoxide,CO),而胆绿素可进一步由BVR 还原为胆红素,HO-1、胆红素、二价铁离子和CO 具有抗氧化、抗炎、减少线粒体损伤、调节细胞凋亡、自噬、焦亡等作用[4-9](图1)。
2 Nrf2/HO-1 信号轴与心肌缺血再灌注损伤
在缺血性疾病抢救和治疗过程中,对组织造成损伤的主要因素,不是缺血本身,而是恢复血液供应后,过量的自由基攻击这部分重新获得血液供应的组织内的细胞造成的,这种损伤,叫做组织缺血再灌注损伤(ischemia reperfusion injury,I/R)。急性心肌梗死(acute myocardial infarction,AMI)为导致心血管病患者死亡的重要原因,挽救濒死心肌的关键在于及时疏通梗死动脉、恢复心肌血液供应[10]。然而,再灌注会引起许多疾病,如ROS 过多、钙超载、线粒体功能障碍、炎症和凋亡等[11-12]。在心肌I/R应激中出现ROS 剧增,导致内源性自由基清除剂酶的耗竭。针对ROS 的抗氧化剂或内源性自由基清除剂的上调已被证明可以减轻心肌I/R 损伤[13]。
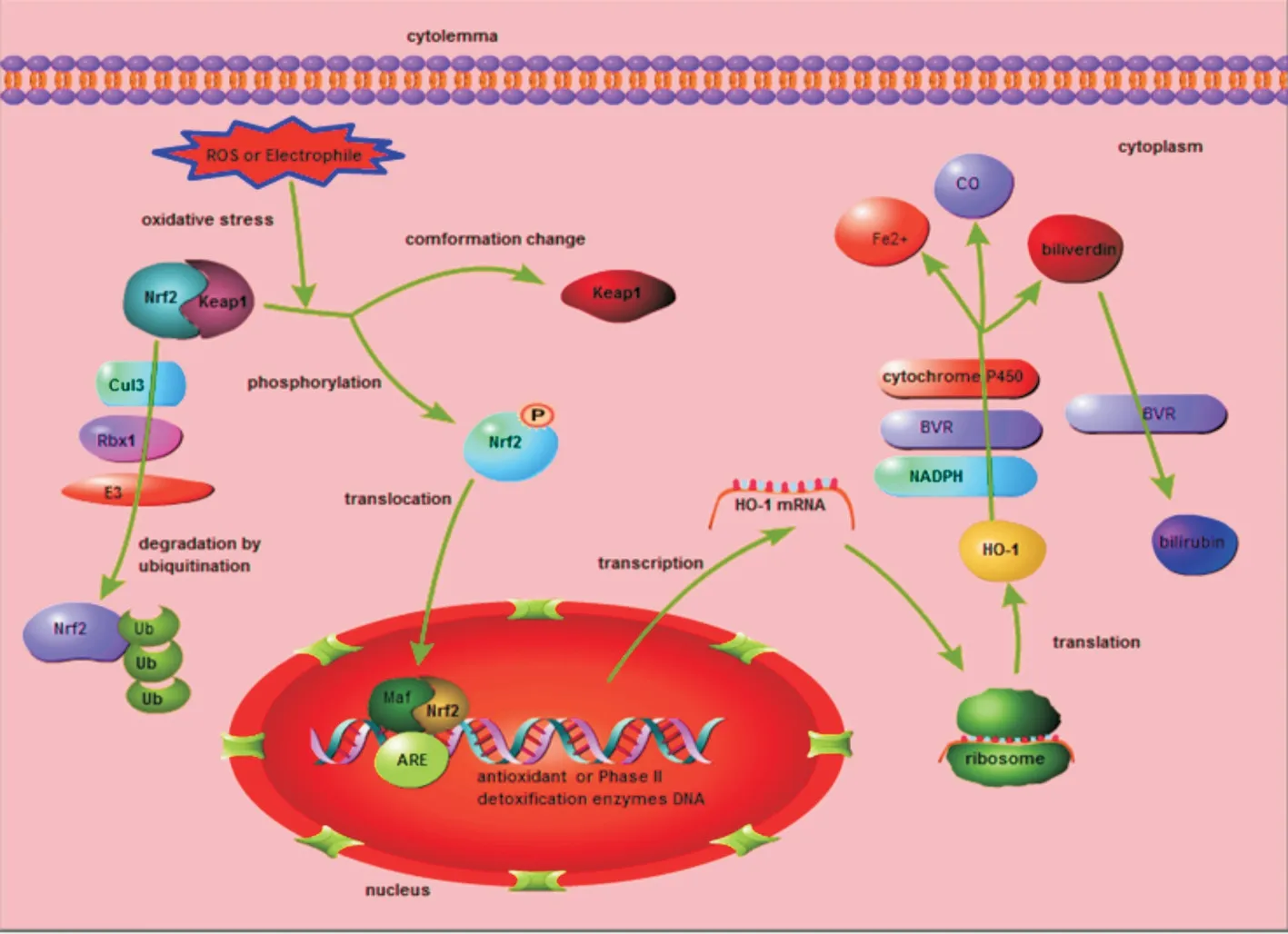
图1 Nrf2/HO-1 信号通路在氧化应激中的调控机制图示
有研究表明,一些抗氧化产物在心肌I/R 损伤的心肌保护作用是通过Nrf2/HO-1 信号轴实现的。Zeng 等[14]对人参皂苷Rd 的研究表明,激活Nrf-2/ HO-1 信号通路可以减轻心肌I/R 损伤。当心脏发生I/R 时,Nrf2 从keap1 分离,转位至细胞核,然后与ARE 结合,激活HO-1、醌氧化还原酶(NQO1)等2 期抗氧化物和解毒基因,HO-1 和醌氧化还原酶的上调可以保护心脏免受I/R 损伤引起的氧化应激。在Langendorff 等[15]灌注的心脏中,用4-羟基壬烯醛、α-硫辛酸,或硫酸氢盐治疗,可以激活I/R 后心脏组织中的Nrf2,增加心肌内的谷胱甘肽(glutathione,GSH)浓度,减小梗死面积,减轻体内心肌细胞凋亡[16]。另外,有研究证实了HO-1 在心脏中的细胞保护作用。在I/R 中过表达的HO-1 能降低离体大鼠心脏缺血损伤,而抑制HO-1 的活性则抵消了这种保护作用,并且在许多情况下增强I/R损伤[17-18]。在用基因治疗或药理学方法治疗后,具有心脏特异性过表达HO-1 或增强心脏HO-1 浓度的转基因小鼠,无论是在短期内还是在缺血事件发生1 年后,其梗死面积均明显减小,心脏功能改善[19]。以上说明Nrf2/HO-1信号轴的激活可以减轻心肌的I/R。
缺血预处理(ischemic preconditioning,IPC)现象被认为是预防心肌缺血损伤、缩小梗死面积的最有效机制之一。IPC 可以作为一种“早期预警”信号,在长时间缺血事件之前激活Nrf2。Nrf2 的急性激活在I/R 后被证明具有心脏保护作用。并且IPC 可诱导蛋白激酶C 的活化,进而促进Nrf2 的易位和对HO-1 的诱导[16,20]。
3 Nrf2/HO-1 信号轴与动脉粥样硬化
动脉粥样硬化是导致冠状动脉疾病的主要原因[21],脂质代谢障碍为动脉粥样硬化的病变基础,其特点是受累动脉病变从内膜开始,一般先有脂质和复合糖类积聚、出血及血栓形成,进而纤维组织增生及钙质沉着,并有动脉中层的逐渐蜕变和钙化,导致动脉壁增厚变硬、血管腔狭窄。在动脉粥样硬化发生过程中,氧化应激和慢性炎症在血管平滑肌细胞(VSMC)的活化中起着至关重要的作用[22]。氧化应激也是内皮功能障碍的主要原因,是内皮组织损伤的主要原因之一,氧化应激产生的ROS 几乎参与了动脉粥样硬化的每一个阶段的发病机制,ROS 可通过改变细胞氧化还原状态而引发内皮功能障碍,进而诱发血管炎症[4,22-23]。慢性血管炎症是由促炎细胞因子(如TNF-α)引起的,肿瘤坏死因子-α(TNF-α)能增加ROS,刺激氧化还原信号通路导致动脉粥样硬化[5]。Nrf2 通过其依赖基因及蛋白包括HO-1 发挥抗氧化、调节炎症的作用[24],表明Nrf2/HO-1 信号轴具有抗动脉粥样硬化作用。但Nrf2 可能同时也具有促动脉粥样硬化作用。
激活Nrf2/HO-1 信号轴有抗动脉粥样硬化作用。动脉粥样硬化斑块形成的一个重要阶段是巨噬细胞浸润内皮和巨噬细胞吸收积累的低密度脂蛋白(low-density lipoprotein,LDL)后形成泡沫细胞。Zhu 等[25]发现Nrf2 能抑制泡沫细胞形成,当巨噬细胞暴露于氧化低密度脂蛋白(oxidized low-density lipoprotein,oxLDL)时,Nrf2 表达的增加,而Nrf2 可以通过激活Ⅱ期抗氧化酶间接保护巨噬细胞免受oxLDL 介导的损伤,从而抑制泡沫细胞的形成,防止动脉粥样硬化斑块的形成。另外,一些研究结果巩固了Nrf2在维持血管完整性和内皮功能中的抗动脉粥样硬化作用,这可能是通过释放NO 和防止细胞凋亡来实现的[26-28]。这进一步提示Nrf2 在抵抗动脉粥样硬化中起重要作用。HO-1 在动脉粥样硬化斑块中高度表达,主要定位于巨噬细胞和泡沫细胞,其抗氧化和抗炎特性可能是抵消早期病变发展的基础。特别是HO-1 降低免疫细胞的招募和浸润,调节巨噬细胞极化,也促使表型向抗炎表型转变,抑制树突状细胞的成熟,从而影响动脉粥样硬化病变的形成[29-35]。此外,Yet 等[36]证明HO-1 在动脉粥样硬化病变形成中起保护作用。当apoE-/-小鼠(缺乏apoE 的小鼠)以西方饮食喂养8 周时,动脉粥样硬化病变在进展,尽管血浆总胆固醇浓度升高,但apoE-/-HO-1-/-小鼠(同时缺乏HO-1 和apoE 的小鼠)的病变比apoE-/-小鼠更大、更严重,这说明HO-1 在动脉粥样硬化损伤形成中起保护作用。以上研究证实Nrf2/HO-1 信号轴具有抗动脉粥样硬化作用,对心血管具有保护意义。
然而,有证据表明,Nrf2 的激活并不总是导致积极的结果,可能会加速某些心血管疾病的发生,例如动脉粥样硬化[20]。虽然Nrf2 能刺激抗动脉粥样硬化的HO-1 表达,但该转录因子同样也能刺激促动脉粥样硬化清道夫受体CD36 蛋白的表达[37]。而羧甲基赖氨酸(carboxymethyl lysine,CML)及CD36 与泡沫细胞的迁移有关,CML/CD36能抑制泡沫细胞向血管旁淋巴结迁移,从而加速apoE-/-小鼠动脉粥样硬化的演进,这可能与CML/CD36 通过细胞游离胆固醇、活性氧、p-FAK、Arp2/3 复合体及F-actin 聚合的介导抑制泡沫细胞迁移有关[38]。Ruotsalainen 等[39]在对LDL 受体缺陷小鼠(LDLR-/-)和只表达apoB-100 的LDLR-/-小鼠(LDLR-/-ApoB100/100)两种动脉粥样硬化的替代模型的研究发现,Nrf2 缺乏明显减少早期和晚期动脉粥样硬化评估的病变大小和范围,另外,Nrf2缺乏增加了斑块钙化,加重了老龄LDLR-/-ApoB100/100 小鼠主动脉斑块的成熟。这些进一步表明Nrf2 可能具有促动脉粥样硬化作用。然而,关于Nrf2 的矛盾作用的报道需要进行更多的研究。
4 Nrf2/HO-1 信号轴与心律失常
心律失常是心血管疾病中重要的一组疾病,是由于窦房结激动异常或激动产生于窦房结以外,激动的传导缓慢、阻滞或经异常通道传导,即心脏活动的起源和(或)传导障碍导致心脏搏动的频率和(或)节律异常。有研究表明ROS、炎症、自噬与心律失常的发生息息相关。心血管组织ROS 浓度的迅速增加会引发异常强烈的炎症,炎症会破坏心肌的协调收缩能力,导致心律失常,而增强自噬可能改善心律失常发生的过程[40]。激活Nrf2/HO-1 信号轴能有效降低ROS 浓度、改善炎症、增强自噬,从而抑制心律失常的发生。Yang 等[41]对大鼠心肌I/R 模型研究发现,牛蒡子苷(arctigenin,ATG)可能通过激活Nrf2 信号通路来减少氧化应激,从而减轻心肌I/R 诱导的室性心律失常。Bak 等[42]证明在心肌I/R 中,HO-1 mRNA 和CO 浓度的升高能有效地预防心室颤动(ventricular fibrillation,VF)的发生。以上说明激活Nrf2/HO-1 信号轴可能能防止心律失常的发生。但目前没有研究直接证明Nrf2/HO-1 信号轴对心律失常的抑制作用。
5 Nrf2/HO-1 信号轴与高血压
高血压是指以体循环动脉血压[收缩压和(或)舒张压]增高为主要特征(收缩压≥140 mmHg,1 mmHg=0.133 kPa,舒张压≥90 mmHg),可伴有心、脑、肾等器官的功能或器质性损害的临床综合征。高血压与下丘脑室旁核的高氧化应激有关,其特点是血管收缩性增强,同时内皮氧化应激增加,血管炎症和血管重建增强[4,43-44]。Nrf2 可诱导HO-1 表达,上调的HO-1 在自发性高血压大鼠中具有降压作用。HO-1 可通过其催化血红素分解产物之一CO 发挥降压作用。CO 具有直接的血管舒张作用,并且还能抑制血管收缩剂内皮素的生成[45-46]。Sun 等[44]采用自发性高血压大鼠模型,发现石榴提取物激活下丘脑室旁核AMPK,进而激活Nrf2/HO-1 信号通路,清除自由基,减轻氧化应激,降低室旁核的慢性交感神经活性,从而降低高血压大鼠交感神经的过度活动和动脉血压。这些研究提示Nrf2/HO-1 信号轴的激活能降低血压。
6 Nrf2/HO-1 信号轴与心力衰竭
心力衰竭是指由于心脏的收缩功能和(或)舒张功能发生障碍,不能将静脉回心血量充分排出心脏,导致静脉系统血液淤积,动脉系统血液灌注不足,从而引起心脏循环障碍症候群,通常是持续的、异常的神经激素和机械应力的结果。导致心力衰竭的关键病理生理过程是心脏重构,心力衰竭发生发展的关键因素是氧化应激[16]。如前所述,激活Nrf2/HO-1 信号轴能诱导一系列抗氧化物质的表达,从而发挥抗氧化作用。Xing 等[47]证明,CDDO-9,11-二氢三氟酰胺(dh404)通过Nrf2 介导的抑制心肌细胞肥大和成纤维细胞增殖,可以抑制压力超载诱导的心肌氧化应激、心脏重构不良和心力衰竭。在Nrf2 缺失的情况下,压力超载和AngⅡ诱导的病理心脏重构和心功能障碍更为严重,Nrf2 在这些病理中起负反馈调节作用。另外,有研究表明,过表达Nrf2 可显著抑制肥大因子诱导的心肌细胞和成纤维细胞ROS 的产生和增加,而敲除Nrf2对心肌细胞和成纤维细胞的抑制作用则相反,因此Nrf2对病理性心肌肥大和心力衰竭具有保护作用[16,20]。虽然Nrf2 的急性激活具有心脏保护作用,但有证据表明,Nrf2的慢性激活可能对心脏功能有害,导致心力衰竭的病理生理过程,这可能与Nrf2 的慢性激活与人B 晶状体蛋白过表达的小鼠心肌肥厚和心力衰竭模型中的“还原应激”理论有关[48]。另外一些研究表明,Nrf2 激活的HO-1 对慢性心力衰竭有治疗作用,在心力衰竭时,HO-1 的上调可减轻病理性左心室重构,减少心肌肥厚、氧化应激和炎症[4]。以上说明Nrf2/HO-1 信号轴激活的快慢对心力衰竭有不同的影响,快速激活能抑制心力衰竭,慢性激活将促进心力衰竭。
心血管疾病是威胁人类健康的最常见的疾病。因此,能找出各种心血管疾病的发病机制将有利于我们防治心血管疾病。心血管疾病的主要原因之一是细胞的氧化应激,而Nrf2/HO-1 信号轴处在氧化应激的中心位置。因此,激活Nrf2/HO-1 信号轴能有效防治各种心血管疾病。这为心血管疾病的靶向药物治疗提供了方向,提示我们研究治疗心血管疾病的药物可以从Nrf2/HO-1 信号轴下手,寻求新的高效的治疗方法。