吉非替尼联合培美曲塞治疗表皮生长因子受体-酪氨酸激酶抑制剂获得性耐药晚期肺腺癌的疗效观察
2020-12-30王辉刘宽杨叶叶
王辉,刘宽,杨叶叶
三门峡市中心医院呼吸与危重症医学科,河南 三门峡 472000
据报道,肺癌的发病率和病死率均居恶性肿瘤的第1位[1]。全部肺癌类型中,非小细胞肺癌(non-small cell lung cancer,NSCLC)居多,而腺癌占50%以上,是最常见的组织亚型[2]。早期肺腺癌常无明显症状,患者就诊时多数已处于中晚期,因此化疗成为了主要的治疗方法[3]。肺腺癌患者化疗后1年生存率为18%,远不能令人满意[4]。近年来由于分子生物学和基因组学联系日益密切,通过二者结合研发的表皮生长因子受体(epidermal growth factor receptor,EGFR)-酪氨酸激酶抑制剂(tyrosine kinase inhibitor,TKI)具有延长生存期、不良反应小、给药方便的优点,逐渐成为中晚期肺腺癌患者特别是伴EGFR突变患者的首选方案[5]。吉非替尼属于EGFR-TKI药物,研究发现,尽管EGFR-TKI对肺腺癌患者疗效显著,但用药超一年后多出现病情进展,进一步研究发现耐药基因发生了扩增,提示EGFR-TKI治疗易产生耐药性[6]。这类对EGFRTKI治疗耐药的晚期肺腺癌患者称为EGFR-TKI获得性耐药晚期肺腺癌患者。研究显示,耐药后立即停用EGFR-TKI,将造成病情恶化加速,坚持用药虽然不能控制病情但可延缓疾病进展速度[7]。目前这类患者尚无理想的治疗方案。培美曲塞可抑制多个靶点代谢,具有低毒、广谱且高效的特点,可有效抑制肿瘤细胞增殖[8]。这使得培美曲塞在晚期肺腺癌一线、二线和维持治疗中的应用日益普遍[9]。研究显示,培美曲塞与EGFR-TKI药物联合治疗EGFR-TKI获得性耐药晚期肺腺癌患者可有效缓解临床症状,延长生存期[10]。本研究分析了吉非替尼联合培美曲塞治疗EGFR-TKI获得性耐药晚期肺腺癌的疗效和不良反应,现报道如下。
1 资料与方法
1.1 一般资料
收集2017年5月至2019年5月于三门峡市中心医院接受治疗的EGFR-TKI获得性耐药晚期肺腺癌患者的病历资料。纳入标准:①年龄≥18岁;②经病理检查确诊为肺腺癌;③临床分期为Ⅲb~Ⅳ期[11];④既往有EGFR-TKI治疗史并出现耐药[12]。排除标准:①合并其他严重器质性疾病;②具有化疗禁忌证;③具有培美曲塞过敏史;④发生脑转移。依据纳入和排除标准,本研究共纳入85例肺腺癌患者。根据EGFR-TKI治疗耐药后用药方案的不同将患者分为观察组(n=45)和对照组(n=40),对照组患者采用培美曲塞治疗,观察组患者采用吉非替尼联合培美曲塞治疗。观察组中,男29例,女 16例;年龄为42~65岁,平均年龄为(52.42±4.55)岁;有吸烟史或被动吸烟史21例;临床分期:Ⅲb期30例,Ⅳ期15例;既往EGFR-TKI治疗后进展用时5~22个月,中位时间为11个月。对照组中,男25例,女15例;年龄为40~65岁,平均年龄为(52.11±4.87)岁;有吸烟史或被动吸烟史20例;临床分期:Ⅲb期28例,Ⅳ期12例;既往EGFRTKI治疗后进展用时4~22个月,中位时间为12个月。两组患者的性别、年龄等临床特征比较,差异均无统计学意义(P>0.05),具有可比性。
1.2 治疗方法
对照组患者采用培美曲塞治疗,每日500 mg/m2,静脉滴注;观察组患者在对照组的基础上口服吉非替尼250 mg,每日1次。21天为1个周期,两组患者均治疗3个周期。
1.3 观察指标及评价标准
1.3.1 近期疗效 采用实体瘤疗效评价标准(response evaluation criteria in solid tumor,RECIST)[13]评价患者的近期疗效:完全缓解(complete response,CR),靶病灶完全消失,至少持续4周;部分缓解(partial response,PR),靶病灶最大径之和缩小≥30%,至少持续4周;疾病进展(progressive disease,PD),靶病灶最大径之和增加≥20%,或出现新病灶;疾病稳定(stable disease,SD),介于PR和PD之间。客观有效率(objective response rate,ORR)=(CR+PR)例数/总例数×100%。
1.3.2 血清学指标 血清学指标包括癌胚抗原(carcinoembryonic antigen,CEA)、神经元特异性烯醇化酶(neuron specific enolase,NSE)、细胞角质蛋白19片段抗原21-1(cyto-keratin 19 fragment antigen 21-1,CYFRA21-1)。治疗前1天和治疗后1周内,于清晨空腹状态下抽取5 ml静脉血,静置1 h后,3000 r/min离心10 min,取上层血清,采用酶联免疫吸附试验测定CEA、NSE和CYFRA21-1水平。
1.3.3 不良反应 依据抗癌药不良反应评价标准[14]评价患者的不良反应,分为0~4级。主要不良反应包括白细胞减少、血小板减少、胃肠道反应、谷丙转氨酶升高。于治疗后1周内,在清晨空腹状态下抽取5 ml静脉血,采用血细胞计数仪检测白细胞、血小板数量,采用赖氏比色法检测谷丙转氨酶水平。
1.3.4 无进展生存期(progression-free survival,PFS)PFS是指从治疗开始到肿瘤发生进展或因任何原因导致死亡的时间。治疗结束后对患者随访1年,随访截止时间为2020年6月,随访方式为电话随访、门诊记录、家访等,每个月随访1次,随访内容包括常规检查、影像学检查等。
1.4 统计学方法
采用SPSS 18.0软件对数据进行统计分析,计量资料以均数±标准差(±s)表示,组间比较采用t检验;计数资料以例数和率(%)表示,组间比较采用χ2检验;采用Kaplan-Meier法绘制生存曲线,组间比较采用Log-rank检验。以P<0.05为差异有统计学意义。
2 结果
2.1 近期疗效的比较
观察组患者的ORR为46.67%(21/45),高于对照组的 22.50%(9/40),差异有统计学意义(χ2=5.416,P=0.020)。(表1)

表1 两组患者的近期疗效[ n(%)]*
2.2 血清学指标的比较
治疗前,两组患者的血清CEA、NSE和CYFRA21-1水平比较,差异均无统计学意义(P>0.05)。治疗后,两组患者的血清CEA、NSE和CYFRA21-1水平均低于本组治疗前,且观察组患者的血清CEA、NSE和CYFRA21-1水平均低于对照组,差异均有统计学意义(P<0.05)。(表2)
表2 治疗前后两组患者血清学指标的比较( μg/L,± s)
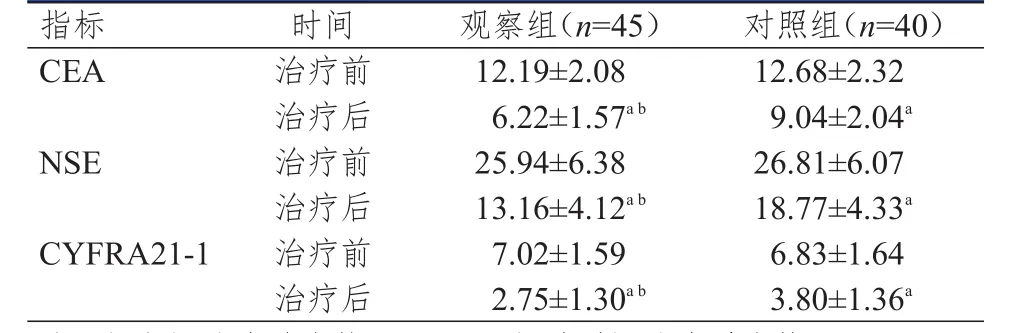
表2 治疗前后两组患者血清学指标的比较( μg/L,± s)
注:a与本组治疗前比较,P<0.05;b与对照组治疗后比较,P<0.05
指标CEA NSE CYFRA21-1治疗前治疗后治疗前治疗后治疗前治疗后12.19±2.0812.68±2.32 6.22±1.57a b9.04±2.04a 25.94±6.3826.81±6.07 13.16±4.12a b18.77±4.33a 7.02±1.596.83±1.64 2.75±1.30a b3.80±1.36a时间 观察组(n=45) 对照组(n=40)
2.3 不良反应发生率的比较
两组患者的不良反应均为1~2级。治疗期间,两组患者白细胞减少、血小板减少、胃肠道反应、谷丙转氨酶升高的发生率比较,差异均无统计学意义(P>0.05)。(表3)

表3 两组患者的不良反应发生情况[ n(%)]
2.4 无进展生存情况的比较
观察组患者的中位PFS为7.9个月,对照组患者的中位PFS为5.4个月。观察组患者的无进展生存情况优于对照组,差异有统计学意义(χ2=4.591,P=0.032)。(图1)
3 讨论
肺癌的病死率居全部恶性肿瘤首位,其中腺癌是最常见的亚型。由于肺腺癌患者早期症状多不明显,因此大多数患者在临床就诊时已处于中晚期。随着对EGFR信号转导通路研究的不断深入,发现EGFR-TKI可显著改善晚期NSCLC患者的生存率,在晚期肺癌患者中应用广泛[15]。吉非替尼作为EGFR-TKI代表性药物,能够与酪氨酸激酶的ATP位点竞争性结合,对磷酸化和信号转导产生抑制作用,进而促进肿瘤细胞凋亡,抑制血管生成[16]。然而研究显示,肺腺癌患者用药1年内易出现EGFR基因继发性突变,使患者出现耐药性[17]。培美曲塞可直接靶向抑制肿瘤细胞代谢,首先影响叶酸的代谢,进一步抑制嘌呤核苷酸和嘧啶核苷酸的合成,使得肿瘤细胞增殖因缺乏物质基础而在S期终止[18]。培美曲塞的靶向性可以实现以较少用量控制疾病进展的效果,因此耐药发生率低,不良反应小,患者生存期明显延长,对EGFR-TKI获得性耐药晚期肺腺癌的治疗效果明显[19]。研究显示,肺腺癌患者耐药后停用EGFR-TKI会使病情迅速恶化,坚持用药虽不能抑制病情进展,却可使疾病进展变缓[7]。因此,吉非替尼与培美曲塞联用对EGFRTKI获得性耐药晚期肺腺癌具有较好的疗效,可能通过降低耐药性促进EGFR-TKI发挥效用,并靶向抑制肿瘤细胞的增殖和扩散,使患者的生存期得以延长。
本研究结果显示,观察组患者的ORR为46.67%,高于对照组的22.50%,差异有统计学意义(P<0.05),说明联合用药对病情的控制效果较好,与靳璐等[20]的研究结果一致。可能是因为培美曲塞可以靶向抑制肿瘤细胞代谢,吉非替尼可以促进肿瘤细胞凋亡,联合治疗可产生协同作用,进而提高疗效。本研究结果还显示,治疗后,两组患者的血清CEA、NSE和CYFRA21-1水平均低于本组治疗前,且观察组患者的血清CEA、NSE和CYFRA21-1水平均低于对照组,差异均有统计学意义(P<0.05)。这3种肿瘤标志物常放在一起检测,标志物水平明显降低说明肿瘤被有效地控制,原因可能是联合用药使EGFR-TKI的耐药性被部分抑制,吉非替尼促进肿瘤细胞凋亡与培美曲塞抑制肿瘤细胞代谢的作用联合,从而使疾病有效地被控制,这与吕巧妹等[21]的研究结果一致。两组患者的不良反应均为1~2级,治疗期间,两组患者白细胞减少、血小板减少、胃肠道反应、谷丙转氨酶升高的发生率比较,差异均无统计学意义(P>0.05),这与王磊等[22]的研究结果一致,原因可能是联合治疗产生了协同作用,可减少吉非替尼用量,使耐药发生率下降,减轻因耐药而大剂量用药带来的不良反应。通过对症支持治疗,不良反应不影响后续疗效。观察组患者的无进展生存情况优于对照组,差异有统计学意义(P<0.05),表明联合用药的远期疗效较好,这与李家琛[23]的研究结果一致。原因可能是单纯吉非替尼治疗会使大部分患者在1年内发生耐药及疾病进展,远期疗效欠佳。联合用药时,一方面培美曲塞具有靶向性,可减少吉非替尼的剂量,降低耐药发生率,进而规避大剂量用药带来的不良反应,另一方面培美曲塞通过抑制肿瘤细胞代谢实现抑制细胞增殖的作用,进而减少肿瘤细胞增量,吉非替尼通过促进肿瘤细胞凋亡减少肿瘤细胞存量,联合用药可较好地抑制疾病进展,因此远期疗效较好。

图1 观察组( n=45)和对照组( n=40)患者的无进展生存曲线
综上所述,吉非替尼联合培美曲塞治疗EGFRTKI获得性耐药晚期肺腺癌可降低相关肿瘤标志物水平,不良反应在可控范围内,并且可延长患者的PFS,整体疗效令人满意。
