献血者HBsAg ELISA检测灰区标本分析
2020-12-14郑小凡徐利虹石洁祝宏
郑小凡,徐利虹,石洁,祝宏
(浙江省血液中心,浙江 杭州310052)
献血者血液标本采用酶联免疫吸附试验(ELISA)检测HBsAg。目前,大多数血站采用两个不同厂家的ELISA试剂对HBsAg进行检测。从血液安全角度出发,针对ELISA检测的特点,血站一般在检测的结果中设置灰区(grey zone),以尽可能避免假阴性的发生,但是各实验室设置灰区的标准存在差异,各机构无统一的质量控制标准[1-2]。李丽平等[3]在58例HBsAg检测灰区标本中发现核酸阳性9例,提出ELISA灰区范围内的血液存在一定的感染风险;但是胡文佳等[4]评估第3、4代抗-HIV ELISA试剂,认为抗-HIV检测可以不必设置灰区。2016年我国对献血者增加了HBV核酸(DNA)的检测[5],本文结合血液核酸检测情况,评估设置灰区对血液安全的影响,报道如下。
1 材料与方法
1.1 材料 选择2017年1月-2019年12月浙江省血液中心无偿献血者的血液样本540372例。实验仪器:STAR 8CH自动加样仪、FAME 24/20和24/30自动酶联免疫处理系统 (瑞士哈曼顿公司);酶标比色仪Spectra(奥地利Anthos公司);核酸检测设备 Panther(西班牙 Grifols公司)、Cobas 201系统(美国罗氏诊断产品有限公司)。实验试剂:HB-sAg检测试剂分别来自英科新创(厦门)科技有限公司、美国Bio-Rad公司;HBV DNA检测试剂为TaqScreen MPX v2.0核酸联合检测试剂(美国罗氏诊断产品有限公司);Procleix Ultrio Elite血液核酸联合检测试剂(西班牙Grifols公司)。
1.2 方法 (1)采用ELISA法检测HBsAg。所有标本均采用两个不同厂家的ELISA方法试剂[英科新创(厦门)科技有限公司(试剂一)、美国Bio-Rad公司(试剂二)]在自动酶联免疫处理系统(型号FAME 24/20及FAME 24/30,瑞士哈曼顿公司)平台上进行,严格按照试剂和仪器说明书操作。(2)ELISA灰区设置[1-4]。参考试剂说明书中S/CO值(标本吸光度值/Cutoff)≥1.00判定为标本检测反应性,<1.00为标本检测无反应性。从血液安全角度设置灰区S/CO值为≥0.85~1.00,>1.00判定为反应性,<0.85则判定为无反应性。(3)HBV DNA核酸检测。按照试剂说明书要求在其配套平台上进行操作和结果判定,每例标本只采用其中一种核酸检测试剂。(4)单个样本结果判定。两种ELISA试剂HBsAg检测以及HBV核酸检测均无反应性,则判定该样本为阴性;两种ELISA试剂HBsAg检测呈反应性或无反应性,HBV核酸检测呈反应性,即判定该样本为阳性。
2 结果
2.1 标本检测情况 检测标本总数为540372例,试剂一反应性标本为1207例,其中灰区标本为39例(3.23%);试剂二反应性标本为1454例,其中灰区标本为107例(7.36%)。试剂一和试剂二均呈反应性966例,合计反应性标本1695例,灰区标本为146例,占整个反应性标本的8.61%。灰区标本核酸检测反应性为22例(15.07%)。试剂一检测为灰区而试剂二检测为反应性的标本有9例,其S/CO值为1.79±0.86;试剂二灰区而试剂一反应性标本18例,其S/CO值为3.49±2.08。以核酸检测呈反应性为真阳性标准,试剂一灰区标本7例真阳性,占17.95%,试剂二灰区标本15例真阳性,占14.02%,即不设置灰区最多可能有22个标本发生漏检,占0.000407‰。详见图 1。
2.2 灰区标本S/CO值分布 将灰区标本分为S/CO 值≥0.85~0.90、>0.90~0.95、>0.95~1.00 三组,试剂一、试剂二的灰区标本S/CO值分布详见表1,显示不同S/CO值水平均存在核酸检测反应性标本和/或另外一种试剂反应性标本。
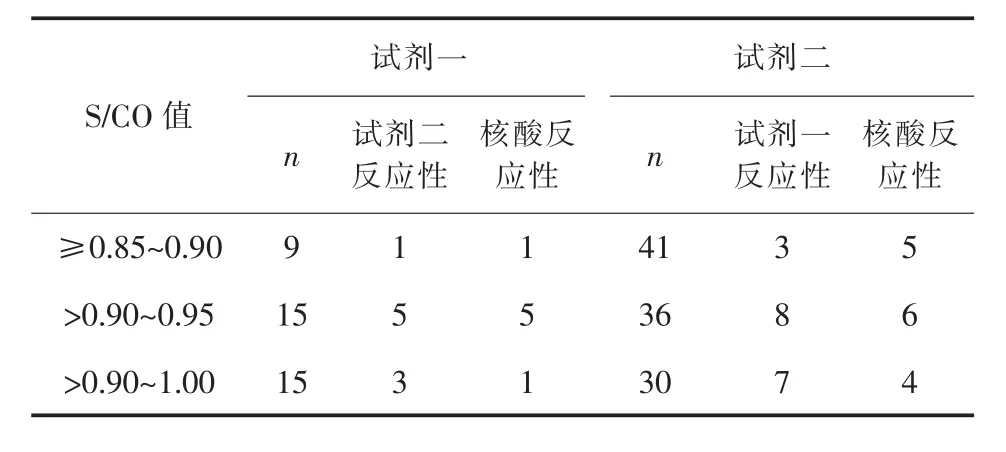
表1 两种检测试剂中灰区标本S/CO值分布情况(n)
3 讨论
血站在检测HBsAg时自动设备控制程序上需等候一定时间,因此不同检测板的酶联反应温育时间略有差异;此外,试剂本身的质量、标本保存时间等因素导致特定标本检测出的吸光度数值有一定的波动。按照《血站技术规程》(2019版)的规定,血站ELISA检测试剂批内变异系数要求在15%以内,批间变异系数在20%以内。为防止潜在弱阳性标本的漏检,血站通常在ELISA试剂检测HBsAg、抗HCV、抗HIV和梅毒抗体时设置灰区[1-4]。
灰区是指在定性的ELISA方法中标本测定值处于临界判定值(Cut off)附近,该标本存在潜在反应性结果的可能。考虑到ELISA试剂读数的可比性,一般采用S/CO值进行描述[1-4],灰区设置值包括Cut off上限、下限两种情况,但其标准不一[1-4];张立波等[6]利用不确定度分析,认为灰区 为临界值下调22%。本研究从血液安全角度出发,只考虑设置Cut off下限的灰区,同时将灰区标本按照反应性标本进行判定和管理[3-4]。从结果看,灰区标本占一定的比例,但是两种试剂反应性标本的灰区占比不同,可能与试剂质量有关。在灰区反应性标本中,共有22例(15.07%)标本核酸呈反应性,说明在灰区标本中有较高比例的真阳性标本,与既往的报道一致[1,7-8]。根据血站标准要求ELISA试剂批内变异系数在15%以内,因此本实验将设置的灰区定为临界值下调15%。如果不设置灰区,则至少有22例HBV DNA反应性标本会漏检。当这些血液用于临床时,可能造成输血传播性疾病的发生,严重影响血液安全。因此,从安全角度考虑并结合现有实际操作因素的影响,提示需要维持现有临界判定值下限的灰区。但应注意到,部分灰区标本在另一试剂检测中其S/CO值较高,可能与试剂包被抗体的特性、不同亚型检测的能力差异有关。本文报道的献血者HB-sAg反应性率为0.31%,远低于普通人群,这与献血前的筛选和健康教育有关[1-4]。从实验结果可知,两个试剂检测HBsAg阴性的标本中,均存在少数HBV核酸反应性标本,分别为10.00%、2.25%,提示该ELISA试剂可能漏检这些标本,试剂质量有待于进一步提高。
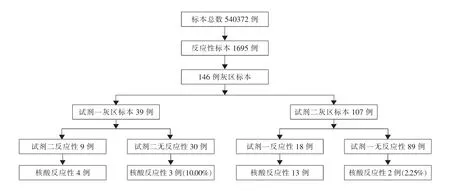
图1 标本检测结果示意图
本文采用双试剂同步检测血液标本HBsAg,结果显示试剂一或试剂二灰区标本在另外一种试剂或核酸检测中绝大多数呈无反应性,提示这部分标本大多数为假阳性反应。按照血站的管理要求,只要有反应性(包括假阳性反应)的献血者均须进行屏蔽和血液报废,淘汰了部分符合标准的献血者。因此,部分学者建议可取消灰区设置[9-10],但灰区设置有助于检出HBsAg真阳性标本,提升了临床用血的安全性。因此,本研究结果支持设置灰区,针对“存在假反应性”的情况,可结合核酸检测再次确认,以便充分地利用血液资源。
