全胚胎体外发育阻滞成功妊娠及分娩1例
2020-12-14杨欢利吴为玲诸溢扬陆文昊蔡娇娇
杨欢利,吴为玲,诸溢扬,陆文昊,蔡娇娇
(浙江省台州医院,浙江 临海 317000)
胚胎发育阻滞是导致辅助生殖中没有可移植胚胎而取消周期及反复移植失败的重要原因,而细胞碎片是导致胚胎质量下降以致发育阻滞的重要诱因。在辅助生殖中,部分胚胎发育阻滞是常见现象,但多个周期全胚胎体外发育阻滞较少见,现结合本院全胚胎体外发育阻滞1例,报道如下。
1 病例介绍
患者,女,37岁,结婚10年,因“未避孕2年,至今未孕”,2015年3月来院就诊。既往人工流产4次,2014年曾进行输卵管造影(HSG)检查,提示宫腔无特殊,双侧输卵管通畅,行促排卵治疗,有排卵而未受孕。后于2015年外院行2次辅助生殖治疗,第1次采用短方案加胞质内单精子注射(ICSI),于月经周期第3天注射曲谱瑞林0.05mg/d,2天后予促性腺激素(Gn)225IU,至注射HCG时停药,注射HCG 5000IU后36小时内获卵14个,受精8个,第3天胚胎伴大量碎片,形态评分为不可移植胚胎,行囊胚培养后胚胎发育阻滞;第2次采用微刺激方案加常规受精,采用来曲唑+Gn方案,于月经周期第3天口服来曲唑2.5~5.0mg/d,持续5天,周期第6天添加Gn 75IU,直至注射HCG时停药,注射HCG 5000IU后36小时获卵5个,受精3个,第3天胚胎形态评分碎片较多,为不可移植胚胎,行囊胚培养后胚胎发育阻滞,最终该周期无可移植胚胎。本次入院后要求行体外受精(IVF)助孕,行妇科及基础内分泌检查,均无异常,男方多次检查未见明显异常,末次精液检查结果:精液体积6mL,浓度117×106个/mL,前向运动型(PR)34%,非前向运动型(NP)11%,完全不动型(IM)55%(参考值:精液体积 1.5mL,浓度 15×106个/mL,PR 32%,PR+NP 40%)。最终诊断:继发不孕,不明原因不孕症。
采用刺激周期短效长方案治疗,在黄体期使用0.05mg/d的曲普瑞林降调,降调至第11天时检测激素为 LH 1.9 mIU/mL、FSH 2.1mIU/mL、E251pg/mL、P 1.12ng/mL,从第12天开始使用Gn促排卵,启动剂量为225IU,Gn使用11天时检测激素为LH 2.7mIU/mL、FSH 23.3mIU/mL、E2 4820pg/mL、P 1.2ng/mL,于当晚注射r-HCG 6500 IU进行扳机并于36小时后取卵。共获卵14个,采用IVF授精,受精后4小时检查发现第二极体出现率低于30%,采用补救ICSI的方法对其中较明确未受精的卵子进行ICSI授精,受精后18小时观察共获得8个正常受精卵,第3天胚胎评分发现所有正常受精发育的胚胎碎片异常的增多,形态评分为Ⅳ或Ⅴ级,属于不可移植胚胎(图1)。与患者充分沟通,患者同意移植受精后第 3 天的 a’、g’、h’3 枚胚胎 (图 2)至体内,移植后第16天测HCG为873mIU/mL,移植40天后B超监测到胎心,确认临床妊娠,妊娠40周后足月分娩正常女婴1例,其余5枚胚胎继续在体外培养,但发育受到阻滞,最终未能形成囊胚。
2 讨论
辅助生殖治疗的患者中40%会出现胚胎发生早期发育阻滞的现象[1]。发生阻滞的可能原因为:(1)卵子染色体异常;(2)精子染色体异常;(3)体外培养系统中的不利因素;(4)母合基因转变受阻[2]。目前多数学者认为胚胎发育阻滞的原因是由母源基因到合子型基因激活失败造成[3]。本例3次辅助生殖治疗周期的胚胎都停滞于4-8细胞期,胚胎都伴有异常多的碎片,影响了正常卵裂球的继续发育;结合既往人工流产史,提示胚胎可在母亲体内发育。综合各种因素分析胚胎体外发育阻滞可能是该患者卵母细胞胞质缺少对发育调节起重要作用的细胞因子。体外培养时由于培养液成分中各种细胞因子种类及数量有限,无法获取或获取不足,可导致胚胎发育停滞,如胚胎在体内发育,则所需细胞因子可从输卵管的分泌物中获取。此外,该患者胚胎均可见异常多的碎片,说明胚胎对外界环境中氧自由基伤害较敏感,对体外发育过程中的有害因素不能自主清除,从而导致胚胎发育停滞。
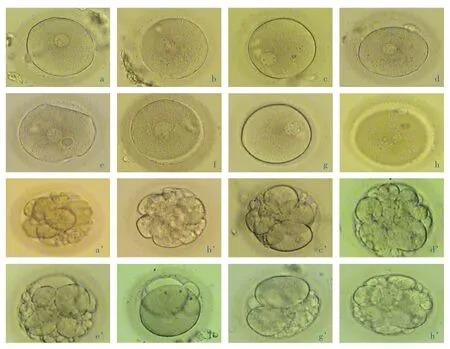
图1 第2天8个正常的受精卵(a-h)及对应的第3天卵裂期胚胎(a’-h’)
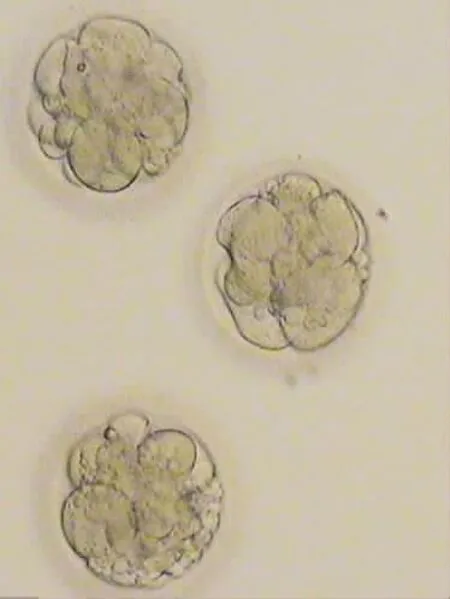
图2 第3天移植的胚胎
胚胎碎片可显著降低临床妊娠率,大量的碎片可能是胚胎凋亡的表现,胚胎碎片不仅影响胚胎发育潜能,而且影响胚胎种植潜能[4]。本例胚胎碎片都是“大而且分布广泛”的类型,形态评分为不可移植胚胎,且前2周期胚胎继续培养时均发生胚胎阻滞。因此,第3周期如对所有胚胎再继续进行体外培养,发育阻滞的机率很大,直接导致无可移植胚胎。有研究比较了发育欠佳的胚胎在卵裂期与囊胚期移植的结局,发现发育欠佳的胚胎体外继续培养的结局较差,导致53.8%的周期没有胚胎移植,而卵裂期移植组的取卵周期临床妊娠率显著高于囊胚培养组,显示体内培养对胚胎继续发育有重要的临床意义[5]。此外,早期胚胎的正常发育必须依赖源于生殖道上皮细胞的信号及各种细胞因子,这些细胞因子在清除微环境中的有害物质、促进早期胚胎发育及提高胚胎质量上都有重要意义[6],进一步证实了体内培养才能满足胚胎特别是体外发育异常胚胎的发育条件。有研究认为,将胚胎与输卵管上皮细胞培养可以增强自身的抗氧化能力和活力,提高胚胎发育潜能并克服胚胎发育阻滞[7],因此,体外发育阻滞的胚胎移回母体后,获得促进母合基因调控过渡的细胞因子并启动阻滞胚胎继续发育的可能性较大。本例进行充分沟通后选择胚胎移植,最终获得正常后代,其他未经移植的胚胎体外培养后最终没能继续发育成囊胚。
总之,胚胎体外培养条件的不断改进提高了大部分胚胎的体外发育潜能,但目前对胚胎体外发育的认识及胚胎发育阻滞的解决能力尚不足。母体是胚胎发育的最优场所,在胚胎体外发育阻滞或异常时应将其转移到母体内,以获得相关因子的调控,维持其发育潜能。
