“容量控制血运重建方法”在急性心肌梗死患者急诊介入治疗中应用4 例报告并文献回顾
2020-12-09何冀芳杨新春吴霞江世猛刘宇李江媛徐世莹王乐丰
何冀芳 杨新春 吴霞 江世猛 刘宇 李江媛 徐世莹 王乐丰
作者单位:100020 北京,首都医科大学附属北京朝阳医院心脏中心
急性心肌梗死患者急诊介入治疗死亡率高达7%左右,心力衰竭发生率接近22%[1]。冠状动脉血流恢复不可避免地引起心肌再灌注损伤(ischemic reperfusion injury,IRI),缺血程度和再灌注损伤相互作用,导致心肌再灌注前缺血损伤区域(area at risk,AAR)心肌细胞发生坏死,增加梗死面积。我们在后适应和逐渐适应的理论基础上提出“容量控制血运重建方法”的设想,2019年11月至2020年1月已经以此为指导进行4例急性下壁心肌梗死急诊介入治疗,评价可操作性和安全性。
1 临床资料
病例1 患者 男,54岁。主因“胸痛6 h”于2019年11月10日就诊于河南省柘城县人民医院。4 h前尿激酶原溶栓失败入院。平素体健,心电图示:Ⅱ、Ⅲ、aVF导联ST段抬高0.4 mV。就诊血压130/80 mmHg(1 mmHg=0.133 kPa),心率80次/分。入院诊断:急性下壁ST段抬高型心肌梗死。术前给予常规肝素、双联抗血小板药物,血小板糖蛋白Ⅱb/Ⅲa抑制药使用不受限。冠状动脉造影示:右冠状动脉粗大,近端完全闭塞,可见血栓影。经桡动脉入径将BMW(雅培)1工作导丝通过闭塞段后出现交界区心律,心率40~50次/分,血压下降至70/50 mmHg。以主动脉球囊封闭前向血流(参照病变部位冠状动脉直径按照小于1∶1选择球囊直径),3.0 mm×15 mm NC SprinterTM(美敦力)球囊于右冠状动脉近端8 atm(1 atm=101.325 kPa)阻断前向血流后,心率及血压逐渐回升。经股动脉入径进入6 F指引导管“乒乓”方式至右冠状动脉开口,使BMW(雅培)2工作导丝至右冠状动脉远端。经BMW2进入抽吸导管至NC球囊远端15 mm处。经抽吸导管少量注射对比剂证实远端血管通畅后(图1),经抽吸导管注射再灌注成分液体20 ml/min(动脉血10 ml+肝素生理盐水10 ml),共5 min。将NC球囊撤压后血流动力学稳定(图1)。冠状动脉造影示:心肌梗死溶栓治疗试验(thrombolysis in myocardial infarction,TIMI)血流分级Ⅲ级,右冠状动脉近端残余节段狭窄70%。常规支架治疗(Firebird 3.5 mm×23 mm,3.0 mm×15 mm,10 atm),3.5~4.0 NC SprinterTM(美敦力)球囊后扩张(图2)。术后患者症状缓解,TIMI血流分级Ⅲ级;生命体征稳定,即刻血压124/70 mmHg,心率60次/分;心电图示:下壁导联ST段回落至等电位线。超声心动图示:左心室后壁下壁运动减低,左心室舒张末期内径(left ventricular end diastolic diameter,LVEDD)55 mm,左心室射血分数(left ventricular ejection fraction,LVEF)58%,二尖瓣中度反流,三尖瓣、主动脉瓣轻度反流,少量心包积液。脑钠肽(brain natriuretic peptide,BNP)115.3 pg/ml(0~100 pg/ml)。

图1 病例1主动球囊封闭前向血流经抽吸导管远端造影/灌注示意图3.0 mm×15 mm非顺应球囊经工作导丝1至闭塞段近端加压扩张至8 atm。保持球囊扩张,经右股动脉入径进入指引导管“乒乓”方式至右冠状动脉开口,使工作导丝2至右冠状动脉远端。沿工作导丝2进入抽吸导管至原球囊远端15 mm处,经抽吸导管少量注射对比剂确认闭塞段远端血管血流通畅,然后经抽吸导管注射灌注液治疗
病例2 患者 男,56岁。主因“胸痛2 h”于2019年12月5日就诊于首都医科大学北京朝阳医院急诊科。2年前,曾行左回旋支、右冠状动脉中段、右冠状动脉后降支近段支架置入术。心电图示:Ⅱ、Ⅲ、aVF ST段抬高0.3 mV。入院诊断:急性下壁ST段抬高型心肌梗死。冠状动脉造影示:右冠状动脉近端闭塞,右冠状动脉粗大,可见疏松血栓影。因桡动脉途径困难,故经股动脉使7 F 4.0指引导管到位,进入双导丝通过闭塞段到达右冠状动脉远端,经导丝1进入GRIPTM(Acrostak)3.5 mm×12 mm球囊至闭塞段近端主动阻断前向血流。经导丝2进入APT(爱普特)1.9 F×130微导管。经微导管少量注射对比剂以明确远端管腔通畅,经微导管注射再灌注成分液体同病例1的NC球囊(图3)。因微导管内径小,推送费力,只灌注3 min。撤NC球囊压力后,血流动力学稳定。冠状动脉造影示:血流通畅,TIMI血流分级Ⅲ级,右冠状动脉中段支架内残余节段狭窄80%,发现原GRIP球囊在狭窄近端操作。再次进入原GRIP球囊扩张60 s后残余狭窄为0,以药物球囊3.5 mm×20 mm 12 atm治疗(图4)。术后患者症状缓解,TIMI血流分级Ⅲ级,生命体征稳定。心电图示:下壁导联ST段回落至等电位线。超声心动图示:左心室后壁下壁运动幅度轻度减低,LVEDD 54 mm,LVEF 60%。肌钙蛋白I(troponin I,TnI)峰值149.5 ng/ml(0~0.04 ng/ml),BNP峰值131 pg/ml(0~100 pg/ml)。


图2 病例1右冠状动脉近端闭塞,经容量灌注血运重建方法治疗后效果 A. 术前右冠状动脉闭塞情况;B. 远端灌注5 min后封闭球囊减压造影结果,右冠状动脉近端节段残余狭窄70%,TIMI血流分级Ⅲ级;C. 支架后,球囊后扩张后影像,TIMI血流分级Ⅲ级,患者血压、心率稳定

图3 病例2主动球囊封闭前向血流经微导管远端造影/灌注示意图7 F指引导管,双工作导丝通过病变。3.5 mm×15 mm非顺应球囊延工作导丝1至闭塞段近端加压扩张至8 atm。保持球囊扩张,延工作导丝2进入1.9 F 130 cm微导管至原球囊远端15 mm处,经微导管少量注射对比剂确认闭塞段远端血管血流通畅,然后经抽吸导管注射灌注液治疗
病例3 患者 男,50岁。主因“胸痛3 h”于2019年12月24日由救护车送至山东省莱芜市中心医院。1 h前诉轻度平卧气促,否认糖尿病、高血压病病史。心电图Ⅱ、Ⅲ、aVF ST段抬高0.2~0.4 mV,V1~V4ST段抬高0.2~0.3 mV。入院诊断:急性前壁、下壁ST段抬高型心肌梗死。患者高枕卧位,血压130/80 mmHg,心率80次/分,双下肺中等量湿啰音。冠状动脉造影示:左前降支近端闭塞,TIMI血流分级0~Ⅰ级,右冠状动脉近端锥形头端闭塞,TIMI血流分级0级。经桡动脉入径常规开通前降支,置入Firebird 3.0 mm×23 mm、2.5 mm×29 mm支架,TIMI血流分级Ⅲ级,可见左前降支远端心外膜血管左向右侧支循环。右冠状动脉操作步骤同病例1,灌注治疗后撤NC球囊压力,血流动力学稳定。右冠状动脉近端残余节段狭窄70%,TIMI血流分级Ⅲ级。Firebird 4.0 mm×29 mm 10 atm支架近端膨胀不全,残余狭窄60%,以4.0 NC球囊多次后扩张。术后患者症状缓解,血流TIMI血流分级Ⅲ级(图5~6)。生命体征稳定,即刻血压105/80 mmHg,心率80次/分。心电图示:下壁前壁导联ST段回落至等电位线。超声心动图示:各房室内径正常,运动幅度未见明显减低,LVEF 60%,三尖瓣、主动脉瓣轻度反流。肌钙蛋白T(troponin T,TnT)峰值5935 pg/ml(0~14 pg/ml),BNP峰值3666 pg/ml(0~125 pg/ml)。
病例4 患者 男,56岁。主因“胸痛4 h”于2020年1月4日就诊于首都医科大学北京朝阳医院急诊科。平素体健。心电图Ⅱ、Ⅲ、aVF ST段抬高0.2 mV。入院诊断:急性下壁ST段抬高型心肌梗死。冠状动脉造影示:右冠状动脉粗大,近端闭塞。分别经桡动脉和股动脉入径“乒乓”方式进入6 F 4.0指引导管至右冠状动脉开口,操作及灌注步骤同病例1、3,于右冠状动脉近端置入支架Resolute IntegrityTM(美敦力)3.0 mm×22 mm,3.5 mm×22 mm支架。NC SprinterTM(美敦力)3.0 mm×15 mm,3.5 mm×15 mm分别后扩张,术后患者症状缓解,TIMI血流分级Ⅲ级。生命体征稳定。心电图示:下壁前壁导联ST段回落等电位线。超声心动图示:各房室内径正常,LVEDD 51 mm,LVEF 65%,各节段运动协调,二尖瓣轻度反流。TnI峰值9.61 ng/ml(0~0.04 ng/ml),BNP峰值133 pg/ml(0~100 pg/ml)。
患者定期临床随访,病例2~4于6个月复查超声心动图示:心功能良好,心脏结构无明确改变。
2 讨论
2. 1 再灌注损伤的病理机制和非药物保护作用
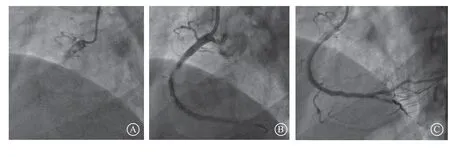
图4 病例2右冠状动脉近端闭塞容量灌注血运重建方法治疗后效果 A. 术前右冠状动脉闭塞情况;B. 远端灌注3 min后封闭球囊减压造影结果,右冠状动脉中段节段残余狭窄90%,TIMI血流分级Ⅲ级,注意近端封闭球囊未能在靶病变扩张;C. 非顺应性球囊后扩张后药物涂层球囊释放后影像,TIMI血流分级Ⅲ级,患者血压、心率稳定
目前认为,再灌注损伤的临床表现和病理机制的关系与以下机制有关:钙超载导致过度收缩介导的心肌细胞膜破裂、线粒体通透性转换孔(mitochondrial permeability transition pore,MPTP)开放、氧自由基作用、炎症反应、内源性信号通路调节和非心肌细胞成分损伤导致的微循环障碍等[2]。

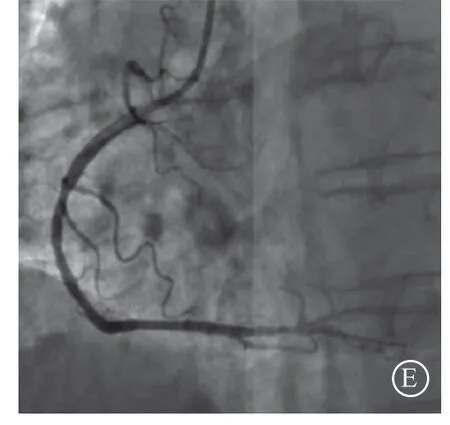
图5 病例3主动球囊封闭前向血流经抽吸导管远端造影/灌注示意图 A. 左冠状动脉造影示左前降支开口闭塞;B. 常规左前降支经皮冠状动脉介入治疗支架术后;C. 右冠状动脉近端闭塞;D. 右冠状动脉灌注治疗后支架近端膨胀不全,残余狭窄60%;E. 非顺应球囊反复后扩张,支架膨胀满意,心肌梗死溶栓治疗试验血流分级Ⅲ级,生命体征稳定

图6 病例3主动球囊封闭前向血流经抽吸导管远端造影/灌注示意图 操作过程同图1(A. 桡动脉途径指引导管;B. 股动脉途径指引导管;C. 3.0 mm NC球囊 8 atm扩张;D. 抽吸导管;.E. 抽吸导管内少量对比剂注射/灌注液注射;F. 工作导丝1;G. 工作导丝2)
Zhao等[3]利用犬心肌梗死动物模型第1次证明缺血后适应(ischemia postconditioning,IPOST)的作用,在早期再灌注时,重复交替缺血操作减轻再灌注损伤。线粒体损伤和调控是再灌注损伤的重要靶点,MPTP开放调控时间窗非常短暂,后适应操作有极其严格的窗口期[4]。后适应操作晚于再灌注60 s以后开始,就难以观察到后适应的心脏保护作用[5-7]。Staat等[8]、Yang等[9]最早报道急性心肌梗死患者后适应操作可以减轻再灌注损伤。大型动物实验和冠状动脉旁路术观察到渐灌注/缓慢灌注对再灌注损伤有一定的保护作用[10-12]。由于当时对于再灌注损伤干预窗口期认识不一致,存在灌注时间过长、灌注量设计偏大、灌注成分为未经稀释的动脉血、灌注同时没有完全闭塞前向血流等原因,没有引起足够的重视。
2. 2 后适应操作方法的自身缺陷
在POST[13]、DANAMI-3-IPOST[14]等大型随机对照试验(randomized controlled trial,RCT)中,后适应对于缩小梗死面积和心力衰竭的保护作用和常规介入操作相比较,差异无统计学意义。荟萃分析发现,后适应早期临床概念验证阶段,抽吸导管使用不普遍[15]。DANAMI-3iPOST的一项事后研究[16]在去除抽吸导管使用的因素后发现,全因死亡率和心力衰竭的风险明显降低,认为抽吸导管的广泛使用明显延长了前向血流恢复到后适应操作启动的时间,提示目前的后适应和相关操作过程可能影响对再灌注损伤的保护作用。
源于预适应操作的后适应操作方法可能存在固有的缺陷,减弱了后适应对再灌注损伤的保护作用:(1)不能明确闭塞段远端血流情况[17],而且后适应球囊可能在位于闭塞段近端血栓中操作(病例2);(2)交替血流阻断期间再灌注血流仍然能够产生有效的信号刺激,通过信号传导通路导致IRI[18-19];(3)操作过程中前向血流量不能有效调节;(4)后适应启动延误导致心脏保护作用明显减弱[5-6](在球囊预扩张或者使用抽吸导管使用过程中常合并血压、心率下降;病例1患者在工作导丝操作过程中出现再灌注损伤[20-21]);(5)机械地进行4~5个交替循环,缺少有效的、可操作的终止目标。国内李世强医师在Traverse等[20]第一时间主动启动后适应操作的基础上增加循环次数,以血流改善和血压稳定为操作终止目标,会议报告显示即刻冠状动脉血流改善。但是缺乏与标准后适应操作的临床对照研究和文献资料。
2. 3 再灌注损伤保护靶点的改变
临床再灌注损伤评价标准主要基于损伤区心肌保护程度,以心肌梗死面积和长期随访心功能指标为主。无法明确心肌梗死AAR范围时,难以直观地了解再灌注效果和再灌注损伤程度,同时缺乏对非心肌细胞再灌注损伤的关注。
内皮细胞、纤维细胞、血管平滑肌细胞和神经细胞等非心肌细胞的再灌注损伤,可能破坏血管内皮屏障导致心肌水肿,激活内皮系统,与循环的血细胞相互作用产生栓子。同时激活的血小板和中性粒细胞形成栓子,形成微血管栓塞(microvascular obstruction,MVO)。MVO也和冠状动脉开通时斑块或血栓脱落以及继发于再灌注后心肌水肿形成的外在压迫有关。MVO是无复流和心肌壁内血肿的基础,导致严重的心肌损伤,与患者的不良预后相关[22]。
Traverse等[20]严格把握适应证,第一时间开始后适应操作。虽然未发现心肌梗死面积改善,但是由于后适应操作明显减少MVO范围,心功能保护作用明显。再灌注损伤是冠状动脉闭塞段截面下血流支配范围内所有细胞的损伤。不同类型细胞对于缺血和再灌注损伤的反应不同,其中血管内皮细胞代谢很大程度上与线粒体呼吸运动无关。虽然血管内皮细胞缺血耐受性高于心肌细胞,但是对再灌注损伤的反应可能更敏感[23]。长期高血压病、高脂血症、糖尿病、高龄因素可能对于内皮系统对再灌注损伤的保护反应有一定影响[19,24-25]。所以针对内皮系统的后适应操作可能需要更缓慢的血流和相对较长的操作时间,这可能也是常规后适应操作研究中出现矛盾结果的一个原因。
血管内皮细胞等非心肌细胞在缺血再灌注时出现MVO,表现为无复流。无复流本身,或者无复流和心肌细胞致命性再灌注损伤协同作用导致AAR损伤加重。抑或无复流是AAR心肌细胞面对再灌注损伤的反馈保护机制,是AAR心肌细胞对于再灌注损伤的后适应反应[20]。严重的缺血再灌注损伤诱导心肌细胞凋亡或坏死性凋亡[26]。如果缺血-再灌注损伤持续时间较短可能会激活心肌细胞存活程序,以控制活性氧的产生和细胞损伤[27]。目前小样本研究提示,后适应操作可以减轻无复流现象,改善心肌梗死再灌注[20,28]。所以通过减轻冠状动脉微血管缺血再灌注损伤来保护心功能可能成为新的研究方向[22]。
2. 4 “容量控制血运重建方法”
在后适应操作和逐渐灌注的基础上,提出“容量控制血运重建方法”。对优势冠状动脉近端闭塞病变,以主动球囊封闭闭塞段前向血流,期间对闭塞段远端通畅的冠状动脉定量再灌注。操作步骤、流量控制、时间长度和灌注液成分的可行性分析如下:
(1)PREPARE研究[29]和PROXIMAL研究[30]使用的冠状动脉内近端保护装置(The Proxis栓塞保护装置,圣犹达医疗设备公司),球囊主动封闭冠状动脉闭塞段近端期间,预扩球囊和支架通过3.5 F导管完成介入治疗,并进行血栓抽吸,操作过程安全。
(2)双路指引导管支持下抽吸导管满足20~40 ml/min的灌注要求,并同时检测主动脉压力,可随时进行常规血栓抽吸操作。单一指引导管途径经桡动脉入径可能会遇到7 F指引导管桡动脉插入困难、锁骨下迂曲指引导管无法通过或操作困难等情况(病例2同时出现这两种情况)。1.9 F微导管内径不能满足20 ml/min以上的灌注要求。冠状动脉内冷灌注研究[31-32]使用OTW灌注球囊(over the wire balloon,OTWB)和基于DIVER CE(美敦力)抽吸导管的灌注球囊。目前常用的OTW球囊直径不足以封闭冠状动脉近端前向血流。部分冠状动脉近端的急性闭塞病变是在纤维斑块或者钙化病变基础上的高度狭窄病变,抽吸导管或OTW球囊需要充分的球囊预扩张才能通过。
(3)中等体重正常人冠状动脉血流量为每百克心肌60~80 ml/min,总的冠状动脉血流量为心输出量的4%~5%,约200 ml/min[33]。假设右冠状动脉血流量为100 ml/分,10 ml/分模拟90%狭窄的冠状动脉血流。动脉血10 ml用10 ml肝素生理盐水稀释,20 ml/min固定灌注流量,共5 min。现有文献报道的冠状动脉灌注液流量为10~30 ml/min,甚至达到40~60 ml/min。传统后适应操作方法操作时间共计4~10 min。
(4)灌注液成分、动脉血液和肝素盐水等量稀释后,便于推送,可减少血栓形成;能改善远端血管网或组织间的pH值,减少离子交换;可以冲洗掉远端血管网甚至微循环中心肌梗死的“代谢副产品”。罪犯血管病变内的高负荷血栓在抽吸导管或微导管操作时可能导致血栓脱落,加重MVO。经管腔注射少量对比剂可能会加剧这种情况。文献提示微血栓存在的情况下,后适应操作对于再灌注损伤的保护作用的净效应仍然减少了梗死面积的大小和心肌梗死的扩展[34]。
联合药物后适应应在再灌注损伤开始前进行药物保护。静脉注射等全身给药方法作用不明显。临床和实验操作中缺少经冠状动脉注射,特别是经冠状动脉在闭塞段远端缺血坏死区域使用的研究。我们的方法提供了在再灌注损伤开始前进行药物后适应的新的操作方法和研究手段。
3 小结
临床研究对于再灌注损伤关注的靶点可能从AAR受损心肌细胞向非心肌细胞如冠状动脉内皮细胞等转变,以充分恢复冠状动脉血流,减少MVO范围,作为再灌注损伤保护的第一终点。对本组患者应用容量控制血运重建方法后术中血压心率稳定,即刻TIMI血流分级Ⅲ级,住院期间无显著并发症。该方法操作可行,临床安全,从原理上改善了传统后适应操作方法和逐渐灌注方法的不足,也为药物后适应治疗提供了新的给药途径。但是需要通过进一步的RCT研究,以明确其对再灌注损伤的保护作用。
