AChE/PVP/Au@Pt/PVP/GC CME 对甲基对硫磷含量的测定
2020-11-18李正陈翊王玉张玉张丽
李正 陈翊 王玉 张玉 张丽
(1.杭州市余杭区疾病预防控制中心 浙江杭州 311100;2.安徽省芜湖市第一中学)
1 前言
有机磷农药是农业上广泛应用的杀虫剂,会对人体神经系统、生殖系统和血液系统等产生不同程度的毒副作用,使人体出现中毒症状,甚至会诱发癌症,危害生命[1,2]。 目前,检测有机磷农药的方法主要有色谱法[3,4]、光谱法(如红外分光光度法[5]、紫外分光光度法[6])、快速检测法[7](酶抑制法、纳米粒子-酶生物传感器法)等。
本文通过静电吸附依次将聚乙烯吡咯烷酮(PVP)、金核铂壳纳米粒子(Au@Pt)、PVP、乙酰胆碱酯酶修饰到玻碳电极(GC CME)上,得到乙酰胆碱酯酶(AChE)/PVP/Au@Pt/PVP/GC CME,考察Au@Pt 双金属纳米粒子对硫代乙酰胆碱的电催化反应,并用该电极测定磷酸盐缓冲溶液(PBS)中的甲基对硫磷。
2 试验部分
2.1 仪器与试剂
仪器:KQ218 型超声波清洗仪 (昆山市超声仪器有限公司);电化学分析仪(上海辰华仪器公司CHI604E 型)。
试剂:四水合氯化金(HAuCl4·4H2O)、氯铂酸(H2PtCl6·6H2O)、柠檬酸钠、PVP(均为 AR,国药集团); PBS 缓冲溶液:磷酸一氢钠(Na2HPO4)+磷酸二氢钠(NaH2PO4)+氯化钾(KCl);氯化乙酰硫代胆碱(ATCl)、AChE(C3899,500 U/mg,Sigma 公司);甲基对硫磷(浓 100 mg/L,美国 o2si 公司)。
HAuCl4·4H2O 与 H2PtCl6·6H2O 储备液:将 0.5 g HAuCl4·4H2O 和 0.5 g HAuCl6·6H2O 分别溶解于水,定容至50 mL。
2.2 AChE/PVP/Au@Pt/PVP/GC CME 的制备
2.2.1 Au@Pt 核壳结构纳米粒子的制备
将 100 mL 含 0.01 g 的 HAuCl·44H2O 与 3 mL 1%的柠檬酸钠搅拌混合均匀,然后加热回流,即得到平均直径为13 nm 的金纳米粒子[8]。 吸取一定浓度的H2PtCl6·6H2O 和适量上述制备的纳米金晶种混合均匀,加入少许新配置的抗坏血酸溶液,在30℃~50℃温度下搅拌15 min,溶液由原来的淡红色变为棕黑色,即得到Au@Pt 核壳结构纳米粒子。
2.2.2 AChE/PVP/Au@Pt/PVP/GC CME 自组装修饰电极的制备
将玻碳电极在2000 目的金相砂纸上打磨,再用氧化铝(Al2O3)粉抛光至镜面,冲洗干净后,超声清洗。 在一定范围内电位下循环伏安扫描约30 圈,直至得到稳定的循环伏安图。
将预处理好的GC CME 在饱和PVP 乙醇溶液中浸泡12 h 后,用水冲洗,再将此电极置于核壳结构纳米粒子溶液中,用电极扫描100 圈,冲洗干净后修饰一层Au@Pt,即得到自组装电极——Au@Pt/PVP/GC CME。再将此电极在饱和PVP 乙醇溶液中浸泡12 h,用去离子水洗净,晾干,并在该电极表面滴涂一定浓度的AChE,得到AChE/PVP/Au@Pt/PVP/GC CME,电极修饰示意详见图1。
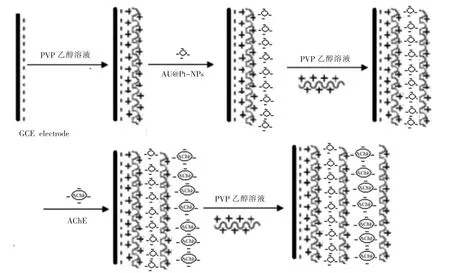
图1 AChE/PVP/Au@Pt/PVP/GC CME 自组装示意图
3 结果
3.1 AChE/PVP/Au@Pt/PVP/GC CME 对 ATCl 的电化学反应
将制得的AChE/PVP/Au@Pt/PVP/GC CME 放入pH=7.4 的 PBS 缓冲溶液中,在电位为 0.2~0.9 V 进行微分脉冲伏安扫描,结果详见图2。
由图2 可知,在0.5 V 左右出现一个氧化峰,这是AChE 水解PBS 中的底物ATCl 产生硫代胆碱(巯基胆碱),而巯基在正电压下被氧化所致。 核壳结构纳米粒子对ATCl 的氧化峰电流响应最大(图2c)。当AChE/PVP/Au@Pt/PVP/GC CME 受到一定浓度的甲基对硫磷农药的抑制后,峰电流相应变小(图2d、2e)。
3.2 试验条件的优化
试验表明,当PBS 的pH 为7.0 时,测得底物的氧化电流最大,说明在中性溶液中酶的活性最大,所以本试验选择pH=7.0 的PBS 溶液作为底液。将AChE/PVP/Au@Pt/PVP/GC CME 在含 5×10-5mol/L 的甲基对硫磷溶液中浸泡不同时间后,发现随着浸泡时间的增加,酶所受的抑制率逐渐增加,在15 min 后抑制率趋于平衡状态,所以本试验选择甲基对硫磷的浸泡时间为15 min。

图2 不同电极在相同底液中的微分脉冲伏安图
3.3 AChE/PVP/Au@Pt/PVP/GCE CME 对甲基对硫磷浓度的测定
随着有机磷浓度的增加,AChE/PVP/Au@Pt/PVP/GC CME 对底物ATCl 的氧化电流减弱(图3),经计算并作图(图4),发现在 1.5×10-5~1.0×10-3mol/L 酶抑制率与有机磷农药浓度的对数成正比关系,相关系数R≥0.998。该电极对PBS 中甲基对硫磷的检出限达 5.0×10-6mol/L。
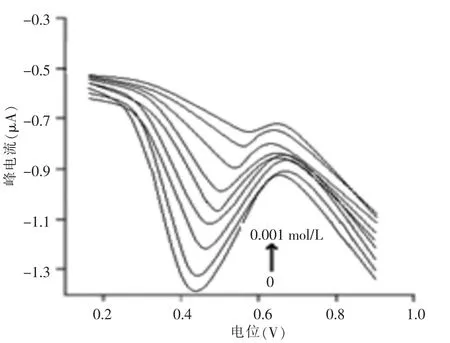
图3 AChE/PVP/Au@Pt/PVP/GC CME 对不同浓度甲基对硫磷的微分脉冲伏安图
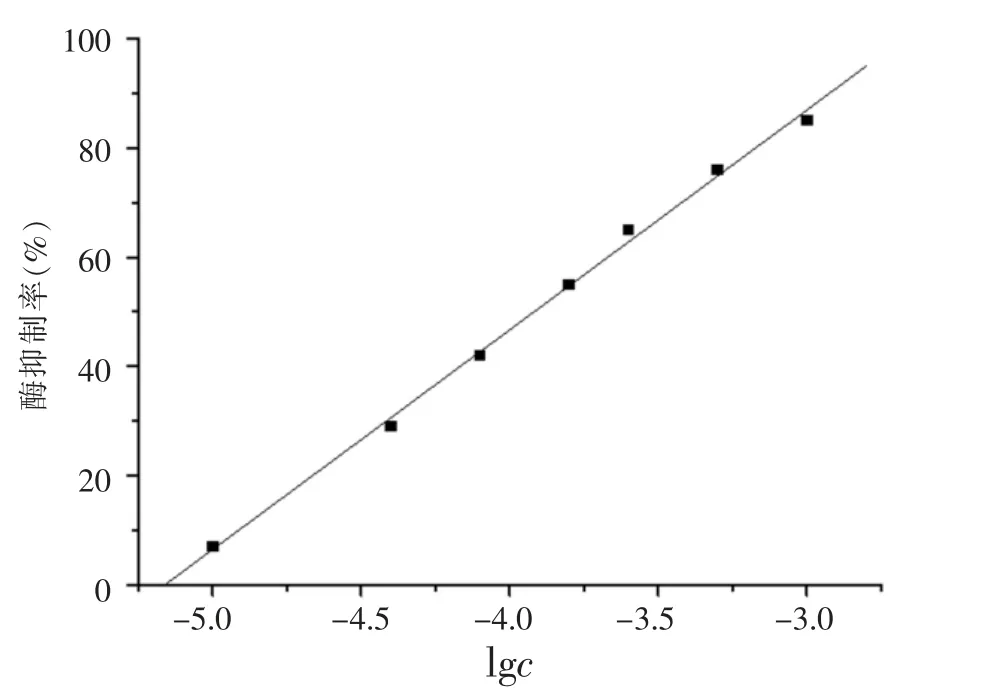
图4 酶抑制率(百分数)与有机磷农药浓度的对数关系图
3.4 AChE/PVP/Au@Pt/PVP/GC CME 的稳定性与选择性
为了考察所修饰电极的稳定性,使用AChE/PVP/Au@Pt/PVP/GC CME 在含 5×10-5mol/L甲基对硫磷的PBS 中浸泡15 min 后,对一定浓度的 ATCl 进行平行测定,相对标准偏差为3.5%,该电极具有良好的重复性。 将修饰电极在冰箱里保存,每隔3 d 对ATCl进行测定,其峰电流没有明显的变化,说明电极的稳定性良好。在优化的条件下,考察了未知样品中可能存在的离子对甲基对硫磷的干扰,结果表明,0.2 mol/L的钠离子(Na+)、镁离子(Mg2+)、铜离子(Cu2+)、锌离子(Zn2+)、钙离子(Ca2+)、硫酸根离子(SO42-)、硝酸根离子(NO3-)和磷酸根离子(PO43-)对 5×10-5mol/L 甲基对硫磷的测定基本没有干扰。
4 结论
本文研究了Au@Pt 核壳纳米粒子修饰的酶电极在中性PBS 介质中对甲基对硫磷的测定。 研究发现,Au@Pt 纳米修饰电极比单独纳米金和纳米铂修饰电极对ATCl 具有更加显著的催化水解性能,说明纳米金和纳米铂具有一定的协同催化能力。 双金属纳米粒子修饰电极测定甲基对硫磷具有良好的稳定性和选择性,且具有较宽的线性范围和较低的检出限。
