兽用疫苗制造检验用C型产气荚膜梭菌菌种的制备与检定标准和方法研究
2020-11-06彭国瑞李旭妮王秀丽李伟杰魏津马欣张一帜田野刘博李建罗玉峰李俊平彭小兵
彭国瑞李旭妮王秀丽李伟杰魏津马欣张一帜田野刘博李建罗玉峰李俊平彭小兵∗
(1.中国兽医药品监察所,北京 100081;2.中国农业大学动物医学院,北京 100193)
产气荚膜梭菌(Clostridium perfringens)是引起各种动物坏死性肠炎、肠毒血症、食物中毒和创伤性气性坏疽的主要病原菌,广泛分布于土壤环境和动物消化道。目前,我国使用的兽用产气荚膜梭菌疫苗有羊快疫、猝狙、羔羊痢疾、肠毒血症三联四防灭活疫苗、羊梭菌病多联干粉灭活疫苗(黑疫),仔猪A、C型产气荚膜梭菌病单价、二价灭活疫苗或是与大肠杆菌、诺魏氏梭菌等其他疫病组成的联苗以及兔A型产气荚膜梭菌病灭活疫苗等,制造这类灭活疫苗主要采用将相应血清型免疫原性良好的产气荚膜梭菌接种适宜的培养基培养后,用甲醛溶液灭活脱毒制成,其中菌株的产毒能力是决定疫苗质量的重要因素之一。
本文对用于兽用疫苗制造和检验用C型产气荚膜梭菌菌种进行了复壮、分离培养、冻干制备,对所制备的菌种形态、生化、培养、血清学、毒力和免疫原性等生物学特性检定方法进行了研究,为该菌种制备和检定操作方法的规范提供了技术基础。
1 材料与方法
1.1 材料
1.1.1 实验动物
3周龄20只SPF级雌性CD-1(ICR)小鼠,体重16~18 g,购自北京维通利华实验动物技术有限公司【SCXK(京)2016-0006】;10只普通级雌性日本大耳白兔,80~100日龄,体重1.5~2.0 kg,购自北京隆安实验动物养殖中心【SCXK(京)2019-0006】;2只普通肉用绵羊,1~2岁,购自河北满城养殖场。试验动物均饲养于中国兽医药品监察所生物实验基地【SYXK(京)2019-0011】。所有操作均符合中国兽医药品监察所动物福利伦理审查要求(编号:中监所(福)【2019】第00016号)。
1.1.2 实验试剂
产气荚膜梭菌CVCC60101(C59-1)株菌种(1960年7月30日冻干)由中国兽医微生物菌种保藏管理中心保藏并提供。A、B、C、D型产气荚膜梭菌定型血清由本实验室保存,普通肉汤、普通琼脂、肉肝胃酶消化汤、厌气肉肝汤、醋酸铅培养基、明胶缓冲液、石蕊牛奶培养基、蔗糖脱脂牛奶、明胶半固体培养基等购自北京中海生物科技有限公司,脱纤绵羊血购自北京索莱宝生物科技公司,细菌微量生化反应管购自杭州天和微生物试剂公司。
1.2 方法
1.2.1 菌种的复壮
开启产气荚膜梭菌CVCC60101菌种,接种厌气肉肝汤37℃培养24 h,转接肉肝胃酶消化汤37℃培养13 h。取培养物2 mL左后肢股内侧肌肉注射绵羊,观察1~2 d,死亡后立即剖检,取心肌、肝、脾、肾、后肢肌肉等组织制作石蜡切片进行病理分析;同时取肝、心血、注射部位肌肉渗出液分别接种肉肝胃酶消化汤,37℃培养24 h,革兰氏染色镜检[1]。
1.2.2 冻干菌种的制备
取死亡羊剖检分离接种的肉肝胃酶消化汤培养物分别接种厌气肉肝汤、普通肉汤、普通琼脂斜面,37℃培养24 h后,用肉肝胃酶消化汤扩大培养,3000 r/min离心30 min,弃上清,在沉淀中加入蔗糖脱脂牛奶混匀,每支0.2~0.3 mL分装安瓿,冻干封口,2~8℃保存。
1.2.3 真空度和剩余水分测定
新制备冻干菌种按照《中国兽药典》(2015年版三部)规定测定真空度,随机取真空度合格安瓿12支,分为4组,每组3支混合测定剩余水分含量。
1.2.4 纯粹检验与培养特性检定
新制备菌种5支开启后,分别用普通肉汤溶解,接种厌气肉肝汤、普通肉汤、普通琼脂斜面、石蕊牛奶小管,37℃培养24 h。取厌气肉肝汤培养物划线接种含2%葡萄糖10%绵羊血的普通琼脂平板,37℃厌氧培养24 h。
1.2.5 形态和生化特性检定
取新制备菌种厌气肉肝汤培养物进行革兰氏染色镜检。同时接种明胶半固体培养基、醋酸铅培养基,另挑取约10μL分别接种糖发酵管,均37℃厌氧培养10 d。
1.2.6 小鼠毒力测定
新制备菌种厌气肉肝汤培养物接种肉肝胃酶消化汤100 mL,37℃培养17 h。取20 mL 3000 r/min离心30 min,上清用0.22μm滤器过滤,分装滤液,-70℃保存作为毒素备用。毒素冷水浴融化后,取0.5 mL加入9.5 mL明胶缓冲液20倍稀释后,按比例稀释,尾静脉注射小鼠,每个滴度2只,每只0.2 mL,24 h后,测定小鼠1 MLD毒素原液量含量。
1.2.7 血清学特性检定
取-70℃保存毒素加入1%胰酶,37℃作用1 h,3000 r/min离心30 min,取上清每只0.2 mL尾静脉注射小鼠2只;另取毒素稀释至3 MLD/0.2 mL,取A、B、C、D型产气荚膜梭菌定型血清各0.3 mL分别加入0.6 mL毒素稀释液中混匀,37℃作用45 min,每型血清中和物分别每只0.3 mL尾静脉注射小鼠各2只;另取小鼠2只,每只0.2 mL尾静脉注射3 MLD/0.2 mL毒素稀释液作为对照,观察24 h。
1.2.8 免疫原性检定
(1)疫苗的制备与免疫
取新制备菌种肉肝胃酶消化汤培养物60 mL,按0.75%加入甲醛溶液(40%),摇匀,37℃灭活脱毒12 d,每日振摇4次。灭活脱毒培养物分别接种厌气肉肝汤小管、普通肉汤小管、普通琼脂斜面小管各1支,37℃培养7 d,检验灭活效果;另取灭活脱毒培养物12 000 r/min离心15 min,取上清每只0.4 mL尾静脉注射小鼠2只,观察72 h,检验脱毒效果。将灭活脱毒完全的肉肝胃酶消化汤培养物用氢氧化钠溶液调节pH值至7.0,按5∶1(体积:质量)加入灭菌氢氧化铝胶佐剂充分混合作为疫苗,每只1.0 mL颈背部皮下注射日本大耳白兔4只,连同对照兔2只、测毒用兔7只在相同条件下饲养。
(2)毒力测定与攻毒
取-70℃保存毒素,冷水浴融化后,0.5 mL加入9.5 mL明胶缓冲液进行20倍稀释后,按适当比例稀释,耳缘静脉注射测毒用兔,每只1.0 mL,观察72 h,测定日本大耳白兔1 MLD毒素原液含量。免疫组日本大耳白兔免疫14 d后,取与测毒同批毒素0.5 mL加入9.5 mL明胶缓冲液进行20倍稀释后,用1 MLD毒素每只1.0 mL耳缘静脉注射攻毒,免疫组注射4只,对照注射2只,观察5 d。
2 结果
2.1 菌种的复壮
注射羊1 d内死亡,进行解剖。取心脏、肝、注射部位肌肉等组织制作石蜡切片进行病理分析,见较大面积组织坏死(黑色箭头),淋巴细胞浸润(红色箭头),大量细菌团块(黄色箭头)(见图1)。接种注射部位肌肉渗出液、肝、心血的肉肝胃酶消化汤浑浊生长且产生大量气体。涂片染色后显微镜下均可见呈紫色大杆菌,革兰氏阳性,两端钝圆,菌形一致,单个散在或成双或多个聚集分布,符合产气荚膜梭菌特征。结果表明,产气荚膜梭菌在攻毒绵羊体内大量繁殖,引起组织病变,动物发生急性死亡。

图1 组织病理学分析(HE染色,×400)Figure 1 Histopathological analysis(HE staining,×400)
2.2 冻干菌种的制备
取致死羊组织接种的肉肝胃酶消化汤培养物,转接厌气肉肝汤,见浑浊生长且大量产气、普通肉汤混浊生长、普通斜面不生长。经扩大培养分装冻干,共制备冻干菌种221支。
2.3 真空度和剩余水分测定
经测定214/221支冻干菌种安瓿真空度均符合规定。剩余水分含量测定结果分别为1.5%、1.5%、1.5%、1.7%,均小于3%,符合规定。
2.4 纯粹检验和培养特性检定
所制备的菌种5/5在厌气肉肝汤中纯粹生长,培养4 h产生大量气体,普通肉汤纯粹混浊生长,普通琼脂斜面不生长,在石蕊牛奶中爆性发酵;在血琼脂表面上形成1~3 mm、半透明、灰白色、表面光滑、边缘整齐的圆形菌落,呈现β、α双溶血环。
2.5 形态和生化特性检定
革兰氏染色显微镜观察,菌体呈紫色大杆菌,为革兰氏阳性菌,两端钝圆,菌形一致,单个散在或成双或多个聚集分布。使醋酸铅培养基颜色变黑,明胶半固体培养基液化;接种糖发酵管10 d内观察,菌种形态和生化特性均符合产气荚膜梭菌特征。
2.6 小鼠毒力测定
按表1稀释毒素尾静脉注射小鼠,观察24 h。结果表明,小鼠1 MLD含0.00075 mL毒素原液,毒力达到《中国兽用生物制品规程》标准[1]。
2.7 血清学特性
毒素原液经胰酶处理后,注射小鼠,未发生死亡,表明该菌种产生的毒素可以被胰酶破坏,因此不是B型或者D型产气荚膜梭菌,为A型或者C型;血清中和实验结果显示,该菌种产生的毒素与A型和D型定型血清中和物注射小鼠全部死亡,与B型、C型定型血清中和物注射小鼠未发生死亡,表明B型和C型血清可以中和该菌种产生的毒素。综上表明,该菌种为产气荚膜梭菌C型。
2.8 免疫原性检定
2.8.1 疫苗的制备与免疫
灭活脱毒培养物接种厌气肉肝汤小管、普通肉汤小管、普通琼脂斜面小管均无细菌生长。离心上清注射小鼠,未见死亡,表明培养物灭活脱毒完全,制成灭活铝胶菌苗免疫日本大耳白兔4只,免疫期14 d内均健活。
2.8.2 毒力测定
按表2方法稀释毒素静脉注射日本大耳白兔,结果表明,1 MLD为0.02 mL毒素原液。
2.8.3 免疫攻毒结果
按照测毒结果将毒素稀释至每毫升含毒素原液0.02 mL,即日本大耳白兔1 MLD,耳缘静脉注射免疫组和对照组,免疫组4/4保护,对照2/2死亡。表明,该菌种的免疫原性符合规定。
3 讨论
C型产气荚膜梭菌毒素含有α、β毒素,B型产气荚膜梭菌毒素含有α、β、ε毒素。其中,α、β毒素对胰酶敏感,胰酶处理可以使其完全失去活性;而ε毒素为前体毒素,需经胰酶、糜蛋白酶等酶的活化,产生毒性[2-5]。若待检菌种为C型产气荚膜梭菌,因其毒素中含有α、β毒素,经胰酶处理后,失去毒性,注射小鼠应存活;若待检菌种为B型产气荚膜梭菌,因其毒素除含有α、β毒素外,还含有无毒性的ε毒素前体,经胰酶处理后ε毒素前体被活化,产生毒性,注射小鼠应死亡。本研究结果显示,待检菌种毒素原液经胰酶处理,注射小鼠,2/2存活;用未经胰酶处理的毒素作为对照注射小鼠,2/2死亡。说明经胰酶处理后,该毒素不表现毒性,故不含有ε毒素。综上,可将待检产气荚膜梭菌判定为C型。
《中国兽用生物制品规程》中的《羊快疫、猝狙(或羔羊痢疾)、肠毒血症三联灭活疫苗制造及检验规程》仅规定用产气荚膜梭菌定型血清做中和试验检查CVCC60101(C59-1)株为血清C型,而《产气荚膜梭菌病定型血清制造及检验规程》也仅规定了中和试验结果判定方法[1]。由于B型和C型血清都可以分别中和B型和C型产气荚膜梭菌毒素,A型和C型血清均不能中和这两种毒素,因此,仅通过中和试验不能对B型和C型产气荚膜梭菌的血清型做出区分,需采用测毒、胰酶处理和血清中和试验三步进行检定。

表1 小鼠毒力测定结果Table 1 Results of virulence testing by mice
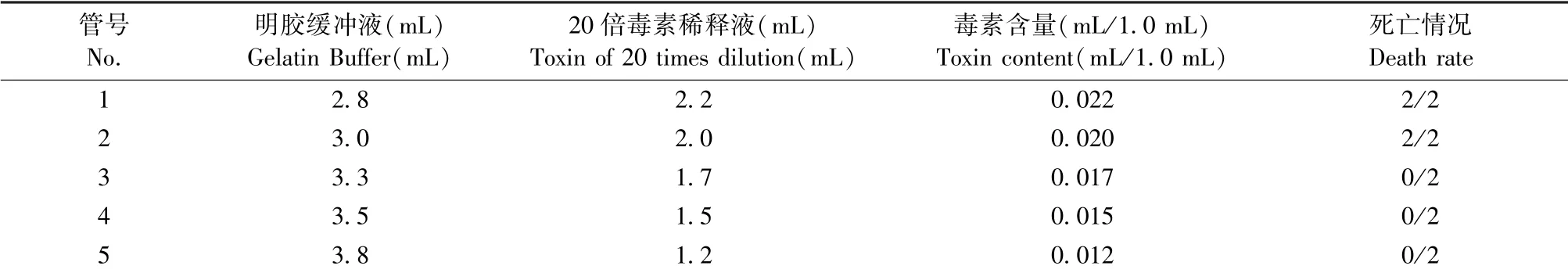
表2 用兔测定毒力Table 2 Results of virulence testing by rabbits
目前,检定生产检验用C型产气荚膜梭菌菌株主要依据《中国兽用生物制品规程》,该“规程”对菌种的形态和生化特性、培养特性、血清学特性、毒力、免疫原性以及纯粹性作出了规定,但仍缺乏对菌种的制备以及检定项目更为详细的操作规范。本研究从菌种的易感动物复壮、冻干制备以及检定操作方法等方面进行了研究,为进一步规范该菌种的制备、质量检定标准和操作方法提供了技术依据。
