化疗患者味觉改变的个体化干预及效果评价
2020-11-04张丽燕国仁秀张婷婷梁亚茹许晨辉
张丽燕,国仁秀,张婷婷,梁亚茹,许晨辉
(北京大学肿瘤医院暨北京市肿瘤防治研究所 消化肿瘤内科,北京100142)
味觉改变(chemotherapy-induced taste alteration,CiTA),是指味觉受损或味觉反常,或一种不愉快的味觉变化[1],包括味觉缺失、味觉减退、味觉不良、味觉倒错和幻味觉等。研究[2-4]显示,肿瘤患者因化疗药物以及疾病等原因导致味觉改变的发生率高达36%~84%,且约有40%的肿瘤化疗患者因味觉改变出现营养不良[5],并最终导致患者的生活质量降低[6]、预后不良。本研究旨在结合国外经验探讨有效的干预策略,以缓解化疗患者味觉改变,提高患者的生活质量。
1 对象与方法
1.1 研究对象 便利抽样选取2018年9月至2019年7月于北京某三级甲等肿瘤医院住院的化疗患者。其中,2018年9-12月入组的患者设为对照组,2019年4-7月入组的患者设为干预组。纳入标准:年龄 ≥18周岁;病理学确诊为恶性肿瘤;化疗2次及以上;经中文版化疗相关味觉改变量表(the chemotherapy-induced taste alternation scale,CiTAS)[5]评估为味觉改变;预计生存期≥6个月,有读写能力;签署知情同意书。排除标准:首次化疗者;同时放疗者;不能经口进食者;有精神或意识障碍者。应用PASS软件计算样本量,结果为每组60人,按10%失访计算,确定样本量为66例。
1.2 研究方法
1.2.1 对照组 行常规宣教,对于恶心、呕吐等症状严重者告知医生予以处理,出院时告知居家饮食和营养的方法及注意事项。
1.2.2 干预组 成立多学科小组,由1名营养师、1名肿瘤医生、1名康复科医生和4名工作5年以上的主管护士组成。入院后,护士应用CiTAS评估患者上一周期味觉改变的程度与表现类型,参照宾夕法尼亚大学肿瘤中心健康管理指南[7]结合患者饮食习惯,制定个体化的干预方案[7-9]:对于味觉缺失者,告知进食味道浓重的食物;经常变换食物种类、菜色搭配及烹调方法;对于味觉减退者,指导吃硬糖、口香糖;增加食盐、糖、香料等调味品;对于口腔异味者,指导其进食清淡食物,采取蒸煮等烹饪方式,避免冷食;对于味觉倒错的患者,指导减少盐、糖等调味品;用果汁、糖、料酒浸泡肉类,以提高对肉类的接受度;出现幻味觉时,指导使用塑料或陶瓷餐具,避免使用金属餐具和罐装饮料;进冷食,避免牛肉;对于出现苦味者,指导使用醋、糖、柠檬汁等调味;口腔干燥者多饮水,注意口腔卫生;对于恶心呕吐等不良反应严重者,告知主管医生或康复科医生予以药物或非药物性干预;对于进食严重减少者,护士用NRS 2002进行筛查,营养师对存在营养不良风险者进一步评定,并与团队共同制定干预策略;对于存在明显不良情绪的患者,由康复科医生予以心理疏导。护士于化疗时、化疗后1周进行电话随访,了解干预措施的执行情况,化疗不良反应缓解以及进食情况,对于患者食物选择制作方式等执行过程中存在的问题和不依从的原因予以分析和进一步指导。必要时联系相关医生,对患者进行门诊访视。
1.2.3 评估工具 (1)患者一般资料问卷:自行设计,包括患者性别、年龄、文化程度、婚姻状况、疾病部位、化疗方案、化疗次数等情况。(2)中文版CiTAS:由Kano等[4]编制,钱立晶等将其汉化为中文版[5]。该量表内部一致性系数为0.766,重测信度为0.705,包括基本味觉减退(5个条目)、味觉异常(3个条目)、整体味觉改变(4个条目)、进食困扰(6个条目)等4个维度18个条目,每个条目采用Likert 5级评分,1分表示没有改变,5分为非常严重。总分18~90,各维度总分/条目数即为各维度标化分值,得分越高说明味觉障碍越严重。(3)欧洲癌症研究与治疗组织开发的生活质量核心问卷(the quality of life questionaire-core 30,QLQ-C30)[10],为癌症患者普适的生活质量测评工具。由万崇华等[11]进行汉化,其中文版有较好的信效度。量表有30个条目,包括5个功能维度(躯体功能、角色功能、情绪功能、认知功能、社会功能)、9个症状维度(疲倦、恶心与呕吐、疼痛、气促、失眠、食欲丧失、便秘、腹泻、经济困难)和1个总体健康状况。其中总体健康状况条目采用1~7分评分,其他条目均采用Likert 4级评分,从“没有”到“很多”依次计1~4分。按照计分规则将各维度得分变换为标准分,分值0~100分。功能维度和总体健康状况得分越高,说明功能和生活质量越好;症状维度得分越高,表明症状越严重。以上(2)、(3)项在所有患者入组及干预3个月时进行评估。
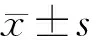
2 结果
2.1 两组患者一般资料比较 两组共132例患者,年龄22~80岁,平均 (55.78±13.48)岁。经比较,干预前两组性别、年龄、文化程度、婚姻状况、疾病部位、化疗方案、化疗次数等方面差异均无统计学意义(均P<0.05,表略)。
2.2 干预前后两组CiTAS得分及生活质量比较 干预组患者中,91%尝试使用了1种干预措施,69%使用了2种以上措施,干预后CiTAS总分明显降低(P<0.01),其中整体味觉、味觉异常及不适症状等维度问题有所改善(均P<0.05)。总体生活质量、躯体功能、社会功能、情绪功能有所提升(均P<0.05),疲乏、恶心呕吐、食欲丧失和便秘等症状明显改善(P<0.01),且以上条目除整体味觉维度外,均优于干预后对照组情况(均P<0.05),具体见表1。
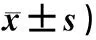
表1 两组患者干预前后味觉改变及生活质量比较(分,
3 讨论
3.1 个体化干预有利于缓解味觉改变程度 肿瘤患者味觉改变的比例高达36%~84%[2-4],但综观国外和国内报道,仅有17.0%和7.6%的患者接受过比较笼统的相关教育,故不能有效帮助其掌握应对策略[12-13]。本研究中多学科团队在参照国外指南基础上结合国人饮食特点,针对不同味觉改变表现类型予以指导,使得干预组患者CiTAS总分明显降低,味觉异常和不适症状两个维度明显好转,且明显优于对照组。分析原因为:个体化干预结合了患者饮食习惯,措施贴近生活、易于操作,其中91%患者尝试使用了1种干预措施、69%使用了2种以上措施。而整体味觉和基本味觉改变未见显著差异,与其他研究类似[10]。分析原因可能与味觉细胞受损有关,难以通过短时间的饮食调整得以改变。提示医务人员需探讨有助于保护或修复味觉细胞的药物、中医等策略,以从根本上予以改善。
3.2 个体化味觉干预须配合持续的健康教育 随访中发现因味觉改变并不威胁生命,患者及家属对味觉改变的重视程度有待提升,这些是影响干预依从性和效果的主要因素。提示护士需详细、多次讲解味觉改变对身心健康乃至治疗效果的潜在影响,以引起患者重视。同时,患者食物的选择和制作方式受到居住环境的影响,提示味觉改变的干预应改变传统的院内宣教,需连续多次随访、个体化分析患者居家的具体饮食结构和偏好,反复宣教强化并纠正存在的误区,提供个体化操作性强的策略,以促进干预效果。
3.3 个体化干预有利于提高味觉改变患者的生活质量 研究[9,14]显示:味觉改变会对患者的生理心理方面带来诸多负面影响,存在味觉改变者,生活质量明显低于无味觉改变者。这是由于味觉改变会使进食的愉悦感与满足感降低、导致患者食欲下降,营养不良,躯体功能下降;同时,味觉改变会给患者带来进食相关社交困扰,更容易产生愤怒、失望以及悲伤等负性情绪,影响其社会和情绪功能。国外研究[14-17]证实有效的味觉干预有助于提升患者生活质量,与本研究结果类似。分析原因为:个体化干预可缓解味觉改变症状,有利于改善患者食欲、提高营养水平,从而改善自理、活动等躯体功能,同时有助于缓解疲乏[18]。另外,干预后患者有针对性的饮食结构调整,有助于缓解便秘和恶心呕吐等不适症状;患者不适症状、进食困扰的改善,进一步有助于缓解患者相关社交压力,使其心情愉悦,增强战胜疾病的信心,最终整体健康水平得以提升。
