食管裂孔疝抗反流术保留迷走神经对术后复发风险影响的Meta分析
2020-10-24邰沁文肖杨张金辉高峰王元喜蔡理全张恒黄金华李宁磊
邰沁文 肖杨 张金辉 高峰 王元喜 蔡理全 张恒 黄金华 李宁磊
胃食管反流病(gastroesophageal reflux disease,GERD)是指胃或十二指肠内容物反流入食管,引起反酸、烧心等不适症状和(或)食管狭窄、出血等并发症的一种疾病[1]。食管裂孔疝(hiatal hernia,HH)和GERD有着极其密切的关系[2]。HH分为Ⅰ型、Ⅱ型、Ⅲ型和Ⅳ型。Ⅰ型指滑动性HH,为胃贲门部进入胸腔;Ⅱ型指食管旁型裂孔疝,为胃底于食管旁疝入胸腔而胃贲门部未进入胸腔;Ⅲ型指复合型裂孔疝,即滑动性HH和食管旁裂孔疝同时存在,即胃贲门部和胃底都疝入胸腔;Ⅳ型指巨大型HH(疝环>5 cm或三分之一以上胃及其他腹腔脏器疝入胸腔),此型约占HH的5%~15%[3]。在HH中,特别是滑动型HH中,抗反流屏障的正常解剖结构被破坏,其抗反流作用减弱,使得食管酸暴露增加;另外,含酸性的物质储存于疝囊中,当吞咽引起食管下括约肌松弛时也易出现酸反流而导致酸清除时间延长。因此,HH和GERD常常合并发生[2]。
目前,HH合并GERD的主要治疗方式为外科手术,手术方式为HH修补联合胃底折叠术。其中,腹腔镜Toupet胃底折叠术将胃底由食管后方作180°~270°包绕缝合,该术式最早在贲门肌层切开术中应用,可加强贲门部的关闭能力,近年来逐渐应用于HH引发GERD的治疗[4,5]。尽管抗反流手术在短期和长期的术后随访中取得了良好结果,却仍然伴随着围手术期并发症及复发风险。据统计,HH修补术后复发率为5%~59%,短食道综合征、膈肌脚修补不全以及身体质量指数值都是术后复发的诱因之一[6]。
早期研究报道了迷走神经切断术对胃溃疡的治疗效果,结果发现迷走神经切断术伴有恶心15%、呕吐4%、腹泻(20%~30%)和倾倒综合征(10%),而在抗反流手术中损伤迷走神经可能导致新的术后并发症及GERD相关症状的复发[7-11]。Van Rijn等[12]通过前瞻性研究发现抗反流术中迷走神经损伤率可达20%,6个月随访期内迷走神经损伤对患者预后无明显影响,而长期随访结果显示损伤迷走神经在一定程度上加重抗反流术后GERD症状及再复发风险。但目前尚无相关文献系统评价抗反流术中联合迷走神经切断对于HH术后复发是否相关。本文旨在使用Meta分析评估抗反流术中迷走神经切断对于术后反流症状控制及HH复发的影响作用。
资料与方法
一、文件检索策略
1.数据库:文献的检索按照PRISMA声明要求检索数据库包括Pubmed、Web of Science、Embase、ScienceDirect、ovid、CNKI数据库,检索时限均从建库至2019年9月。
2.检索词与检索式:包括“anti-reflux surgery”、“hiatal hernia or hiatus hernia”、“hernia repair”、“vagotomy”、“surgery”、“recurrence”
3.文献质量评估:选择所有关于抗反流手术过程中迷走神经切断与保留对HH术后复发风险的临床研究,包括这些原始研究中参考文献及相关文献。为了扩大检索结果,用相关文献功能,纳入和排除文献、数据的提取及文献质量评估有2名研究者独立进行,有分歧者通过研究组讨论决定。本研究使用Cochrane5.1.0系统评价手册进行文献质量评估,每篇纳入的文献都进行独立质量评估。
二、纳入与排除标准
1.纳入标准:(1)国内外比较抗反流手术中切断与保留迷走神经对术后HH复发风险比较的临床实验;(2)行抗反流手术的HH患者,迷走神经切断组在采用抗反流手术中切断迷走神经,迷走神经保留组抗反流手术保留迷走神经,比较术后HH的复发风险(按诊断方式分为解剖复发和临床复发);(3)英文和中文文献。
2.排除标准:(1)重复报道;(2)综述性文献;(3)病例报道;(4)动物研究;(5)非外科手术的抗反流治疗方法;(6)数据不完整或无法提取数据的文献。
三、方法
(一)文件检索策略
1.数据库:文献的检索按照PRISMA声明要求检索数据库包括Pubmed、Web of Science、Embase、ScienceDirect、ovid、CNKI数据库,检索时限均从建库至2019年9月。
2.检索词与检索式:包括“anti-reflux surgery”、“hiatal hernia or hiatus hernia”、“hernia repair”、“vagotomy”、“surgery”、“recurrence”
3.文献质量评估:选择所有关于抗反流手术过程中迷走神经切断与保留对HH术后复发风险的临床研究,包括这些原始研究中参考文献及相关文献。为了扩大检索结果,用相关文献功能,纳入和排除文献、数据的提取及文献质量评估有2名研究者独立进行,有分歧者通过研究组讨论决定。本研究使用Cochrane5.1.0系统评价手册进行文献质量评估,每篇纳入的文献都进行独立质量评估。
(二)数据收集与分析
1.选取研究:阅读初步检索文献的摘要并根据纳入标准确定最终进入Meta分析的文献源。如摘要未提供足够数据,则分析全文以决定是否纳入本研究。
2.相关资料:相关资料内容包括一般信息(作者、发表年月)、病例数、随访时间、抗反流手术类型、迷走神经切断方式、评估指标,即影像学(X线食管吞钡摄片)诊断复发阳性率、临床(临床胃食管反流症状表现及24 h pH监测或胃镜)诊断复发阳性率。
3.数据分析:采用Review Manager 5.3软件进行数据分析。根据Cochrane循证医学指南的建议,二分类数据(HH复发与否)表示为比值比(odds ratio,OR)和95%可信区间。合并效应量的统计推断采用Z检验,以P<0.05为差异有统计学意义。纳入研究结果间的异质性统计推断采用Q检验计算I2,如果I2<50%,并且P>0.1,则说明合并不存在异质性,采用固定效应模型进行合并,反之则用随机效应模型进行合并。明显的临床异质性采用亚组分析或敏感性分析等方法进行处理。
3.偏倚评估:应用Cochrane风险偏倚评估工具评估了一下几个方面的偏移,有序列生成,分配隐藏、盲法、不完整的结果数据。各项偏倚被评估分级。“高风险”和“低风险”表明文章中阐述明确。对于不明确的偏移,评级为“未知风险”。
结 果
一、文献检索结果及特征
通过检索式初选出共505篇文献,剔除重复发表的文献8篇、综述型文献41篇。按纳入和排除标准进一步筛选文献,最终纳入11篇文献[12-22]。见图1。选自发表时间自1967年至2007年作为纳入研究的随访时间,抗反流手术和迷走神经切断术方式,以及纳入分析的病例数(见表1),不同亚组的研究结果(见表2),抗反流术后X线食管吞钡钡餐摄片诊断为HH复发组相关研究、入组病例数及复发病例数(见表3),抗反流术后由食管24 h pH监测及胃镜诊断为HH复发组的相关研究、入组病例数及复发病例数等(见表4)。
二、入选研究的偏倚
所有入选研究在设计阶段即存在至少一个局限性,所有研究在随机数产生及分配隐藏方面存在选择偏倚,半数以上研究在盲法及盲法结果评价方面不存在偏倚,其原因在于手术治疗的特殊性,难以实施盲法,除一项研究不确定盲法外,其他研究均未采用盲法(见表5)。
三、Meta分析结果
1、HH解剖的复发情况
通过上消化道造影诊断抗反流术后HH复发,比较迷走神经切断组及迷走神经保留HH复发风险[13-18,22]。主要通过食管吞钡摄片证实,随访期内亚组分析显示,迷走神经切断与迷走神经保留异质性检验,无异质性,差异无统计学意义(I2=32%,P>0.05)。术后HH复发风险比较,OR=1.96,95% CI=1.45~2.64,差异有统计学意义(Z=4.41,P<0.05)。结果表明,迷走神经切断HH复发风险高于迷走神经保留。
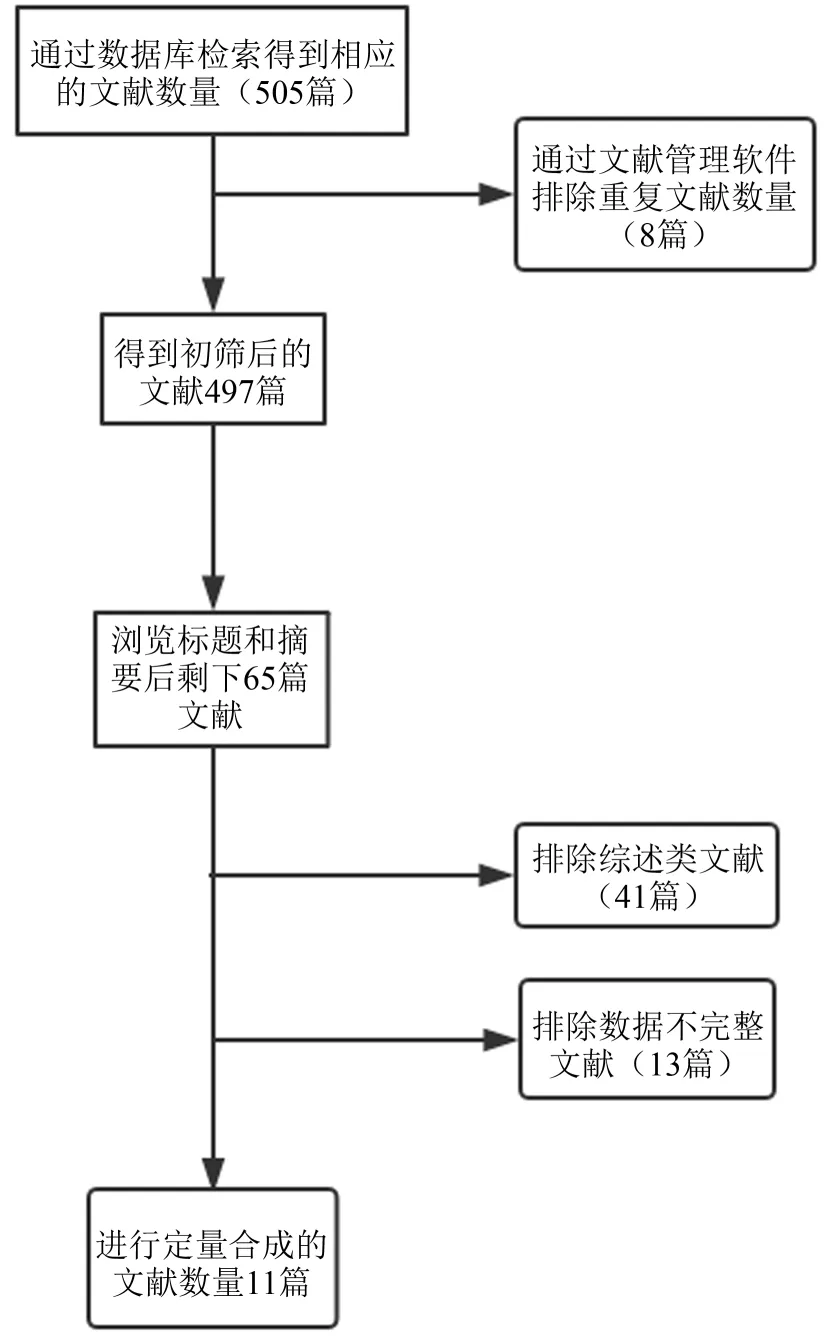
图1 文献检索流程图
2、HH临床复发
通过临床GERD症状表现及食管24 h pH监测或胃镜结果诊断抗反流术后HH复发(GERD症状包括反酸、烧心、胸骨后疼痛等典型症状)[14,15,17-22]。同时比较迷走神经切断及迷走神经保留HH复发风险。依据灵敏度分析显示占异质性权重最大的研究来自Woodward等[15]。将该研究排除外,异质性则消除(I2=31%,P>0.05),HH复发风险比较,OR=1.56,95% CI=1.10~2.22,差异具有统计学意义(Z=2.52,P<0.05)。同解剖复发组结果相似,迷走神经HH临床复发风险同样高于迷走神经保留。
3、HH总体复发率分析
合并临床复发与解剖复发两组分析显示,迷走神经切断与迷走神经保留抗反流术后HH复发风险不存在异质性(I2=27%,P>0.05),术后复发风险比较,OR=1.78,95% CI=1.42~2.24,差异具有统计学意义(Z=5.01,P<0.05)。亚组组间卡方检验显示组间差异不存在异质性(I2=0%,P>0.1)。
讨 论
GERD是常见的消化系统疾病,其发病率有逐年增高的趋势[23]。对质子泵抑制剂治疗有效但需长期服药的患者,抗反流手术是最佳选择。最常见的手术方式包括腹腔镜HH修补术联合胃底折叠术。大多数患有GERD的患者同时合并食管裂,而肥胖(体质量指数>35 kg/m2)、食管过多游离等因素可能是HH抗反流术后复发的原因之一[24,25]。
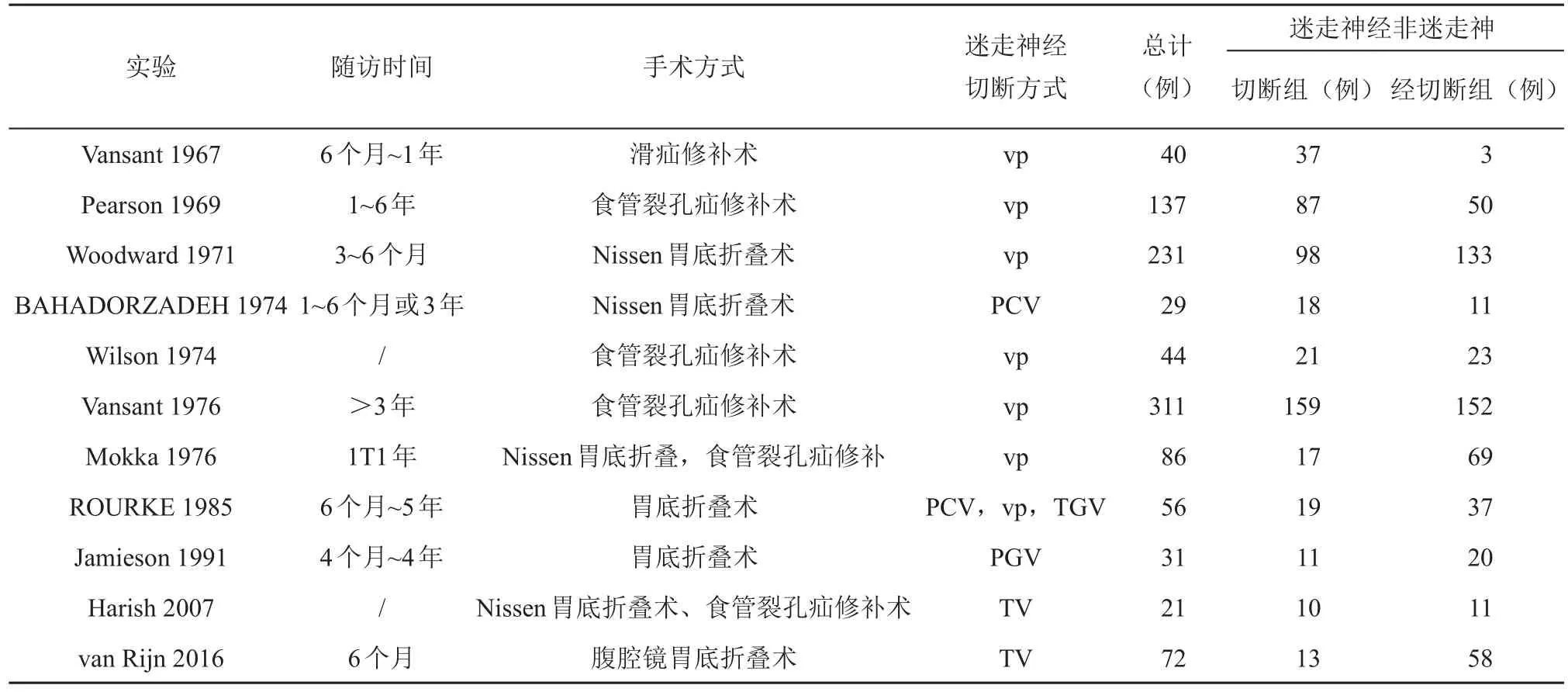
表1 入选Meta分析的对照实验
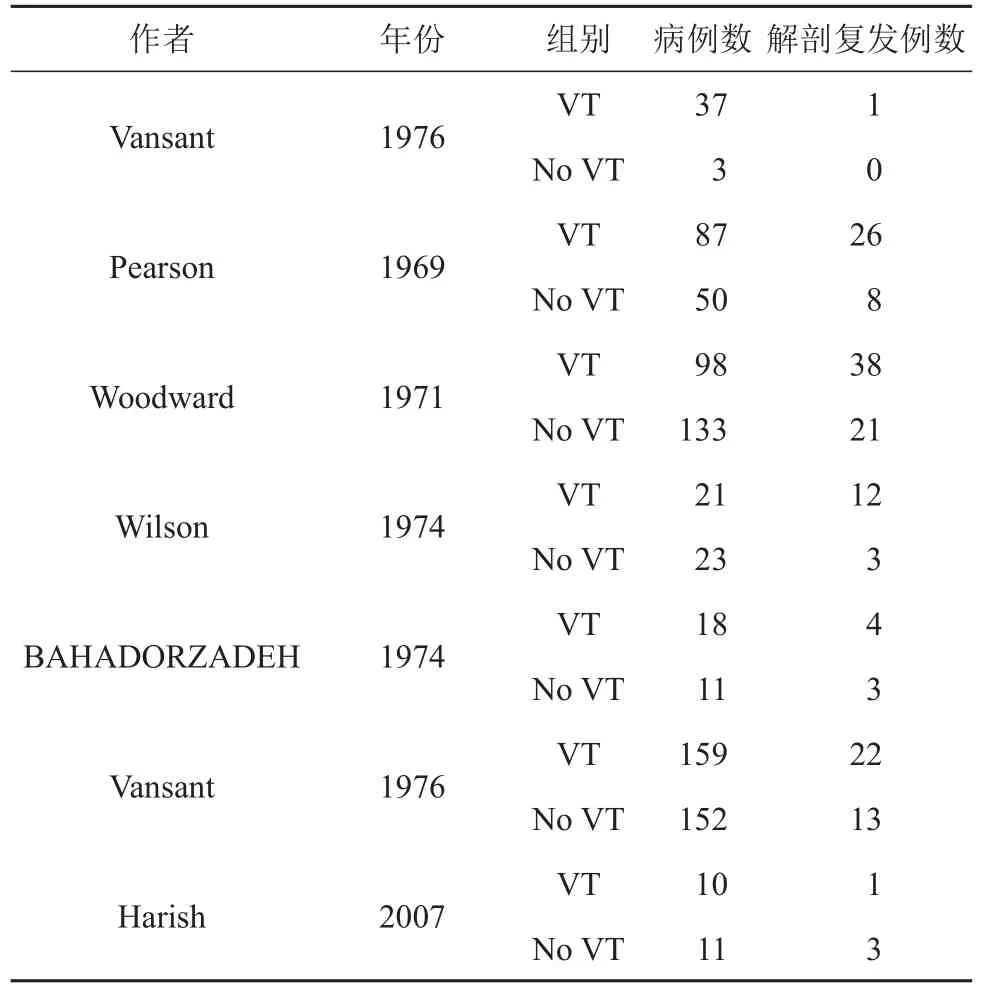
表2 纳入解剖复发组的研究结果
目前,抗反流术中关于迷走神经保留与否是否影响HH术后复发及症状改善等问题的相关研究却寥寥无几,且已有的研究数据尚不能得出确切结论。因此,本文立足于这一目的,查阅并搜集分析大量文献,探讨分析抗反流术中迷走神经切断对术后HH复发风险的影响。
HH修补术后的复发主要分为如下两种。一是解剖复发。即通过影像学检查有HH的表现,如X线、胃镜、电子计算机断层扫描等影像学检查,而患者并无临床相关症状。二是症状复发。症状复发又分为两种,一种情况是有影像学复发即解剖复发的证据,同时患者又出现了HH的临床症状或GERD的症状;而另一种情况就是患者仅出现症状的复发,而影像学不表现出解剖复发的证据[26]。本研究则通过吞钡X线摄片诊断HH的解剖复发,而临床GERD症状和(或)胃镜及24 h pH监测结果诊断HH临床复发。
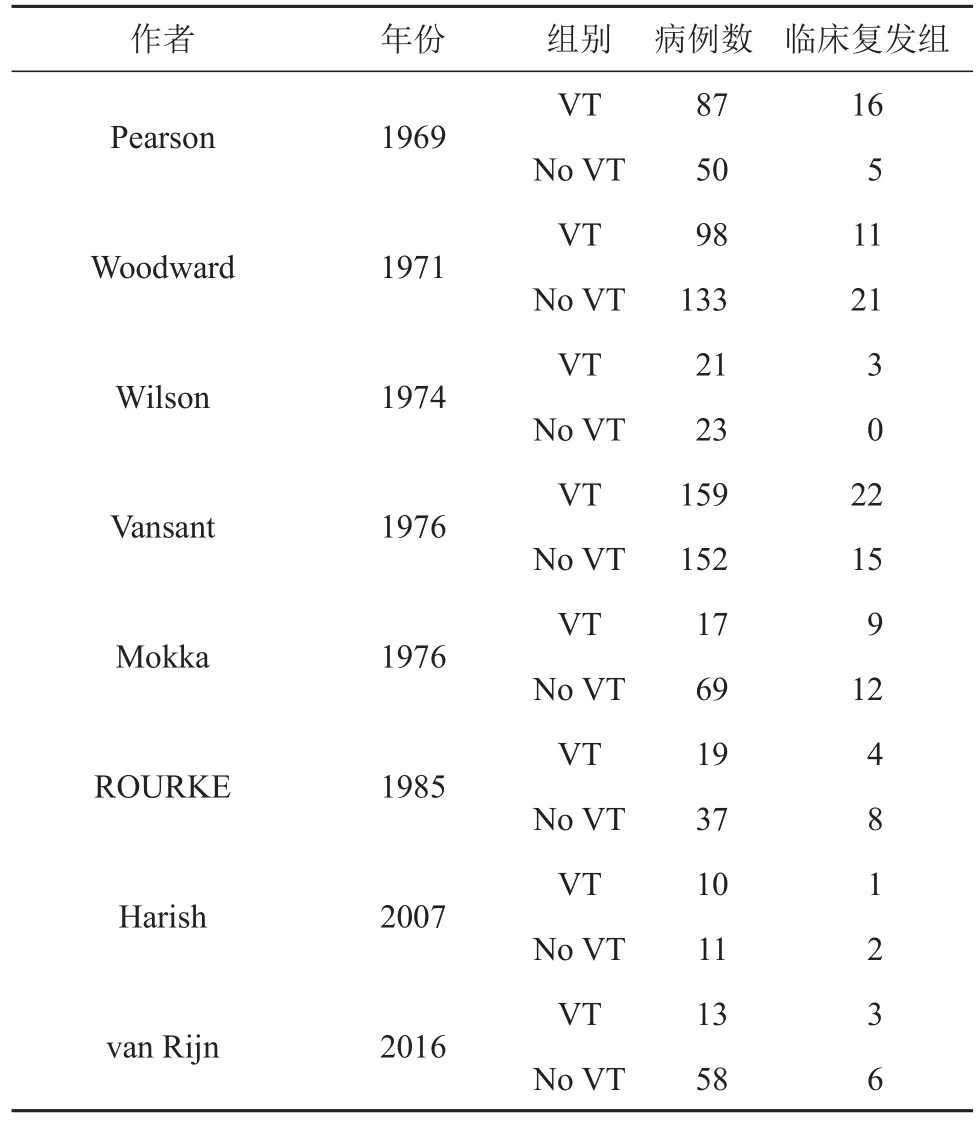
表4 纳入临床复发组研究结果
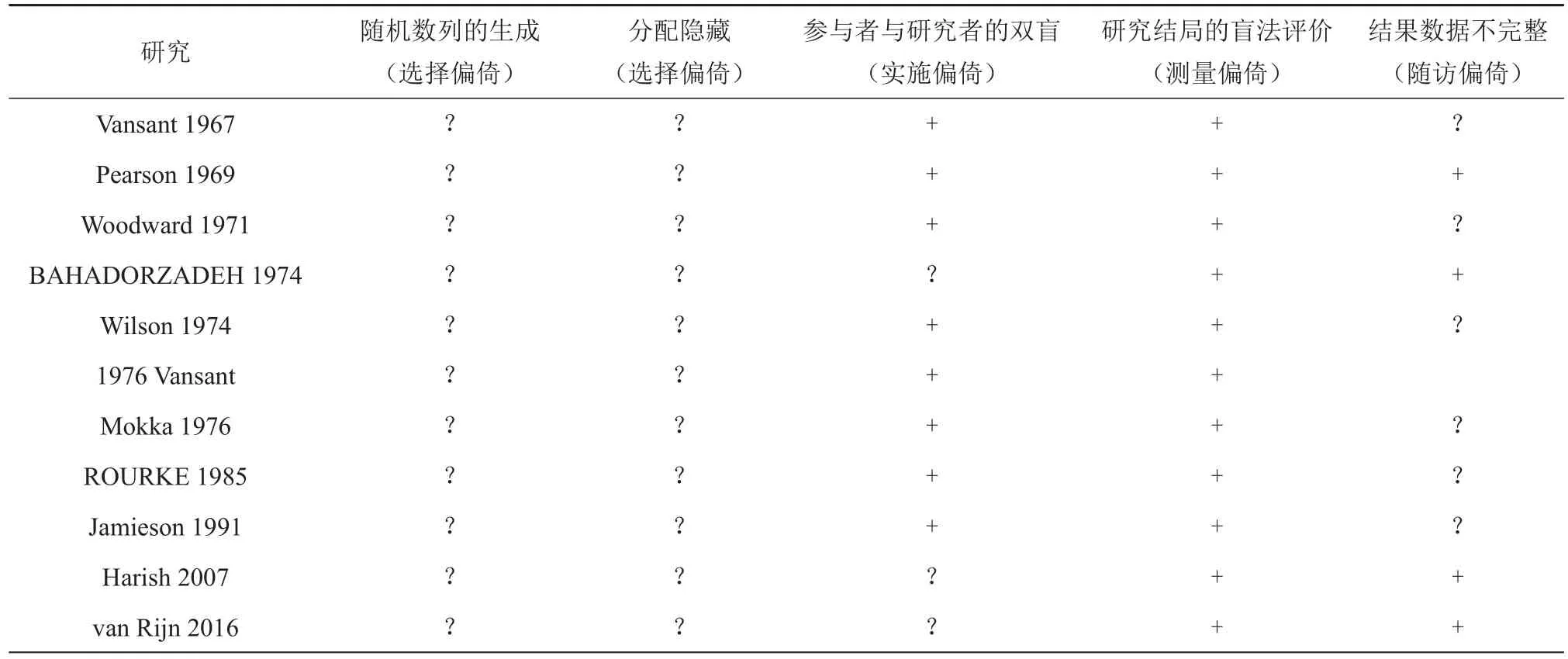
表5 纳入研究的偏倚风险
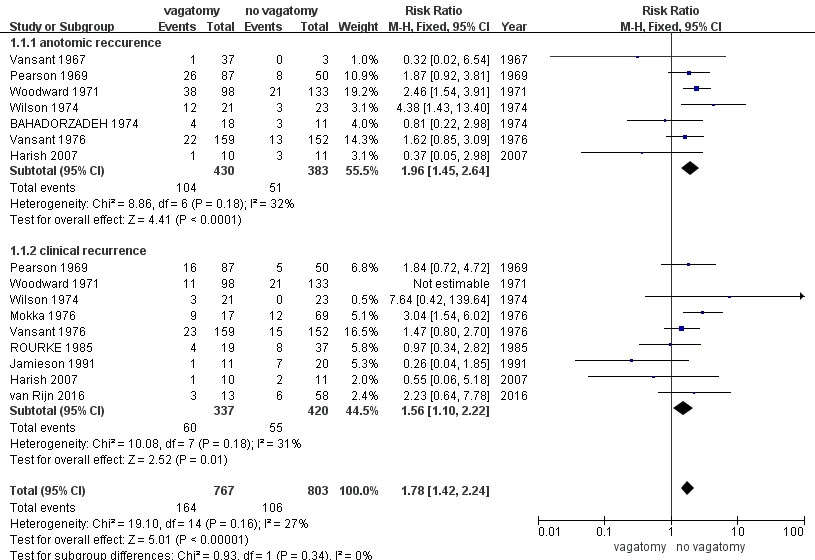
图2 森林图显示解剖复发亚与临床复发亚在抗反流术后迷走神经切断组与迷走神经保留HH复发风险的比较
本研究通过多因素分析,比较抗反流术后迷走神经切断与迷走神经保留在随访期内HH的复发风险,结果表明,相比较于迷走神经保留,迷走神经切断术后临床复发及解剖复发风险都更高,且两因素间的差异不存在异质性。这表明抗反流手术中保护迷走神经对于减少术后HH的复发风险具有一定意义。
上述结果引发迷走神经对于HH手术中加强抗反流、减少术后复发原因的思索。程林江[27]研究提出食管神经主要有两个来源;一是食管颈段及胸上段的迷走神经来自喉返神经,二是食管胸中、下段和腹段迷走神经主要来自迷走神经干,食管颈段及胸上段神经分支分布相对较密,而食管胸中、下段分支相对较稀疏。左右迷走神经纤维束在隆突下方发出粗细不等的分支,在食管周围相互吻合成食管迷走神经丛,并在膈肌上方组成前、后迷走神经干,两干均通过食管裂孔进入腹腔,前后两干的数目和位置在膈肌上下往往存在诸多变异[28]。传统迷走神经切断术往往术后并发症较多,如胃排空延迟、胃食管反流、倾倒综合征等。而保留迷走神经则能保留胃分泌、运动和储库功能,术后患者具有正常的营养胃肠道调节功能,并且无体重减轻,且胃肠道恢复快、影响小[28]。四川大学华西医院韩冰教授团队在分析保留迷走神经在食管切除术后胃消化的功能,食管测压结果显示,保留迷走神经组患者,术后在吻合口上方产生了一段的压力较高的区域,且保留迷走神经的患者手术前后体重无明显变化[29]。本文的研究与上述研究结果在一定程度上是吻合的,即保留迷走神经对于食管静息压维持具有不可或缺的作用,这对于减少HH复发及反流性食管炎症状具有重要意义;其次,保留迷走神经有助于胃肠道功能性调节,对患者体重影响不大,而肥胖正是HH发病的主要诱因之一。但本文也因诸多原因而存在以下几不足。其一,纳入的研究中并未明确阐明迷走神经切断是否是双侧同时切除,也未比较迷走神经干左支及右支单独保留时对减少HH术后复发的意义。其二,本研究纳入的样本数量较少,HH的修补方式也不统一;其三,吞钡X线摄片及胃镜诊断的灵敏度及特异度暂不明确;其四,纳入研究的试验均为回顾性临床研究,对于结果的准确性造成一定影响,可能为异质性的主要原因之一。因此,需要进一步的大样本随机对照研究来证实迷走神经保护在抗反流术中的统计学意义。
综上所述,抗反流术中迷走神经的保护可以减少术后HH复发风险,但考虑到样本数量、迷走神经切断方式及抗反流手术方式的不同可能对研究结果的影响,及纳入研究的类型所限,有待进一步的研究证实迷走神经保护在减少HH复发方面的意义。
