3-亚甲基异吲哚啉-1-酮的硅氢化反应
2020-10-15张晓梅代兴杰王周玉
张晓梅,代兴杰,龙 燕,王周玉
(西华大学理学院,四川 成都 610039)
3-取代异吲哚啉-1-酮是许多天然产物和药物活性分子的核心结构单元,具有广泛的生理活性。如图1 所示:(+)-Lennoxamine 和Nuevamine 是从小檗属植物Berberis darwinii 中提取分离得到的生物碱[1];Chilenine 是从Berberis empetrifolia lam 中分离得到的[2];Mariline C 是从海绵衍生的指轮枝孢属类真菌中分离得到的生物碱[3];Thiazoloisoindolone是一种非核苷类逆转录酶抑制剂[4];Pazinaclone 是一种抗焦虑药物[5]。
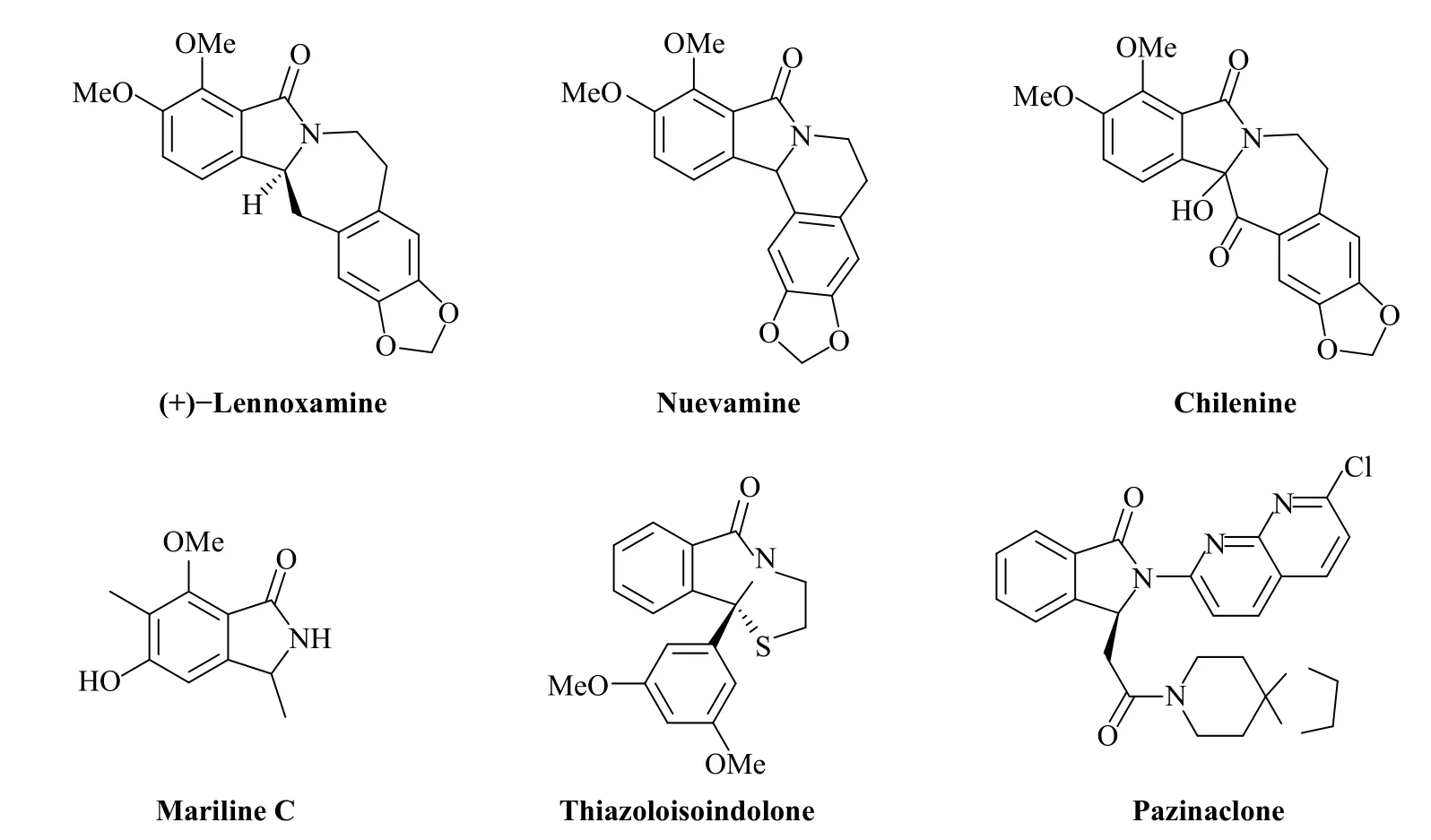
图1 含3-取代异吲哚啉酮骨架的天然产物和药物分子
由于3-取代异吲哚啉-1-酮对天然产物的合成及新药研发具有重要价值,其合成新方法的研究受到越来越多化学家和药学家的广泛关注,近年来已开发出多种合成方法。但是,目前大部分合成方法反应条件苛刻,底物不易制备,并需要使用昂贵的金属试剂或催化剂[6-14];因此,研究开发出操作简便、条件温和、经济环保的合成异吲哚啉-1-酮的方法具有重要意义。
三氯硅烷是工业上生产多晶硅的原料,价格便宜、来源丰富,在有机合成中常用作还原剂,可用于碳碳双键、碳氧双键、碳氮双键等的还原。本文以廉价易得的三氯硅烷为还原剂,以易于合成的吡啶甲酰胺-磺酸酯类路易斯碱为催化剂,在室温条件下实现了3-亚甲基异吲哚啉-1-酮的硅氢化反应,以中等到优良的收率(63%~99%)得到了一系列3-甲基异吲哚啉-1-酮类化合物。该方法底物适用范围广、反应条件温和、操作便捷、成本低廉。
1 实验部分
1.1 仪器与试剂
1H NMR 和13C NMR 用Bruker-300 和Bruker-400 核磁共振仪测定(1H NMR 和13C NMR 在CDCl3,Acetone-d6中测定,均以TMS 为内标);高分辨质谱由Bruker-FT-MS 质谱仪测定;熔点用Buchi B-545 熔点测定仪测定。HPLC 由岛津高效液相色谱仪测定。手性柱Chiralpak OD-H 由Daicel Chemical Industries 生产。
二氯甲烷、氯仿、1,2-二氯乙烷、1,1,2,2-四氯乙烷和乙腈等经氢化钙干燥后蒸出。甲苯、乙醚和四氢呋喃用金属钠和二苯甲酮处理后蒸出。其他溶剂除特别说明外均为国产市售分析纯试剂,其他试剂和原料均为购买后直接使用。H 型薄层析硅胶由青岛海洋化工有限公司生产,薄层层析硅胶板由烟台江友硅胶开发有限公司生产。
1.2 实验步骤
1.2.1 路易斯碱催化剂2 的合成
路易斯碱催化剂2 的合成路径如图2 所示。
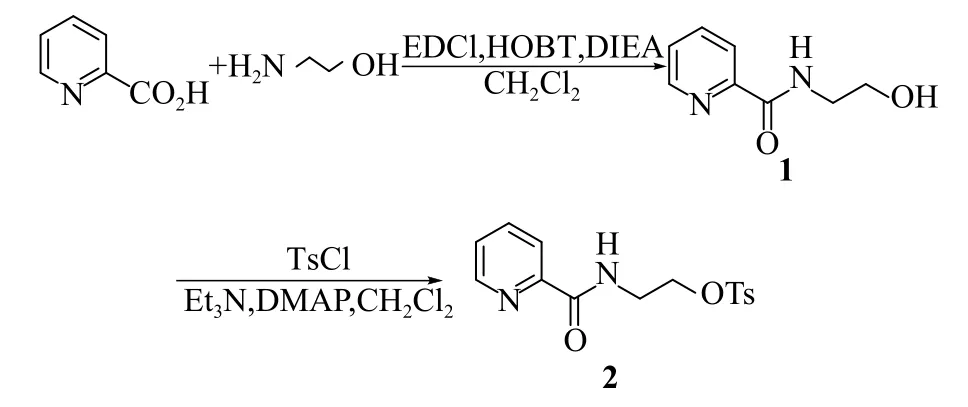
图2 路易斯碱催化剂2 的合成路径
将吡啶-2-羧酸(2.46 g,20 mmol)溶于100 mL二氯甲烷中,在冰浴条件下依次加入氨基乙醇(1.47 g,24 mmol),HOBT(1-hydroxybenzotriazole,1-羟基苯并三唑)(3.24 g,24 mmol),EDCI(1-ethyl-3(3-dimethylpropylamine) carbodiimide,1-乙基-3(3-二甲基丙胺)碳二亚胺)(4.70 g,2.4 mmol),DIEA(N,N-diisopropylethylamine,N,N-二异丙基乙胺)(8.0 mL,48.0 mmol)加入至反应液中,然后自然升温至室温反应。反应完毕,蒸出溶剂,加入乙酸乙酯溶解,饱和碳酸氢钠溶液和饱和食盐水洗涤,无水硫酸镁干燥,浓缩后经柱层析得1。
将1(10 mmol)溶于60 mL 二氯甲烷中,在冰浴条件下依次将三乙胺(2.90 mL,20.0 mmol)和DMAP(0.24 g,2.0 mmol)加入至反应液中,0 ℃下搅拌5~10 min 后分批加入对甲苯磺酰氯(15.0 mmol 溶于 40 mL 二氯甲烷),然后自然升温至室温反应。反应完毕,蒸出溶剂,加入乙酸乙酯溶解,饱和碳酸氢钠溶液和饱和食盐水洗涤,无水硫酸镁干燥,浓缩后经柱层析得2。
1.2.2 3-亚甲基异吲哚啉-1-酮的硅氢化反应
3-亚甲基异吲哚啉-1-酮的硅氢化反应如图3所示。
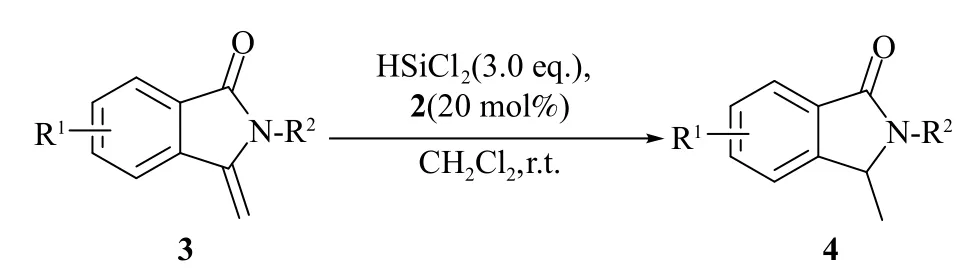
图3 3-亚甲基异吲哚啉-1-酮的硅氢化反应
于干燥的试管中加入3-亚甲基异吲哚-1-酮3(0.1 mmol),催化剂2(0.02 mmol)和二氯甲烷(1.0 mL)。试管用橡胶塞封口后,加入配制好的三氯硅烷(0.3 mmol),室温反应。反应完毕后用水溶液淬灭10 min。二氯甲烷萃取,合并有机相,饱和食盐水洗,并用无水硫酸钠干燥。过滤,减压蒸出溶剂,粗产物经柱层析(石油醚/乙酸乙酯=5/1)分离得纯的还原产物4。
三氯硅烷在使用前现配制成三氯硅烷的二氯甲烷溶液(1 mL HSiCl3+4 mL CH2Cl2)。
2 结果与讨论
2.1 化合物的表征
2-(Picolinamido)ethyl 4-methylbenzenesulfonate (2):白色固体,m.p.:79.2-80.8 ℃,收率48% 。1H NMR (300 MHz,CDCl3) δ 8.57-8.55 (m,1H),8.29 (br s,1H),8.12-8.08 (m,1H),7.84 (td,J1=7.7,J2=1.7 Hz,1H),7.77 (d,J=8.3 Hz,2H),7.47-7.42(m,1H),7.22 (d,J=8.0 Hz,2H),4.20 (t,J=5.1 Hz,2H),3.75-3.70 (m,2H),2.35 (s,3H).13C NMR (100 MHz,CDCl3) δ 164.5,149.3,148.2,144.9,137.3,132.6,129.8,128.0,126.4,122.1,69.0,38.5,21.6.HRMS (ESI) Calcd.for [C15H16N2O4+H]+321.090 4;Found:321.088 9。
2-(4-Methoxyphenyl)-3-methylisoindolin-1-one (4a):白色固体,m.p.:88.1-89.4 ℃,收率96% 。1H NMR (300 MHz,CDCl3) δ 7.90 (d,J=7.4 Hz,1H),7.60-7.55 (m,1H),7.50-7.40 (m,4H),6.99-6.94(m,2H),5.08 (q,J=6.7 Hz,1H),3.81 (s,3H),1.40(d,J=6.7 Hz,3H),the same as literature[10]。
2-(4-Methoxyphenyl)-3,6-dimethylisoindolin-1-one (4b):白色固体,m.p.:134.6-136.3 ℃,收率91%。1H NMR (300 MHz,CDCl3) δ 7.72 (s,1H),7.48-7.32 (m,4H),6.97 (d,J=9.0 Hz,2H),5.05 (q,J=6.6 Hz,1H),3.82 (s,3H),2.46 (s,3H),1.39 (d,J=6.7 Hz,3H),the same as literature.[101]HRMS (ESI)Calcd.for C17H18NO2+[M+H]+268.133 2;Found:268.1336。
6-Chloro-2-(4-methoxyphenyl)-3-methylisoindolin-1-one (4c):白色固体,m.p.:145.2-146.6 ℃,收率71% 。1H NMR (300 MHz,CDCl3) δ 7.84 (d,J=8.8 Hz,1H),7.51-7.45 (m,1H),7.44-7.37(m,1H),6.98 (d,J=9.0 Hz,2H),5.07 (q,J=6.7 Hz,1H),3.83 (s,3H),1.42 (d,J=6.7 Hz,3H).13C NMR (100 MHz,CDCl3) δ 165.9,157.7,147.9,138.2,130.4,129.5,129.0,125.5,125.3,122.5,114.5,57.2,55.5,18.7.HRMS (ESI) Calcd.for C16H15ClNO2+[M+H]+288.078 6;Found:288.079 2。
6-Bromo-2-(4-methoxyphenyl)-3-methylisoindolin-1-one (4d):白色固体,m.p.:153.4-154.6 ℃,收率67% .1H NMR (400 MHz,CDCl3) δ 7.79 (d,J=7.4 Hz,1H),7.66-7.65 (m,2H),7.45-7.41(m,2H),7.02-6.98 (m,2H),5.08 (q,J=6.7 Hz,1H),3.85 (s,3H),1.43 (d,J=6.7 Hz,3H),13C NMR (100 MHz,CDCl3) δ 166.0,157.7,148.1,131.9,130.87,129.5,126.5,125.5,125.5,114.5,57.1,55.5,18.7.HRMS(ESI) Calcd.for C16H15BrNO2+[M+H]+332.028 1;Found:332.029 0。
2-(4-Methoxyphenyl)-3,5-dimethylisoindolin-1-one (4e):白色固体,m.p.:194.5-195.4 ℃,收率95%。1H NMR (300 MHz,CDCl3) δ 7.80 (d,J=7.6 Hz,0H),7.43 (d,J=8.6 Hz,1H),7.31-7.27 (m,1H),6.97 (d,J=8.5 Hz,1H),3.83 (q,J=6.0 Hz,1H),2.49 (s,3H),1.40 (d,J=6.5 Hz,3H).13C NMR (100 MHz,CDCl3) δ 167.1,157.4,146.8,142.6,130.1,129.4,125.4,123.8,122.5,114.4,57.3,55.5,22.0,18.8.HRMS (ESI) Calcd.for C17H18NO2+[M+H]+268.133 2;Found:268.133 9。
5-Chloro-2-(4-methoxyphenyl)-3-methylisoindolin-1-one (4f):白色固体,m.p.:144.3-146.7 ℃,收率 63%。1H NMR (300 MHz,CDCl3) δ 7.88 (s,1H),7.55 (d,J=7.9 Hz,1H),7.41 (d,J=8.2 Hz,3H),6.98 (d,J=8.4 Hz,2H),5.09 (d,J=5.8 Hz,1H),3.83 (s,3H),1.41 (d,J=6.4 Hz,3H),13C NMR(100 MHz,CDCl3) δ 157.7,144.5,134.6,133.7,132.0,129.5,125.6,124.2,123.3,114.5,57.3,55.5,18.7.HRMS (ESI) Calcd.for C16H15ClNO2+[M+H]+288.078 6;Found:288.078 7。
4-Chloro-2-(4-methoxyphenyl)-3-methylisoindolin-1-one (4g): 白色液体,收率68% 。1H NMR (300 MHz,CDCl3) δ 7.51-7.35 (m,5H),6.96 (d,J=9.0 Hz,2H),5.04 (q,J=6.6 Hz,1H),3.82 (s,3H),1.40 (d,J=6.7 Hz,3H),13C NMR (100 MHz,CDCl3) δ 164.5,157.6,148.8,132.5,131.8,130.1,129.6,127.8,125.5,120.6,114.4,56.3,55.5,18.9.HRMS (ESI) Calcd.for C16H15ClNO2+[M+H]+288.078 6;Found:288.079 5。
3-Methyl-2-phenylisoindolin-1-one (4h): 白色固体,m.p.:80.7-82.2 ℃,收率97% 。1H NMR (300 MHz,CDCl3) δ 7.93 (d,J=7.4 Hz,1H),7.64-7.58(m,3H),7.53-7.43 (m,4H),7.26-7.21 (m,1H),5.21(q,J=6.6 Hz,1H),1.46 (d,J=6.6 Hz,3H),the same as literature[10]。
3-Methyl-2-(p-tolyl)isoindolin-1-one (4i): 白色固体,m.p.:82.7-84.1 ℃,收率99% 。1H NMR (300 MHz,CDCl3) δ 7.93 (d,J=7.5 Hz,1H),7.63-7.58(m,1H),7.53-7.43 (m,4H),7.27-7.24 (m,2H),5.16(q,J=6.5 Hz,1H),2.38 (s,3H),1.44 (d,J=6.7 Hz,3H),the same as literature[12]。
2-(4-Fluorophenyl)-3-methylisoindolin-1-one(4j): 白色固体,m.p.:122.8-124.4 ℃,收率92%。1H NMR (300 MHz,CDCl3) δ 7.93 (d,J=7.5 Hz,1H),7.65-7.59 (m,1H),7.54-7.48 (m,4H),7.18~7.11(m,2H),5.15 (q,J=6.7 Hz,1H),1.44 (d,J=6.7 Hz,3H),13C NMR (100 MHz,CDCl3) δ 167.0,160.3 (d,1J=246.3 Hz),146.2,133.1 (d,3J=2.8 Hz),132.2,131.6,128.5,125.43,125.35,124.19,122.01,116.09,116.0 (d,2J=22.6 Hz),57.26,18.71.HRMS (ESI)Calcd.for C15H13FNO+[M+H]+242.097 6; Found:242.097 2。
2-(4-Chlorophenyl)-3-methylisoindolin-1-one(4k): 白色固体,m.p.:130.8-132.6 ℃,收率86% 。1H NMR (300 MHz,CDCl3) δ 7.92 (d,J=7.5 Hz,1H),7.65-7.60 (m,1H),7.57-7.48 (m,4H),7.44-7.40(m,2H),5.18 (q,J=6.7 Hz,1H),1.46 (d,J=6.7 Hz,3H),the same as literature[10]。
2-(4-Bromophenyl)-3-methylisoindolin-1-one(4l):白色液 体,收率 92%。1H NMR (300 MHz,CDCl3) δ 7.92 (d,J=7.5 Hz,1H),7.65-7.60 (m,1H),7.58-7.48 (m,6H),5.18 (q,J=6.7 Hz,1H),1.46 (d,J=6.7 Hz,3H),the same as literature[13]。
3-Methyl-2-(m-tolyl)isoindolin-1-one (4m): 白色液体,收率94%。1H NMR (300 MHz,CDCl3) δ 7.93 (d,J=7.4 Hz,1H),7.64-7.58 (m,1H),7.53-7.44(m,3H),7.34-7.32 (m,2H),7.09~7.03 (m,2H),5.19(q,J=6.7 Hz,1H),2.41 (s,1H),1.45 (d,J=6.7 Hz,3H),13C NMR (100 MHz,CDCl3) δ 166.9,146.4,139.0,137.0,132.0,131.9,128.9,128.4,126.4,124.4,124.1,122.0,120.6,57.1,21.6,18.8.HRMS(ESI) Calcd.for C16H16NO+[M+H]+238.122 6;Found:ak/>238.122 9。
2-(3-Chlorophenyl)-3-methylisoindolin-1-one(4n): 黄色固体,m.p.:108.4-109.6 ℃,收率92% 。1H NMR (400 MHz,CDCl3) δ 7.95 (d,J=7.5 Hz,1H),7.69 (t,J=1.9 Hz,1H),7.65 (td,J1=7.5,J2=0.9 Hz,1H),7.56~7.51 (m,3H),7.40 (t,J=8.1 Hz,1H),7.23 (d,J=8.9 Hz,1H),5.22 (q,J=6.6 Hz,1H),1.50 (d,J=6.7 Hz,3H).13C NMR (100 MHz,CDCl3)δ 166.9,146.1,138.4,134.8,132.4,131.4,130.1,128.6,125.3,124.3,123.0,122.0,121.0,56.8,18.8.HRM S (ESI) Calcd.for C15H13ClNO+[M+H]+258.068 6;Found:258.068 7。
3-Methyl-2-(o-tolyl)isoindolin-1-one (4o): 白色固体,m.p.:110.0-111.2 ℃,收率68% 。1H NMR(400 MHz,CDCl3) δ 7.96 (d,J=7.5 Hz,1H),7.63 (t,J=7.4 Hz,1H),7.53 (dd,J1=14.0,J2=7.4 Hz,2H),7.38~7.28 (m,3H),7.20 (s,1H),5.08~4.85 (m,1H),2.31-2.24 (m,3H),1.41 (s,3H).13C NMR (100 MHz,CDCl3) δ 147.2,131.8,131.6,131.3,128.3,126.7,124.2,122.0.HRMS (ESI) Calcd.for C16H16NO+[M+H]+238.123 2;Found:238.124 2。
2-(2-Iodophenyl)-3-methylisoindolin-1-one(4p): 白色固体,m.p.:144.1-145.8 ℃,收率82%。1H NMR (300 MHz,CDCl3) δ 8.02-7.95 (m,2H),7.64 (td,J1=7.5,J2=0.9 Hz,1H),7.55-7.43 (m,3H),7.30-7.21 (m,2H),7.17-7.08 (m,2H),5.15 (q,J=6.5 Hz,0.6H),5.03 (q,J=6.5 Hz,0.3H),1.51 (d,J=6.7 Hz,1.0H),1.42 (d,J=6.7 Hz,2.0H).13C NMR(100 MHz,CDCl3) δ 167.7,147.1,140.1,139.4,132.1,131.7,131.5,130.3,129.5,129.3,128.5,128.3,124.4,122.3,122.0,100.0,99.1,60.5,57.3,18.9,18.1.HRMS (ESI) Calcd.for C15H13INO+[M+H]+350.004 2;Found:350.005 1。
2-(Benzo[d][1,3]dioxol-5-yl)-3-methylisoindolin-1-one (4q): 白色固体,m.p.:156.4-157.8 ℃,收率 86% 。1H NMR (400 MHz,CDCl3) δ 7.91 (d,J=7.5 Hz,1H),7.60 (t,J=7.4 Hz,1H),7.49(dd,J1=11.9,J2=7.5 Hz,2H),7.12 (d,J=1.7 Hz,1H),6.91-6.86 (m,2H),6.00 (d,J=3.3 Hz,2H),5.06 (q,J=6.6 Hz,1H),1.44 (d,J=6.7 Hz,3H).13C NMR (100 MHz,CDCl3) δ 167.0,148.1,146.3,145.6,132.0,131.7,131.0,128.4,124.1,122.0,117.5,108.3,106.2,101.5,57.8,18.7.HRMS (ESI)Calcd.for C16H14NO3+[M+H]+268.097 4;Found:268.0981。
3-Methyl-2-(naphthalen-2-yl)isoindolin-1-one(4r): 白色固体,m.p.:124.5-126.7 ℃,收率93%。1H NMR (400 MHz,CDCl3) δ 8.02-7.99 (m,2H),7.94 (d,J=8.8 Hz,1H),7.89-7.86 (m,2H),7.84-7.81(m,1H),7.67-7.63 (m,1H),7.57-7.47 (m,4H),5.35(q,J=6.7 Hz,1H),1.51 (d,J=6.7 Hz,3H),13C NMR (100 MHz,CDCl3) δ 167.1,146.4,134.7,133.7,132.2,131.8,131.2,128.9,128.5,127.8,127.7,126.5,125.7,124.2,122.4,122.1,121.1,57.1,18.9.HRMS (ESI) Calcd.for C19H16NO+[M+H]+274.122 6;Found:274.122 9。
2-Benzyl-3-methylisoindolin-1-one (4s): 白色固 体,m.p.:140.8-142.4 ℃,收 率 94%。1H NMR(300 MHz,CDCl3) δ 7.89 (d,J=7.2 Hz,1H),7.55-7.50 (m,1H),7.48-7.43 (m,1H),7.36 (d,J=7.4 Hz,1H),7.33-7.22 (m,5H),5.34 (d,J=15.2 Hz,1H),4.37 (q,J=6.7 Hz,1H),4.26 (d,J=15.2 Hz,1H),1.42 (d,J=6.7 Hz,3H),the same as literature[14]。
2-(4-Hydroxybenzyl)-3-methylisoindolin-1-one(4t): 白色固体,m.p.:126.1-128.1 ℃,收率95% 。1H NMR (300 MHz,CDCl3) δ 7.88 (d,J=7.5 Hz,1H),7.52 (dd,J1=7.8,J2=6.8 Hz,1H),7.44 (t,J=7.3 Hz,2H),7.36 (d,J=7.3 Hz,1H),7.11 (d,J=8.4 Hz,2H),6.82 (d,J=8.5 Hz,2H),5.24 (d,J=15.0 Hz,1H),4.39 (q,J=6.3 Hz,1H),4.17 (d,J=15.1 Hz,1H),1.43 (d,J=6.8 Hz,3H).13C NMR (100 MHz,CDCl3) δ 168.5,156.0,147.1,131.7,131.5,129.4,128.4,128.2,123.8,122.0,115.8,55.2,43.3,17.9.HRMS (ESI) Calcd.for C16H15NO2Na+[M+Na]+276.100 0;Found:276.099 8。
2.2 反应条件的优化
我们首先对3-亚甲基异吲哚啉-1-酮的硅氢化反应条件进行了优化,如表1所示。我们以3-亚甲基异吲哚啉-1-酮3a为模板底物,在路易斯碱催化剂DMF(0.2 当量)的作用下,与三氯硅烷进行反应,得到了3-甲基异吲哚啉-1-酮4a,收率仅有42%(表1,条目1)。当提高DMF的用量至0.5当量时,收率提高至46%(表1,条目2)。而进一步提高DMF的用量至1.0当量时,收率反而略有下降(表1,条目3)。考虑到可能是DMF的催化活性较低,我们选用了易制备的吡啶甲酰胺-磺酸酯类路易斯碱催化剂2来催化该反应,仅需0.2当量的催化剂2,反应收率就高达96%(表1,条目4)。因此,我们选定2为最优催化剂。当催化剂用量为0.1当量时,反应时间延长且收率有所降低(表1,条目5)。因此,我们确定催化剂用量为0.2当量。接着我们对反应溶剂进行了筛选,发现在4种含氯溶剂中,反应的收率都很高(表1,条目5—8)。在乙醚和四氢呋喃两种醚类溶剂中反应时间有所延长,且收率明显降低(表1,条目9 和 10)。而甲苯中的反应收率更低至61%(表1,条目11)。乙腈作溶剂时,反应几乎不发生(表1,条目12)。所以我们选定二氯甲烷为最优溶剂。
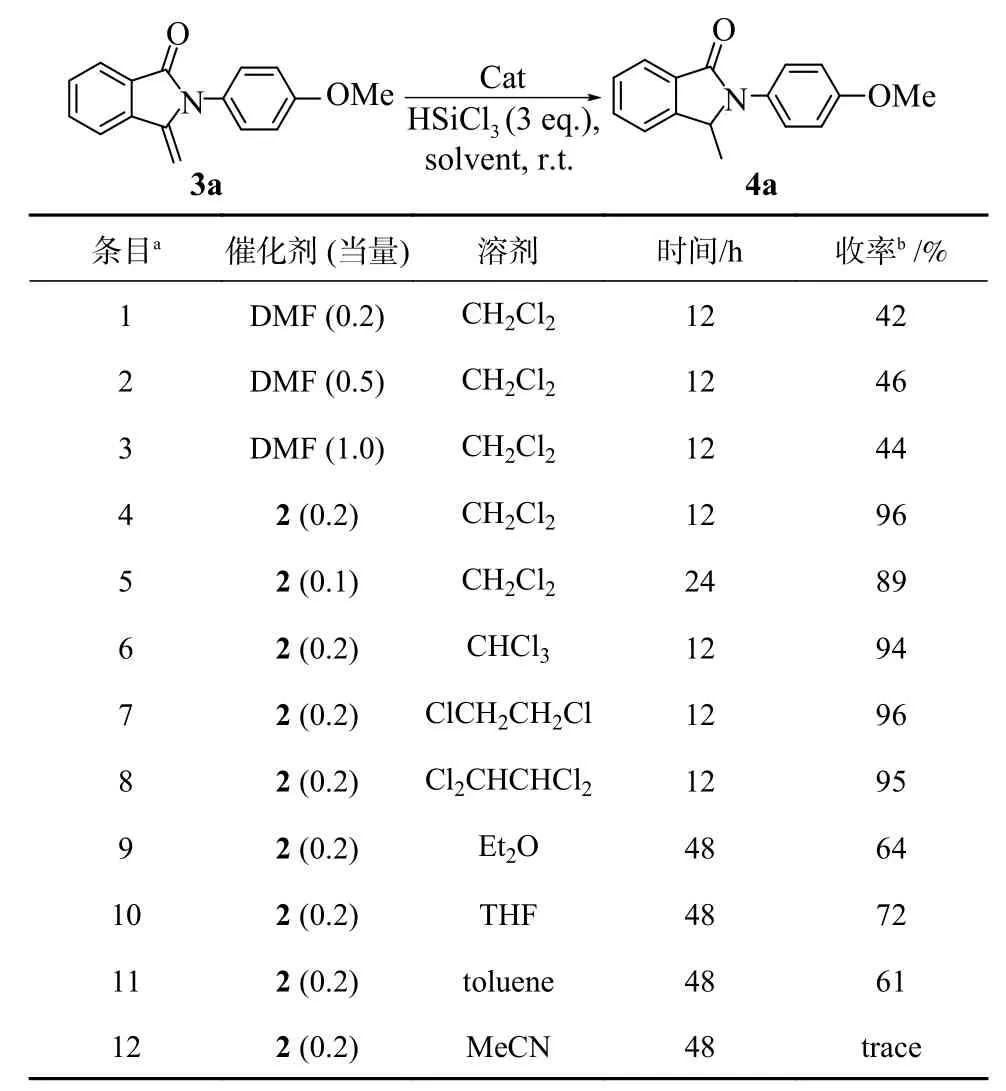
表1 反应条件的优化
2.3 底物拓展
为了考察该方法的底物适用性,我们在最优的反应条件下进行了底物拓展研究,如图4所示。首先考察了苯并环上的取代基R1对反应活性的影响,当苯环的6-位或5-位为甲基时,收率达到90%以上(图4,4b和4e);当6-位取代基为吸电子取代基如氯和溴时,收率有大幅下降(图4,4c和4d);当5-位或4-位为吸电子取代基氯时,收率下降也很明显,分别降为63%和68%(图4,4f和4 g),说明苯并环上有给电子取代基时,底物的反应活性不受影响。苯并环上有吸电子取代基能够显著降低底物的反应活性,可能是因为吸电子取代基降低了N上的电子云密度,从而使得底物不易从烯胺形式异构化为亚胺形式参与反应。接着我们考察了N上的取代基R2对反应活性的影响,当R2为苯基或对甲基苯基时,收率分别高达97%和99%(图4,4h和4i);苯基的对位为吸电子取代基氟、氯和溴时,收率有所降低(图4,4j—4l),同样也可能是因为吸电子取代基降低了N上的电子云密度,从而使得底物不易从烯胺形式异构化为亚胺形式参与反应;而苯基的间位无论是甲基还是氯,收率分别高达94%和92%(图4,4m和4n);苯基的邻位为甲基或碘时,收率有明显下降(图4,4o和4p),可能是因为底物位阻较大的原因;当R2为胡椒基或2-萘基时,也可以得到很高的收率(图4,4q和4r)。当R2为苄基和对羟基苄基时,也能达到很高的收率(图4,4s和4t)。
3 结论
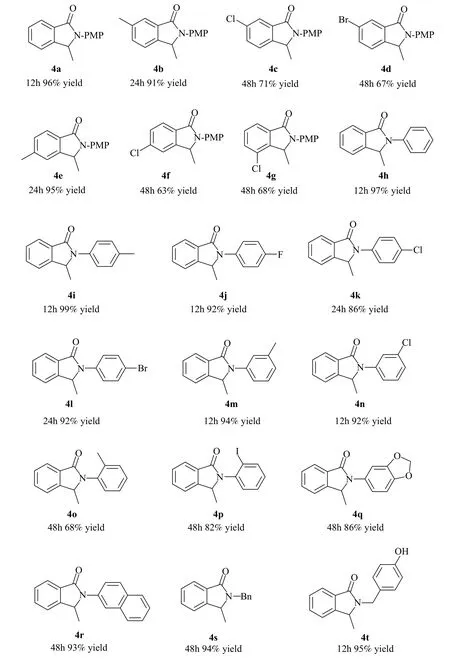
图4 底物普适性的研究a,b
本文以廉价易得的三氯硅烷为还原剂,在易于合成的吡啶甲酰胺-磺酸酯类路易斯碱催化剂作用下,实现了3-亚甲基异吲哚啉-1-酮的硅氢化反应,以中等及以上的收率(63%~99%)得到了一系列3-甲基异吲哚啉-1-酮,从而找到了一种条件温和、操作便捷、成本低廉的合成3-甲基异吲哚啉-1-酮类化合物的新方法。
