抗Ⅹa因子活性测定用于80岁及以上高龄患者口服利伐沙班的监测
2020-10-11沈姞李传保朱愿超武文斌刘洋袁莹李晶施红
沈姞 李传保 朱愿超 武文斌 刘洋 袁莹 李晶 施红
100730 北京医院老年医学科 国家老年医学中心 中国医学科学院老年医学研究院(沈姞、武文斌、刘洋、袁莹、李晶、施红),检验科(李传保),药学部(朱愿超)
利伐沙班(rivaroxaban)是一种新型口服抗凝药,可通过高度选择性和竞争性抑制游离及结合的Ⅹa因子,中断凝血瀑布的内源性和外源性途径,从而抑制凝血酶产生和血栓形成,已被国内外指南推荐用于预防成人非瓣膜病心房颤动(non-valvular atrial fibrillation,NVAF)缺血性脑卒中及系统性栓塞,以及治疗不伴有恶性肿瘤的急、慢性深静脉血栓、肺动脉栓塞及预防复发的首选药物[1-2]。利伐沙班药代动力学稳定,无须监测药物浓度。然而,有些情况下进行利伐沙班的实验室监测是必要的,如在紧急手术前,对接受利伐沙班的患者进行围术期管理、发生血栓栓塞或出血事件、怀疑服药过量、肝肾功能不全等[3]。有研究指出,尽管观察到利伐沙班浓度与凝血酶原时间、国际标准化比值和活化部分凝血活酶时间呈中等程度相关,但常规凝血检测不足以证实与手术相关的利伐沙班浓度,对于接受利伐沙班的围术期患者建议测定抗Ⅹa因子活性[4]。有研究表明,利伐沙班的出血问题与剂量及肾功能(肌酐清除率)显著相关[5]。高龄患者往往合并多种慢性病,肾功能不全的比例高,出血风险亦高,对于高龄NVAF患者,因担心出血和跌倒等风险,抗凝比例低。而抗凝的高龄患者,临床上往往减少利伐沙班的剂量,但能否达到预期的抗凝效果,尚无临床研究证实。因此,我们在老年科开展了高龄患者口服利伐沙班的抗Ⅹa因子活性测定,以探讨其在临床中的监测意义。
1 对象和方法
1.1 研究对象
本研究为横断面研究。2019年1~12月于北京医院老年医学科门诊就诊和住院、正在服用利伐沙班治疗的NVAF和静脉血栓栓塞症(venous thromboembolism,VTE)患者共61例,选取其中23例高龄患者作为研究对象。入选标准:年龄≥80岁,确诊为NVAF或VTE,正在接受利伐沙班抗凝治疗。排除标准:病例资料不全;有其他可逆转因素造成的心房颤动(如围术期发作、甲状腺功能亢进等)。本研究经我院伦理委员会批准(伦理批号:2020BJYYEC-143-01),患者或家属签署知情同意书。
1.2 研究方法
1.2.1 资料收集 根据病历记录获取患者的一般资料、临床诊断(NVAF/VTE)和合并疾病(高血压、糖尿病、冠心病、慢性心功能不全、慢性肾功能不全、恶性肿瘤等)、既往脑卒中/短暂性脑缺血发作(transient ischemic attack,TIA)史、既往出血史、抗栓药物使用情况等,确诊NVAF/VTE时间,服用利伐沙班的时间和剂量,以及服用利伐沙班之后的脑卒中/TIA、出血、血栓栓塞等事件的发生情况。
1.2.2 诊断标准及相关定义 NVAF定义为心房颤动无中度或重度二尖瓣狭窄或机械性心脏瓣膜;VTE包括肺血栓栓塞症和深静脉血栓形成。
1.2.3 危险评分 采用2014年美国心脏协会/美国心脏病学会/美国心律协会(AHA/ACC/HRS)心房颤动治疗指南中的CHA2DS2-VASc评分标准和抗凝出血危险评估(HAS-BLED)评分标准[6],对NVAF患者进行血栓栓塞危险度评分和出血危险度评分。
1.2.4 处理原则 NVAF和VTE患者除利伐沙班抗凝治疗外,对NVAF患者进行常规的控制心室率治疗,对VTE患者采取常规的辅助治疗如弹力袜等。
1.2.5 利伐沙班监测 患者口服利伐沙班至少4 d后(其中VTE患者需在利伐沙班剂量改为每日1次后),晨起抽取空腹血测定抗Ⅹa因子活性的谷浓度,服用利伐沙班后3 h再次抽血测定峰浓度。检测方法:采用抗Ⅹa测定试剂盒(美国IL公司,批号:N0386762),应用发色底物法检测抗Ⅹa因子活性(anti-FⅩa)。
1.2.6 随访 采用电话和门诊形式,每月随访患者的服药情况以及出血事件、脑卒中、心血管事件、血栓栓塞事件等情况。
1.3 统计学方法
2 结果
2.1 一般临床资料
共23例高龄患者临床资料完整并进行了抗Ⅹa因子活性的谷、峰浓度监测,见表1。其中男性12例,女性11例,年龄80~92(85.7±3.0)岁,体质指数(25.79±3.29)kg/m2,包括NVAF患者19例和VTE患者4例。其中20例(87.0%)患者合并高血压,8例(34.8%)糖尿病,10例(43.5%)冠心病,4例(17.4%)陈旧性心肌梗死,16例(70.0%)慢性心功能不全(NYHA心功能分级Ⅱ级6例、Ⅲ级10例),11例(47.8%)慢性肾功能不全[依据 CKD-EPI公式计算肾小球滤过率(eGFR)<60 ml·min-1·1.73 m-2],4例(17.4%)有恶性肿瘤病史,3例(13.0%)既往出血病史,6例(26.1%)既往脑卒中/TIA史,1例(4.3%)合并抗栓(因发生急性非ST段抬高型心肌梗死,合并抗栓3个月)。NVAF患者CHA2DS2-VASc评分3~9(5.5±1.5)分,HAS-BLED评分1~5(2.0±1.0)分。
2.2 抗Ⅹa因子活性的谷峰浓度
23例高龄患者的利伐沙班服用时程为2~75(16.7±15.8)个月,服用剂量15例为15 mg/d、7例为10 mg/d、1例为5 mg/d。抗Ⅹa因子活性的谷峰浓度测定结果显示,4例患者的谷浓度大于200 ng/ml,8例峰浓度大于400 ng/ml(其中2例超过700 ng/ml),2例患者的谷峰浓度差距较小,谷浓度分别为324和352 ng/ml、峰浓度分别为400和372 ng/ml(CrCl分别为47.0和71.2 ml/min)。
根据CrCl分组,服用不同剂量利伐沙班患者的抗Ⅹa因子活性谷峰浓度如表2所示。在CrCl≥30 ml/min组中,利伐沙班剂量15 mg/d的患者抗Ⅹa因子活性的谷、峰浓度均大于剂量10 mg/d的患者;而在CrCl 15~29 ml/min组中,利伐沙班剂量15 mg/d的患者抗Ⅹa因子活性的谷、峰浓度反而小于剂量10 mg/d的患者。在CrCl 30~49和≥50 ml/min组中,服用相同剂量利伐沙班的患者抗Ⅹa因子活性的谷、峰浓度均相当;而服用剂量15 mg/d的患者,在CrCl 15~29 ml/min的谷、峰浓度反而较CrCl≥30 ml/min更低;剂量10 mg/d的患者,在CrCl 15~29 ml/min的谷、峰浓度均较CrCl≥30 ml/min更高。

表1 患者一般临床资料
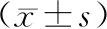
表2 抗Ⅹa因子活性的谷峰浓度
将抗Ⅹa因子活性的谷、峰浓度与利伐沙班服用剂量进行相关性分析,结果显示抗Ⅹa因子活性的峰浓度与利伐沙班剂量的Spearman相关系数为0.575(P=0.004),二者呈中度相关,利伐沙班剂量越高,抗Ⅹa因子活性的峰浓度越高;而谷浓度与利伐沙班剂量的Spearman相关系数为0.222(P=0.308),二者无显著相关性。
2.3 服药依从性和血栓、出血事件
23例高龄患者中有2例(8.7%)NVAF患者出院后自行停用利伐沙班,原因为同时服用多种药物;其他21例患者服药依从性较好。
19例NVAF患者抗凝过程中均未发生脑卒中事件,其中1例患者抗凝1.5个月时突发急性心功能不全死亡。1例肺栓塞患者(CrCl 47 ml/min)口服利伐沙班15 mg/d抗凝过程中再次出现下肢深静脉血栓,继续抗凝后复查血栓消失,查抗Ⅹa因子活性的谷浓度为324 ng/ml,建议其减量至10 mg/d再复查谷浓度(目前患者暂未复查)。1例深静脉血栓患者抗凝4个月时发生急性ST段抬高型心肌梗死行经皮冠状动脉介入术。
23例患者抗凝过程中有4例发生出血事件(表3),将利伐沙班减量后未再出血;其他19例无出血事件发生。
3 讨论
虽然老年心房颤动患者有更高的出血风险,但与年轻人相比,老年患者的有效抗凝治疗可带来更大获益[8]。2016欧洲心脏病学会指南[9]推荐,高龄(75岁以上)心房颤动患者起始抗凝治疗首选新型口服抗凝药。日本的J-ROCKET AF研究[10]纳入中高危NVAF患者,根据日本指南建议利伐沙班剂量为15 mg/d(CrCl 30~49 ml/min的患者为10 mg/d),结果提示与华法林相比,利伐沙班非显著性地降低了卒中和非中枢神经系统性栓塞风险,两组整体出血比例无显著性差异。低剂量利伐沙班(10 mg/d)在亚洲国家的真实临床实践中被广泛应用[11-13]。《心房颤动抗凝治疗中国专家共识》[14]指出,对于肾功能减退、高龄等患者应用新型口服抗凝剂应注意出血危险,必要时减小用药剂量。中国台湾的一项回顾性研究纳入了3 162例使用利伐沙班的心房颤动患者,在2 320例eGFR≥50 ml·min-1·1.73 m-2的患者中,分别有384和1 936例接受了ROCKET AF(20 mg/d)和J-ROCKET AF(15 mg/d)的推荐剂量,在842例eGFR<50 ml·min-1·1.73 m-2的患者中,分别有422和420例接受了ROCKET AF(15 mg/d)和J-ROCKET AF(10 mg/d)的推荐剂量。结果显示,eGFR≥50 ml·min-1·1.73 m-2的患者的临床事件风险在两个利伐沙班剂量组间无显著性差异;eGFR<50 ml·min-1·1.73 m-2的患者中,与J-ROCKET AF剂量相比,ROCKET AF剂量与较高的大出血风险相关(HR:2.70,P=0.0445),缺血性事件无显著性差异[15]。
表3 4例出血患者的服药剂量调整和抗Ⅹa因子活性的谷峰浓度测定
定量检测利伐沙班药物浓度的“金标准”是液相色谱串联质谱法(liquid chromatography-tandem mass spectrometry,LC-MS/MS),特异性好,灵敏度高,但该方法需要复杂且昂贵的仪器和熟练的专业人员,限制了其广泛使用[16]。Al-Aieshy等[17]的研究显示,抗Ⅹa因子试验与LC-MS/MS检测利伐沙班血药峰值浓度的相关性为0.91,谷值浓度的相关性为0.92,目前已有用于利伐沙班的抗Ⅹa因子试剂盒,可在普通实验室完成检测。日本一项研究显示,不同CrCl水平的患者抗Ⅹa因子活性峰浓度不同,Cox多因素分析显示峰值水平是与大出血及非临床相关大出血事件独立相关的因素[18]。国外共识指出,与剂量相关的预期谷峰浓度分别为44(12~137)ng/ml和249(184~343)ng/ml(预防NVAF患者脑卒中及系统性栓塞20 mg/d);26(6~87)ng/ml和270(189~419)ng/ml(肺栓塞/深静脉血栓的抗凝治疗20 mg/d)[19]。
本研究纳入80岁及以上高龄患者,包括了CrCl 15~29 ml/min的患者,对于这部分患者,目前国内还缺乏抗Ⅹa因子活性和相关治疗浓度的报道,国外也缺乏大规模的临床研究数据,尚无推荐的治疗浓度[20]。我们在临床上减少利伐沙班剂量的同时进行药物浓度监测,希望能够指导临床用药。我们将抗Ⅹa因子活性的谷峰浓度和利伐沙班服用剂量进行相关性分析,显示峰浓度水平与服药剂量中度相关(Spearman相关系数为0.575,P=0.004),谷浓度水平与剂量无显著相关性,考虑与本研究样本量偏少有关,目前还不能得出抗Ⅹa因子活性与服药剂量的相关性结果。本研究中对于谷峰浓度明显高于国外报道的患者,特别是肾功能不全者,我们减少了利伐沙班服药剂量,可能有助于减少出血等不良事件的发生,而对于肾功能正常的患者我们未调整服药剂量,密切观察无临床不良事件发生,本研究中4例发生出血事件的患者均减少了服药剂量。通过本研究发现,对于高龄患者,特别是肾功能不全者,谷峰浓度个体差异性较大,不除外与多重用药的影响有关,建议此类患者完善抗Ⅹa因子活性的谷峰浓度检测,根据抗Ⅹa因子活性测定结果和临床不良事件进行利伐沙班剂量调整。
本研究局限性和不足:单中心研究,样本量较少,未同时进行LC-MS/MS检测利伐沙班的血药浓度,后期我们会继续扩大样本量,探索抗Ⅹa因子活性在高龄患者口服利伐沙班中的适宜水平,同时判断抗Ⅹa因子活性与LC-MS/MS检测利伐沙班血药浓度的相关性。
利益冲突:无
