“介入无置入”时代临床试验替代终点的选择与统计学考虑
2020-10-09刘小云赵延延朱熠冰李思冬尹潞徐波李卫王杨
刘小云 赵延延 朱熠冰 李思冬 尹潞 徐波 李卫 王杨
作者单位:100037 北京,国家心血管病中心 北京协和医学院 中国医学科学院阜外医院医学统计部(刘小云、赵延延、朱熠冰、李思冬、尹潞、李卫、王杨),介入导管室(徐波)
自21世纪初,经皮冠状动脉介入治疗(percutaneous coronary intervention, PCI)心血管疾病的年手术量已逼近八百万的数量级,按2001年开展的577 767例计算,相当于在每100万人口中有1108例进行PCI术,且该数字以每年15%~25%的速度持续增长[1]。药物洗脱支架(drug-eluting stent, DES)凭借其对支架内再狭窄的有效控制,成为当前PCI的“金标准”[2]。但有研究表明,DES置入可能导致动脉粥样硬化过程加速、炎症反应和支架小梁断裂等风险[3]。因此,近5年研究的热点逐渐转移到了以药物洗脱球囊(drugcoated balloon,DCB)和生物可吸收支架(bioresorbable scarfold, BRS)为代表的新型治疗器械[4-9]。新型治疗器械可为血管提供“一过性”支撑、且没有永久的残留物,从而在理论上避免了残留物对血管造成的远期潜在影响[10-11]。DCB及BRS的临床应用促进PCI进入了“介入无置入”的时代。
随着冠状动脉介入治疗从普通球囊(plain old balloon angioplasty,POBA)、裸金属支架(bare-metal stent,BMS)、DES到BRS和DCB的器械不断创新,在临床试验中采用的主要终点指标也在不断发生变化,基于影像学的替代终点[如:支架内再狭窄、晚期管腔丢失(late lumen loss,LLL)等],虽然可以有效节约试验的样本量规模,其临床价值和临床意义却受到广泛质疑[12-22]。以主要不良心血管事件(major adverse cardiac event,MACE)或靶病变失败(target lesion failure,TLF)等为代表的临床终点,又会使试验的规模直接达到千例甚至更高的数量级[12,23-24]。而针对创新器械(如:全降解支架)设定的心绞痛或血管收缩功能改善等为试验指标,多未能获得预期阳性结果[4,25],或只能在相对局限的人群中进行验证[16,26]。这些问题都使得“介入无置入”时代的试验设计面临诸多的困难和挑战。
基于上述问题,本综述的目的在于系统性整理“介入无置入”理念下开展的临床试验,重点关注新型冠状动脉介入器械(包括DCB和全降解支架),提取每一项研究在设计阶段制定的主要终点指标情况,及其与最终结果间的对应关系。探讨“介入无置入”相关研究中,选择适宜的评价指标的重要性,期待从方法学角度,为相关领域研究的试验设计与统计分析提供一定的参考和依据。
1 冠状动脉介入器械临床试验常用评价指标
冠状动脉介入器械临床试验疗效的评价主要通过影像和临床两个方面,前者多基于冠状动脉造影或血管内超声(intravascular ultrasound,IVUS)等影像学检测,后者则多为死亡、心肌梗死和再次血运重建等MACE。目前相关医疗器械临床试验中,常用的安全性、有效性评价指标可简单归纳如下。
1.1 影像学指标——定量冠状动脉分析(quantitative coronary analysis, QCA)
以冠状动脉造影为基础的QCA,常用于测量介入术前以及术后的相关指标,如参考血管直径(reference vessel diameter,RVD)、病变长度(lesion length,LL)、直径狭窄百分比(diameter stenosis,DS)、最小管腔直径(minimal lumen diameter,MLD)、再狭窄率(restenosis rate,RR)、LLL以及LLL指数(late lumen loss index,LLLI)等。
其中,LLL水平目前是DES试验中较常用的主要评价指标。由于金属支架内部的回缩问题可忽略,所以LLL(无论支架还是节段内)被用作对(新生)内膜增生程度的间接测量指标。假如造影随访显示LLL水平较低,则说明置入支架内部的内膜增生程度较低。虽然对支架丝(梁)的覆盖本身需要一定程度的内膜增生,但过度增生则导致再狭窄,所以什么程度的LLL水平是最优的,目前尚未定论。相反,如果LLL水平为负值,则提示存在支架贴壁不良。
1.2 血管内影像学检查——IVUS和光学相干断层成像(optical coherence tomography, OCT)
IVUS通过三维重建技术能够对管腔、支架以及外部弹力膜(external elastic membrane, MMB)轮廓进行测量。在支架置入段以及各子节段,能够分别测量平均总血管面积(mean total vessel area,VA)、平均支架面积(mean stent area,SA)和平均管腔面积(mean lumen area,LA)。平均新生内膜增生面积(mean neointimal hyperplasia area,NIHA)和围支架面积(peristent area,PSA)可通过SA和LA或者VA和SA分别计算获得。IVUS是对支架不完全贴壁的可靠测量方法,如果支架丝(梁)与血管壁分离,IVUS检查能够提供支架丝(梁)存在血流的证据。
OCT是能提供更高分辨率的腔内影像学技术,其轴向分辨率可达10 μm,是IVUS的10倍左右,且成像速度快。与IVUS相比,OCT可提供冠状动脉管壁更加细微和清晰的信息,可用于评价斑块纤维帽厚度、脂核大小、钙化及确定血栓的存在和性质。相比于IVUS更多被用于指导支架的置入,OCT以其高分辨率的优势,在目前临床试验中多用于支架置入术后、对支架小梁内皮覆盖程度的测量,同时OCT也可以用于对斑块稳定性做准确的鉴别,或检测斑块的破裂[27]。
1.3 临床终点的设定
MACE是被普遍设定经典临床终点指标,是多个单项临床事件复合后的指标,包括死亡(心血管死亡或者全因死亡)、心肌梗死[Q波或非Q波、ST段抬高型心肌梗死(STsegment elevation myocardial infarction,STEMI)或非ST段抬高型心肌梗死(non-ST-segment elevation myocardial infarction,NSTEMI)]和再次血运重建等硬终点。有些研究会采用更有针对性的定义方式,如:患者相关事件复合终点(patient-oriented composite endpoint,PoCE),其组分与MACE类似;PoCE与TLF一类的器械相关复合终点(device-oriented composite endpoint,DoCE)相对应,属于类似的复合终点定义方式。
靶病变血运重建(target lesion revascularization,TLR)和靶血管血运重建(target vessel revascularization,TVR)也是临床上普遍使用,临床试验一般会同时报告TLR和TVR的结果。需要注意的是,无论TLR还是TVR,前提都是患者接受了再次的心脏导管治疗;若患者在PCI术后发生了MACE,如左前降支(left anterior descending artery,LAD)所致的前壁心肌梗死,但却没有接受再次PCI或外科治疗,则该事件不会体现在TLR或TVR中。另一方面,对影像学发现的无症状再狭窄、可能增加不必要的再次血运重建治疗,所以目前临床试验中多采用“有缺血证据驱动的再次血运重建”作为评价指标。
2 新型冠状动脉介入器械的随机对照临床试验(randomized controlled clinical trial,RCT)研究
本综述总结了近年来PubMed收录的针对DCB或BRS开展的RCT,首先按适应证的不同划分为支架内再狭窄病变和小血管/侧支/其他病变,并根据试验选择的对照器械差异做进一步分组。通过系统性检索及文献筛选,共有18项针对DCB的RCT研究(表1~4)[28-49],其中治疗支架内再狭窄病变的11项,治疗小血管/侧支/其他病变的7项,对照器械多选择DES或POBA。此外,共检索到10项针对BRS开展的RCT研究[6-9,50-56](表5),均选择了DES作为对照器械,且均为冠状动脉原位原发病变。
2.1 与评价指标相关的统计学考虑
通过分析发现,大多数RCT研究都选择影像学替代指标作为主要终点。但在不同的研究中,具体替代终点的选择会存在一定差异,为进一步对比不同指标对应的效应值(试验组和对照组的疗效差异)的区别,本综述中引进一个新指标,即相对获益(差异)程度,计算方法为:[(试验组疗效—对照组疗效)/对照组疗效]×100%。比如,Nishiyama等[41]比较DCB与DES治疗原位冠状动脉病变,术后8个月影像学随访显示,DCB组与DES组节段内LLL水平分别为[(0.25±0.25)mm比(0.37±0.40)mm,P=0.19],则DCB组LLL相对获益程度为(0.25-0.37)/0.37×100%=-32%,同理可计算节段内MLD的相对获益为-9%[DCB 比 DES:(2.12±0.42)mm 比(2.32±0.52)mm,P=0.12]以及DS的相对获益程度-10%[(14.4±8.3)%比(16.0±15.9)%,P=0.64]。在该研究中,虽然试验组和对照组术后LLL、MLD和DS比较,差异均无统计学意义,但三个指标计算得到的相对获益程度是不同的。在同一试验且同样基于造影检查的指标中,LLL上获得的效应值相比其他两项指标(MLD和DS)更为明显,说明不同替代指标之间可能存在对治疗效果估计的偏差。
笔者还发现,在以替代指标作为主要终点的临床试验中,其中以评价再狭窄程度作为替代终点最为常用,主要归结为两类:一类是反映狭窄变化程度(随访相对基线或术后检查)的替代终点,例如LLL;另一类则是直接反映各随访时血管狭窄程度的替代终点,包括DS和MLD。但是,即便在同一项研究中,上述替代指标提示的治疗效应值却存在差异,将重点针对这一问题进行探讨。
2.2 DCB临床试验的终点指标
通过总结观察18项DCB的RCT研究发现,仅有1个研究以临床终点[术后24周靶血管失败(target vessel failure,TVF)]为主要终点;15项研究以替代指标为主要终点,其中10项以术后LLL为主要终点,3项为术后DS,2项为术后MLD; 另2项研究未预先指明主要指标。在以LLL为主要终点的RCT中,有6项研究的随访时间在术后6个月进行,3项研究在术后9个月进行。关于DCB研究的随访时间的确定,影像学随访多在术后6个月进行,而临床终点一般在术后6个月及1年时分别进行报告。
首先聚焦DCB治疗支架内再狭窄病变的临床试验结果(表1)。Claessen等[49]最新研究对比了依维莫司药物洗脱支架(everolimus-eluting stent,EES)与紫杉醇洗脱球囊(paclitaxel-coated balloon,PCB)在伴有糖尿病的支架内再狭窄患者中的疗效(DARE trial)。结果表明,术后6个月两组节段内LLL的差异有统计学意义[EES比DCB为:(0.22±0.67)mm比(0.03±0.32)mm,P=0.004],而两组MLD[(1.46±0.66)mm比(1.67±0.46)mm,P=0.15]以及DS[(42.4±23.1)%比(36.8±15.0)%,P=0.26]差异均无统计学意义。Wong等[48]比较DCB和二代EES(Xience)治疗DES形成支架内再狭窄,两组术后9个月节段内LLL比较差异无统计学意义(P=0.54),DCB组LLL相对获益减少21%;两组MLD差异有统计学意义(P=0.03),相对获益减少14%;两组DS差异虽然无统计学意义(P=0.05),但其相对获益较大(31%)。上述两项研究均选择了LLL为主要终点指标。第一项研究中,试验组和对照组的差异虽然有统计学意义,但是MLD或DS等指标差异无统计学意义。第二项研究虽然两组LLL差异无统计学意义,但MLD差异有统计学意义,而且DS的相对获益较大。因此,在应用DCB治疗支架内再狭窄病变的RCT研究中,两类替代终点的获益不同,单纯使用LLL作为主要终点指标,并不能真实有效地反映试验结果。
若关注DCB治疗小血管病变或分叉病变的RCT研究(表2)。以DES为对照器械,如阜外医院牵头的RESTORE-SVD研究[46-47],术后随访9个月试验组与对照组LLL比较,差异无统计学意义(P=0.73),但两组MLD(P<0.001)和DS(P=0.04)差异有统计学意义;而BELLO研究[31]两组患者LLL、MLD及DS的差异均无统计学意义,但是三个指标的相对获益不同,LLL相对减少71%,而MLD相对减少7%,DS相对增加5%。以POBA为对照器械,Kleber等[40]研究显示,LLL、MLD及DS三个指标的组间比较差异均有统计学意义,但是三个指标相对获益差异较大,其中LLL相对减少83%,而MLD相对增加29%,DS相对减少37%。上述研究提示在应用DCB治疗冠状动脉小血管或分叉病变的研究中,无论选择DES或POBA为对照器械,单纯使用LLL为主要终点指标,其结果存在较大的差异,不能准确完整地描述试验疗效。
2.3 BRS临床试验的终点指标
笔者还观察了针对BRS的RCT研究,在总共10项研究中有4项以临床终点为主要终点,其中3项为TLF,1项为TVF;另有5项研究明确以替代指标为主要终点,均选择术后LLL,但随访时间窗口不同,1项为术后9个月,1项为术后3年,3项为术后1年;另1项研究未预先指明主要指标。总之,对于BRS试验的随访时间,造影随访基本要延后到1年时开展,往往与1年临床终点同时报告,并且还将开展更为远期的随访观察(包括影像和临床)。
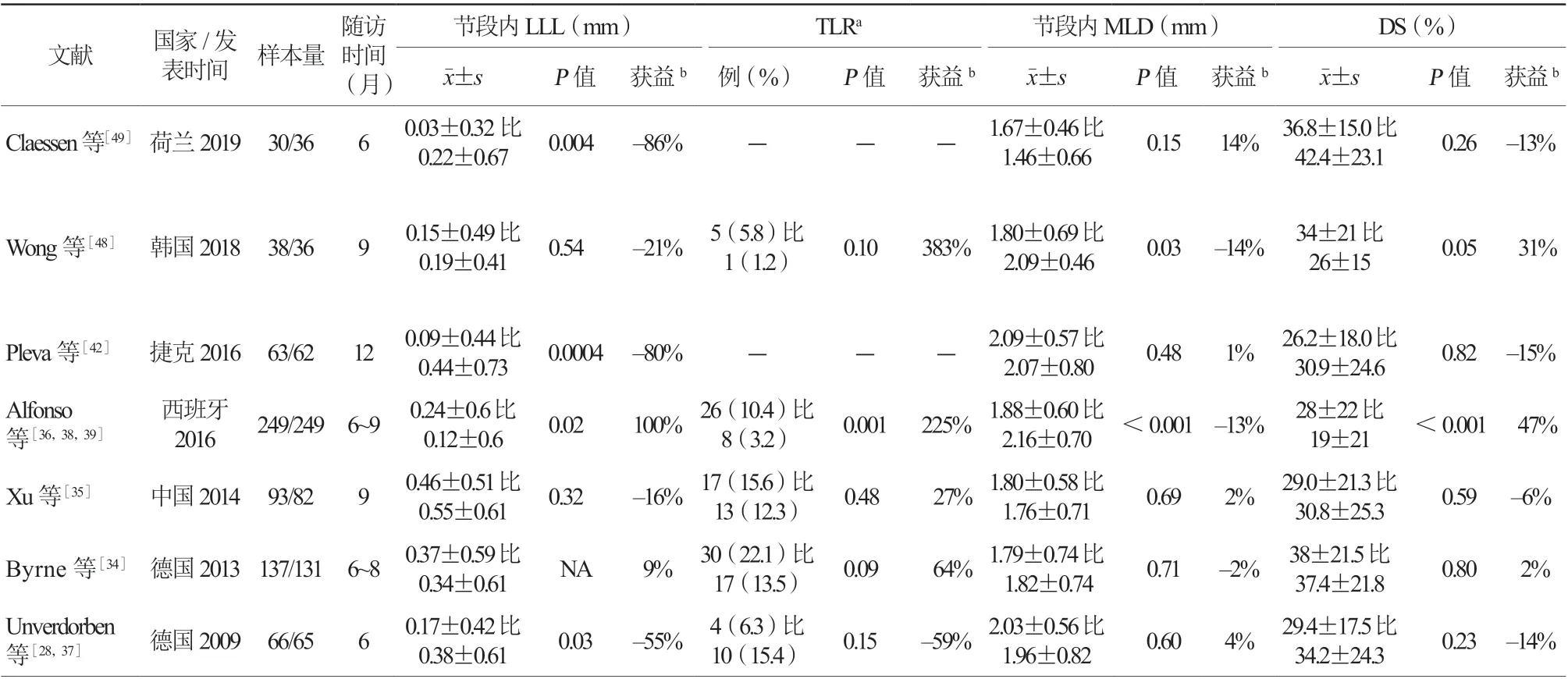
表1 DCB 与DES 治疗支架内再狭窄病变的RCT 研究
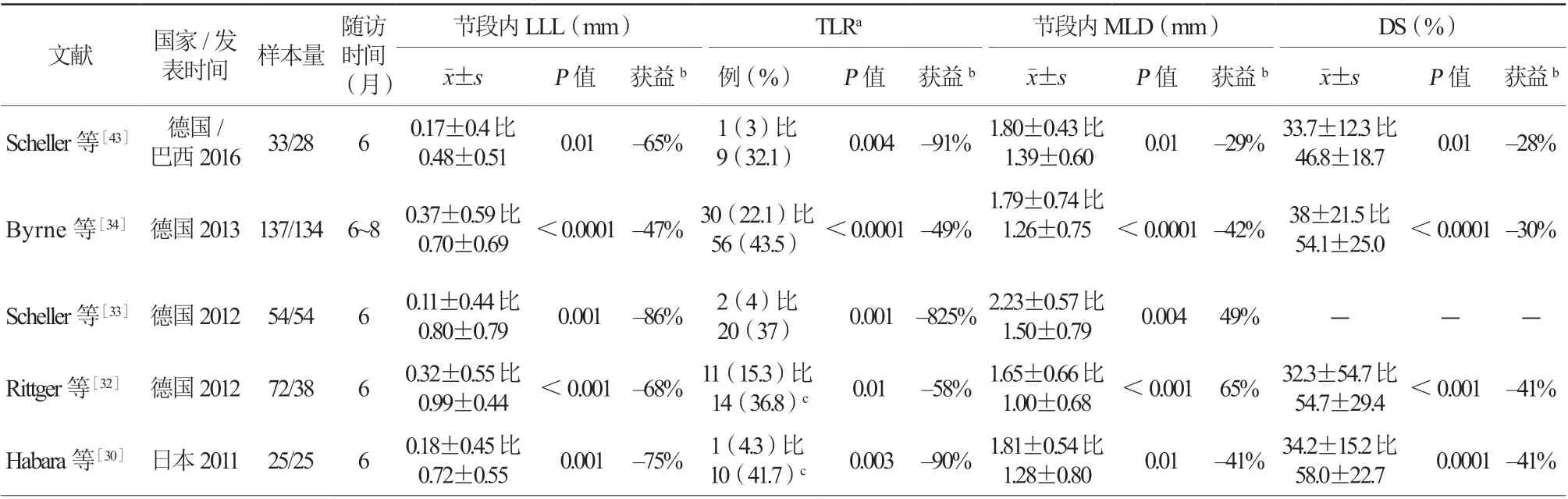
表2 DCB 与 POBA 治疗支架内再狭窄病变的RCT 研究

表3 DCB 与DES 治疗小血管/侧支/其他病变的RCT 研究

表4 DCB 与 POBA 治疗小血管/侧支/其他病变的RCT 研究
比较各终点指标设置情况,其结果也存在差异(表5)。Han等[54]选择了单个冠状动脉原位病变患者,随机接受中国自行研制的新型西罗莫司洗脱聚L-乳酸(PLLA)BRS或钴铬合金依维莫司洗脱支架(cobalt chromium-everolimus eluting stent,CoCr-EES),术后随访两组LLL、MLD及DS的差异均无统计学意义,但相对获益不同,分别为27%、-3%及2%。同样,ABSORB Japan研究[7]和ABSORB China研究[8],都是将BRS与CoCr-EES对比,也得出相似结论,上述三个指标两组比较,差异均无统计学意义,但相对获益却相差较大。EVERBIOⅡ 研究[6]将240例有症状的冠心病或无症状冠状动脉缺血患者按1∶1∶1随机分为EES、生物可降解聚合物Biolimus洗脱支架(biolimus-eluting stent,BES)或BRS组,术后随访BRS与EES对比三个指标组间比较,差异均无统计学意义,而LLL的相对获益明显高于MLD和DS;BRS与RES相比,两组间LLL比较,差异有统计学意义(P=0.03),而两组MLD差异无统计学意义且相对获益很小(仅0.5%)。通过上述汇总分析,全降解支架的RCT研究同样提示,LLL水平在不同试验中所得结果并不一致(相比于其他造影替代指标),单纯用其作为主要终点不能有效地评估临床试验结果。
3 “介入无置入”时代替代终点指标的选择
通过上述分析,发现以LLL为代表的传统替代终点指标和以MLD和DS为代表的新替代终点指标之间存在显著差别,两类替代终点结果的获益相差较大甚至获益方向(正负)也不一致。Mauri等[57-59]在2005年发表的“三部曲”文章奠定了LLL作为评价临床试验疗效的有效替代终点的关键“证据”,证明了LLL的增加与TLR有关,且该关联明显强于再狭窄对TLR的提示作用。欧洲心脏杂志2018年的最新文章,进一步巩固了LLL作为有效替代终点的地位,证实LLL对TLR的预测能力或关联现象甚至适用于5年的长期随访结果[60]。但是,上述研究结果均是基于DES试验所获得的结果,其对DCB或BRS的适用性还有待验证。而且在治疗技术快速发展的当代,再狭窄等传统指标已很难看到明显获益[19-21,61]。另外,将LLL作为主要指标能够使试验的样本量规模控制在可行的范围[12]。因此,从某种意义上可以说LLL是为DES“量身定做”的评价指标。
在DES试验中,用LLL作为替代终点评价再狭窄程度的前提条件是假设DES充分扩张后的血管弹性回缩忽略不计[59]。LLL是由术后即刻与随访时的MLD的差值计算得来,其不依赖于参考血管直径(reference vessel diameter,RVD),且术后MLD不受弹性回缩影响。因此,在DES时代会认为LLL比DS更具“优势”[57-59]。但是,该结论在DCB和BRS的研究中并不成立。国内首个DCB的RCT研究显示[35,62],术后9个月随访DCB组LLL水平低于DES组[(0.54±0.46)mm比(0.62±0.68)mm],提示DCB组术后再狭窄程度低于DES组。如果进一步比较两组术后即刻MLD,会发现DCB组的MLD水平低于DES组[(2.39±0.37)mm比(2.56±0.44)mm]。因此,随访时DCB组LLL更低的原因有可能是术后即刻MLD更小造成的。因此,看似“更优”的DCB患者,其管腔再狭窄程度反而更严重[术后即刻DS显著高于DES组:(10.51±7.22)%比(7.05±6.28)%]。造成这一现象的原因可能是,DCB因治疗后缺少支架置入提供的支撑,从而使血管出现一定的弹性回缩,故术后即刻MLD更小,从而不能准确地反映狭窄程度。对BRS也存在同样问题,由于高分子材料未能提供和金属支架相当的有效支撑导致血管弹性回缩,使LLL的计算基础出现问题。而MLD或DS则不存在这一干扰,其可直接反映狭窄程度,不受血管弹性回缩的影响。因此,在“介入无置入”时代用MLD或DS作为替代终点,其与临床终点的相关性应会更强。
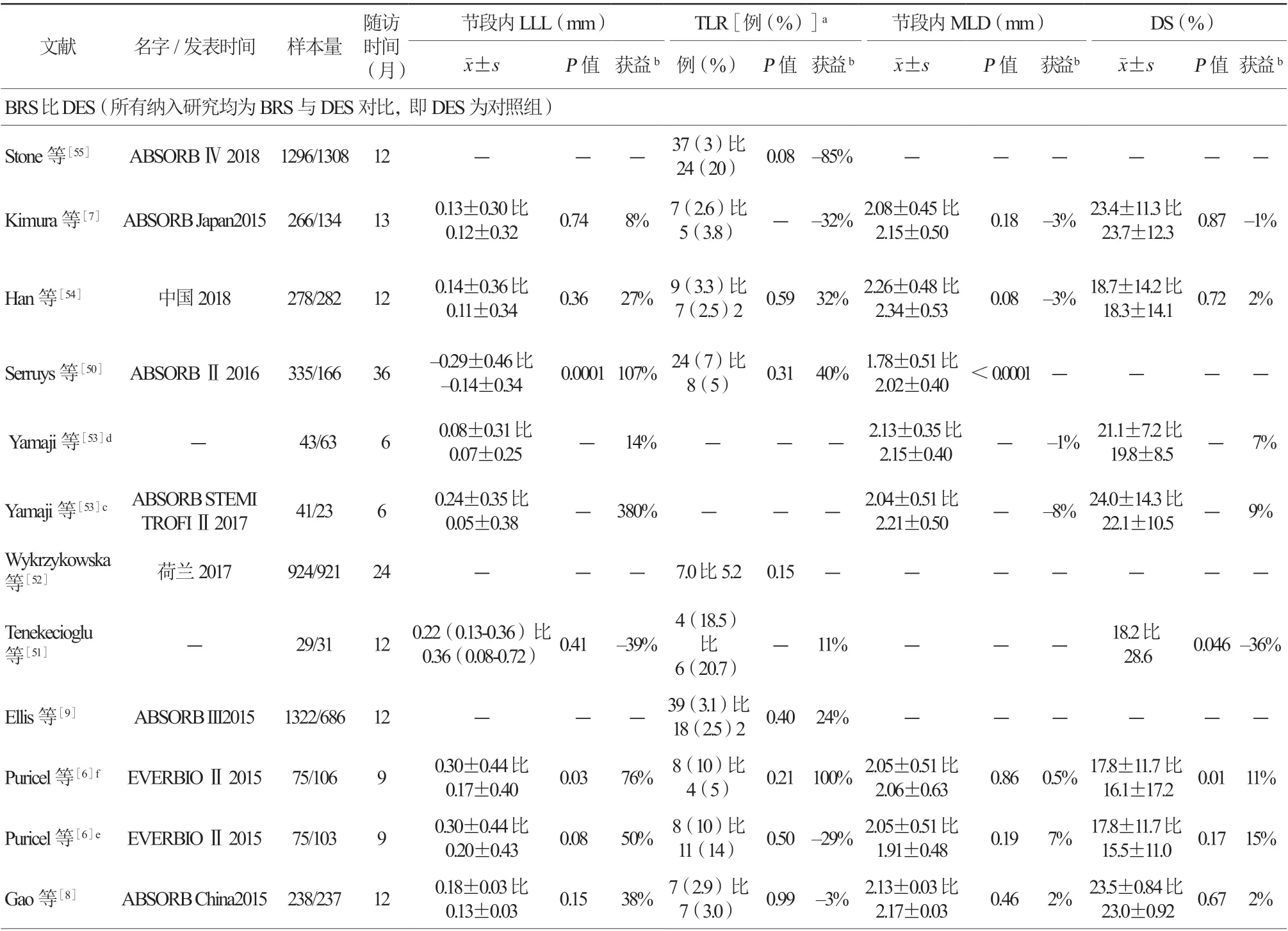
表5 BRS 治疗冠状动脉原位病变的RCT 研究
无论选择什么样的替代指标,临床终点始终是验证新器械安全性和有效性的“金标准”。雅培公司针对全降解支架开展的系列研究,其中ABSORB Ⅱ研究[50]在3年时血管收缩及LLL两个共同主要终点指标全部失败; ABSORB Ⅲ研究[25]则提示在中长期随访中(2~3年)BRS组的TLF有潜在的增加趋势,间接导致了产品的撤市。该系列研究提示在对新型冠状动脉介入器械开展评价时,应做更全面的考虑,无论是LLL为代表的传统替代终点还是以MLD和DS为代表的新替代终点,其最终传递到的还是临床结局。因此,评估替代终点与临床终点的相关性很重要。通过上述分析发现新的替代终点(MLD,DS)与临床终点可能相关性更强,但仍需要更进一步的研究验证。此外,在新的影像学检查工具层面,虽有IVUS和OCT的引入可以提供更多的测量学信息,但这些指标对应结果的可靠性尚需进一步的验证与评估,尤其是与临床终点的相关程度还有待明确。
4 总结
冠状动脉治疗已进入“介入无置入”时代,新型器械在材料、原理、治疗方式和检测方法上发生的改变,使得单纯沿用经典DES研究中的主要终点可能存在风险,除在疗效评价上可能引入偏倚外,在以临床终点为基础的安全性结果上也应提供更充分的证据。因此,如何通过对主要评价指标的合理选择,在可行性允许的样本量规模下开展试验,并能获得对干预方法性能的可靠估计,将成为方法学研究努力实现的目标。
