基于LC-MS/MS分析酒炙车前子治疗奶牛胎衣不下活性组分的化学成分
2020-09-25鲁文赓曹立明许美花罗英花原冬伟徐郑美杜珍珍司琳清金吉东付世新申贵男
鲁文赓,曹立明,许美花,罗英花,原冬伟,徐郑美,刘 庆,杜珍珍,司琳清,金吉东,付世新,李 婧,申贵男*
(1.黑龙江八一农垦大学 动物科技学院,黑龙江 大庆 163319;2.黑龙江八一农垦大学 图书馆,黑龙江 大庆 163319;3.科菲特饲料(长春)有限公司,吉林 长春 130062;4.黑龙江八一农垦大学 生命科学技术学院,黑龙江 大庆 163319)
胎衣不下(retained fetal membrane,RFM)是指奶牛分娩后8~12 h胎衣未能完全自然排出而滞留于体内的兽医产科疾病[1]。奶牛胎衣不下与子宫内膜炎、子宫炎以及子宫积脓等繁殖障碍疾病的发生存在密切联系,其可导致空怀期延长、配种次数增加、子宫炎和乳房炎等的发病率增加,严重影响奶牛生产性能,致使奶牛过早淘汰,给奶牛业带来了巨大的经济损失[2]。目前,临床上多采用宫内灌注和肌注抗生素、激素,灌服活血化瘀的中草药及手术剥离等传统方法治疗胎衣不下[3]。由于奶源易存在抗生素和激素残留等问题,有悖于绿色食品发展理念,因此研发高效、安全、便捷、廉价的治疗奶牛胎衣不下的中草药制剂至关重要。
我国中草药具有上千年的发展历史,因其具有安全、高效等特点,在中兽药临床应用方面有着显著优势,成为绿色奶牛业着重研发的药物之一。酒炙车前子治疗胎衣不下的验方最早见于《元亨疗马集·牛经》,并且近些年许多研究者对其疗效进行验证,其治愈率均在60%以上[4-5]。为了研究该药的有效物质基础,本实验室前期研究创建了酒炙车前子有效物质分离体系,并确定了其有效物质为活性组分Ⅲ和Ⅵ[6],但其活性组分的化学成分并未明确。而液质联用(LC-MS/MS)技术作为目前应用最为广泛的中草药成分分析鉴定方法之一,能够快速、精确地对中药化学成分进行定性分析,例如雒晓梅等[7]使用此方法对杜仲进行定性分析,共鉴定出98种化合物。有鉴于此,本试验采用LC-MS/MS技术对酒炙车前子治疗奶牛胎衣不下活性组分Ⅲ和Ⅵ的化学成分进行分析及鉴定,进而阐明其治疗奶牛胎衣不下的有效物质基础。
1 材料与方法
1.1 主要试剂与器材车前子(购于哈尔滨市仁人试剂经销部),无水乙醇、石油醚、二氯甲烷和乙酸乙酯(分析纯,辽宁泉瑞试剂有效公司),乙腈、甲醇、超纯水(色谱级,默克集团有限公司,德国)。RE52-99型旋转蒸发仪(上海荣亚生化仪器厂),LyoQuest -55型冷冻干燥机(泰事达科技公司,西班牙),DK-S12型恒温水浴锅(上海森信实验仪器有限公司),Ultimate 3000高效液相色谱仪(赛默飞世尔科技有限公司,美国),Q ExactiveTM组合型四极杆 Orbitrap 质谱仪(赛默飞世尔科技有限公司,美国)。
1.2 酒炙车前子治疗奶牛胎衣不下活性组分Ⅲ和Ⅵ的提取通过实验室前期药效筛选试验,确定酒炙车前子治疗奶牛胎衣不下活性组分。参照本实验室前期分离体系[6],在二氯甲烷∶甲醇(30∶1)洗脱剂中获得其活性组分Ⅲ、Ⅵ,冷冻蒸干得浸膏备用。
1.3 供试液样品的制备称取50 mg冻干样本,加入800 μL体积分数0.8的甲醇和5 μL内标(2.8 g/L,二氯苯丙氨酸),超声30 min,置于4℃离心机中,14 800×g离心15 min,取上清液以同等条件离心后,取上清液即得,备用。
1.4 液相检测条件采用Hyper gold C18 色谱柱(100.0 mm×2.1 mm,1.9 μm);以水(含5%乙腈,0.1%甲酸)(A),乙腈(含0.1%甲酸)(B)为流动相进行梯度洗脱,梯度洗脱程序见表1;进样体积为10 μL,自动进样器温度4℃,柱温40℃,流速0.3 mL/min。
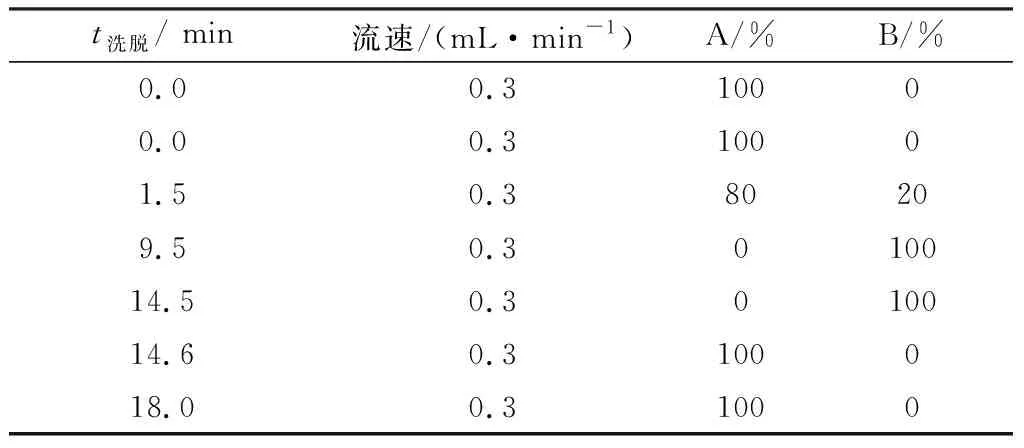
表1 流动相梯度洗脱程序
1.5 质谱检测条件采用ESI电喷雾离子源,在正、负离子模式扫描检测,质量扫描范围为70~1 500,分辨率为140 000;离子源温度为300℃,鞘气流速为45 arb,辅助气流速为15 arb,尾气流速为1 arb,S-Lens RF Level为30,扫描电压在正、负离子模式下分别为3.0 kV和3.2 kV。
1.6 数据分析基于Compound discoverer软件(Thermo公司)对LC-MS所采集的原始数据通过 Thermo Xcalibur 分析软件进行分析处理并结合网络数据库Metlin、HMDB、MassBank、PubChem及文献数据进行碎片及精确相对分子质量匹配,筛选相对分子质量实测值与理论值偏差绝对值小于1×10-5的化合物,即为酒炙车前子治疗奶牛胎衣不下活性组分中的化合物。
2 结果
2.1 活性组分Ⅲ化学成分分析与鉴定采用LC-MS/MS对酒炙车前子治疗奶牛胎衣不下活性组分Ⅲ进行定性分析,图1为ESI (+) 和ESI (-) 的质谱总离子流图(TIC)。通过LC-MS/MS检测得到活性组分Ⅲ中各化学成分的色谱保留时间、精确化合物相对分子质量等质谱信息,并结合提取离子流图与网络数据库Metlin、HMDB、MassBank、PubChem及文献数据进行化学成分匹配,筛选质量偏差值小于绝对值1×10-5的化合物进行碎片离子匹配确定化学成分。在正负离子模式下共分析出31个化合物,5个酰胺类化合物,4个有机杂环类化合物,4个苯甲酸盐,3个有机酸,3个生物碱,3个胺类化合物,2个脂类化合物,1个甾体,1个香豆素,5个其他(表2,3)。
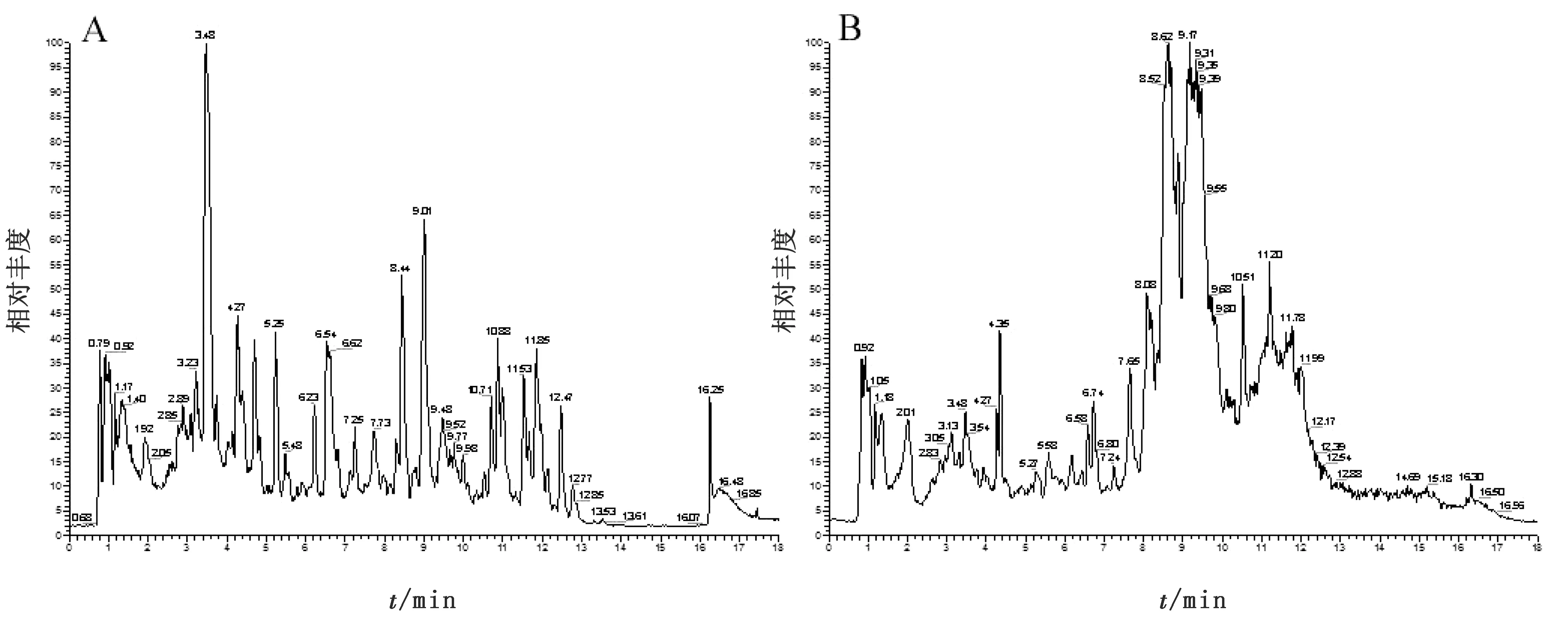
图1 活性组分Ⅲ正离子模式 (A) 和负离子模式 (B) 下的 TIC 图
2.2 活性组分Ⅲ根据质谱裂解特征分析正离子模式下以鞘氨醇、二氢鞘氨醇为例,在保留时间(t保留)为6.626 min正离子模式下准分子离子峰为m/z317 [M+H]+,脱去OH后形成特征碎片m/z300 [M+H-OH]+,再脱去C2H5N形成m/z257 [M+H-OH-C2H5N]+等碎片离子峰,裂解途径见图2。根据元素组成分析,该化合物分子式为 C18H39NO3,相对分子质量实测值为317.292 9。据参考文献[8]报道,鞘氨醇其碎片离子峰信息及Metlin数据库鞘氨醇单同位素相对分子质量为317.292 8,据此推测该化合物可能为鞘氨醇。而在t保留为7.662 min正离子模式下准分子离子峰为m/z302 [M+H]+,脱去1分子H2O形成特征离子碎片m/z284 [M+H~H2O]+,裂解途径见图3。由元素成分分析,该化合物分子式为C18H39NO2,相对分子质量实测值为301.298 1。据参考文献[9]报道,二氢鞘氨醇其碎片离子峰信息及Metlin数据库二氢鞘氨醇单同位素相对分子质量为301.298 1,据此推测该化合物可能为二氢鞘氨醇。
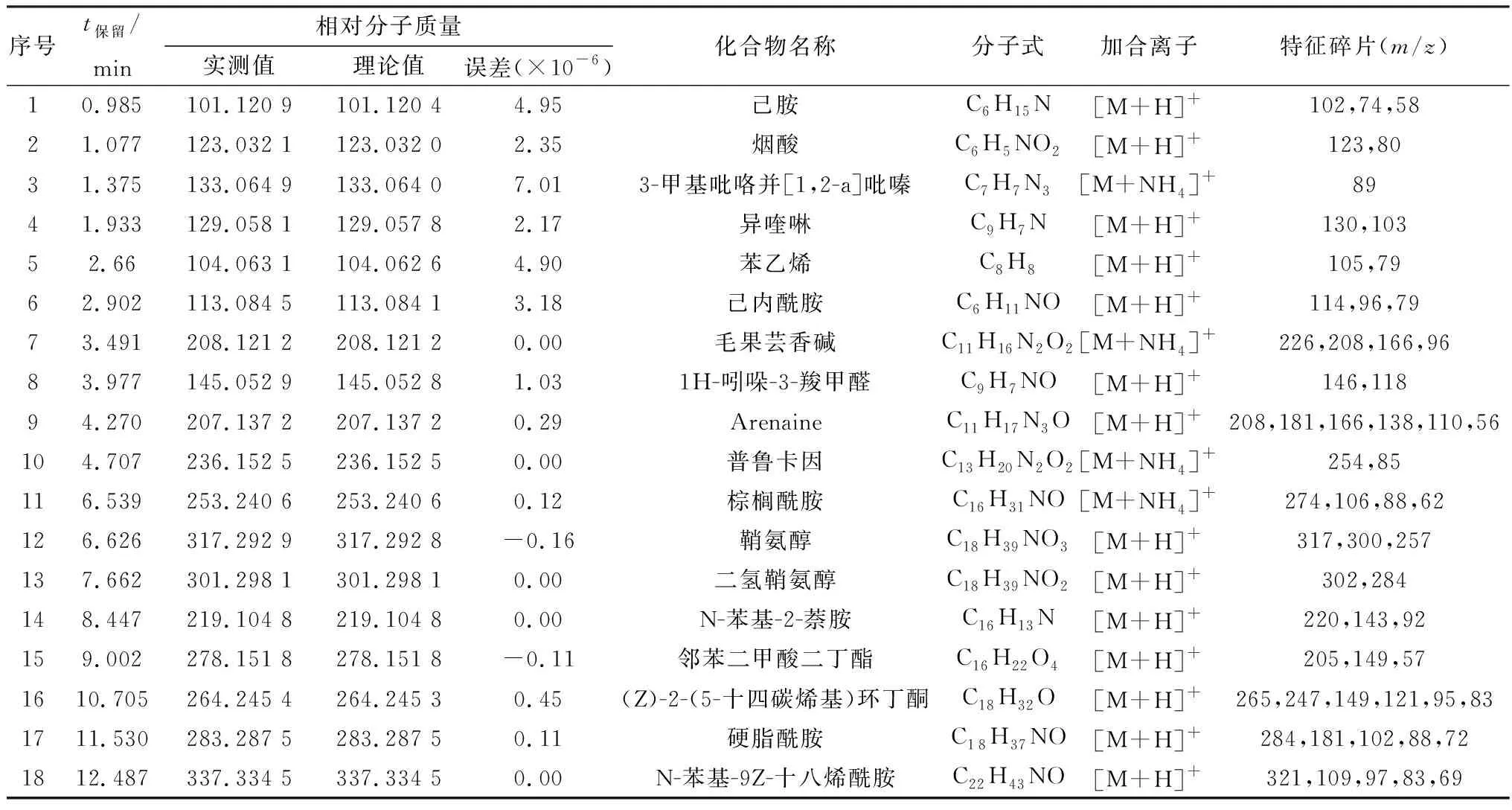
表2 正离子模式下酒炙车前子治疗奶牛胎衣不下活性组分Ⅲ的主要化合物
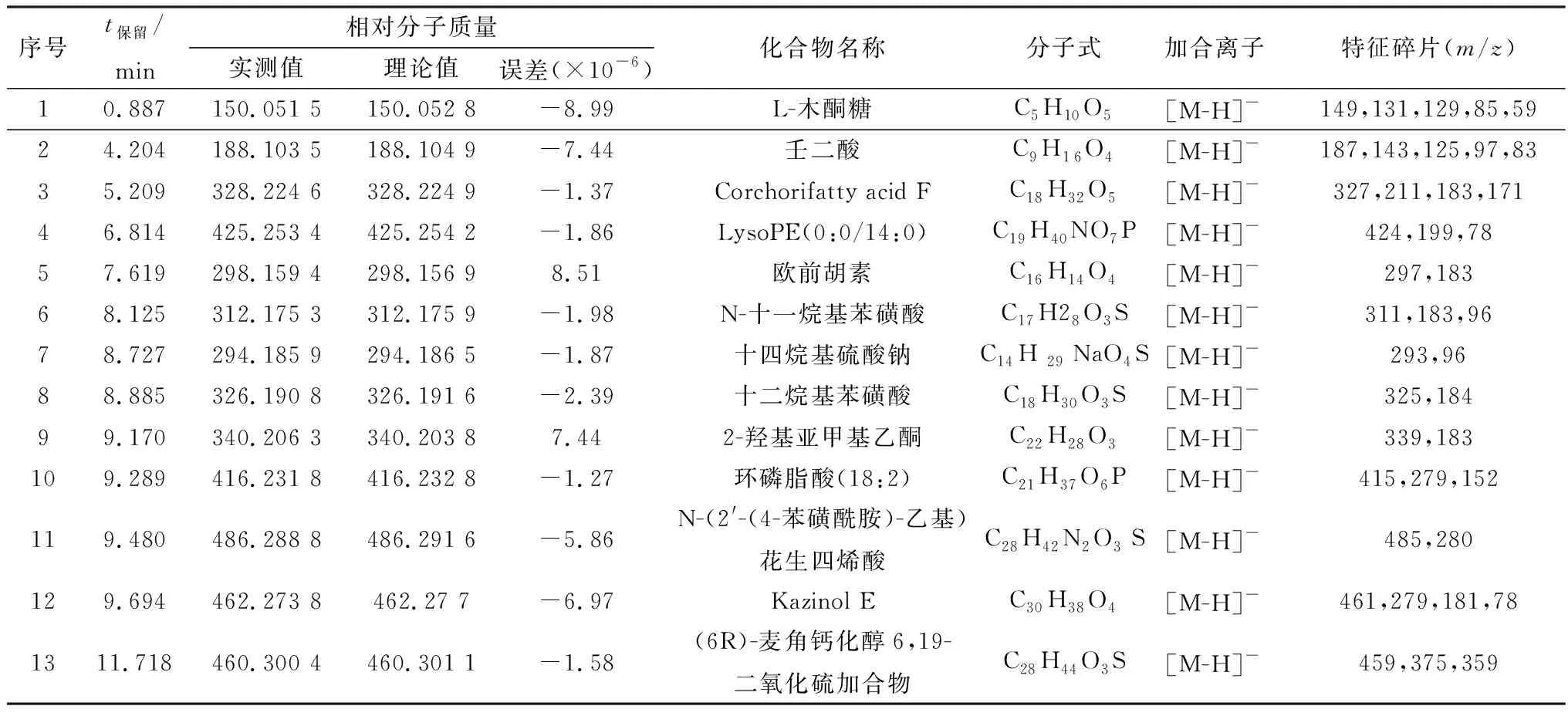
表3 负离子模式下酒炙车前子治疗奶牛胎衣不下活性组分Ⅲ的主要化合物
负离子模式下以壬二酸为例,在t保留为4.204 min负离子模式下准分子离子峰为m/z187 [M-H]-,脱去CO2后形成特征碎片m/z143 [M-H-CO2]-,再脱去1分子H2O形成特征碎片m/z125 [M-H-CO2-H2O]-,再依次脱去C2H4和CH2形成m/z97 [M-H-CO2-H2O-C2H4]-和m/z83 [M-H-CO2-H2O-C2H4-CH2]-等碎片离子峰,裂解途径见图4。根据元素组成分析,该化合物分子式为 C9H16O4,相对分子质量实测值为 188.103 5。据参考文献[10]报道,壬二酸其碎片离子峰信息及Metlin数据库壬二酸单同位素相对分子质量为188.104 9,据此推测该化合物可能为壬二酸。
2.3 活性组分Ⅵ的化学成分分析与鉴定采用LC-MS/MS对酒炙车前子治疗奶牛胎衣不下活性组分Ⅵ进行定性分析,ESI(+) 和ESI (-) 的质谱总离子流图(TIC)见图 5。通过LC-MS/MS检测得到活性组分Ⅵ中各化学成分的色谱保留时间、精确化合物相对分子质量等质谱信息,并结合提取离子流图与网络数据库Metlin、HMDB、MassBank、PubChem及文献数据进行化学成分匹配,筛选质量偏差绝对值小于1×10-5的化合物进行碎片离子匹配确定化学成分。正负离子模式下共分析出34个化合物,5个有机酸,4个酰胺类化合物,4个有机杂环类化合物,4个苯甲酸盐,3个胺类化合物,3个酚类化合物,2个生物碱,2个脂类化合物,1个甾体,1个香豆素,5个其他(表4,5)。
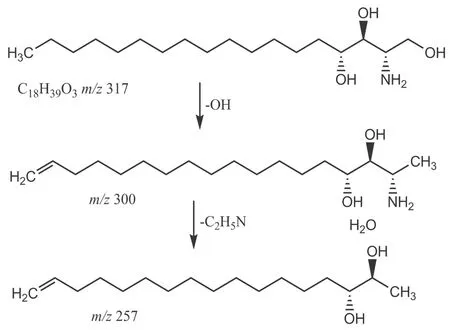
图2 正离子模式下鞘氨醇的裂解途径
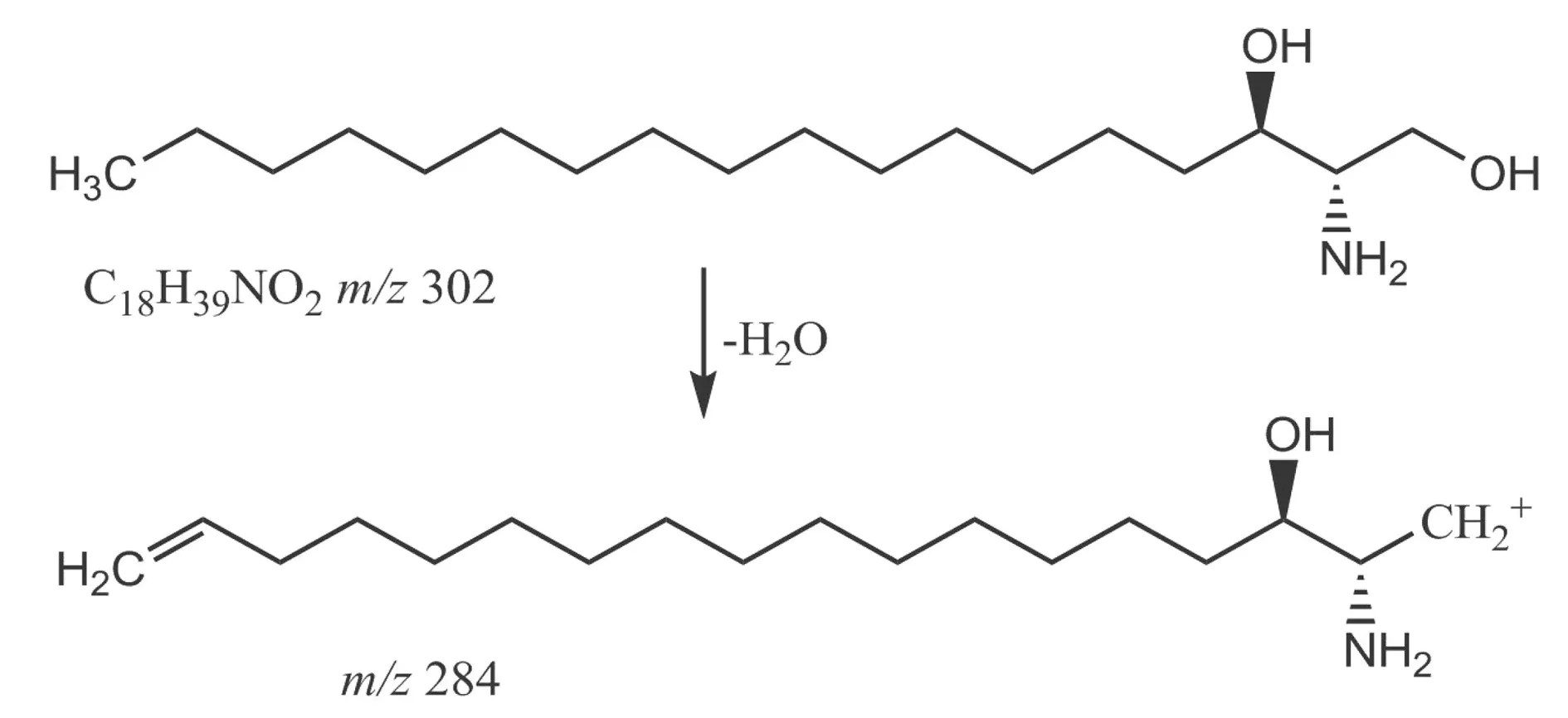
图3 正离子模式下二氢鞘氨醇的裂解途径
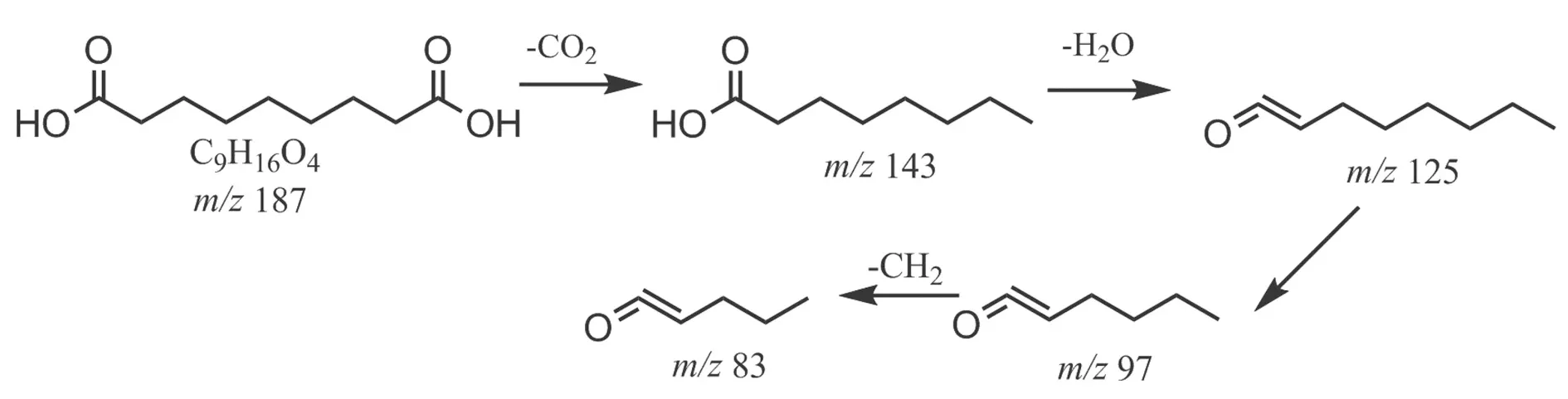
图4 负离子模式下壬二酸的裂解途径
2.4 活性组分Ⅵ根据质谱裂解特征分析正离子模式下以烟酰胺为例,在t保留为1.181 min正离子模式下准分子离子峰为m/z123 [M+H]+,脱去CNOH后形成特征碎片m/z80 [M+H-CNOH]+,再脱去CNH形成m/z53 [M+H-OH-CNOH-CNH]+等碎片离子峰,裂解途径见图6。根据元素组成分析,该化合物分子式为 C6H6NO2,相对分子质量实测值为 122.048 0。根据文献[10]报道,烟酰胺其碎片离子峰信息及Metlin数据库烟酰胺单同位素相对分子质量为122.048 3,据此推测该化合物可能为烟酰胺。
负离子模式下以丁香酸为例,在t保留为1.224 min负离子模式下准分子离子峰为m/z197 [M-H]-,脱去COOH后形成特征碎片m/z153 [M-H-COOH]-,再脱去CH3O形成m/z121 [M-H-OCH3-COOH]-等碎片离子峰,裂解途径见图 7。根据元素组成分析,该化合物分子式为 C9H10O5,相对分子质量实测值为198.052 8。根据文献[11]报道,丁香酸其碎片离子峰信息及Metlin数据库丁香酸单同位素相对分子质量为198.051 7,据此推测该化合物可能为丁香酸。

图5 活性组分Ⅵ正离子模式(A)和负离子模式(B)下的 TIC 图
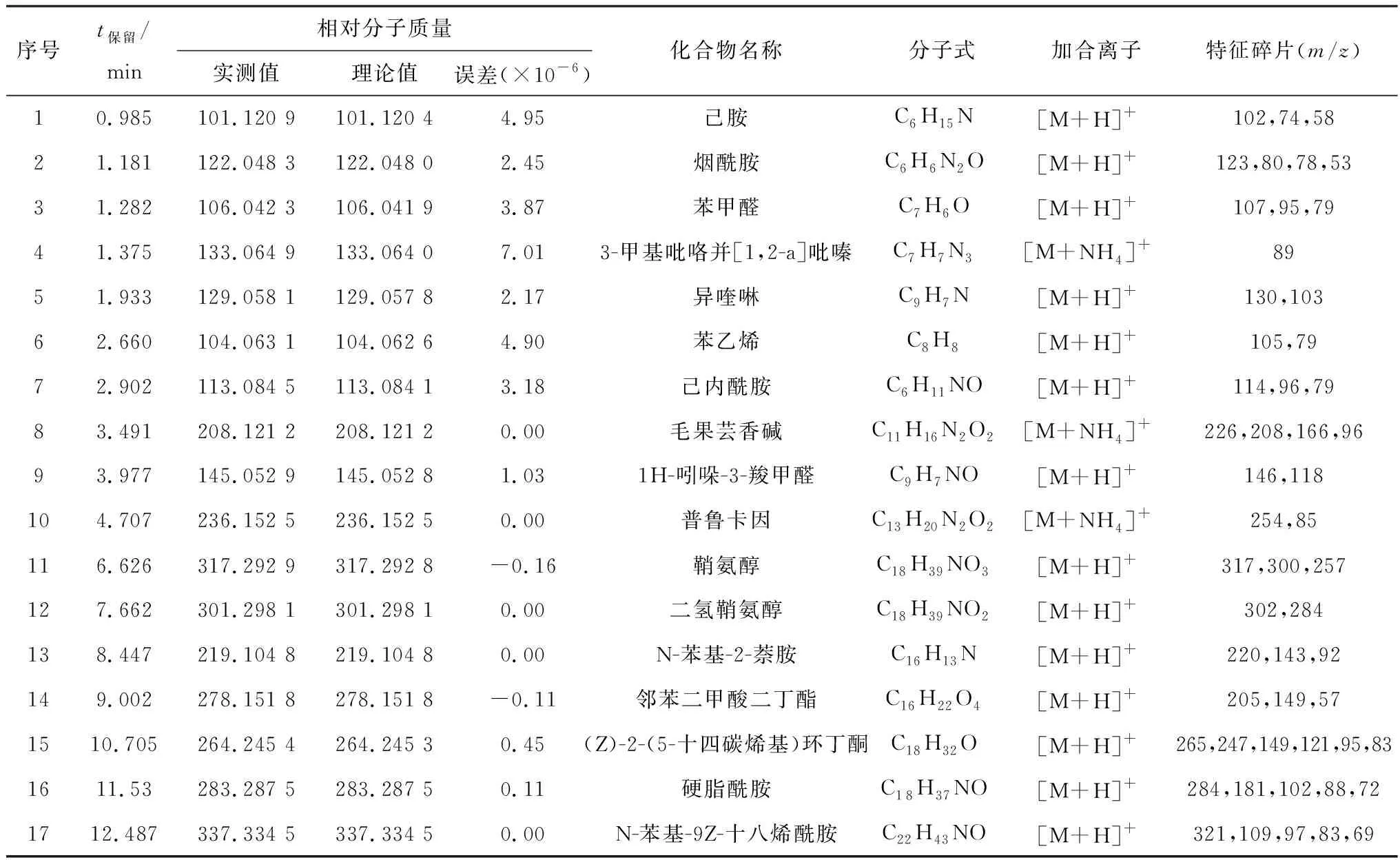
表4 正离子模式下酒炙车前子治疗奶牛胎衣不下活性组分Ⅵ的主要化合物
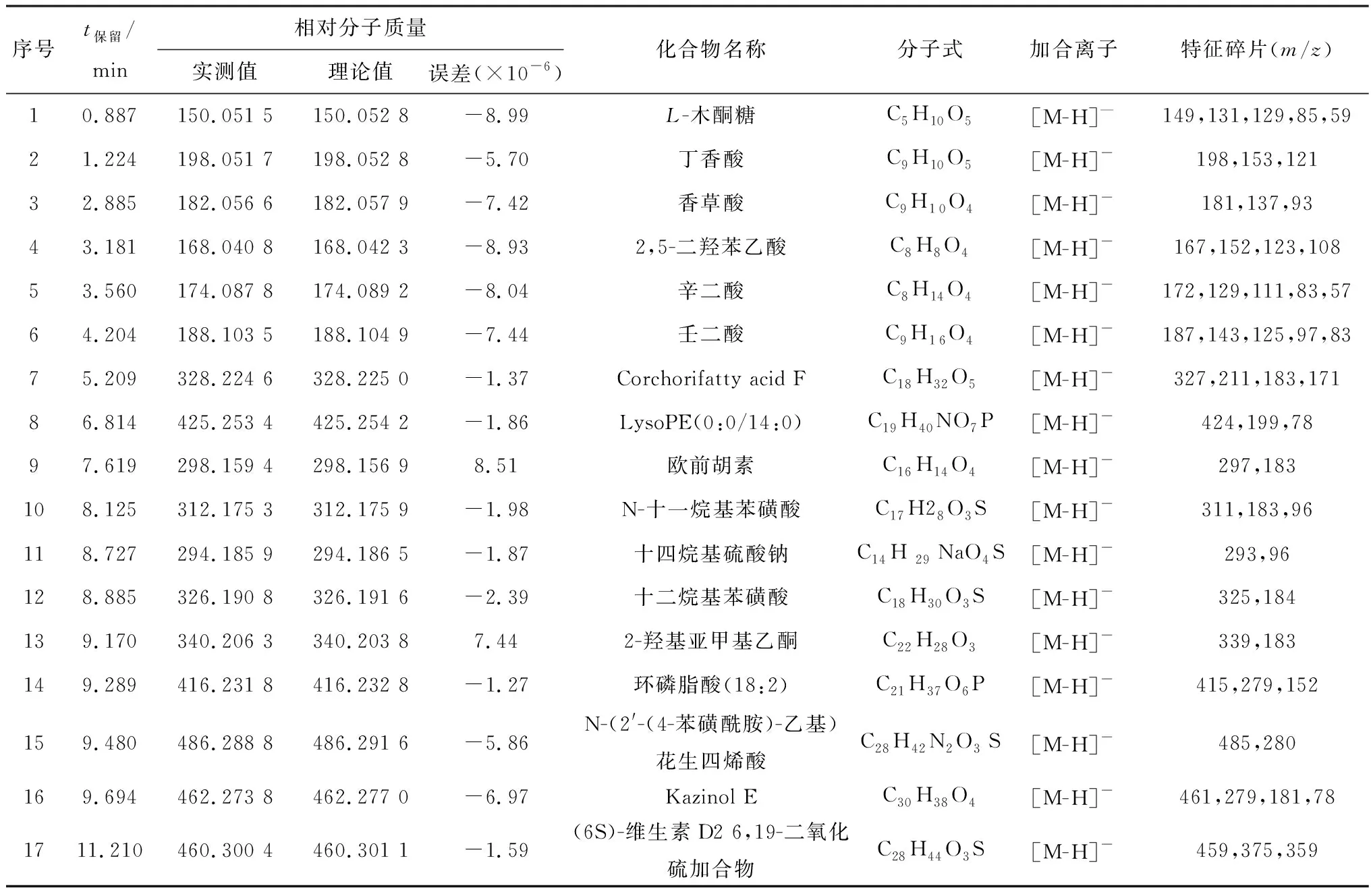
表5 负离子模式下酒炙车前子治疗奶牛胎衣不下活性组分Ⅵ的主要化合物
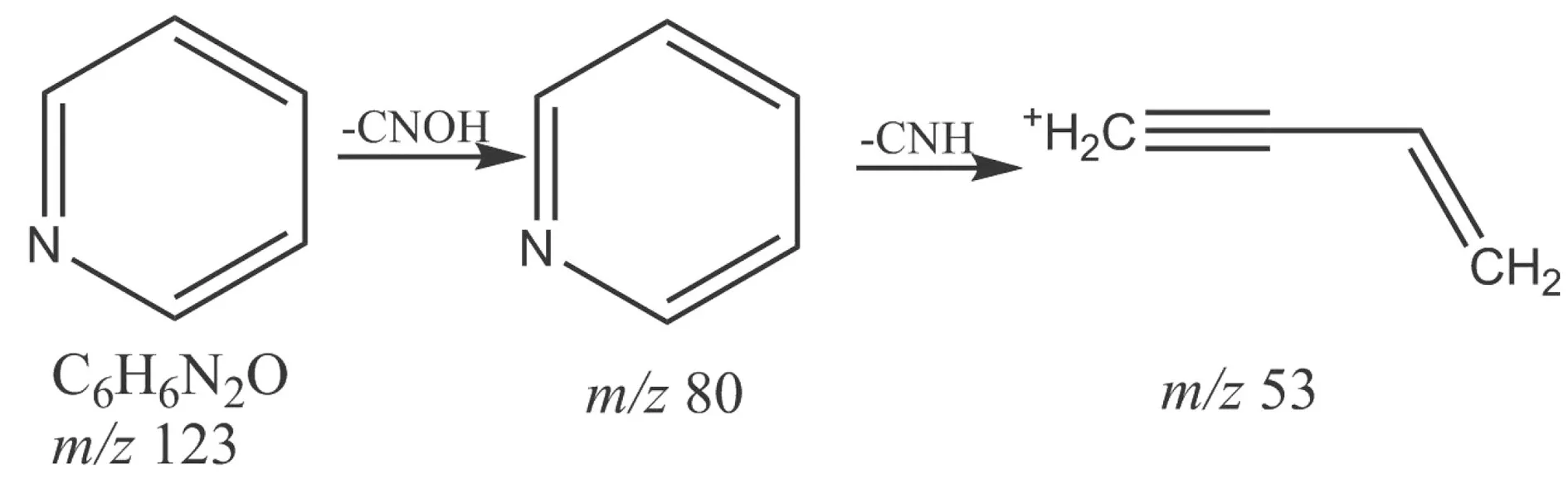
图6 正离子模式下烟酰胺的裂解途径
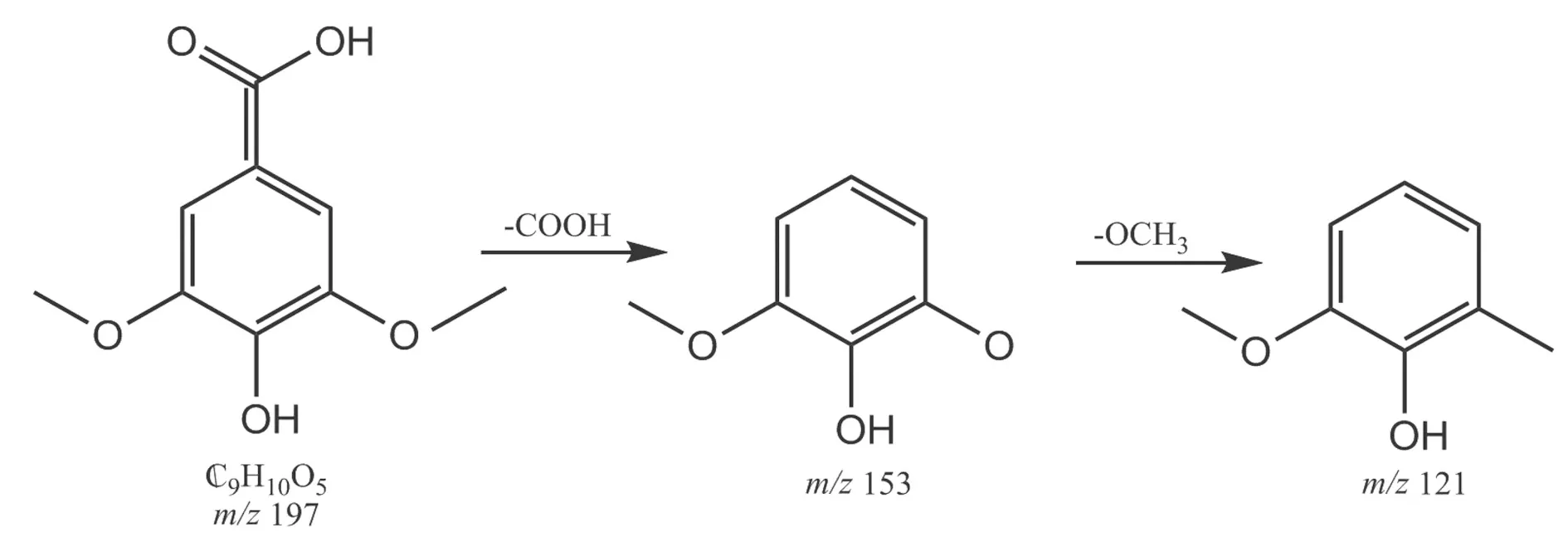
图7 负离子模式下丁香酸的裂解途径
3 讨论
据国家药典记载,车前子为车前科植物车前(PlantagoasiaticaL.)或平车前(P.depressaWilld)的成熟干燥种子,性味甘寒,入肾、肺、小肠经[12]。药理活性方面,其在利尿、消炎、降血压、降血脂、抗氧化和调节免疫力等方面具有显著疗效[13]。自古以来,我国兽医师利用酒炙车前子防治牛胎衣不下取得了良好的效果,成为民间的验方。本实验室前期也验证了酒炙车前子防治奶牛胎衣不下的疗效,同时进一步确定了其有效部位及其活性组分Ⅲ和Ⅵ[14-15],但其活性组分Ⅲ和Ⅵ的化学成分尚未阐明。因此,本研究运用LC-MS/MS技术对酒炙车前子活性组分Ⅲ和Ⅵ的化学成分进行分析及鉴定。利用LC-MS/MS对活性组分Ⅲ进行分析,通过正、负离子模式下共鉴定了31个化合物。其中正离子模式下根据质谱裂解特征分析确定为含有二氢鞘氨醇,而二氢鞘氨醇作为酰胺类化合物在机体内可经神经酰胺合成酶作用与酰基辅酶A合成二氢神经酰胺(dhCer),二氢神经酰胺则可通过引入双键的去饱和酶作用,调节红细胞表面电荷以防止凝集[16],这一作用可改善瘀血,进而对胎衣不下发挥治疗作用。另外,负离子模式下根据质谱裂解特征分析确定为含有壬二酸,壬二酸作为有机酸类化合物能够清除自由基和抑制氧化应激的发生[17],从而促进奶牛产后胎衣的排出。
与此同时,利用LC-MS/MS对活性组分Ⅵ进行分析,在正、负离子模式下共鉴定34个化合物。其中正离子模式下根据质谱裂解特征分析确定为含有烟酰胺,烟酰胺在机体多种氧化应激途径中,具有氢传递作用,可改善氧化应激状态。据YOMNA等[18]报道,在对乙酰氨基酚诱导的大鼠肝脏损伤模型中,经烟酰胺处理后,丙二醛(MDA)的含量降低,增加了GSH-Px活性,进而抑制氧化应激。而奶牛处于氧化应激状态时,MDA含量显著增加,影响细胞功能和代谢,易使胎盘功能受损,导致胎衣不下的发生[19]。基于此,可推测烟酰胺的抗氧化功能可防治奶牛胎衣不下的发生。此外,负离子模式下根据质谱裂解特征分析确定为含有丁香酸,其具有抗氧化、抗菌、抗癌、抗糖尿病和保护心脏、肝脏和脑/中枢神经系统的功能[20]。据报道,丁香酸其抗氧化功能,可显著降低一氧化氮(NO)、MDA含量,并且对小鼠CCl4诱导的肝损伤氧化应激起到保护作用[21-22]。当奶牛处于氧化应激状态时,机体内一氧化氮合酶(nitric oxide synthase)高表达,促使NO的大量产生,NO作为血管舒缩因子,可抑制子宫肌的收缩,进而影响胎儿胎盘与母体胎盘的分离[23-24]。由此可知丁香酸可通过抑制NO和MDA的生成而对治疗奶牛胎衣不下发挥作用。
综上所述,本试验运用LC-MS/MS技术,分析并鉴定了酒炙车前子治疗奶牛胎衣不下的活性组分Ⅲ和Ⅵ的化学成分,其分别含有31个和34个化合物,其中根据质谱裂解特征分析确定含有二氢鞘氨醇、壬二酸、烟酰胺和丁香酸,而它们均可能是治疗奶牛胎衣不下的关键药物成分。本试验阐明了酒炙车前子治疗奶牛胎衣不下活性组分Ⅲ和Ⅵ发挥药效的物质基础,为今后研发高效、安全和廉价的防治奶牛胎衣不下的中药制剂奠定基础。
