维生素E纳米乳液冻干粉末的制备及结构特性研究
2020-09-01张潇元朱鸿维王中江江连洲谢凤英赵玉莹张晓南
张潇元 潘 悦 朱鸿维 王中江 江连洲 谢凤英 赵玉莹 张晓南,2*
(1 东北农业大学食品学院 哈尔滨150030 2 黑龙江省学勤科技有限公司 哈尔滨150030)
目前, 纳米技术被广泛应用于营养物质与药物运送,具有智能化、靶向性的纳米级营养物质运送系统, 使芯材的生物利用率得到极大地提高。ABBAS 等[1]和YUAN 等[2]分别通过超声及高压均质法制备得到稳定性较好的纳米乳液, 尽管该纳米乳液在生物利用率和稳定性等方面与普通乳液相比具有极为显著的优势,然而,由大豆分离蛋白(SPI)等天然表面活性剂制备的纳米乳液在长时间储存后其有关物质含量偏离纳米乳液的合格标准。 随着人们生活节奏的加快及对健康营养饮食的追求,在最大化载量、强稳定性基础上开发方便及易储藏的纳米乳液成为研究热点。 将纳米乳液做成冻干固体制剂是一种可行的选择, 在提高其稳定性的同时实现长期保存。
冻干纳米乳液的制作采用新型的纳米级真空冷冻干燥技术。 该技术将冷冻技术同真空技术有机的联系起来,是一种新型干燥技术[3]。 与其它干燥工艺相比, 真空冷冻干燥技术能够最好地留存食品原有的色泽、香味以及营养成分,并可最佳地保持食品原有形态, 兼具优异的速溶性和水复溶性,进而提高某些营养物质的稳定性,扩大其应用范围[4]。
本试验中, 联合真空冷冻干燥技术与高压均质技术制备一种水包油型(O/W)维生素E 纳米乳液粉末复原乳液, 为提高维生素E 的稳定性和生物利用率提供一定的理论基础。
1 材料与方法
1.1 试验材料与设备
1.1.1 原料与主要试剂 大豆分离蛋白(蛋白含量89.21%),山东高唐蓝山集团;葵花籽油,中粮集团福临门;无水乙醇、乙醚、氢氧化钠、维生素E、磷酸二氢钠(以上试剂全部为分析纯试剂)。
1.1.2 主要设备、仪器 高压均质机,英国安盛联合科技有限公司;ALPHA 1-4 LSC 型冷冻干燥机,美国SIM 公司;Gemini HR Nano 流变仪,英国Malvern 仪器有限公司; Zetasizer Nano-ZS90 粒度分析仪,德国Christ 公司; Hitachi S-3400 扫描电子显微镜,日立高新技术公司英国马尔文公司;MAGNA-IR560 傅里叶红外光谱仪, 美国尼高丽公司。
1.2 试验方法
1.2.1 纳米乳液粉末的制备 将参考Sungje 等[5]的方法得到的维生素E 纳米乳液, 真空冷冻干燥得维生素E 纳米粉末。 冷冻条件:-50 ℃, 冻干12 h。
将真空冷冻干燥维生素E 纳米粉末按照原始乳液的配方, 加入pH 7.0 的0.1 mol/L 磷酸盐缓冲溶液复溶。
1.2.2 维生素E 复原纳米乳液单因素试验 以大豆分离蛋白(SPI)质量浓度、葵花籽油质量浓度、高压均质压力、 高压均质次数为观测因子做单因素试验。 分别测定不同条件下制备的维生素E 复原纳米乳液样品的平均粒径、 多分散性指数、ζ 电位、包埋率。
1)大豆分离蛋白质量浓度的选择 分别配制质量浓度为5,10,15,20,25 mg/mL 的SPI 溶液,室温持续搅拌120 min,逐渐添加质量浓度45 mg/mL 的葵花籽油,均质后完成粗乳液制备。设置均质参数:100 MPa,4 次。
2)葵花籽油质量浓度的选择 配制15 mg/mL (质量浓度)的SPI 溶液, 室温连续搅拌120 min, 分别添加质量浓度35,40,45,50,55 mg/mL的葵花籽油,均质后完成粗乳液制备。设置均质参数:100 MPa,4 次。
3)均质压力 配制质量浓度15 mg/mL 的SPI 溶液,逐渐添加45 mg/mL 的葵花籽油,制备粗乳液。 设置均质压力分别为60,80,100,120,140 MPa,次数4 次。
4)均质次数 配制15 mg/mL 的SPI 溶液,逐渐添加45 mg/mL 的葵花籽油,制备粗乳液。 设置均质参数:压力100 MPa,2,3,4,5,6 次。
5)复原纳米乳液响应面优化 基于单因素试验结果,使用Design-Expert 软件进行响应面试验设计与分析。 选取大豆分离蛋白质量浓度A(mg/mL)、葵花籽油质量浓度B(mg/mL)、高压均质压力C(MPa)及高压均质次数D(次)作为自变量,将复原纳米乳液的平均粒径Y1(nm)和包埋率Y2(%)作为响应值,做四因素三水平试验。
1.2.3 复原纳米乳液的平均粒径、ζ 电位测定 采用粒度分析仪对上述复原维生素E 纳米乳液样品的油滴平均粒径及ζ 电位进行检测。 设置粒度分析仪折射率参数:水相为1.33,葵花籽油油滴为1.45。 在测定平均粒径及ζ 电位前,先将纳米乳液样品用磷酸盐缓冲溶液(pH 7.0)稀释,稀释梯度分别为1 000 倍和50 倍。
一天,佛陀问他的弟子:未受过佛法教化的人,每天吃饭、劳作、睡觉,经历生老病死以及种种烦恼;受过佛法教化的人,一样每天吃饭、劳作、睡觉,一样经历生老病死和种种烦恼。那么,受过佛法教化的人和未受过佛法教化的人,又有什么区别呢?他的弟子一时不知如何回答。
1.2.4 复原纳米乳液包埋率的测定 采用紫外分光光度法测定复原乳液包埋效果,1.0 g 产品中加入20 mL 乙醚,在25 ℃条件下剧烈振摇1 min,将溶剂过滤到旋转蒸发瓶中旋转蒸发, 以提取出未被包埋的VE,即表面VE。 在1.0 g 复原乳液中加入20 mL 无水乙醇,25 ℃条件下剧烈振摇10 min,将溶剂过滤到旋转蒸发瓶中旋转蒸发,以提取出复原纳米乳液中的VE,即总VE。以无水乙醇为溶剂,将前两者分别稀释至合适浓度,置紫外分光光度计中,测定波长285 nm 处吸光值,得表面VE 含量和总VE 含量。 包埋率计算公式:
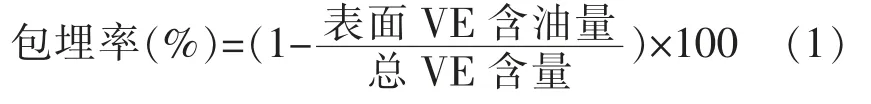
1.2.5 真空冷冻干燥纳米乳液粉末的微观形态观察 将获得的真空冷冻干燥粉末进行氮气填充并密封,置遮光处存储。在微观形态观察前先用导电双面胶把粉末样品固定于金属台上, 缓缓吹除多余粉末,于真空条件下镀金,最后把样品粉末放在扫描电子显微镜(15 kV)下观察其微观形态。
1.2.6 维生素E 原始乳液及复原纳米乳液的流变学特性测定 用流变仪分析维生素E 溶液的流变学性质,用直径60 mm 的锥形板,设置板间距50 μm。取1 mL 原始维生素E 乳液、复原纳米乳液和大豆蛋白溶液置于平板上, 在温度25 ℃条件下剪切,流变仪剪切速率为0.01~1 000 s-1。
1.2.7 真空冷冻干燥纳米乳液粉末的红外光谱测定 参考QIN 等[6]的方法。 称取1 mg 冻干干燥的维生素E 纳米乳液粉末,向其中加入100 mg 溴化钾与之充分混合, 再将上述混合物进行压片便可接受FT-IR 检测。为保证有效降低由水蒸汽IR 吸收给测量带来的干扰, 向测量室内通入干燥的N2持续淋洗。 设置FT-IR 测定参数: 波数精度0.01 cm-1,分辨率4 cm-1,扫描64 次,波数范围4 000~400 cm-1。 使用Peakfit Version 4.12 拟合FT-IR 检测所得波谱图, 按照所得积分面积分析各二级结构的相对含量。
1.2.8 数据统计及分析 以上所有试验至少重复3 次, 数据ANOVA 差异显著性分析采用软件SPSS Statistics 22,其中P<0.05 为显著性差异。 数据的分析, 图表结果处理及检测图谱分析处理采用Origin9.1 软件及PeakFit 4.12 软件。
2 结果与分析
2.1 壁材浓度对复原纳米乳液粒径、电位的影响
由图1 可知, 复原纳米乳液的粒径和PDI 呈现相同的变化趋势, 均随壁材浓度的增加先减小后增加。 壁材质量浓度过低时,其结构松散,乳化能力低[7],复原后液滴易聚结,体系粒径较大而不稳定。 当壁材质量浓度15 mg/mL 时,壁材中高分子空间结构最紧密,能够大量滞纳芯材[8],冻干后粉末包埋率增加,复原纳米乳液平均粒径最小,体系最稳定。壁材的浓度过大时,极大地阻碍芯材的扩散和运动, 并严重阻碍壁材网状结构的形成[9],其包封率出现降低趋势。根据陈岩等[10]的研究,SPI具有一定的黏性,使粉末间发生粘连,因而降低了复原纳米乳液的包埋率,增大了乳液粒径,导致体系不稳定。 这与BURGESS 等[11]的研究结果一致。大豆分离蛋白在体系pH7.0 时带负电, 由图1 可知,当SPI 质量浓度为15 mg/mL 时,电位达到最大值。这是由于随着壁材浓度的增加,纳米乳液液滴表面的蛋白吸附逐渐饱和, 体系电位达到最大值,冻干粉末颗粒间的排斥力达到最大[12],复原后液滴不易聚集,体系稳定。 若ζ 电位低,则纳米冻干粉末之间吸引力超过排斥力[13],复原后液滴更易于聚集,体系不稳定。
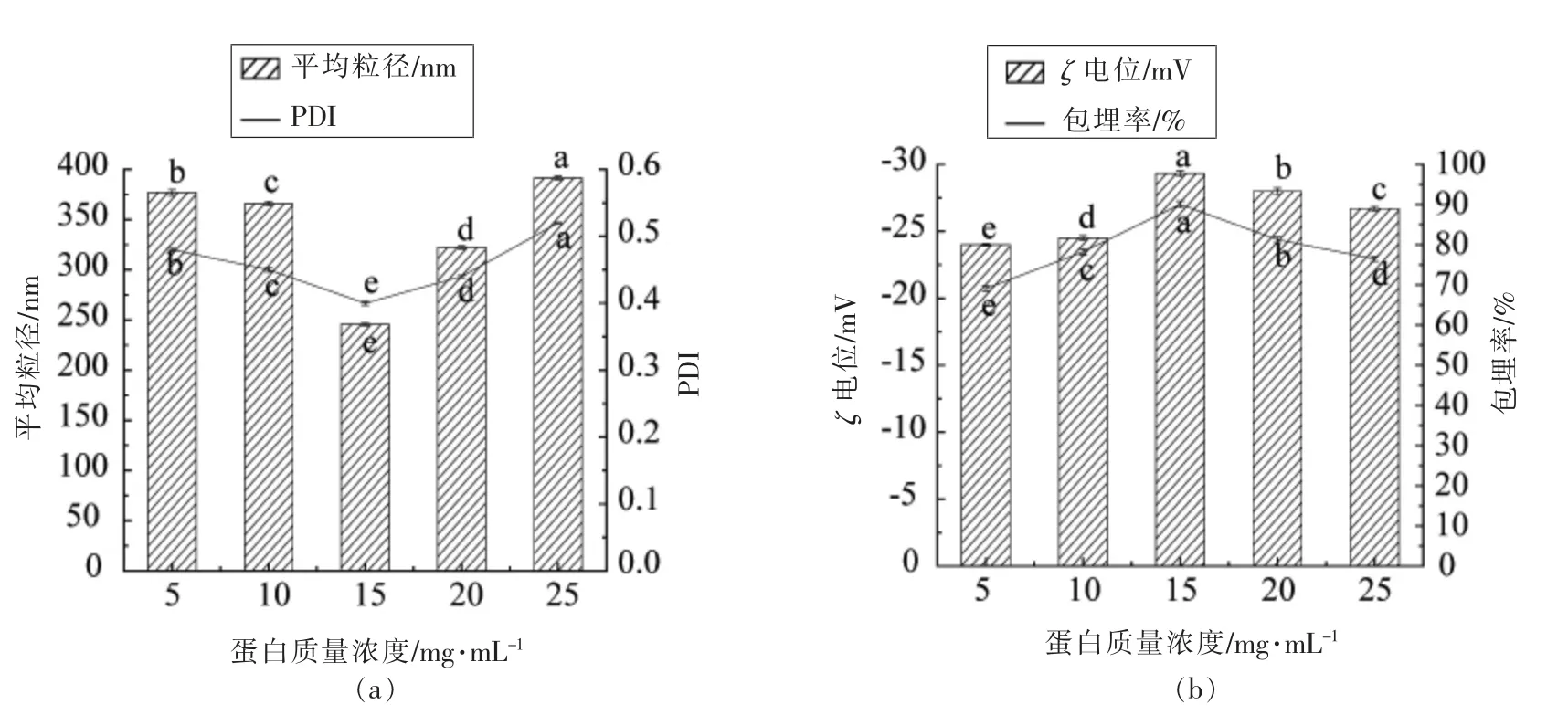
图1 SPI 质量浓度对维生素E 复原纳米乳液理化稳定性的影响Fig.1 Effect of SPI concentration on the physicochemical stability of vitamin E reconstituted nanoemulsion
2.2 芯材浓度对复原纳米乳液粒径、电位影响
由图2 可知,复原纳米乳液的粒径、PDI 随芯材浓度的增加先减小后增加。 原因可能是芯材的载入降低原有壁材的流动性[7],冻干粉末包埋率增加,复原后液滴平均粒径降低;随着芯材含量的增加,达45 mg/mL 时,芯材与壁材间的一些次级相互作用使壁材具有相对刚性的结构, 包埋率达到最大, 此时复原纳米乳液体系平均粒径、PDI 最小,体系最稳定;然而芯材添加量过多,降低了壁材比重,芯材不能被全部乳化包埋,包埋率降低,使乳液体系不稳定。 根据路HINRICHS 等[14]的研究,当芯材用量增加时,乳状液滴的密度增加,彼此之间更倾向于互相碰撞以及聚积成不规则状态。以上因素均导致复原纳米乳液粒径增大,液滴分布不均匀,体系不稳定。 由图2 可知,芯材质量浓度为45 mg/mL 时,电位达到最大值,这是因为壁材浓度升高, 复原纳米乳液液滴周围吸附更多的负离子,包埋率达到最大值,乳液体系稳定。
2.3 均质压力对粒径、电位的影响
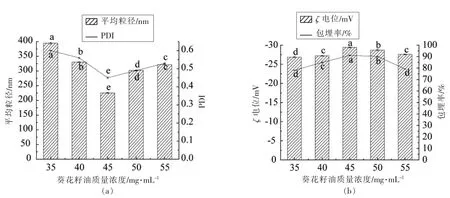
图2 葵花籽油浓度对维生素E 复原纳米乳液理化稳定性的影响Fig.2 Effect of sunflower oil concentration on the physicochemical stability of vitamin E reconstituted nanoemulsion
由图3 可知,当均质压力增加时,复原纳米乳液的粒径呈现减小的趋势, 当压力增到100 MPa时,粒径最小,此时复原乳液稳定性最高。 当均质压力继续增加时,粒径逐渐增大。出现这种趋势的原因可能在于压力逐渐增加, 有利于芯材均匀分散于壁材体系中[15],冻干后粉末的包埋率提高,复原乳液滴平均粒径减小。 施加过高的均质压力会形成较小粒径的液滴, 此时具有较大的表面积及较高的表面能[16],使得液滴间出现聚结现象,导致冻干后粉末的包埋率降低,平均粒径增加,复原乳稳定性降低。由图3 可知,均质压力对复原乳液的ζ 电位影响显著, 随着均质压力的增大,ζ 电位先增加后下降, 当均质压力为100 MPa 下时ζ 电位绝对值最高。可能是由于随着均质压力的增加,维生素E 纳米乳液冻干粉末体积变小,大小更均匀,形成复原乳后液滴之间的静电排斥力增大, 乳化体系的稳定性提高。 然而,均质压力过高,形成的冻干粉末粒径过小,表面能过高,且ζ 电位的绝对值在复原后减小,稳定性降低[17]。
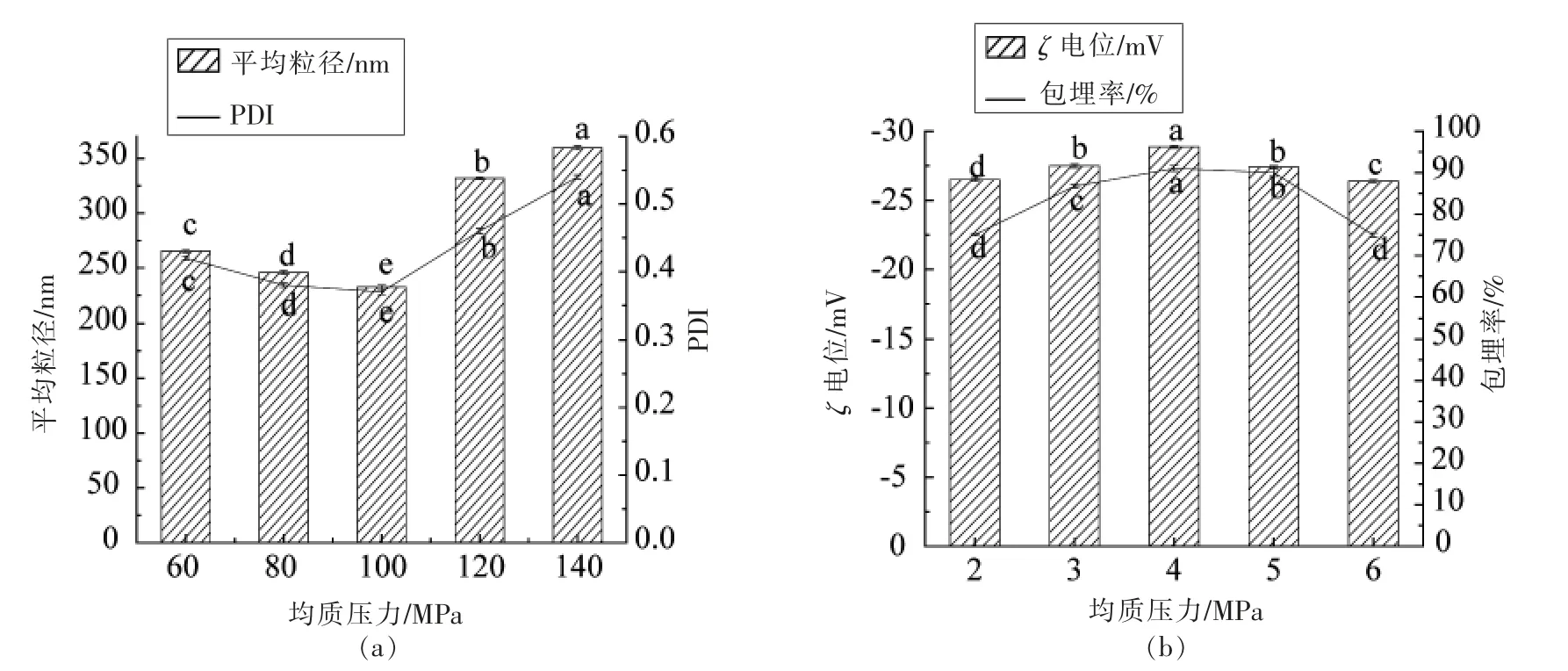
图3 均质压力对维生素E 复原纳米乳液理化稳定性的影响Fig.3 Effect of homogeneous pressure on the physicochemical stability of vitamin E reconstituted nanoemulsion
2.4 均质次数对粒径、电位的影响
由图4 可知,随着均质次数的增加,复原乳液粒径减小,当均质循环次数超过4 次时,复原乳平均粒径开始增加,包埋率增大。其原因可能是均质时产生强剪切、撞击和空穴效应等作用,均质次数越多该作用越强,制得的颗粒粒径便越小[18]。 随着均质次数的增加,冻干粉末的粒径没有持续减小。均质次数过多,破坏壁材体系的包埋,复原后液滴易聚合,使粒径增加。 由图4 还可知,复原乳的ζ电位随均质次数的增加先增加后减小, 均质4 次时ζ 电位最高; 均质次数的增加使SPI 的分散性最高,更好地吸附在油水界面[19],增加油相的包埋效果,此时乳液体系最稳定。当高压均质次数过多时,过处理效应促使乳液液滴聚合,导致纳米乳液的ζ 电位和乳化产率下降[20]。

图4 均质次数对维生素E 复原纳米乳液理化稳定性的影响Fig.4 Effect of homogenization times on the physicochemical stability of vitamin E reconstituted nanoemulsion
2.5 葵花籽油复原纳米乳液响应面试验
借助Design-Expert 对上述试验进行响应曲面法过程优化。 遵循中心组合设计原理,设计响应面优化试验。分别选取大豆分离蛋白质量浓度A(mg/mL)、葵花籽油质量浓度B(mg/mL)、均质压力C(MPa)、均质数量D(次)为自变量,响应值的设置分别为平均粒径(R1)和包埋率(R2),具体试验方案与结果如表2 所示。
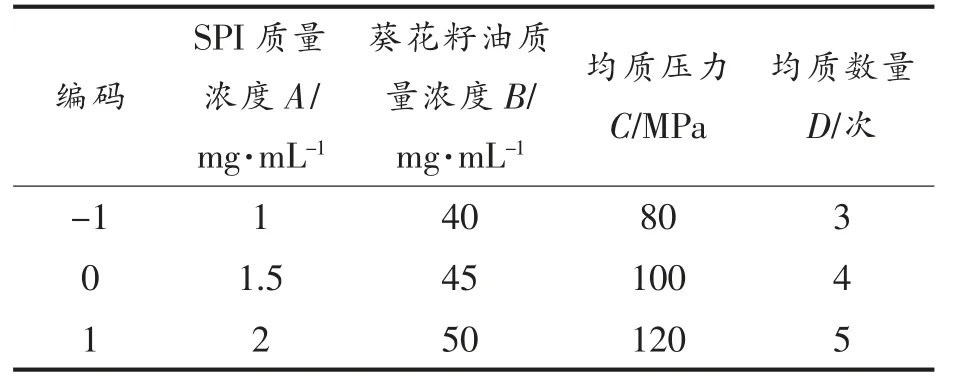
表1 因素水平编码表Table 1 Encode table of factors and levels
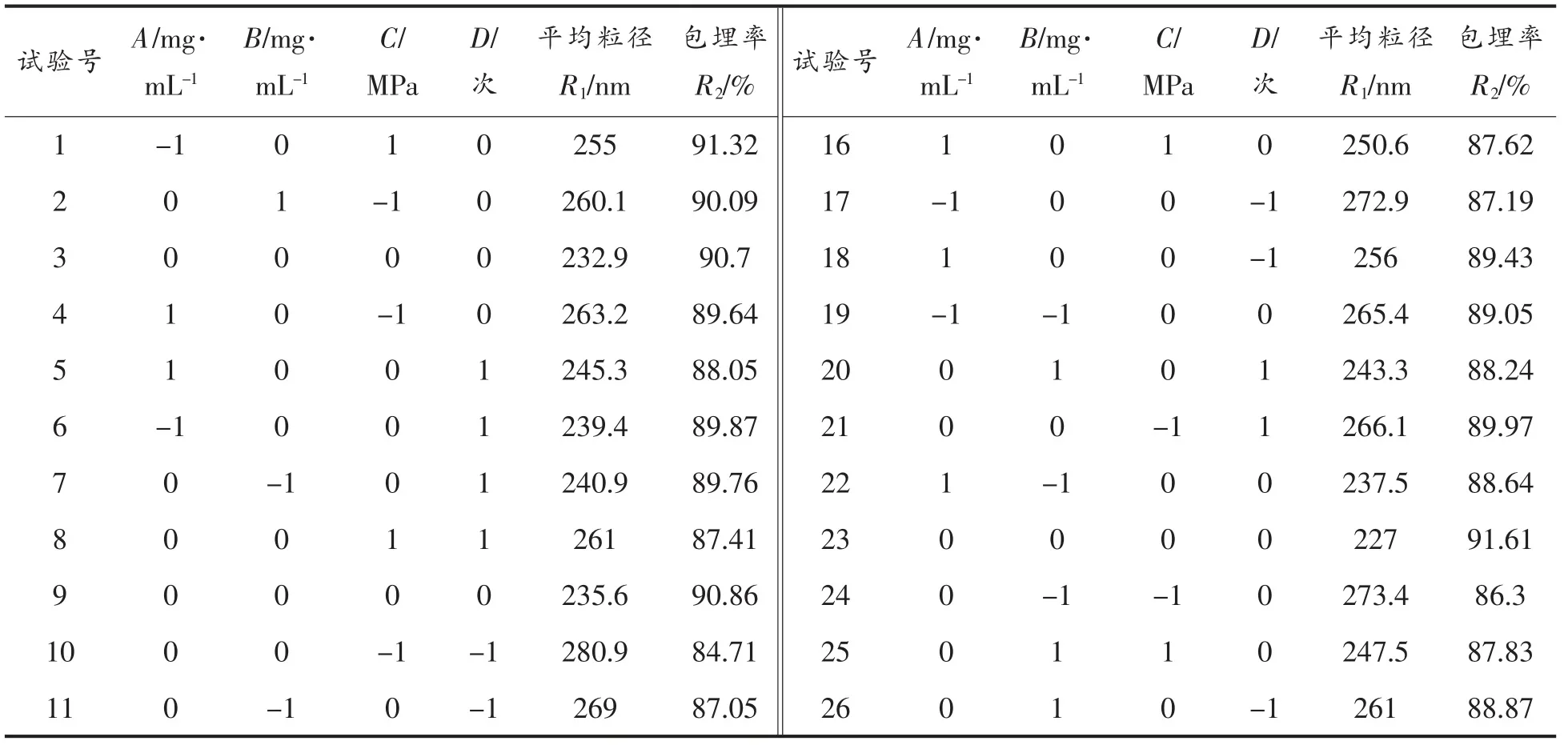
表2 试验安排及结果Table 2 Experiment scheme and results

(续表2)
利用Design-Expert 对平均粒径R1进行数采集和分析,构建二次响应面回归模型:
R1= 232.66 - 3.69A - 2.58B - 8.05C - 9.01D+10.27AB+2.45AC+5.70AD+3.67BC+2.60BD+2.87CD+8.28A2+5.97B2+19.97C2+14.28D2
由表3 可知,此模型能有效模拟试验数据,拟合方程中因变量和各自变量表现显著的线性相关性,且回归项极显著(P<0.0001),而模型拟合方程失拟项不显著(P>0.05),响应面回归模型拟合度R2=95.58%,R2Adj=91.17%,响应值最优值可通过此模型来推测。 采用F 检验进行比较分析得到各变量的贡献率排序为D>C>A>B, 即均质次数>均质压力>大豆分离蛋白质量浓度>葵花籽质量浓度。通过响应面寻优分析获得最佳工艺参数为:大豆分离蛋白质量浓度15.40 mg/mL,葵花籽油质量浓度45.16 mg/mL,均质压力103.47 MPa,均质数量4 次,响应值平均粒径有最优值为230.51 nm。

表3 回归与方差分析结果Table 3 Results of regression and variance analysis
利用Design-Expert 对包埋率R2进行数采集和分析,构建二次响应面回归模型,如下所示:
R2=90.82-0.038A+0.24B+0.60C+0.47D -0.085AB - 1.92AC - 1.02AD - 1.24BC - 0.84BD -2.07CD-0.88A2-1.09B2-1.40C2-1.28D
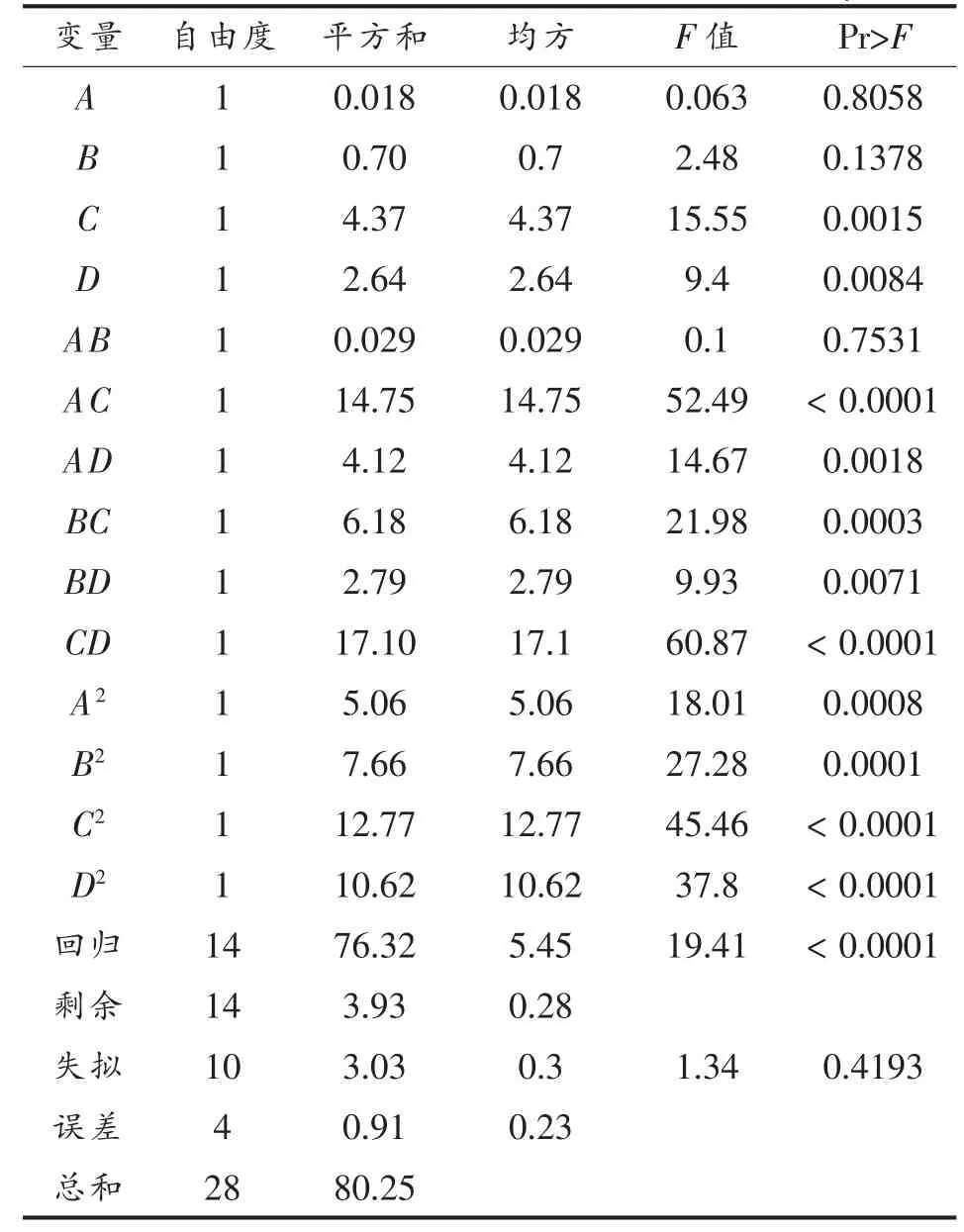
表4 回归与方差分析结果Table 4 Results of regression and variance analysis
由表4 可知,此模型能够模拟试验数据,此拟合方程中因变量和各自变量表现出显著的线性相关性,且回归项极显著(P<0.0001),而模型拟合方程的失拟项不显著(P>0.05),响应面回归模型拟合度R2=95.10%,R2Adj=90.20%,响应值最优值可通过此模型来推测。 采用F 检验比较得到各变量的贡献率排序为C>D>B>A(均质压力>均质数量>葵花籽油质量浓度>大豆分离蛋白质量浓度)。 通过响应面寻优分析获得最佳工艺参数为: 大豆分离蛋白质量浓度10 mg/mL, 葵花籽油质量浓度43.07 mg/mL,均质压力120 MPa,均质4 次,响应值乳化产率有最优值为91.30%。
采用联合求解法确定平均粒径、 包埋率均优的条件为: 大豆分离蛋白质量浓度14.52 mg/mL,葵花籽油质量浓度45.24 mg/mL,均质压力103.11 MPa,均质4 次,此条件下平均粒径230.88 nm,包埋率为90.89%。 为适应生产,将制备条件优化为大豆分离蛋白质量浓度15 mg/mL,葵花籽油质量浓度45 mg/mL,均质压力100 MPa,均质4 次,此条件下平均粒径232.66 nm,包埋率为90.82%。 此结果表明响应值的试验值与回归方程预测值之间具有较高的吻合度。
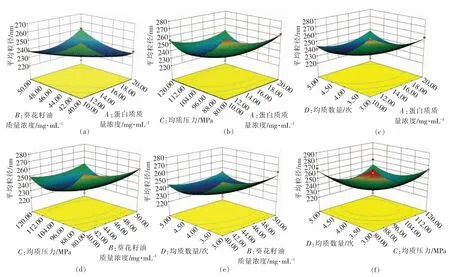
图5 交互作用对复原纳米乳液平均粒径的影响Fig.5 Effect of interaction on the average particle size of reconstituted nanoemulsion

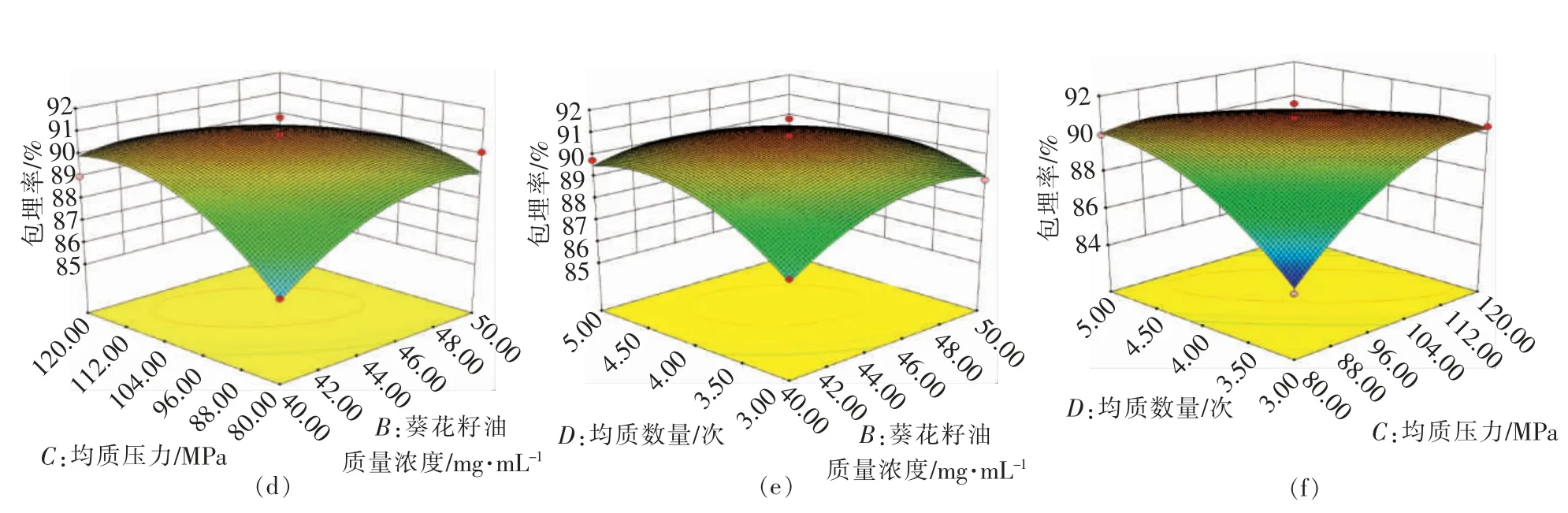
图6 交互作用对复原纳米乳液乳化产率的影响Fig.6 Effect of interaction on emulsification yield of reconstituted nanoemulsionQ
2.6 扫描电镜观察
图7a 为大豆分离蛋白粉末的扫描电镜图片,图7b 为纯的维生素E 粉, 两种物质形态不规则,表面粗糙,且颗粒直径较大[21]。 图7c 为维生素E纳米乳液冻干粉末,其表面完整光滑,结构致密,平均粒径变小, 说明高压均质可以提高壁材的乳化作用,使其包埋率增加。 该结果支持了江连洲等[22]的研究结果。 冷冻干燥粉末表面有凹陷、无收缩, 粉末表面的孔洞是小冰晶由固态到气态升华所致, 该结构对被包封的物质具有一定保护作用[23]。 通过比较3 个图的粒径,发现图7c 粒径最小,说明此时维生素E 纳米乳液已形成,体系最稳定。

图7 扫描电镜图像Fig.7 Microscope images by scanning electron microscopy
2.7 纳米乳液及冻干粉末复原流变学特性
由图8 可知, 制备的纳米乳液为牛顿型纳米流体,在0.1~400 s-1范围内表观黏度降低,呈现剪切稀化特征,这是因为随着剪切速率的増大,最初杂乱排布的纳米粒子沿流线方向呈有序排列,纳米粒子间的摩擦逐渐减小,流动阻力随之减小,其黏度呈逐渐下降的趋势,最终达到稳定[24-26]。 而在大于400 s-1范围,黏度基本保持不变,由于高压均质的剪切稀化作用降低了乳液的黏度, 不易被测出。 这时高压均质乳液和复原乳液均表现出牛顿流体特性,说明纳米复原乳液特性没有改变。
2.8 纳米乳液及冷冻干燥粉末复原乳液的红外光谱
红外光谱是依据分子在不同波长下的振动,而吸收相应红外辐射所形成的吸收谱图, 可以检测分子中含有的化学基团及化学键[27]。 图9 为大豆分离蛋白粉末和真空冷冻干燥维生素E 纳米乳液粉末的红外光谱图, 其显示大豆分离蛋白分子中的氨基基团,包括蛋白质环状结构中的C-C 振动,C-O-O 糖苷键振动波段信息,酰胺I 带(由HO-H 弯曲振动和C=O 伸缩振动产生)、 酰胺Ⅱ带(由N-H 弯曲产生)及酰胺Ⅲ带(由C-O 和C-OC 振动产生)[28]。 由图9 可知,在3 270 cm-1处真空冷冻干燥维生素E 纳米粉末的-OH 伸缩振动峰峰形较窄且强度变强。 真空冷冻干燥维生素E 纳米粉末在1 744 cm-1处的C=O 振动吸收峰强度减弱甚至消失,蛋白质酰胺Ⅰ带从1 631.4 cm-1移动到1 637 cm-1, 酰胺Ⅱ带从1 535.1 cm-1移动到1 515 cm-1,以上变化说明维生素E 的载入对蛋白质的二级结构产生影响, 蛋白质与维生素E 之间存在氢键作用。 在1 077 cm-1处是-NH 的伸缩振动,由1 097 cm-1移动到1 077 cm-1,且吸收峰强度减弱, 说明由于维生素E 的载入使大豆分离蛋白的氢键发生变化。

图8 维生素E 纳米乳液、真空冷冻干燥维生素E粉末复原纳米乳液、大豆分离蛋白乳液的流变性Fig.8 Rheological property of Vitamin E nanoemulsion,vacuum freeze drying vitamin E powder reconstituted nanoemulsion, soy protein isolate emulsion
采用FT-IR 法分析大豆分离蛋白的二级结构,FT-IR 酰胺Ⅰ带(1 600~1 700 cm-1)反映维生素E 纳米乳液粉末中蛋白质的二级结构。 通过Omnic 9.1 软件选取特定波段(1 600~1 700 cm-1),利用分析软件PeakFit 4.12 对以上述波段进一步处理, 包括二阶导数拟合、 基线校正及高斯去卷积。 参考Meng 等[29]研究,可得到每个子峰波段和冻干粉末, 以及蛋白粉末中大豆分离蛋白二级结构之间的对应关系, 分别表示为: β-折叠结构1 615~1 637 cm-1和1 682~1 700 cm-1;α-螺旋结构1 646~1 664 cm-1[30];无规则卷曲构1 637~1 645 cm-1;β-转角结构1 664~1 681 cm-1[31]。 根据谱带指认,将拟合的各子峰的峰面积百分含量进行加和,得出蛋白质各二级结构含量的百分比。 各种二级结构的种类及含量计算结果如表5 所示。
由图10 可知,在维生素E 纳米乳液及真空冷冻干燥维生素E 纳米粉末酰胺Ⅰ带二阶导数拟合图谱中均有8 个峰。 表5 列出大豆分离蛋白各二级结构含量,真空冷冻干燥后大豆分离蛋白的α-螺旋和β-转角均增加,而β-折叠和无规则卷曲含量减少。 α-螺旋含量增加,β-折叠含量降低,说明压力对大豆分离蛋白分子间氢键影响较大, 此时蛋白质分子结构发生改变, 由初始的紧凑状态变为松散状,空间位阻效应降低,更容易迁移并吸附到油水界面[32],形成更厚的界面膜,能有效防止液滴碰撞聚合,使体系更加稳定。
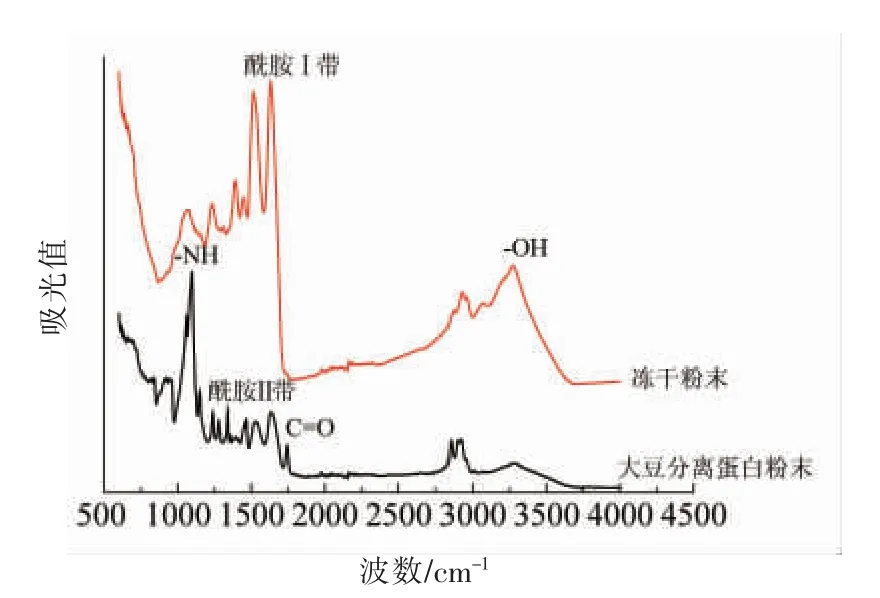
图9 真空冷冻干燥维生素E 纳米乳液粉末、大豆分离蛋白粉末的FTIR 光谱图Fig.9 IR spectrogram of vacuum freeze drying vitamin E nanoemulsion powder,soy protein isolate powder

表5 维生素E 纳米乳液、真空冷冻干燥维生素E纳米乳液粉末中大豆分离蛋白的二级结构特征Table 5 Percentages of protein secondary structure of vitamin E nanoemulsion, vacuum freeze drying vitamin E powder reconstituted nanoemulsion
3 结论
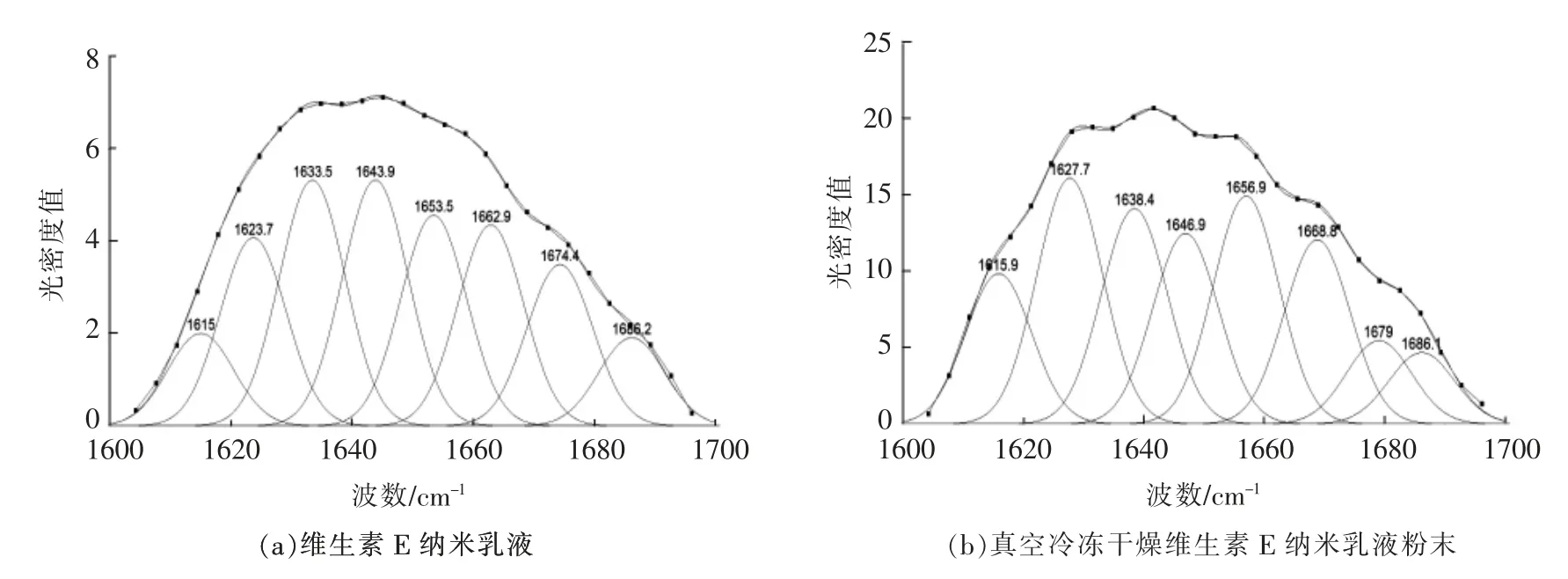
图10 维生素E 纳米乳液、真空冷冻干燥维生素E 纳米乳液粉末去卷积酰胺Ⅰ带二阶导数拟合图谱Fig.10 Second-derivative FTIR spectra in the amide I region and Gaussian curve fitting for Vitamin E nanoemulsion,vacuum freeze drying vitamin E powder reconstituted nanoemulsion
联合真空冷冻干燥技术与高压均质技术制备了一种水包油型(O/W)真空冷冻干燥维生素E 纳米粉末复原乳液, 通过单因素试验及响应面分析法优化,其最佳工艺条件为:大豆分离蛋白质量浓度15 mg/mL,葵花籽油质量浓度45 mg/mL,均质压力100 MPa, 均质4 次。 所得平均粒径232.66 nm,包埋率为90.82%。 通过扫描电子镜、流变仪、红外光谱等手段对维生素E 纳米乳液、 冷冻干燥粉末以及复原乳液的物理化学性质进行研究。 扫描电镜结果表明, 维生素E 纳米乳液冻干粉末具有致密、均匀的结构和光滑平整的表面。流变仪扫描结果表明, 冻干粉末复原乳液具有剪切稀释流变现象,呈现牛顿流体的典型特征。红外光谱试验结果表明冻干粉末的蛋白α-螺旋和β-转角结构增加,β-折叠和无规则卷曲结构降低。 综上所述,本研究不仅提高了维生素E 吸收利用率和生物利用率,增加了其稳定性,而且拓展了其运用范围,为其在食品工业生产中的应用提供了理论基础。
