椎间孔镜手术两种软组织扩张方法比较
2020-08-29吴洁石徐瑞生
吴洁石,薛 骏,徐瑞生
椎间孔镜等脊柱内窥镜手术在建立工作套管时,第一步是扩张软组织,需使用直径逐渐增加的3个导管对皮肤、皮下脂肪组织、深筋膜和肌肉组织进行扩张。传统方法是沿较细的Ⅰ级导杆插入逐渐增粗的3根导管和工作套管,但在导管旋转拧入致密深筋膜时,患者会产生明显的疼痛和牵拉不适感。笔者设计一款可在深筋膜上制作放射状小切口的深筋膜放射状切开器(实用新型专利号ZL 2018 2 0325717.7,图1)。在椎间孔镜手术中,先用切开器在腰部深筋膜上切出放射状的切口,再使用导管进行软组织扩张。本研究的目的在于比较其与传统方法的效果差异,为椎间孔镜软组织扩张提供新的方法选择。
1 资料与方法
1.1 一般资料
临床研究方案经医院伦理委员会批准。纳入标准:①诊断为单节段腰椎间盘突出症或腰椎管狭窄症,临床表现为严重腰腿痛,经正规保守治疗6周症状无缓解或反复发作;②CT或MRI检查提示腰椎间盘突出症或椎管狭窄症,神经受压部位与临床症状体征吻合;③患者签署知情同意书。排除标准:①既往有腰背部外伤或在本次手术区域中触及增生软组织结节;②椎间孔镜术后相同节段复发,需要再次手术者。
将2018年1月至2019年12月行腰椎侧路经皮内窥镜腰椎间盘摘除术(percutaneous endoscopic lumbar discectomy,PELD)手术、符合纳入标准的63例患者按照随机数字表法随机分为标准组和切开器组。其中标准组30例,采用标准法进行软组织扩张;切开器组33例,运用深筋膜切开器切开深筋膜后再进行软组织扩张。实验分组为双盲设计。患者性别、年龄、体质量指数(body mass index,BMI)、腰椎病变节段、术前腰腿痛视觉模拟量表(visual analogue scale,VAS)评分[1]等一般资料比较,差异无统计学意义(P>0.05),具有可比性(表1)。
1.2 深筋膜切开器
该器械包括圆锥体的头端和与之相连的圆柱形尾端,内部是一贯穿的中央孔,外观类似一支削尖的铅笔(图1)。头端圆锥体底面直径5 mm、高度10 mm、锥度为2;头端设计有6条刀刃,相互之间呈60°夹角;圆柱体外径4.0 mm、中央孔直径2.8 mm。

图1 深筋膜切开器外观图和截面图 1圆锥体头端 2头端刀刃 3圆柱体体部 4中央孔 Do圆柱体外径 Di中央孔直径
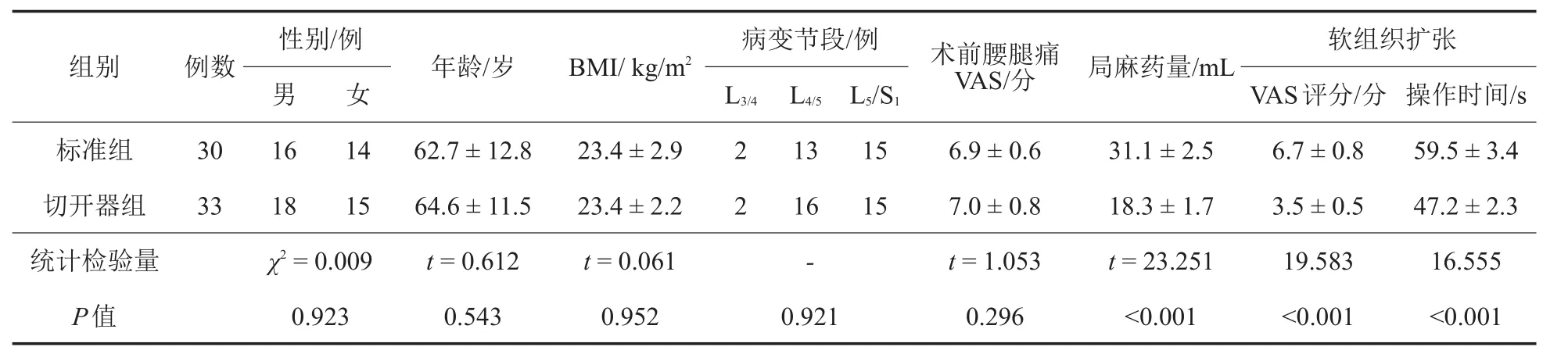
表1 两组PELD手术患者观察指标比较
1.3 手术方法
手术由同一组医师完成。按照PELD手术方法,以质量浓度为1%的利多卡因进行局部麻醉,然后完成穿刺、导丝和Ⅰ级导杆(外径2.5 mm)置入等操作。根据患者分组情况进行软组织扩张。
标准组:沿Ⅰ级导杆插入外径为4.0 mm的Ⅰ级导管,顺时针旋转推进至椎间孔外口,以撑开肌肉等软组织;采取同样手法拧入Ⅱ级和Ⅲ级导管,进一步扩大软组织通道,最后边旋转边拧入外径7.5 mm的工作套管。
切开器组:沿Ⅰ级导杆(外径2.5 mm)插入头端有6条放射状刃口、内径2.8 mm、外径4.0 mm的深筋膜切开器,切开器头端抵达深筋膜时可感觉到插入阻力增加,稍微用力推进切开器即可在深筋膜上形成一个以Ⅰ级导杆为中心、呈放射状分布的6条小切口(图2,3)。保留Ⅰ级导杆,撤出深筋膜切开器,继续逐级插入3级导管,沿之前的放射状小切口进一步扩大深筋膜层,完成软组织扩张(图4)。后续操作和标准组相同。
此后两组按照PELD手术步骤,进行椎间孔成形、工作套管置入、腰椎间盘突出物摘除、神经减压等操作。
1.4 观察指标
①软组织扩张疼痛VAS评分:在患者完成软组织扩张后的相对平静期,由对软组织扩张方法不知情的一位研究者进入手术间,协助患者对之前软组织扩张带来的疼痛不适进行VAS评估。②软组织扩张操作时间:标准组为Ⅰ级导管接触皮肤到完成工作套管插入的操作时间;切开器组为深筋膜切开器接触皮肤到完成工作套管插入的操作时间。③记录术中、术后并发症;术后1个月门诊随访,观察伤口处是否发生肌疝。
1.5 统计学分析
采用SPSS 22.0统计软件进行数据分析,计量资料以均数±标准差(±s)表示,两组比较采用两独立样本t检验,计数资料以例表示,比较采用卡方检验或Fisher确切概率法。P<0.05为差异有统计学意义。
2 结果
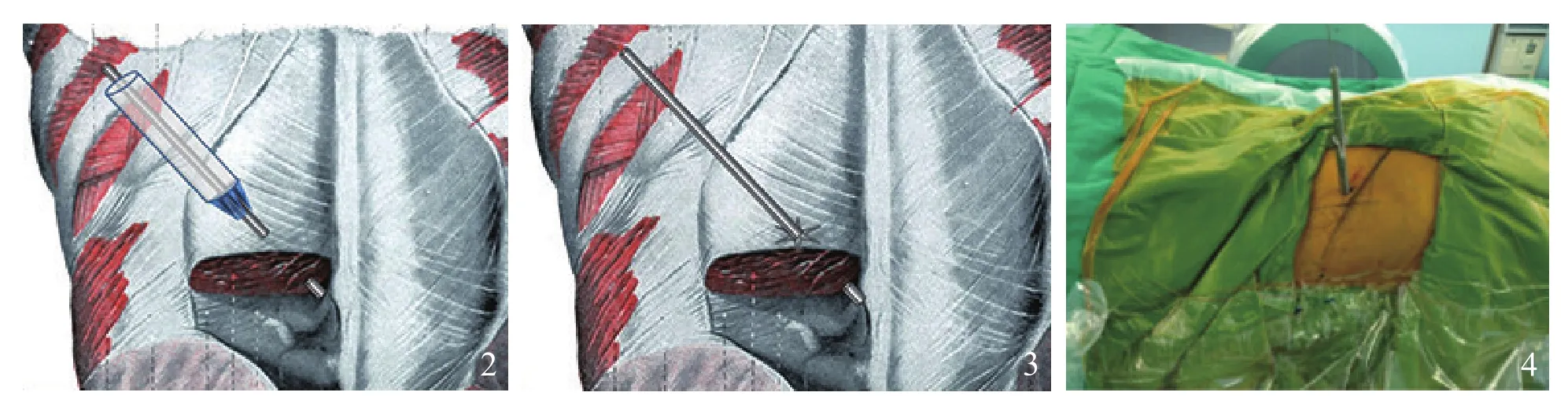
图2 深筋膜切开器沿直径2.5 mm导杆插入软组织深部示意图 图3深筋膜切开后形成的6条放射状切口 图4椎间孔镜术中照片
如表1所示,标准组患者软组织扩张疼痛VAS评分高于切开器组,操作时间长于切开器组,两组比较,差异有统计学意义(P<0.05)。术中未发生神经根损伤或硬膜囊撕裂,术后无一例出现穿刺处血肿、手术切口感染、椎间隙感染并发症。术后1个月门诊复查时检查手术切口,两组患者无一例发生肌疝。
3 讨论
3.1 软组织扩张术中的患者体验
随着脊柱微创外科的快速发展,近年来PELD逐渐成为治疗腰椎间盘突出症等腰椎退行性疾病的常用术式[2-4]。遵循腰椎间孔镜手术的操作步骤,在完成局部麻醉、椎间盘穿刺、椎间盘造影、穿刺针插入导丝等操作后,需沿导丝插入Ⅰ级导杆,然后沿导杆依次插入Ⅰ级~Ⅲ级导管,逐步扩大软组织通道。Ⅰ级导杆较细,外径为2.5 mm,头端设计成锥形,易于穿过致密的深筋膜组织[5-6];而Ⅰ级导管外径为4.0 mm,较Ⅰ级导杆明显增粗,导管壁又较薄,其头端无法实现锥度较小、相对较尖的锥形设计,故在Ⅰ级导管沿导杆进行软组织扩张时,即使采用边旋转边推进的方法,也会在致密的深筋膜部位遇到明显阻挡,需用较大的力量才能突破并扩张深筋膜[7-8]。由于是局部麻醉,患者往往会有明显的软组织牵拉感觉,并产生较为剧烈的疼痛[9]。研究表明,在椎间孔镜手术中,绝大多数患者不适感最强烈、疼痛反应最为明显的就是这一步骤,部分患者甚至因此对椎间孔镜手术产生恐惧,不能很好地配合后续操作,影响手术的顺利完成[10-11]。因此,如何减轻软组织扩张的强烈疼痛感,对于改善患者手术体验、提高手术效果具有重要意义。但目前未有针对椎间孔镜软组织扩张方法、技术和器械的进一步相关研究。
3.2 深筋膜切开器的作用原理
笔者设计一款沿Ⅰ级导杆在深筋膜上制作放射状切口的深筋膜切开器,其目的在于令其后Ⅰ级~Ⅲ级导管插入扩张软组织的操作变得简单易行。研究结果显示,未采用深筋膜切开器的标准组其软组织扩张疼痛VAS评分高于切开器组。原因就在于标准组借助导管在深筋膜上造口,是钝性损伤,对深筋膜的推挤牵张力量大;而切开器组利用切开器先在深筋膜切出放射状小切口,这一人工干预方法均匀分担了后期扩张导管的扩张应力,因此在之后插入逐步增粗的各级导管时,软组织可轻易扩张至各级导管和工作套管的大小,拧入导管所需的力量也较小,患者局部疼痛感和深筋膜钝性损伤及牵拉痛均明显减轻。
3.3 深筋膜切开器的应用效果
虽然切开器组额外增加了插入深筋膜切开器这一步骤,但由于患者疼痛反应减轻,每一操作步骤均较为快捷;由于软组织扩张操作简单易行,没有多余的阻滞,亦未受到致密深筋膜的阻挡,因此旋转和推进均较为顺畅。而标准组在患者疼痛反应剧烈时,术者往往会减慢或暂停导管的旋转拧入,因此操作时间较切开器组更长。
肌疝是骨科术后常见并发症,主要是由于深筋膜完整性丧失,其所包裹的肌肉失去解剖学和力学的附着点与约束,收缩时向力量最薄弱且富有弹性的皮肤区域隆起[12-13]。切开器组在拔出工作套管后,切开器切开深筋膜所形成的六瓣状切口可自然闭合,不会导致深筋膜裂口和肌疝,术后随访结果也证实了这一点。
总之,本研究对深筋膜切开器的临床应用进行初步探讨,同时与标准方法进行前瞻性比较,结果表明,使用深筋膜切开器放射状切开坚韧致密的腰背筋膜后再行软组织扩张操作,能够减轻软组织扩张时患者的疼痛感,缩短操作时间,术后深筋膜裂口能够顺利愈合,不会发生肌疝,方法安全有效。
