红土镍矿黄铵铁矾法除铁及杂质铁的高值化利用
2020-08-22常龙娇翟玉春
梁 栋 常龙娇 翟玉春
(1.渤海大学 新能源学院,辽宁 锦州 121013;2.东北大学 冶金学院,沈阳110819)
随着高品位硫化镍矿的日渐枯竭,高效开发红土镍矿尤为急切,而目前国内外对红土镍矿主要通过矿热炉火法冶炼和湿法冶金,仅限于提取镍,剩余部分则作为废渣排放,占地面积大,且矿中很多重金属离子还对土壤造成了极大污染[1-6]。由于红土镍矿中杂质铁元素含量较高,为其他元素的分离提取带来难度。为了寻找除去铁离子的有效方法,研究黄铵铁矾法除铁来改善沉淀和过滤性能是十分必要的。此外,随着智能手机和笔记本电脑等移动互联网设备的普及,锂离子电池面临着更高的性能和成本要求[7],降低电极材料的成本势在必行。
研究采用硫酸铵焙烧—黄铵铁矾沉铁—矾水解工艺处理红土镍矿,实现了杂质Fe元素的分离,同时获得制备电极材料LiFePO4/C的原料Fe2O3,较好地回收了杂质铁,可为商业化考虑使用黄铵铁矾除铁提供更经济实惠的思路,也是将来工业应用的一大优势[8-11]。使用含碳材料在较高温度下产生的还原性气体将Fe3+还原为Fe2+,锂离子与磷酸根离子相结合形成磷酸铁锂材料,该工艺可制备高附加值材料,既环保又耗能较低,可作为综合利用红土镍矿的新工艺技术。
1 实验
1.1 红土镍矿的化学成分
表1为红土镍矿的主要化学成分分析结果。由表1可知,红土镍矿中的镍含量为2.38%,钴含量为0.06%,铁的含量相对很高,高达23.41%,说明此矿是褐铁型红土镍矿[12]。

表1 原矿主要化学成分Table 1 Main chemical composition of raw ore /%
1.2 红土镍矿的主要物相
低品位红土镍矿的XRD图谱如图1所示。从图1中可以看出,红土镍矿的物相主要为硅酸盐和镁酸盐,氧化铁以赤铁矿(Fe2O3)的形式存在。
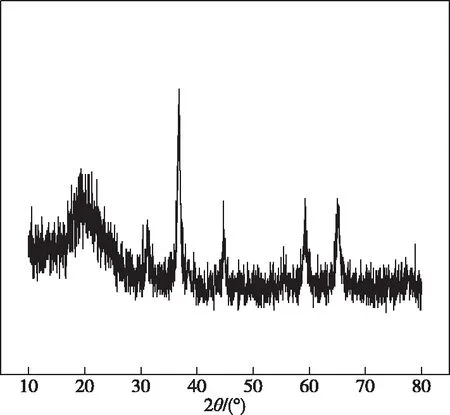
图1 红土镍矿的XRD图谱Fig.1 XRD pattern of laterite nickel ore
1.3 红土镍矿的微观形貌
图2为低品位红土镍矿磨细后的SEM图片。从图2可以清楚地看出,低品位红土镍矿形状不规则、表面毛糙、结构疏松、颗粒大小不均匀。

图2 红土镍矿的SEM图像Fig.2 SEM images of laterite nickel ore
1.4 黄铵铁矾沉铁原理
黄铵铁矾是一种纯黄色或者是浅黄色结晶体,六方体是其晶系特点,其结构是明矾石型,通常存在形式以土状、粒状、壳状以及核状和致密块状聚集体。黄铵铁矾的分子通式可写成为NH4Fe(SO4)2(OH)6[13-14]。
黄铵铁矾法沉铁法[15-21]通常是在高温、常压和有NH4+离子存在的条件下将溶液中的Fe3+从弱酸性的硫酸盐溶液中以晶体形式沉淀。黄铵铁矾结构非常稳定、难溶于水、易沉降,且过滤性能好。
在黄铵铁矾法沉铁这个反应过程中,操作相对比较复杂,铁在水解时的主要反应见式(1)至(4)。
4Fe(OH)SO4+4H2O=2Fe2(OH)4SO4+
2H2SO4
(1)
3Fe2(SO4)3+6H2O=6Fe(OH)SO4+3H2SO4
(2)
2Fe(OH)SO4+2Fe2(OH)4SO4+2NH4OH=(NH4)2Fe6(SO4)4(OH)12
(3)
向溶液中加入适量铵盐,上述几个反应依然成立并且能够生成水解产物黄铵铁矾。
3Fe2(SO4)3+10H2O+2NH4OH=
(NH4)2Fe6(SO4)4(OH)12+5H2SO4
(4)
1.5 实验方法
1.5.1 黄铵铁矾制备
准确称取一定量的红土镍矿与硫酸铵,研磨均匀后放入坩埚并将坩埚置于马弗炉,在500 ℃下恒温焙烧2 h,冷却至室温。熟化物经研磨后放入烧杯并加去离子水搅拌均匀,放入适当的双氧水,以400 r/min的搅拌转速持续搅拌4 h。期间用碳酸氢钠溶液(浓度为0.1 g/L)调节溶液pH值至2.5,得到黄铵铁矾。然后将黄铵铁矾与去离子水按照液固比3∶1的比例放入水浴锅中搅拌升温至90 ℃后,缓慢加入碳酸氢钠溶液(浓度为0.1 g/L)调节其pH值至12,反应10 min后过滤、洗涤、干燥,得到片状Fe2O3。
采用邻菲罗啉吸光光度法测定铵铁矾铁离子浓度。
1.5.2 磷酸铁锂制备
向Fe2O3中加入Li2CO3、NH4H2PO4及蔗糖,按照摩尔质量比1∶1.2∶1.2∶0.2放入50 mL酒精中分散搅拌均匀,然后将混合物放入管式炉中于氮气保护下进行煅烧,煅烧温度为750 ℃,时间10 h,之后冷却,得到LiFePO4/C粉末。
1.5.3 电化学性能测试
将质量比为8∶1∶1的活性材料、乙炔黑和粘结剂(聚偏氟乙烯)溶解在1-甲基-2-吡咯烷酮中混合并搅拌4 h,将得到的浆体用专用刮刀涂在铝箔上,120 ℃烘干后冲压成直径为13 mm的圆形极片。在压片机上用6 MPa的压力压片后将其转移至氩气气氛的手套箱内,以其为正极,金属锂为负极,1 mol/L LiPF6溶解于碳酸乙烯酯(Ethylene Carbonate,EC)/碳酸二甲酯(Dimethyl Carbonate,DMC)(体积比为1∶1∶1)的混合物为电解液,正、负极间采用Celgard2400隔膜,加不锈钢垫片和弹簧片组装扣式电池并在Land系统下进行充放电测试。测试采用恒流充放电式,充放电倍率分别为0.1 C、0.5 C、1 C、2 C、5 C。
2 结果与讨论
2.1 温度对除铁率的影响
反应时间 4 h、终点pH值2.5、搅拌速度400 r/min时,反应温度对除铁率的影响如图3所示。
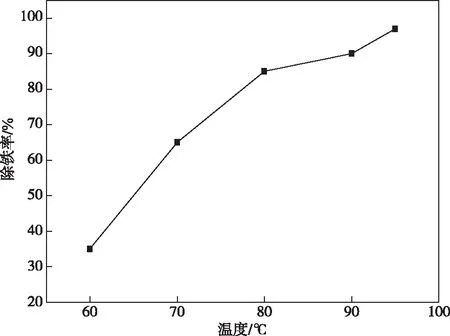
图3 除铁率与反应温度的关系Fig.3 Relationship between iron removal rate and reaction temperature
从图3可以看出,反应温度对除铁率的影响较大,随着温度的升高,除铁率不断增加。在60~80 ℃增加明显,80 ℃以上升幅变小,当温度达到95 ℃时,除铁率可达98.35%。由于温度比较低时,成矾速度比较缓慢而且很难过滤[22],因此推荐95 ℃为最佳温度。
2.2 反应时间对除铁率的影响
在反应温度95 ℃、终点pH值2.5、搅拌速度400 r/min条件下,反应时间与除铁率之间关系如图4所示。
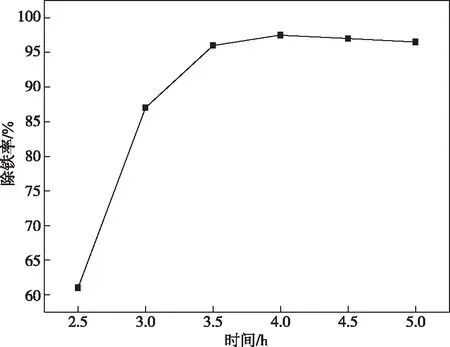
图4 除铁率与时间的关系Fig.4 Relationship between iron removal rate and time
如图4可以看出,反应时间对整个过程黄铵铁矾除铁率影响十分显著,随着反应时间的延长,除铁率逐渐升高,反应时间在2.5~4.0 h时,除铁率升高幅度相比于其他时间段更加明显,反应4 h以后基本趋于平衡。由于4 h时除铁率即可达到98.35%,因此选择反应时间为4 h。
2.3 终点pH值对除铁率的影响
在反应温度95 ℃、反应时间4 h、搅拌速度为400 r/min条件下,考察黄铵铁矾制备终点pH值对除铁率的影响,结果如图5所示。
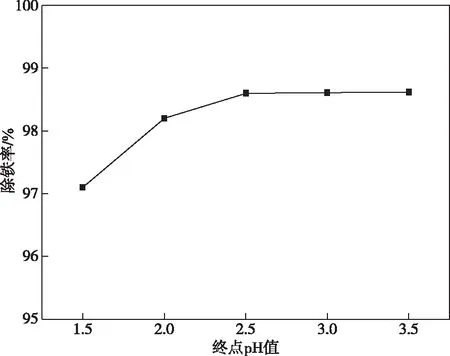
图5 除铁率与终点pH值的关系Fig.5 Relationship between iron removal rate and end point pH values
从图5可以看出,反应终点pH值对黄铵铁矾除铁率影响较大,随着终点pH值的增加,黄铵铁矾的除铁率逐渐上升,当pH值达到2.5以后再提高pH值,除铁率变化不明显,pH值为2.5时除铁率最大,为98.35%,因此最佳反应终点pH值为2.5。需要注意的是,在实验中,需要缓慢添加pH值调节剂,因为如果结晶太快,颗粒太细,或局部溶液pH值太高,会导致Fe(OH)3胶体生成[23]。
2.4 搅拌速度对除铁率的影响
在反应温度95 ℃、终点pH值2.5、反应时间4 h时,考察黄铵铁矾搅拌速度对除铁率的影响,结果如图6所示。
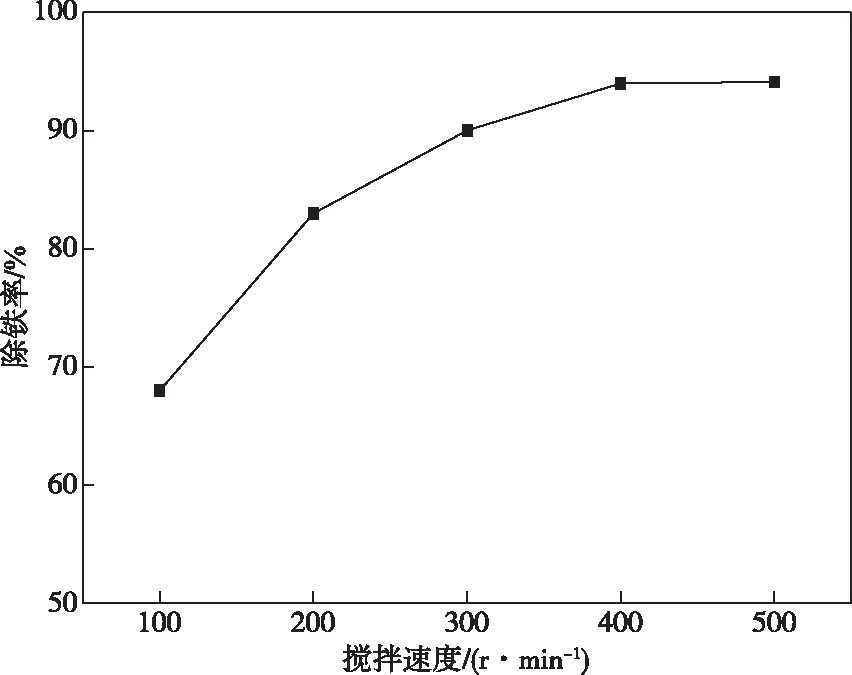
图6 除铁率与搅拌速度的关系Fig.6 Relationship between the iron removal rate and stirring speed
从图6可以看出,搅拌速度对黄铵铁矾除铁率影响显著,随着搅拌速度的增加,铁的提取率逐渐增大,从100 r/min到400 r/min时,除铁率有大幅度的上升,但当搅拌速度大于400 r/min之后,铁的提取率基本达到平衡。由于搅拌速度为400 r/min时除铁率即可达到98.35%,因此,反应最佳转速选择为400 r/min。
2.5 搅拌速度对黄铵铁矾形貌的影响
在反应温度95 ℃、水解实践4 h、终点pH值为2.5条件下,考察搅拌速度对黄铵铁矾形貌的影响,结果如图7所示。
从图7可以看出,搅拌速度为100~300 r/min时所得黄铵铁矾的形貌不规则,且颗粒表面粗糙、结构松散、颗粒大小不均;搅拌速度为400 r/min时所得黄铵铁矾颗粒主要呈片状、颗粒均匀、表面光滑、分散性好;继续增加搅拌速度至500 r/min时所得黄铵铁矾颗粒虽然仍呈片状,但颗粒不均。后续实验发现,用搅拌速度为400 r/min时所得黄铵铁矾制备的Fe2O3为原料再制备的磷酸铁锂正极材料电化学性能良好。这是因为材料本身规则的片状结构和良好的分散性,有利于提高材料的电导率和锂离子扩散速率,从而使材料的倍率性能有大幅度提高[24]。因此,选择最佳搅拌速度400 r/min,并对该搅拌速度下所得黄铵铁矾进行了进一步的XRD分析,结果如图8所示。从图8可以看出,400 r/min时所得黄铵铁矾的X射线衍射峰峰形尖锐,表明黄铵铁矾结晶良好。

图7 不同转速时所得黄铵铁矾的SEM图像Fig.7 SEM images of ammonium jarosite obtained at different rotating speeds
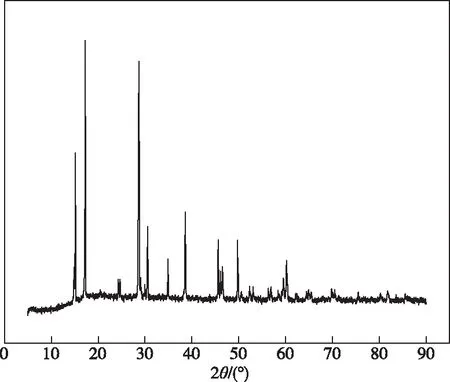
图8 搅拌速度为400 r/min时所得黄铵铁矾的XRD图谱Fig.8 XRD pattern of ammonium jarosite obtained at 400 r/min rotating speeds
表2为黄铵铁矾的化学成分分析结果。由表2可知,黄铵铁矾的主要成分是三氧化二铁,含量高达56.85%,含硫、铝和钛等杂质。
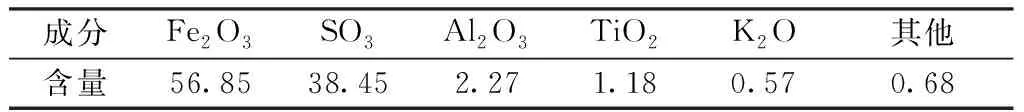
表2 黄铵铁矾的主要化学成分Table 2 Main chemical composition of ammonium jarosite /%
3 LiFePO4倍率性能分析
在研究实验所得片状黄铵铁矾为原料所制LiFePO4材料的电化学性能时同时选择商业颗粒状磷酸铁锂材料作为比对。图9为片状与颗粒状实验样品在室温0.1 C、0.5 C、1 C、2 C、5 C倍率下的放电比容量图。
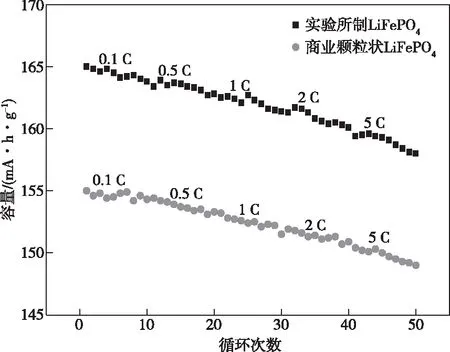
图9 不同倍率下的放电比容量图Fig.9 Discharge specific capacity diagram at different times
从图9可以看出,实验所得片状LiFePO4材料在0.1 C、0.5 C、1 C、2 C、5 C倍率下循环充放电,经过10周循环,容量保持率分别为99.83%、98.28%、97.26%、96.73%、95.82%,平均放电比容量分别为164.12、163.34、162.11、160.86、158.96 mA·h/g。商业颗粒状LiFePO4材料在0.1 C、0.5 C、1 C、2 C、5 C倍率下循环充放电,经过10周循环,容量保持率分别为95.19%、94.26%、93.89%、92.24%、90.87%,平均放电比容量分别为154.23、153.72、152.43、151.32、149.77 mA·h/g。二者相比,本文实验所得磷酸铁锂材料在不同倍率下的首次放电比容量和放电比容量均高于商业颗粒状磷酸铁锂材料的,而且不同倍率下循环10周的容量保持率也是本文实验所得磷酸铁锂材料的较好。
4 结论
1)采用红土镍矿为原料,经过硫酸铵焙烧、焙烧熟料水浸、浸出液黄铵铁矾法除铁可得到结晶良好、颗粒均匀的片状黄铵铁矾。然后以所制黄铵铁矾为原料制备磷酸铁锂正极材料的原料Fe2O3,再用所制的Fe2O3制备锂电池用LiFePO4/C正极材料,可得到放电比容量较大且稳定的正极材料LiFePO4/C。
2)黄铵铁矾法除铁过程反应温度、反应时间、反应终点pH值以及搅拌速度对除铁率均有较大影响。最佳除铁实验条件为反应时间4 h、反应温度95 ℃、终点pH值2.5、搅拌速度400 r/min,该条件下除铁率可达到98.35%,所得黄铵铁矾以片状存在,颗粒均匀且表面光滑,有利于成为磷酸铁锂的铁源,可以改善锂离子迁移路线,提高电池的电化学性能。
3)与商业颗粒状磷酸铁锂为原料所制LiFePO4/C电极材料的电化学性能相比,采用硫酸铵焙烧—水浸—黄铵铁矾法除铁所得片状黄铵铁矾为原料制备的片状磷酸铁锂材料在0.1 C倍率下的首次比容量和其他不同倍率下的平均放电比容量均高于颗粒状的磷酸铁锂材料,具有更好的电化学性能。
