孕14周高效抗逆转录病毒疗法母婴阻断HIV感染疗效观察
2020-08-17杨冬梅吴亚楠刘怡蓝
杨冬梅 吴亚楠 刘怡蓝
青岛市市立医院(266011)
人类免疫缺陷病毒(HIV)可大量破坏人体CD4+T淋巴细胞,令免疫功能逐渐丧失,导致易感各种疾病点[1]。HIV母婴传播是导致儿童感染的重要途径。高效抗逆转录病毒疗法(HARRT)是艾滋病主要治疗手段,且随着多种新型抗HIV药物推出,该方案得到较多优化,且在HIV感染的母婴阻断效果获得一定成效[2-3]。既往研究中,通常在孕28周行母婴阻断,但近年有报道认为,HIV感染孕妇在妊娠期任何阶段均推荐使用抗病毒治疗[4]。因此,本研究分析孕早期应用HARRT对HIV感染孕妇母婴阻断疗效。
1 资料与方法
1.1 一般资料
选择2014年2月-2017年8月在本院接受治疗的HIV感染孕妇作为研究对象。纳入标准:①经HIV核酸实验阳性,有中度以上细胞免疫缺陷,表现为CD4+T淋巴细胞大量衰竭,外周血淋巴细胞明显降低等[5];②年龄18~45岁;③婴儿出生后均行人工喂养;④签署研究知情同意书。排除标准:①孕期有严重妊娠合并症;②有酗酒史、药物成瘾史;③纳入研究前已接受过相关治疗;④未按规定服药,中途退出研究。研究已通过本院伦理委员会批准实施。
1.2 治疗方法
通过治疗时间不同分为观察组和对照组。两组HARRT方案均为齐多夫定(浙江海正药业股份有限公司,0.1g)0.3g,2次/d,;拉米夫定(福建广生堂药业股份有限公司,0.1g)0.3g,1次/d;洛匹那韦利托那韦片(AbbVie Ltd,200mg/50mg)250mg,2次/d。观察组于孕14周时用药,对照组于孕28周时用药,两组均持续用药至胎儿分娩后6周。所有婴儿出生后均使用人工喂养方式,出生后6h给予韦拉平口服混悬液(美国Boehringer Ingelheim Pharmaceuticals Inc,240ml:2.4g)单剂量口服,剂量2mg/kg,最高不超过6mg,并给予齐多夫定口服溶液(葛兰素史克制药,100ml:1g)4mg/kg,2次/d,连续用药1周。
1.3 观察指标
①CD4+T淋巴细胞,分别于治疗前(T0)、预产期前1个月(T1)、产后3个月(T2)采集两组空腹静脉血,采用Epics XL-MCL型流式细胞仪(美国Beckman Coulter公司)检测;并记录T1、T2时点CD4+T淋巴细胞较T0时点升高程度>30%的患者;②HIV病毒载量,分别于T0、T1、T2,使用核酸全自动提取仪(COBAS Ampliperp )实时荧光定量逆转录酶法检测HIV病毒载量,并记录各时点HIV病毒载量<50拷贝数/ml的患者[5];③记录分娩情况;④分娩后均进行婴儿随访,于产后6周、3个月、18月时行HIV核酸实验检查,记录HIV阳性例数。
1.4 统计学分析
2 结果
2.1 两组一般临床资料
共纳入60例,每组30例,两组一般资料比较无差异(P>0.05),见表1。
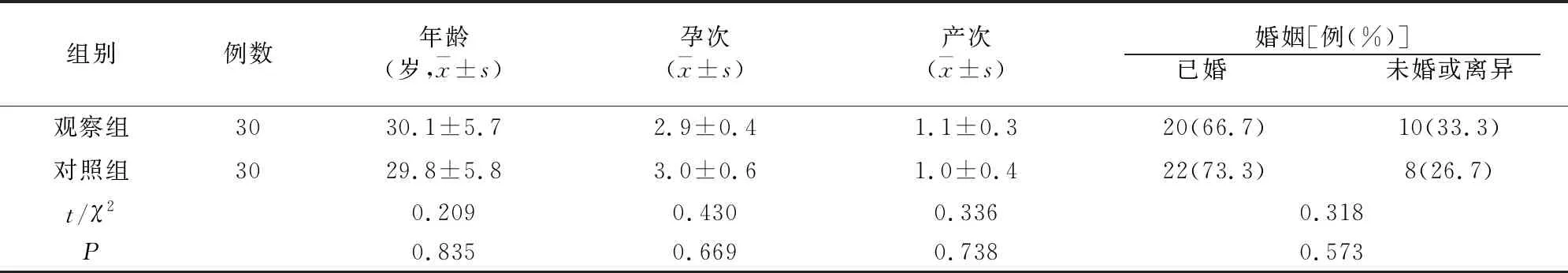
表1 两组一般资料比较
2.2 两组不同时期CD4+T淋巴细胞比较
治疗后CD4+T淋巴细胞表达两组均逐渐升高,观察组升高幅度高于对照组,且不同时间点两组比较有差异(P<0.05),见表2。

表2 两组不同时间点CD4+T淋巴细胞比较
2.3 两组CD4+T淋巴细胞升高程度比较
较T0时CD4+T淋巴细胞升高程度>30%的患者,观察组在T1(20例,66.7%)、T2(25例,83.3%)均高于对照组(12例,40.0%)(18例,60.0%)(P<0.05)。
2.4 两组HIV病毒载量比较
T1、T2时点HIV病毒载量<50拷贝数/ml的患者两组比较无差异(P>0.05),见表3。

表3 两组不同时点HIV病毒载量<50拷贝数/ml患者比例[例(%)]
2.5 两组分娩情况比较
所有产妇均获得顺利分娩,新生儿均存活,无外观畸形;在早产(分娩孕周<37周)原因中,观察组1例为胎膜早破,对照组1例为胎膜早破、1例为双胎,两组剖宫产、早产、低体重儿、新生儿轻度窒息发生比例未见差异(P>0.05),见表4。

表4 两组分娩情况比较[例(%)]
2.6 两组母婴阻断效果比较
随访显示,观察组婴儿HIV阳性0例(0.0%),对照组有1例(3.3%),两组婴儿HIV阳性率比较未见差异(χ2=1.017,P=0.313)。
3 讨论
截止2015年6月,全球获得存活的HIV感染病例仅有3700万[6]。艾滋病母婴传播主要指病原体通过母体宫内、产道、生殖细胞、母乳喂养等途径传播给后代,积极的抑制病毒复制在减少HIV母婴传播中具有重要意义。相关数据显示,尽早开展抗病毒治疗,可将母乳喂养的HIV垂直传播率由35%降低至5%,而针对人工喂养的婴儿,可由25%降低至2%[7]。
自我国2003年开始实施HIV母婴阻断治疗方案以来,已经历了从单药至双药再至三药的联合变化,三药联合不仅可提高阻断效果,还可避免单药或双药阻断期间病毒变异所致的药物耐受,疗效更好[8-9]。HARRT是一种联合3种或4种以上抗逆转病毒药物的治疗方案,在临床治疗中,通常是选择两种核苷类药物+蛋白酶抑制剂,其中应用较多的药物方案为齐多夫定+拉米夫定+洛匹那韦利托那韦片(或奈韦拉平),疗效已被较多研究证实[10-11]。在母婴阻断时间上,既往多在孕28周时实施。但有研究显示,孕14周内开始HARRT治疗可将HIV感染传播率降低至1%以上,而在孕14~36周治疗为4%[12-13]。但也有学者指出,孕13周前是胎儿器官形成的重要阶段,在此阶段开始用药易诱发胎儿畸形,建议从孕14周开始HARRT治疗[14]。
本研究结果显示,孕14周接受HARRT治疗的患者在CD4+T淋巴细胞改善程度上更优,分析认为:孕28周属孕晚期,在此阶段用药仅是短时间内改善免疫功能;而孕14周应用HARRT可更好的帮助患者重建免疫功能,进一步改善CD4+T淋巴细胞。Braga LP[15]等研究显示,无论选择何种抗病毒药物和分娩方式,若孕妇HIV病毒载量<50拷贝数/ml,则母婴传播风险可降低至0.09%。而本研究结果,两组T1时点HIV病毒载量<50拷贝数/ml的患者比例与T2时点未见差异,显示无论在孕14周还是孕28周开始接受HARRT治疗,预产期前1个月时患者均可获得较好的病毒阻断效果。但随访发现,孕14周开始治疗者其HIV母婴阻断率达100%,显示早期接受HARRT可能会取得更明显疗效。两组患者分娩结局上,均无畸形胎儿,且剖宫产、早产、低体重儿、新生儿轻度窒息发生率也未见差异,显示出孕14周接受HARRT治疗,并未增加分娩风险和新生儿不良结局,安全性好。
但需注意的是,洛匹那韦利托那韦片既往多用于一线药物(奈韦拉平)治疗失败的患者,价格较高,临床应用时应合理考虑患者经济情况选择用药。本研究治疗前两组患者CD4+T淋巴细胞表达量相似,在今后临床上选择HARRT抗病毒治疗中,需进一步考虑不同患者的治疗方案。虽然本研究中显示早期应用HARRT可获得更好的疗效,但在我国艾滋病预防工作中,较多地区对疾病认知薄弱,部分患者在临近分娩时才检测出HIV感染,此时仅能在产时进行母婴阻断。因此在临床工作中,需加强艾滋病科普宣传工作,在妊娠早期、定期筛查HIV,加强婚检、孕期保健等服务质量,对艾滋病产妇应早期给予规范化治疗,婴儿出生后尽量选择人工喂养,早期开展核酸实验并定期随访和管理。由于本研究观察例数有限,后期有待更多的样本来支持研究结论。
综上所述,孕14周应用HARRT可更好的促进HIV感染的孕妇免疫功能重建,临床上需加强孕期检查,尽早帮助患者接受治疗。
