纳米二氧化硅粒径尺寸调控及其对表面化学修饰的影响研究
2020-08-12徐本梁严顺洪肖立鲜
杨 威,徐本梁,严顺洪,肖立鲜
(十九冶成都建设有限公司,成都 610073)
0 引 言
纳米SiO2因其具有大的比表面积、力学强度、极高的稳定性和耐老化性而被广泛应用于树脂基杂化材料的改性,塑料和橡胶中的添加剂以及用于改性粘接剂[1-4]。气相法制备的粉末状纳米SiO2已经工业化,但无法控制粒子尺寸的单分散性和形貌。溶胶-凝胶法是通过硅酸酯(如TEOS)的水解缩合反应制备纳米SiO2,已成为制备单分散纳米SiO2的主要方法,采用硅氧烷前驱体水解的方法,通过调整反应温度、组成和pH值,可以获得不同粒径的纳米SiO2。为拓展纳米SiO2应用领域和功能,其表面常需要进行化学改性。在SiO2的表面改性材料中,有机硅氧烷被广泛用于纳米SiO2的表面改性[5-6]。大量的研究结果表明,改性后的纳米SiO2表面能够接枝有机分子链段,增加了其与聚合物之间的相容性并能够有效提高SiO2的分散性。尽管已有大量研究提出了关于纳米SiO2的表面修饰方法,但纳米SiO2表面改性的影响因素,尤其是纳米粒子尺寸及其表面的化学状态对化学修饰的影响机制,仍未被研究者关注和报道。
为了深入研究纳米SiO2粒径尺寸与表面特性的关系以及表面特性对化学修饰的影响,本文通过制备不同粒径的纳米SiO2,通过硅氧烷MPS改性,研究SiO2表面羟基的结合状态与粒子尺寸之间的关系及其对化学改性的影响并提出了反应机理。
1 实 验
1.1 原料及仪器
实验原料为:无水乙醇(99.5%,北京化工厂),正硅酸乙酯(TEOS,广州西陇化工有限公司),去离子水,氨水(25%~28%,北京化工厂),甲基丙烯酰氧丙基三甲氧基硅烷(MPS,南京向前化工有限公司)。
实验仪器为:FESEM JSM-7500F场发射扫描电子显微镜(JEOL,日本),康塔气体吸附系统Quantachrome Autosorb Automated Gas Sorption System(美国),红外光谱仪NEXUS-470(Nicolet,美国)。
1.2 实验过程
1.2.1 纳米SiO2的制备
将无水乙醇、去离子水和氨水加入带有温度计,冷凝管和磁力搅拌器的250 mL三口瓶中,然后将TEOS的乙醇溶液滴加到三口瓶中,并于15 min内滴完,搅拌反应24 h,得到不同粒径的纳米SiO2分散液[7]。
图1是TEOS水解制备纳米SiO2的过程,采用TEOS制备纳米SiO2粒子的过程分为两个阶段:首先TEOS在碱性条件下水解生成羟基(Si(OH)4),随后羟基之间发生缩合反应,生成三维网络结构。
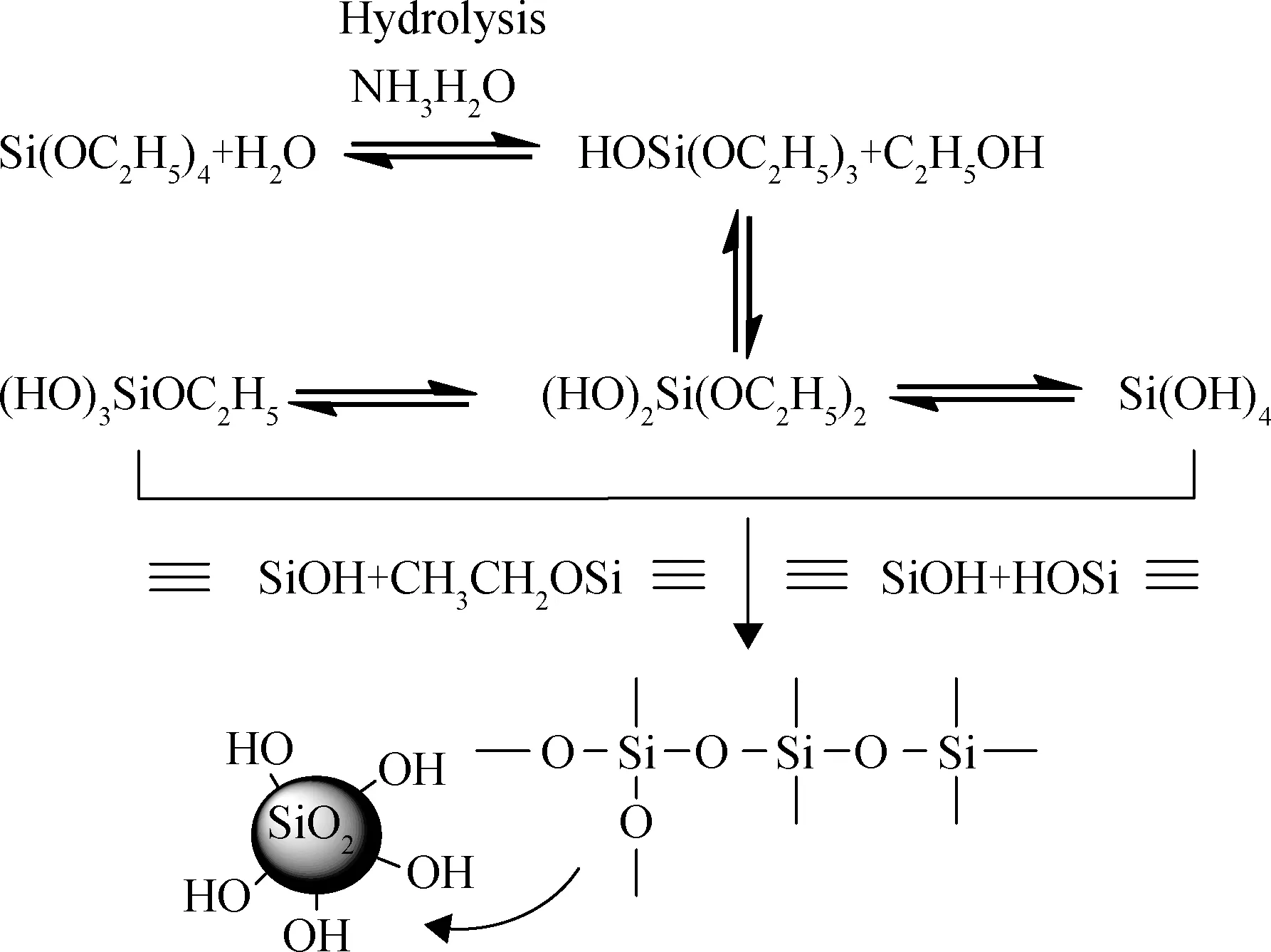
图1 TEOS在碱性条件下生成纳米SiO2机理Fig.1 Growth mechanism of nano SiO2 in alkaline condition
1.2.2 分析测试
扫描电子显微镜表征(SEM),将SiO2悬浮液离心干燥后重新分散到乙醇中,取一滴乙醇分散液于硅片表面,待溶剂挥发后对样品表面喷金(Pt),采用FESEM JSM-7500F场发射扫描电子显微镜(JEOL,日本)表征SiO2的形貌。
透射电子显微镜表征(TEM),将SiO2用乙醇分散后取一滴样品滴在铜网表面,待溶剂挥发后进行测试,使用JEM-2100型透射电子显微镜(JEOL,日本)对样品的形貌进行分析,测试过程的电子加速电压为200 kV。
比表面积测试(BET),采用康塔气体吸附系统Quantachrome Autosorb Automated Gas Sorption System(美国)测试纳米SiO2的比表面积,将干燥的纳米SiO2粉末于100 ℃中脱气16 h,通过Brunauer-Emmett-Teller(BET)法测试纳米SiO2的比表面积S(m2/g)。
傅里叶变换红外光谱分析(FT-IR),将纳米SiO2与KBr粉末共混压片制样,采用红外光谱仪NEXUS-470(Nicolet,美国)分析纳米SiO2表面特征基团,红外光谱的扫描范围500~4 000 cm-1,分辨率为6 cm-1,扫描32次。
三是积极培育内部人才市场,完善人才内部流动机制。逐步建立分区域、分板块,有形和无形市场相结合的人才市场体系,不断完善市场功能,扩大信息量,增加覆盖面,进一步疏通三支队伍之间、板块之间、企业之间的人才流动渠道,促进人才系统内部合理流动,减少人才流失。
2 结果与讨论
2.1 纳米SiO2粒径尺寸与比表面积
表1是纳米SiO2的制备条件以及颗粒比表面积,由表1可知,当反应温度为室温25 ℃,TEOS用量为3.5 g,水用量为5 mL,乙醇为50 mL,氨水2 mL时,纳米SiO2的平均粒径为330 nm。当反应温度升高到40 ℃时,纳米SiO2平均粒径为180 nm,表明升高温度会导致纳米SiO2粒径尺寸下降。
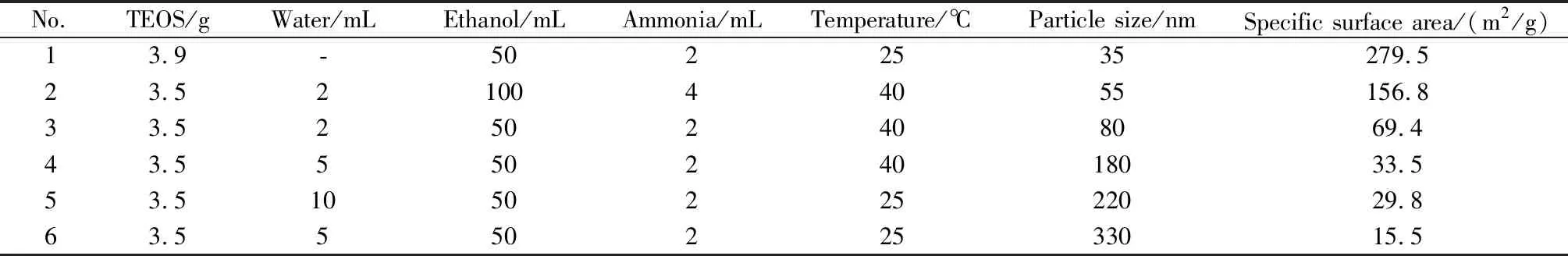
表1 不同粒径纳米SiO2的制备条件及其比表面积Table 1 Condition of preparation for nano SiO2 with various particle size and the specific surface area
在室温反应时,TEOS的水解速率和Si-OH的缩合速率较慢,颗粒容易聚集生长,有利于纳米粒子的长大。当温度升高时,TEOS的水解和Si-OH的缩合速率都明显提高,在反应体系中短时间内即产生大量颗粒,导致最终形成的SiO2粒子尺寸较小[7]。当TEOS用量3.5 g,反应温度为40 ℃,乙醇用量为50 mL,水的用量为2 mL时,纳米SiO2的尺寸为80 nm,当水的用量提高到5 mL而乙醇和氨水的用量不变时,所得SiO2的粒径尺寸增加到180 nm,表明水的用量增加,能够提高SiO2粒径尺寸。这是由于当反应体系中水量为2 mL时,TEOS的水解速率较低,水解反应受到抑制,进而限制了缩合反应的发生,因而所得SiO2粒径较小,而增加水的用量之后,提高了TEOS水解程度,促进缩合反应的进行,使SiO2粒径增长。
当TEOS用量为3.5 g,乙醇50 mL,氨水2 mL,并于室温下反应时,随着水的用量由5 mL增加到10 mL,SiO2的粒径尺寸由330 nm下降到220 nm,表明水的用量提高使得SiO2粒子尺寸下降。由于水含量的增加促进了TEOS的水解和Si-OH缩合反应,形成大量的生长中心和微小颗粒,在反应的后期没有足够的TEOS水解补充,粒子的生长幅度不大,导致纳米SiO2粒径变小。
由表1可知,随着纳米SiO2粒子尺寸由35 nm增加到330 nm,其比表面积由279.5 m2/g下降到15.5 m2/g,粒径尺寸的增加导致比表面积大幅下降。
2.2 纳米SiO2表面形貌
图2是纳米SiO2的SEM和TEM照片,由图2可知,当纳米SiO2的平均粒径由35 nm提高到220 nm时,粒子表面由比较粗糙逐渐变为形状规整的球形。如图2(a)所示,35 nm SiO2表面比较粗糙,由于反应体系中的水来源于氨水,反应体系中的水不足以促进TEOS水解,TEOS水解程度较低,导致Si-OH较少,限制了Si-OH的缩合,使得SiO2粒子的表面出现粗糙的形貌。随着水用量的增加,TEOS的水解和缩合程度提高,因此粒子表面逐渐变得平滑,得到形状规整的球形SiO2。由图2可知,反应条件的改变对SiO2粒子的单分散性影响较小,对SiO2粒径尺寸影响较大。尽管不同粒径的纳米SiO2表面微观形貌存在差别,但基本都具有粒径尺寸单分散的特点。

图2 不同粒径SiO2的SEM和TEM照片Fig.2 SEM and TEM images of nano SiO2 with different particle size
2.3 纳米SiO2的红外光谱分析
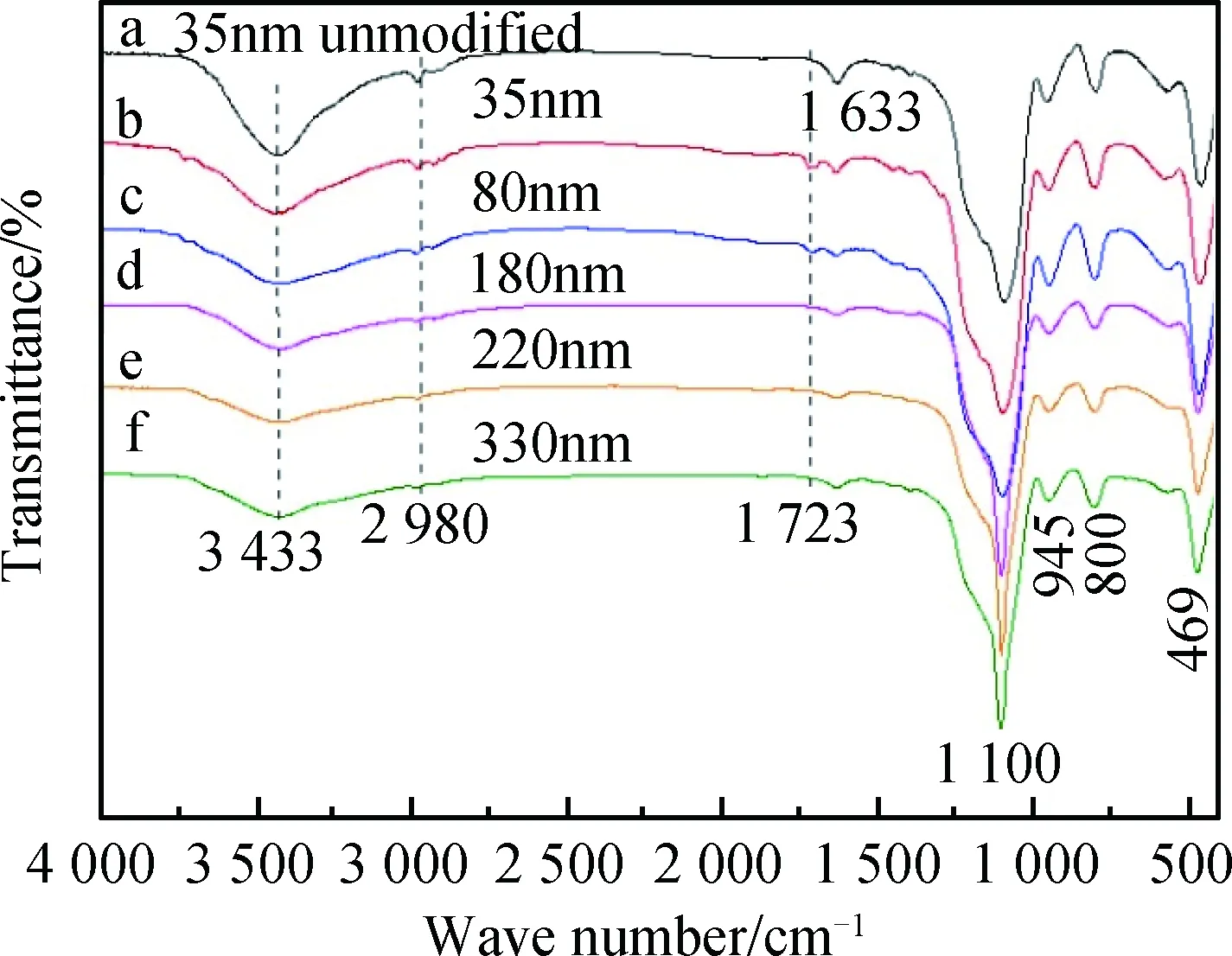
图3 SiO2改性前后的红外光谱Fig.3 FT-IR spectra for nano SiO2 before and after modification
由此可知,35 nm SiO2表面的-OH主要以孤立的状态存在,而220 nm SiO2表面的-OH主要以氢键相结合的方式存在。Kamiya等[8]认为,不同粒径的纳米SiO2表面羟基的结合状态存在明显差别,当粒径尺寸小于30 nm时,SiO2表面羟基主要以孤立羟基的形式存在,当粒径大于60 nm时,粒子表面的羟基主要以氢键的方式结合。图3(b),图3(c),图3(d)和图3(f)是不同粒径纳米SiO2经MPS改性后的红外光谱。由图3(b)可知,35 nm SiO2改性后,红外光谱在1 723 cm-1出现了C=O的吸收峰,表明MPS成功接枝到了SiO2表面。如图3(c)所示,当纳米SiO2粒径为80 nm时,改性后的粒子红外光谱也出现了C=O吸收峰,说明MPS与80 nm SiO2表面的羟基发生了反应。由图3(d)可知,当SiO2粒径尺寸大于180 nm时,经MPS改性后红外光谱中没有出现C=O的吸收峰,说明MPS没有与SiO2表面的羟基发生反应,对大粒径纳米SiO2不能发生有效的化学接枝。
Rahman等[9-10]认为,随着粒子尺寸的增长,SiO2表面的羟基数量增加,但SiO2的比表面积下降,表面Si-OH浓度下降。由此可知,当采用MPS对SiO2进行修饰改性时,能够接枝到SiO2表面的MPS取决于单位质量的SiO2粒子表面的Si-OH浓度,与35 nm SiO2相比,180 nm SiO2表面的羟基浓度下降,而且羟基之间主要以氢键结合的方式存在,孤立的羟基少于小粒径SiO2,表面化学修饰的空间位阻增大,因此MPS无法对纳米粒子进行化学修饰。
有研究结果指出,纳米SiO2表面的Si-OH主要存在两种结合形式,分别是孤立的Si-OH和以氢键结合的Si-OH[11-12]。当SiO2粒子尺寸大于60 nm时,大部分的硅羟基(Si-OH)以氢键的方式结合。当SiO2粒子尺寸小于30 nm时,其表面Si-OH主要以孤立的形式存在[13],如图4所示。
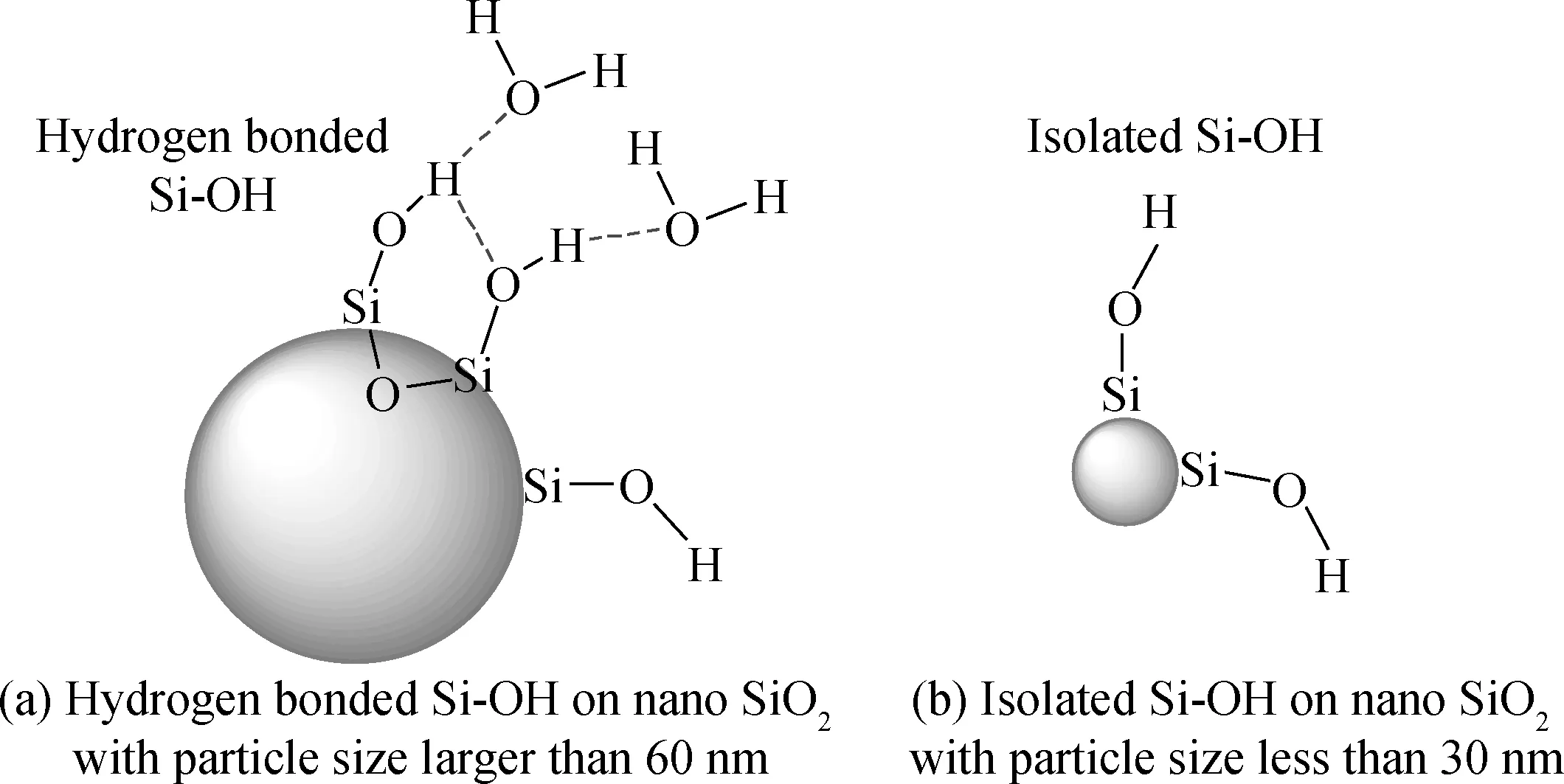
图4 不同粒径SiO2表面羟基的结合形式Fig.4 The bonded condition of Si-OH on surface of nano-silica with different particle size
根据上述分析可知,SiO2纳米粒子的尺寸决定其与MPS的反应活性,表面含有大量孤立Si-OH的小粒径纳米SiO2能与MPS发生化学接枝反应,从而得到MPS改性的SiO2纳米粒子。35 nm的SiO2表面存在大量孤立的羟基,因此容易与MPS发生反应,生成MSiO2纳米粒子。而180 nm以上的大粒径SiO2表面的羟基主要以氢键的方式结合在一起,限制了其与MPS的缩合反应,不利于粒子表面的化学修饰。
3 结 论
(1)反应温度由25 ℃升高至40 ℃时,SiO2粒径尺寸下降。当水的用量增加时,SiO2粒子尺寸先增大后减小。当体系中的水含量较低时,TEOS水解不完全,抑制了缩合反应的进行,所得SiO2粒径较小,表面粗糙。
(2)随着SiO2粒径尺寸的增大,比表面积下降,表面孤立的羟基浓度降低,小粒径纳米SiO2表面的羟基主要以孤立的形式存在,大粒径纳米SiO2表面的羟基主要以氢键的结合形式存在。
(3)对于纳米SiO2,表面孤立的羟基浓度高,有利于MPS与其发生反应,生成MPS改性的纳米SiO2,与小粒径纳米SiO2相比,大粒径纳米SiO2无法通过MPS进行化学修饰。
