利妥昔单抗联合CHOP方案治疗非霍奇金淋巴瘤的效果
2020-08-07张肇铱赵琼
张肇铱,赵琼
(河南科技大学第一附属医院 肿瘤科,河南 洛阳 471003)
非霍奇金淋巴瘤(non-hodgkin’s lymphoma,NHL)为临床常见恶性肿瘤,我国发病率较高,病变位置主要在淋巴器官,分为NK/T细胞、T细胞、B细胞3种类型,其中B细胞型占总数的70%~85%,且约95%的B细胞型NHL表达CD20[1]。现阶段,CHOP方案(泼尼松、长春新碱、多柔比星、环磷酰胺)为治疗NHL的一线方案,但长期缓解率<50%,且大量使用易损伤骨髓造血细胞,临床应用存在局限性[2]。利妥昔单抗是一种新型免疫制剂,可结合CD20抗原杀伤肿瘤细胞,目前在NHL治疗中得到广泛应用。本研究选取62例NHL患者,探讨利妥昔单抗联合CHOP方案的治疗效果。
1 资料与方法
1.1 一般资料选取2017年1月至2018年8月河南科技大学第一附属医院收治的62例NHL患者为研究对象,按随机数表法分为对照组与观察组,各31例。对照组:男20例,女11例;年龄39~77岁,平均(57.85±9.32)岁;Ann arbor分期Ⅰ~Ⅱ期8例,Ⅲ期17例,Ⅳ期6例;国际预后指数(international prognostic index,IPI)评分0~1分5例,2分11例,3分9例,4~5分6例。观察组:男19例,女12例;年龄40~77岁,平均(58.54±9.19)岁;Ann arbor分期Ⅰ~Ⅱ期7例,Ⅲ期18例,Ⅳ期6例;IPI评分0~1分6例,2分12例,3分8例,4~5分5例。两组年龄、性别、Ann arbor分期、IPI评分比较,差异无统计学意义(均P>0.05),具有可比性。本研究经河南科技大学第一附属医院医学伦理委员会审核通过。
1.2 选取标准(1)纳入标准:①签署知情同意书;②经病理诊断证实为NHL;③首次入院治疗。(2)排除标准:①伴有肝肾功能异常、化疗禁忌证、其他恶性肿瘤;②预计生存期<3个月;③卡氏评分<60分;④妊娠期或哺乳期妇女。
1.3 治疗方法对照组接受CHOP方案治疗:泼尼松(广东三才医药集团有限公司,国药准字H44023869)口服,每日100 mg,第1~5天;长春新碱(广东岭南制药有限公司,国药准字H20065857)静脉滴注,1.4 mg·m-2,第1天;多柔比星(汕头经济特区明治医药有限公司,国药准字H44024476)静脉滴注,50 mg·m-2,第1天;环磷酰胺(菏泽睿鹰制药集团有限公司,国药准字H20055196)静脉滴注,750 mg·m-2,第1天。21 d为1个疗程,持续用药6个疗程。观察组在对照组基础上接受利妥昔单抗(f.hoffmann-la roche limited,批准文号S20080045)治疗,在实施CHOP方案前1 d,将375 mg·m-2利妥昔单抗加入50 g·L-1葡萄糖溶液中,稀释至1 g·L-1,静脉滴注,初始速度≤50 mg·h-1,若无明显不适,提高滴速到100 mg·h-1。
1.4 观察指标
1.4.1疗效 治疗6个疗程后评估两组疗效。病变完全消失,至少维持28 d为完全缓解(complete response,CR),病灶缩小>50%为部分缓解(partial response,PR),病灶缩小≤50%或增大≤25%为稳定(stable disease,SD),病灶增大>50%或有新病灶出现为进展(progressive disease,PD)[3]。将完全缓解和部分缓解计为总有效。
1.4.2血清学指标 分别于治疗前、治疗6个疗程后各抽取3 mL空腹静脉血,离心取上清液,以酶联免疫吸附法测定血清血管内皮生长因子(vascular endothelial growth factor,VEGF)、胸腺嘧啶脱氧核苷激酶-1(thymidine kinase 1,TK-1)水平,以全自动生化分析仪(济南金浩峰技术有限公司,型号KHA-200)测定血清乳酸脱氢酶(lactate dehydrogenase,LDH)水平。
1.4.3不良反应 观察治疗期间不良反应发生情况,包括恶心呕吐、肝功能受损、脱发、白细胞减少、血小板减少等。
1.4.4复发 随访1 a,统计复发率。
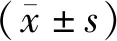
2 结果
2.1 疗效对照组CR 8例,PR 13例,SD 6例,PD 4例,总有效率为67.74%(21/31)。观察组CR 16例,PR 12例,SD 2例,PD 1例,总有效率为90.32%(28/31)。观察组总有效率高于对照组,差异有统计学意义(χ2=4.769,P=0.029)。
2.2 血清VEGF、TK-1、LDH水平治疗前,两组血清VEGF、TK-1、LDH水平比较,差异无统计学意义(均P>0.05);治疗6个疗程后,观察组血清VEGF、TK-1、LDH水平低于对照组,差异有统计学意义(均P<0.05)。见表1。

表1 两组治疗前后血清VEGF、TK-1、LDH水平比较
2.3 不良反应发生率和复发率观察组出现8例恶心呕吐、3例肝功能受损、5例脱发、17例白细胞减少、7例血小板减少。对照组出现9例恶心呕吐、2例肝功能受损、4例脱发、16例白细胞减少、6例血小板减少。两组恶心呕吐、肝功能受损、脱发、白细胞减少、血小板减少等不良反应发生率比较,差异无统计学意义(均P>0.05)。随访1 a,两组各脱落1例,观察组复发2例,复发率为6.67(2/30),对照组复发6例,复发率为20.00(6/30),两组复发率比较,差异无统计学意义(P>0.05)。
3 讨论
NHL发病机制复杂,与艾滋病、器官移植、遗传性免疫缺陷导致的免疫功能异常有关,近年来发病率呈上升趋势,对患者生命安全造成极大威胁[4]。目前临床主要通过化疗治疗NHL,其中CHOP方案的应用较为成熟,疗效确切,但单独给予化疗药物治疗,加大剂量会增加不良反应发生风险,且会产生耐药性,影响治疗效果。临床研究证实,在NHL治疗中选择适宜配伍药物对提高缓解率具有积极意义[5]。
利妥昔单抗是一种人鼠嵌合抗体,能特异性地与跨膜抗原CD20结合,诱导抗体、补体介导细胞毒作用,促进B细胞溶解,抑制其增殖,并加速其凋亡,提高肿瘤细胞对化疗药物的敏感性,且还能有效调节机体内环境,阻止肿瘤血管新生[6]。在CHOP方案基础上应用利妥昔单抗,能在保证机体正常细胞功能、生理状态的情况下消灭肿瘤细胞,发挥与化疗药物的协同作用,从而提升化疗效果。本研究发现,观察组治疗总有效率高于对照组,可见利妥昔单抗联合CHOP方案治疗NHL患者效果显著。研究发现,利妥昔单抗不会加剧化疗药物毒副作用[7]。本研究结果显示,两组随访1 a复发率、不良反应发生率无显著差异,提示利妥昔单抗联合CHOP方案治疗NHL患者,未增加不良反应发生率,且复发率低。VEGF属于血管生长因子,能促进血管生成,增强肿瘤细胞攻击力,在NHL肿瘤组织内具有较高表达水平;TK-1参与嘧啶合成,可调控细胞周期,其水平高低能反映细胞增殖情况。LDH属于糖降解酶,广泛分布于机体体液与各组织细胞中,NHL细胞增殖能力强大,侵袭周围组织时,会刺激正常组织大量释放LDH[8]。本研究结果显示,治疗6个疗程后,观察组血清VEGF、TK-1、LDH水平低于对照组,提示利妥昔单抗联合CHOP方案治疗NHL患者,可抑制肿瘤细胞增殖、新生血管形成。
综上可知,利妥昔单抗联合CHOP方案治疗NHL患者效果显著,可抑制肿瘤细胞增殖、新生血管形成,安全性高,复发率低。
