小鼠感染Chinese1型弓形虫慢性期中枢神经系统的损伤和包囊分布研究
2020-07-22郭子璇苏瑞景肖传斌仝宗喜杨玉荣
郭子璇,苏瑞景,肖传斌,仝宗喜,杨玉荣
(河南农业大学 牧医工程学院,河南 郑州 450002)
弓形虫(Toxoplasmagondii)是一种细胞内寄生原虫,可以侵染几乎所有温血动物的有核细胞,诱发弓形虫病,免疫功能受抑制的动物和患者表现为急性弓形虫病,健康动物和人感染弓形虫常表现为无明显症状的慢性感染。进入弓形虫慢性感染阶段,弓形虫形成包囊,可寄生于多个器官,但分布于横纹肌和中枢神经系统的包囊最多[1]。研究发现,我国人和肉用动物弓形虫的感染率约为8.2%和23.7%,其主要流行的虫株为Chinese1型弓形虫[2],但同为基因型Chinese1型弓形虫的不同分离株,其致病性还存在很大差异[3-4]。目前,Chinese1型弓形虫慢性感染对大脑的致病性方面研究,还不丰富。张义华等[5]发现,Chinese1(TgCtwh6)慢性弓形虫感染小鼠脑部的损伤与小胶质细胞活化有关。本试验研究虎源Chinese1(TgTigerCHn1)弓形虫对BALB/c小鼠大脑的致病性和包囊分布,旨在为慢性弓形虫病致人和动物中枢神经系统损伤方面研究提供参考数据,增进对我国人和动物慢性弓形虫病危害的认识和了解。
1 材料与方法
1.1 弓形虫虫株与抗体TgTigerCHn1(Chinese1)弓形虫虫株分离于河南省动物园老虎[6]。兔抗弓形虫多克隆抗体和弓形虫抗原由美国农业部Dubey试验室馈赠,小鼠/兔HRP/DAB(ABC)IHC检测试剂盒购自Abcam公司(货号:ab64264)。
1.2 试验分组健康BALB/c小鼠10只,弓形虫检测阴性,购于郑州大学实验动物中心(实验动物处理遵守动物伦理与福利相关规定)。小鼠随机分为2组,每组5只,试验组小鼠腹腔注射无菌生理盐水稀释的弓形虫速殖子1个/只(速殖子浓度采用<100,101,102,103,104,105梯度稀释后,经小鼠生物学测定确定[6]),每只小鼠接种量为1 mL,对照组小鼠腹腔注射无菌生理盐水1 mL/只。自由采食饲料和饮水,每日观察小鼠临床情况并记录。接种后60 d(60DPI),采集小鼠血清,乙醚麻醉后处死,10%的中性福尔马林溶液固定小鼠中枢神经组织。
1.3 弓形虫检测方法采用改良凝集实验(Modified Agglutination Test,MAT)方法检测小鼠血清中弓形虫IgG[7],确定小鼠是否感染弓形虫。组织压片方法检查大脑皮质中是否含有弓形虫包囊,光学显微镜观察。
1.4 小鼠中枢神经系统连续切片制作及染色运用常规病理学技术制作脑组织连续石蜡切片,切片厚度7 μm。全脑的矢状面,1/2大脑全部制做连续切片,约110张/只小鼠。中枢神经系统全长(1.43±0.20)cm,采用石蜡切片技术制片后,观察到的中枢神经系统体积略小于真实体积。显微镜下观察可见,含大脑的切片110张,厚度(0.43±0.05)cm;含脑干的切片90张,脑干厚度(0.42±0.02)cm;含小脑的切片73张,厚度(0.39±0.14)cm。
采用苏木素与伊红对比染色法 (Hematoxylin-Eosin staining,H&E)观察大脑皮质、基底核、间脑、中脑、后脑、小脑蚓部和半球部位的病理损伤,统计全部脑组织内的弓形虫的包囊数量、血管周围炎症反应数量和包囊周围炎症程度。正常脑组织评为0分,包囊周围单核细胞浸润数量为10个到30个评为1分;30个到50个评为2分;50个以上评为3分[8-9]。采用免疫组织化学染色方法(immunohistochemical staining,IHC)观察弓形虫抗原分布。
1.5 数据处理采用软件GraphPad prims 5.0(Graphpad Software Inc.,San Diego,CA,USA)对得到的数据进行分析,并制图。
2 结果
2.1 BALB/c小鼠弓形虫的感染情况试验组、对照组小鼠存活期均达60 d,未见明显临床异常表现。60 d后,试验组小鼠(n=5)腹腔注射TgTigerCHn1弓形虫速殖子后,其MAT滴度均1∶200,且大脑皮质压片均可观察到弓形虫包囊,显示100%小鼠成功感染弓形虫。对照组小鼠,其MAT滴度均<1∶25,且大脑皮质压片未检查到弓形虫包囊,显示未感染弓形虫(表1)。

表1 BALB/c小鼠感染TgTigerCHn1弓形虫的发病情况(感染后60 d,1个速殖子/只,腹腔注射)
2.2 慢性弓形虫病小鼠中枢神经系统病理组织学变化小鼠感染TgTigerCHn1弓形虫速殖子60DPI,眼观,其大脑轻微肿大,蛛网膜充血。显微镜下,小鼠脑组织呈非化脓性脑炎特征。弓形虫生长于神经元内,并形成包囊,其周围可见嗜神经元现象和神经细胞坏死,小胶质细胞、少突胶质细胞和单核细胞增生形成胶质结节(图1 A);弓形虫包囊周围的血管周围浸润单核细胞、淋巴细胞,形成袖套现象(图1 B);有的多个弓形虫包囊呈卫星样分布(海马较明显),周围可见明显的神经细胞坏死和炎症反应(图1 C);此外,蛛网膜下腔可见多量单核细胞、淋巴细胞浸润,炎症附近可见弓形虫包囊(图1 D);多数弓形虫包囊分布于神经元,也可见生长于小脑浦肯野细胞中的包囊(图1 E);免疫组织化学方法验证这些包囊呈弓形虫抗原阳性(图1 F)。
2.3 慢性弓形虫病小鼠中枢神经组织弓形虫包囊的分布弓形虫包囊在慢性弓形虫病小鼠中枢神经组织切片中呈近圆形,且不均匀分布(图1;图2A,B)。小鼠感染TgTigerCHn1弓形虫,从颅侧到尾侧的大脑皮质、基底核、脑干、中脑、后脑、小脑蚓部和半球部位,其弓形虫包囊数量、血管周围炎症反应数量和包囊周围炎症程度均有显著性差异。弓形虫包囊数量从高到低依次为,大脑皮质>中脑>基底核>间脑>后脑>小脑蚓部>小脑半球。其中,大脑皮质的弓形虫包囊数量最多,为(16.06±1.01)个/cm2脑组织(图2 B),包囊周围的炎症程度也最重,弓形虫包囊数量与炎症程度呈正相关(图2 A,C)。基底核的血管周围炎反应最为剧烈(图2 D)。小脑蚓部和半球的弓形虫包囊数量最少,为(1.44±0.15)个/cm2小脑蚓部,包囊周围的炎症反应程度也较轻(图2 B,C)。脑干中,中脑的弓形虫包囊数量最多,为(12.51±1.05)个/cm2脑组织(图2 B)。其大脑包囊总数量可达约10 700个。
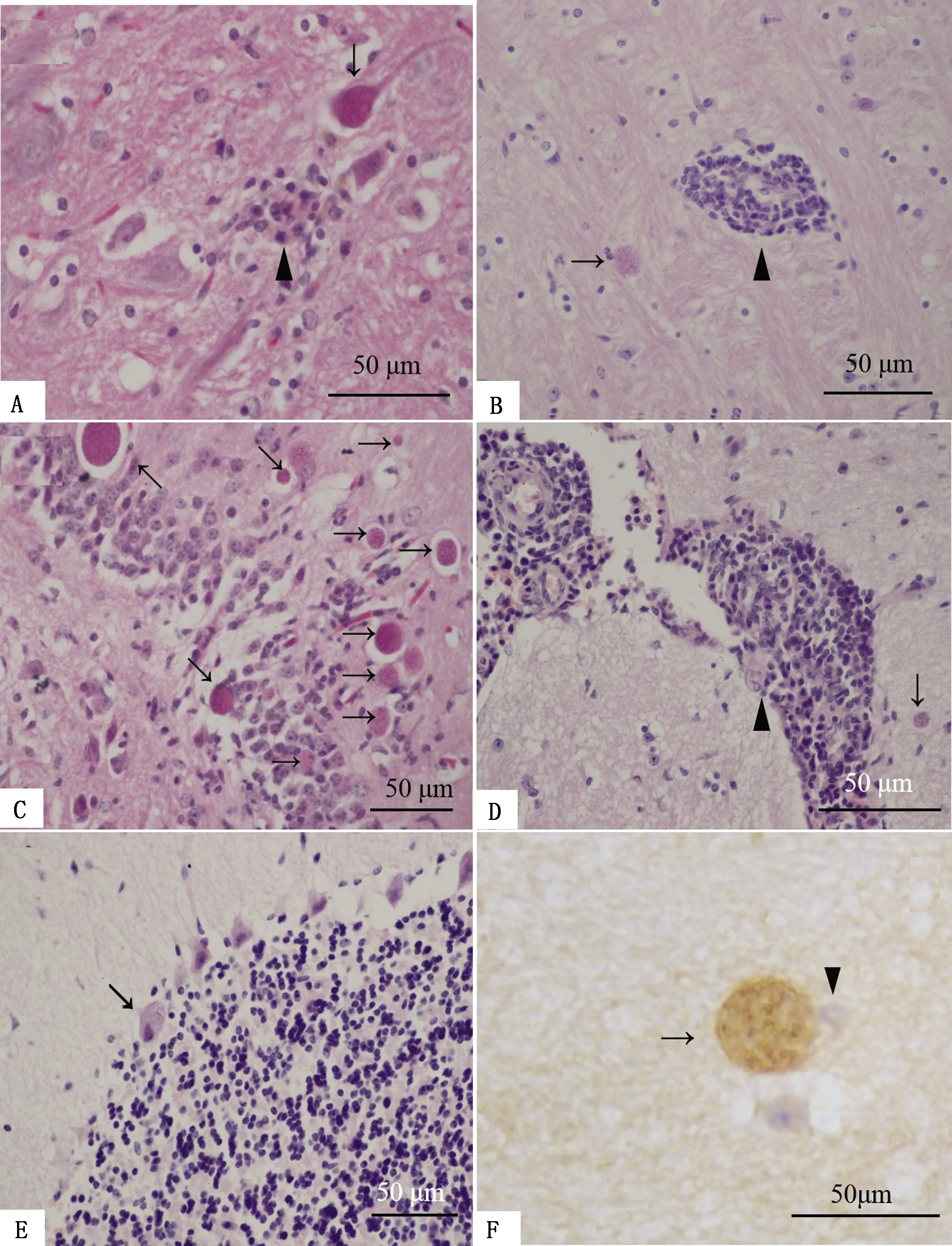
图1 BALB/c小鼠感染TgTigerCHn1弓形虫慢性期中枢神经系统病理变化 A.大脑中神经元内弓形虫包囊(箭头)和周围的胶质结节现象(三角形),H&E染色;B.血管袖套(三角形)和附近的弓形虫包囊(箭头),H&E染色;C.海马多个弓形虫包囊(箭头),H&E染色;D.大脑中蛛网膜下腔炎性细胞浸润(三角形)和附近的弓形虫包囊(箭头),H&E染色;E.小脑浦肯野细胞中的包囊(箭头),H&E染色;F.大脑弓形虫包囊(箭头)和神经元细胞核(三角形),IHC染色
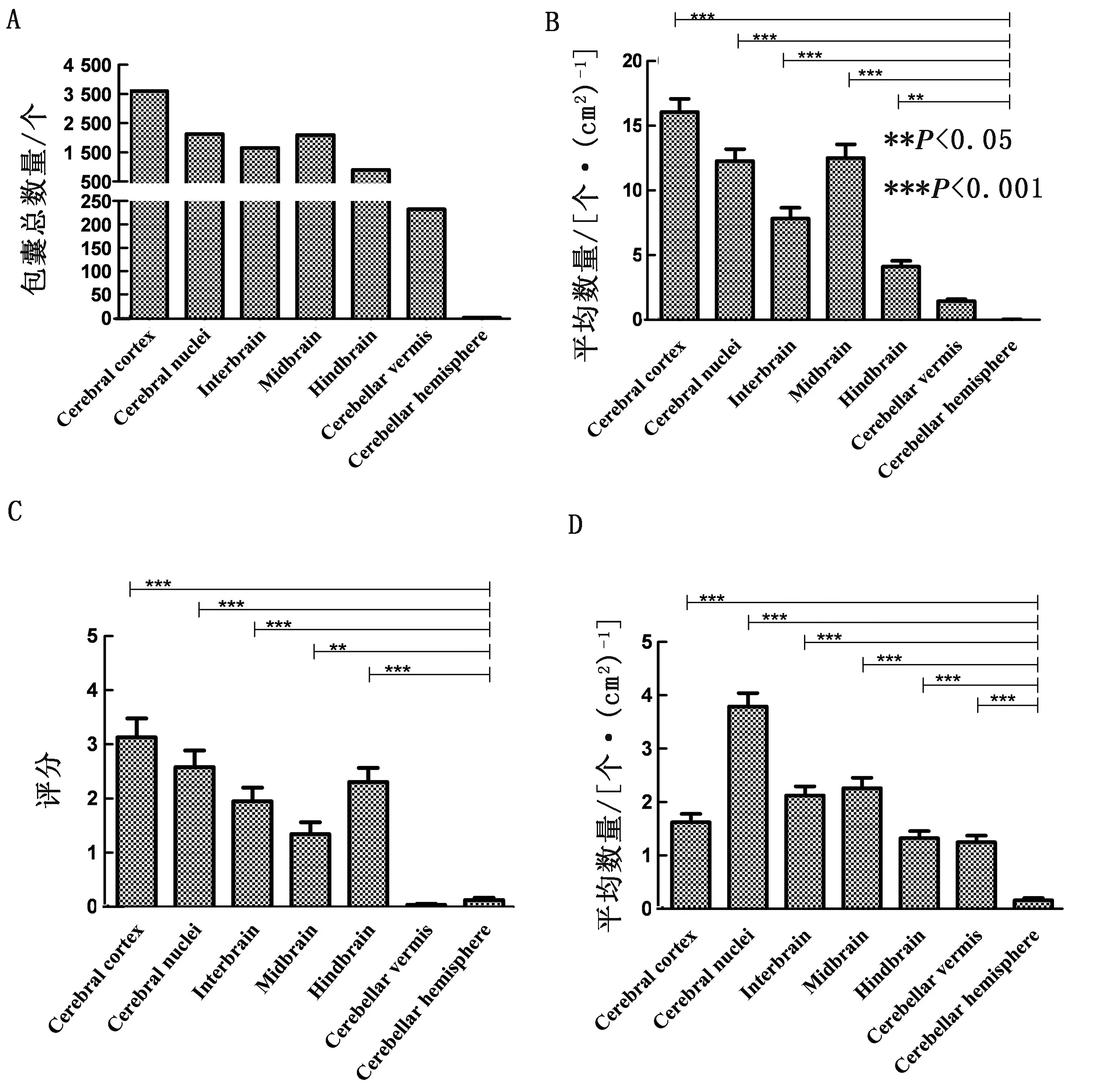
图2 BALB/c小鼠感染TgTigerCHn1弓形虫后中枢神经系统弓形虫包囊分布、数量和损伤 A.弓形虫包囊总数量;B.弓形虫包囊平均数量;C.弓形虫包囊周围炎症评分;D.发生血管周围炎症的平均数量
3 讨论
弓形虫急性感染期的速殖子,受到宿主免疫反应抑制后转化为缓殖子,并形成包囊,转变为慢性感染期;而慢性感染期的缓殖子,在宿主免疫功能低下时又可以活化成为速殖子,重新转变为急性感染,造成严重的临床症状和后果。关于急性和慢性感染阶段没有严格的界定,一般,弓形虫急性感染期可在感染后持续3周,超过3周,动物未表现明显的临床症状,则进入慢性感染期。本研究结果显示,虎源Chinese1型弓形虫(TgTigerCHn1株,1个)感染小鼠60 d后,全部存活,且无明显临床症状,病理组织学观察发现中枢神经系统多量的弓形虫包囊,未见弓形虫速殖子,说明这些小鼠已进入慢性感染阶段。
一般认为,弓形虫感染宿主后,弓形虫包囊可长时间存在于脑组织或横纹肌中(大约一生),免疫能力正常的宿主可建立有效的Th1型细胞免疫反应抑制包囊激活,并抵抗弓形虫所引发的脑炎[10]。本研究发现,小鼠感染虎源弓形虫慢性期,中枢神经系统分布大量的弓形虫包囊,且存在与弓形虫包囊相关的病理组织损伤,并引发了弓形虫性非化脓性脑炎。关于Chinese1型弓形虫对神经系统的损伤和分布,尚未见报道。Prugniuad(Pru)株弓形虫感染小鼠70 d后,大脑也可见明显的病理损伤(炎性细胞浸润)[11]。弓形虫慢性感染阶段,可改变或颠覆宿主神经元的活性,从而永久性的影响宿主行为[12]。这些结果说明,弓形虫慢性感染期对中枢神经系统的结构有损伤,并推测影响其神经功能。本课题组在日常管理弓形虫慢性感染的小鼠过程中,发现其存活期明显低于健康小鼠(P<0.05)。因人类抵抗弓形虫免疫反应与小鼠完全不同,因此弓形虫慢性感染期是否引起人和其他动物的中枢神经系统的病理损伤,还不确定。但对自然感染弓形虫的黑猩猩研究发现,弓形虫可改变其行为[13]。而且,流行病学调查发现,弓形虫血清阳性患者与患精神分裂症和躁郁症存在相关性[14]。Chinese1型弓形虫是我国人和动物的优势虫株,其慢性感染期潜在的危害尚需更多的客观评价。
根据对照组小鼠中枢神经系统未见明显损伤,以及试验组小鼠中枢神经系统损伤周围可见弓形虫包囊分布这一特点,说明这些损伤和炎症反应是弓形虫感染引起的。大脑皮质的弓形虫包囊数量和损伤程度均处于较高水平,而小脑半球的弓形虫包囊分布最少(P<0.05)。这一结果提示,临床病理诊断弓形虫脑炎时,大脑皮质是理想的检查部位。绵羊弓形病急性感染时,也发现大脑皮质和视交叉的损伤程度最重,弓形虫虫体分布最多[15]。弓形虫感染后,中枢神经系统的病原分布和损伤特点推测弓形虫可影响宿主的认知功能和视野缺损,表现在不能集中注意力进行观察和思考问题、健忘、情绪波动和视力障碍。
弓形虫速殖子腹腔注射感染小鼠,弓形虫可经淋巴和血液循环扩散至脑部中枢神经。弓形虫速殖子进入大脑血管内皮细胞,并在大量复制后裂解内皮细胞,从而攻破血脑屏障,进入中枢神经系统[16]。速殖子主要进入神经元和神经干细胞进行复制,活化小胶质细胞,并导致脑组织的损伤[17]。但弓形虫嗜中枢神经系统的机制,还不清晰。
该研究丰富了我国Chinese1型弓形虫虫株对宿主中枢神经系统的损伤特征研究,展示了小鼠感染Chinese1型弓形虫慢性感染期中枢神经系统包囊的分布和炎症反应程度,为探讨人和动物的慢性弓形虫病的神经系统致病机理提供了基础数据。
