有限采样法估算重症感染患者卡泊芬净的药-时曲线下面积
2020-07-15陈文倩王晓雪刘慧芳杜雯雯王芊霖詹庆元张相林李朋梅
陈文倩,王晓雪,刘慧芳,杜雯雯,王芊霖,张 丹,詹庆元,张相林,李朋梅
(中日友好医院,北京 100029)
卡泊芬净是棘白素类抗菌药物,抗真菌活性强,与其他药物相互作用少,安全性较好。棘白菌素类与唑类药物无明显交叉耐药性,且与三唑类或多烯类药物联用可产生协同作用,故临床常将卡泊芬净与其他药物联合用于治疗重症感染患者的侵袭性深部真菌感染[1-3]。卡泊芬净为浓度依赖性药物,且有长效抗真菌后效应,其药-时曲线下面积(AUC)与最低抑菌浓度(MIC)的比值是预测疗效的药动学/ 药效学参数。重症感染患者生理状态不稳定,治疗药物在此类患者中的药动学差异较大,治疗时需药物监测,以提高疗效,降低不良反应[4]。但若需获得卡泊芬净的AUC0-24,则需监测多个血药浓度点,实际监测难以实施。国内外多采用有限采样法(LSS),可用较少的血药浓度点准确估算AUC,目前已在霉酚酸、白消安、抗病毒药物等中得到应用[5-10]。本研究中考察了中国重症感染患者中的卡泊芬净药动学特征,并建立了LSS 模型,为进行治疗药物监测及个体化用药提供参考。现报道如下。
1 材料与方法
1.1 仪器与试药
仪器:Acquity UPLC 型超高效液相色谱仪,Quattro PremierXE 三重四级杆质谱仪,电喷雾离子化源(ESI)及Masslynx4.1 数据处理系统(美国Waters 公司);Milli-Q Advantage A10 型超纯水机(美国密理博公司)。
试药:注射用醋酸卡泊芬净(70 mg,批号为R012746;50 mg,批号为R012821),购自美国默沙东制药有限公司);卡泊芬净对照品(纯度为99.68% ,美国CFW 公司,批号为P8307305);卡泊芬净-d4 对照品(纯度为99.30% ,加拿大TRC 公司,批号为10 -GJF162 -1);甲酸(色谱纯,德国CNW 有限公司,批号为175162);乙腈(色谱纯,美国FisherScientific 有限公司,批号为186351)。
1.2 病例选择
纳入标准:年龄18 ~70 岁;采用卡泊芬净进行抗真菌治疗的重症感染。本研究经我院医学伦理委员会批准,患者自愿受试并签署知情同意书。
排除标准:卡泊芬净给药未达到稳态即停止治疗或死亡;孕妇;肝功能异常。
病例选择:共纳入24 例患者,其中男18 例,女6 例;年龄53 ~70 岁;体质量45 ~75 kg。
1.3 方法
1.3.1 给药及采血方案
受试者第1 日给予卡泊芬净负荷剂量70 mg,第2日开始给予50 mg,每日1 次,输注时间为0.5 h。至少给予4 剂达稳态后,下次给药前即刻及给药后0.5,1,2,3,5,9,12,24 h 时取静脉血1.5 mL,置乙二胺四乙酸(EDTA)抗凝采血管中,3 000 g 离心5 min 分离血浆,采用超高效液相色谱-串联质谱(UPLC -MS/MS)法测定血浆中卡泊芬净质量浓度。
1.3.2 血药浓度测定
自建卡泊芬净的血药浓度检测方法[11-12]:精密吸取血浆样品50 μL,分别加入20 μL 卡泊芬净- d4 内标液(25 μg/mL)及580 μL 甲醇(含0.1%甲酸),涡旋3 min,12 000 r/min 离心10 min,转移上清液500 μL 于样品瓶,2 μL 进样。
测定条件:色谱柱为Waters BEH C18柱(50 mm ×2.1 mm,1.8 μm);流动相为水溶液(含2 mmol/L 乙酸铵及0.1%甲酸,A1)-乙腈(含0.1%甲酸,B1),梯度洗脱(0 ~1 min 时10%B ~95%B,1 ~1.5 min 时95%B,1.5 ~2.0 min 时95%B ~10%B,2.0 ~3.0 min 时10%B,比例变化为线速变化;流速为0.2 mL /min。质谱检测采用电喷雾离子源(ESI),ESI 正离子模式进行扫描,多离子反应监测(MRM),母离子/子离子质荷比为m / z 547.80 /538.8( 卡 泊 芬 净) 和 m / z 549.60 /540.60(卡泊芬净-d4)。
方法学考察结果:卡泊芬净质量浓度线性范围为0.391 ~25.0 μg/mL(R2=0.998 7);方法的专一性、日内及日间精密度、提取回收率、基质效应及稳定性均符合生物样本分析要求。
1.4 数据处理
对数据进行非参数药动学模型分析,峰浓度( Cmax)及谷浓度( C0)由数据直接获得,以梯形面积法计算0 ~24 h 药-时曲线下面积(AUC0-24)。
以SPSS 22.0 统计学软件对数据进行LSS 模型拟合,以卡泊芬净AUC0-24作为因变量,各个时间点血浆浓度作为自变量进行多元逐步回归分析,得出用于估算卡泊芬净AUC0-24的简化计算公式,线性回归方程见公式1。考察AUC0-24与Ct1,Ct2,…和Cti任意1 点和多点间的相关性(r2,调整相关系数),并采用逐步多元回归法,遴选出r2较好的回归方程。以预测误差(PE%,见公式2)评价模型的准确性,绝对误差(AE%,见公式3)评价模型的精密度[13-14],分别计算其平均值及相应的标准差(S)。同时,考察AUC0-24估算值与实测值的相关性,并作相关性散点图。

2 结果
2.1 药动学分析
24 例患者输注卡泊芬净后的血药浓度见图1。主要PK 参数:Cmax为(18.13 ±4.24)μg /mL,C0为(3.56 ±1.73)μg/mL,AUC0-24为(167.81±46.03)μg/ (mL·h)。
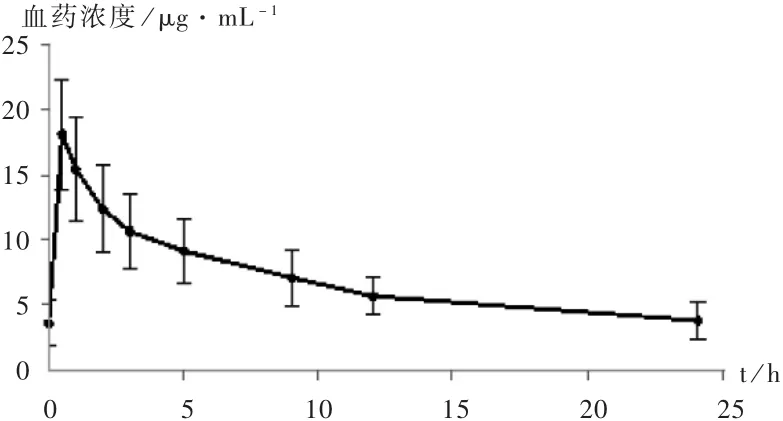
图1 重症感染患者卡泊芬净血药浓度
2.2 LSS 模型拟合及最佳采样方案
以单一或多个时间点卡泊芬净浓度与AUC0-24进行多元逐步回归分析,选择1 ~4 个样本点中调整决定系数最佳的回归方程。结果见表1。可见,不同单个时间点血药浓度与AUC0-24相关性之间有较大差异,r2范围为0.190 ~0.942,其中C0,C0.5,C5,C9单点与AUC 相关性较好,相关性最好的为C9(r2=0.942)。多元逐步回归分析结果显示,随着纳入2 ~4 个时间点血药浓度,计算公式的计算结果与实际AUC 值更接近。其中,2 个时间点浓度中C9和C24预测性能最好,r2为0.962,LSS 计算公式为24.323 +18.263 × C9+4.375 × C24;其次 为 C0.5, C9,其 r2为0.953,2 个 公 式 相 比 较,虽 然C0.5和C9方案的PE 为(0.23 ±6.11)%,稍低于C9和C24的(0.86 ±5.82)% ,但其代表数据离散度的参数AE% 为(4.79 ±3.66)% ,略 高 于 C9和 C24方 案 的(4.14 ±3.50)%,且出现1 例患者估算AUC 的偏差大于-15%。3 个时间点中,C0.5,C9,C24拟合效果最好,r2为0.977,LSS 公 式 为7.911 +2.606 × C0.5+13.765 ×C9+4.662 × C24;其次为C0.5,C5,C9方案,r2为0.955,相比前者方案拟合效果更优,且AP%小于后者,同样后者方案出现1 例患者估算AUC 的偏差大于-15%。4个 时 间 点 方 案 普 遍 预 测 能 力 较 好,其 中C0.5,C1, C9,C24, r2为0.983,LSS 公 式 为8.354 +1.949 × C0.5+1.032 ×C1+13.504 × C9+4.075 × C24,PE%为(0.53 ±3.42)%,AE%为(2.44 ±1.93)%。由图2 可知,2 个时间点方案C9和C24,3 个时间点方案C0.5,C9,C24及4个时间点方案C0.5,C1,C9,C24经回归模型计算均可很好地实现对卡泊芬净的AUC0-24值的估算。

表1 卡泊芬净AUC0 -24 的多元线性回归模型

表2 AUC 简化模型公式的预测效果(n =24)

图2 AUC0 -24 实测值与回归模型估算值相关图
3 讨论
重症监护病房患者体内药物的药动学特征常与健康人群差异较大,且存在明显个体差异,导致部分患者易发生体内药物暴露量过高或过低。此外,该类患者常因患重症感染而联合使用多种抗菌药物,故难以评判各单一药物的治疗是否达标,而治疗药物监测可对药物体内暴露量进行定量监测,是保障这类患者用药的有效性和安全性的重要手段。对伏立康唑、泊沙康唑、伊曲康唑等常用抗真菌药物的治疗药物监测已有较多研究[15],并有明确的C0目标推荐,但对卡泊芬净的相关研究仍有限。既往研究已明确,卡泊芬净的疗效指标为AUC/ MIC,因其具有高蛋白结合率(约97%)和主要通过肝代谢,其体内药动学可能受低蛋白血症和肝功能影响较大。本研究中纳入了肝功能正常的重症感染患者的,其AUC0-24为(167.81 ±46.03)μg / (mL·h),仍存在较明显的个体差异。因此,对此群体进行卡泊芬净的治疗药物监测均有必要,且应根据血药浓度监测结果对AUC 进行估算。
LSS 是通过检测较少的血药浓度样本来准确估算患者AUC 的传统方法,已应用于多个药物研究,但国内外尚未见卡泊芬净的相关报道。本研究中考察了重症感染患者不同时间点的药物浓度与AUC0-24间的相关性,结果表明,采集2 ~4 个时间点血药浓度方案的回归方程预测能力优于单点采血。其中,2 个时间点的C9,C24,3 个时间点的C0.5,C9,C24,4 个时间点的方案C0.5,C1,C9,C24预测性能良好,调整r2均达到0.96 以上。根据患者采样配合程度及对预测结果精准性的要求可选择不同的采血方案,综合考虑,本研究中推荐采用C0.5,C9,C243 点采血方案。估算AUC 与实际检测AUC 符合程度良好,相对误差均在±15%内,在临床治疗中可以此为基础结合致病菌的MIC 进一步估算药物代谢动力学-药物效应动力学指标AUC / MIC。
对于以AUC / MIC 为疗效指标的抗菌药物,多采用监测给药达稳态后C0,根据AUC 与C0之间的线性相关性推测C0的治疗目标范围,如万古霉素、伏立康唑等药物均采用此方法。本研究中AUC 虽与C0呈现一定的相关性,但其相关性不强,用单点C0推测AUC 可能带来较大偏差,因此对卡泊芬净的治疗药物监测更推荐采用LSS 法。进一步研究还可收集更多数据进行群体药动学分析,定量分析患者病生理指标、疾病状态等因素对药动学的影响,并可通过1 ~2 个血药浓度点结合贝叶斯反馈法进行AUC 的估算。
本研究中采用LSS 法建立了重症感染患者根据2 ~4 个卡泊芬净血药浓度估算AUC0-24的方法,避免了患者过多采集检测血样带来的生理创伤和经济负担。结果表明,以给药后0.5,9,24 h 的卡泊芬净浓度可准确估算AUC0-24,结合致病菌的MIC 可获得其疗效指标AUC / MIC 水平,可为此患者群体的个体化给药提供参考。
