贝伐单抗联合FOLFIRI 或CAPIRI 治疗晚期转移性结直肠癌疗效与安全性M eta 分析
2020-07-15刘黔川白鍊刘飞廖健
刘黔川,白鍊,刘飞,廖健
(重庆医科大学附属永川医院,重庆 402160)
近年来,结直肠癌已成为全球发病率居第3 位的恶性肿瘤,并呈上升趋势[1]。世界卫生组织(WHO)2019 年的统计资料显示,2018 年全球结直肠癌新发病例约184.9 万例,男性和女性发病率分别居癌症的第3 位和第2 位,死亡近88.1 万例[2]。随着医学诊疗水平的不断提高,大部分能早期诊断的结直肠癌患者均能通过根治性手术获得痊愈,但仍有部分患者在发现肿瘤时已伴随有远处转移或术后复发,失去了手术机会。对于晚期不可切除的转移性结直肠癌(mCRC)患者,主要采用综合治疗和个体化治疗,以延长患者的生存时间,提高生活质量。姑息性化学治疗(简称化疗)是综合治疗的重要手段[3]。目前靶向药物(贝伐单抗、西妥昔单抗等)联合化疗成为治疗晚期mCRC 的一、二线方案[4-5]。本研究中总结了近年来FOLFIRI(氟尿嘧啶+伊立替康)+Bev(贝伐单抗)和CAPIRI(卡培他滨+伊立替康)+Bev 的临床随机对照试验(RCT),采用Meta 分析比较两组治疗方案的疗效与安全性。现报道如下。
1 资料与方法
1.1 文献纳入标准与排除标准
纳入标准:经病理组织学检查证实为结直肠癌,影像学提示至少有1 个可测量转移病灶;年龄18 岁,美国东部肿瘤协作组(ECOG)评分0 ~2 分;入组前至少4 周内未行任何放化疗;血常规参数、肝肾功能基本正常。
排除标准:合并有其他恶性肿瘤或有脑转移;肠梗阻、未控制的高血压;凝血功能障碍,有出血或血栓形成史,需长期服用抗凝药物;无法获取全文或全文中无法提取定量数据,如无相关数据的会议摘要、文献综述等;交叉试验。
1.2 检索策略
检索The Cochrane Library,PubMed,Embase,以及中国期刊全文数据库(CNKI)、维普数据库(VIP)、万方数据库等,以“氟尿嘧啶”“伊立替康”“卡培他滨”“贝伐单抗” “ 转 移 性 结 直 肠 癌” “fluorouracil” “irinotecan”“capecitabine”“bevacizumab”“colorectal”及各类似词为检索词,检索时间为2000 年1 月至2019 年10 月。
1.3 质量评价及资料提取
2 名研究者按纳入和排除标准,独立阅读文献摘要及全文,评价文献质量,提取数据,如有分歧则与第3 名研究者协商解决,提取数据的主要包括文献基本信息、受试人群基线特征、干预措施、结局指标、安全性指标。参考Cochrane 协作网偏倚风险评价标准,对文献质量进行评价,评价内容包括随机分配方法、分配隐藏方法、盲法、结局资料的完整性、选择性报告结果、其他偏倚。
1.4 统计学处理
采用Stata15.0 统计软件进行Meta 分析。计数资料以RR 值及其95% CI 为效应指标,生存资料以HR 值及其95% CI 为效应指标。异质性检验结果I2<25%表明异质性较低,采用固定效应模型;25% <I2<50%提示中度异质性,采用随机效应模型;I2>50%提示异质性较大,采用随机效应模型。由于纳入文献小于10 篇,根据Cochrane 手册,不适用于使用漏斗图检查发表偏倚,故对连续型资料采用Egger′s 检验、二分类资料采用Harbord 检验进行发表偏倚检验。P <0.05 为差异有统计学意义。
2 结果
2.1 文献检索结果
共检索出文献222 篇。其中,中文90 篇,英文132 篇;中国知网44 篇,万方数据库31 篇,维普(VIP)15 篇,The Cochrane Library 23 篇,PubMed 44 篇,Embase 65 篇。剔除重复文献119 篇;阅读文摘,排除不合格文献91 篇;初步获得文献12 篇;阅读全文后,排除非RCT文献7 篇,文献原始数据不全且无法获得、文献质量差2 篇。逐级筛选后纳入文献3 篇[6-8],均为英文文献。
2.2 纳入文献基本信息
纳入的3 项研究共有763 例患者,其中FOLFIRI +Bev 组381 例,CAPIRI +Bev 组382 例,均 为 前 瞻 性RCT,纳入文献基本特征见表1。各项研究基线基本相似,其中2 项研究为多中心试验,1 项为单中心试验。3项研究均为RCT,,结局资料均完整,均未选择性报告结果和其他偏倚;文献[6,8]为多中心研究,文献[7]为单中心研究;仅文献[8]为参与者盲法和结局评价盲法。
2.3 疗效指标分析
安全缓解率(CR):3 项研究均报道了CR。各研究间无明显异质性(I2=0.0%,P =0.576),采用固定效应模型分析。结果显示,两组的CR 无明显统计学差异[RR =0.90,95% CI(0.49,1.64),P =0.732]。详见图1。
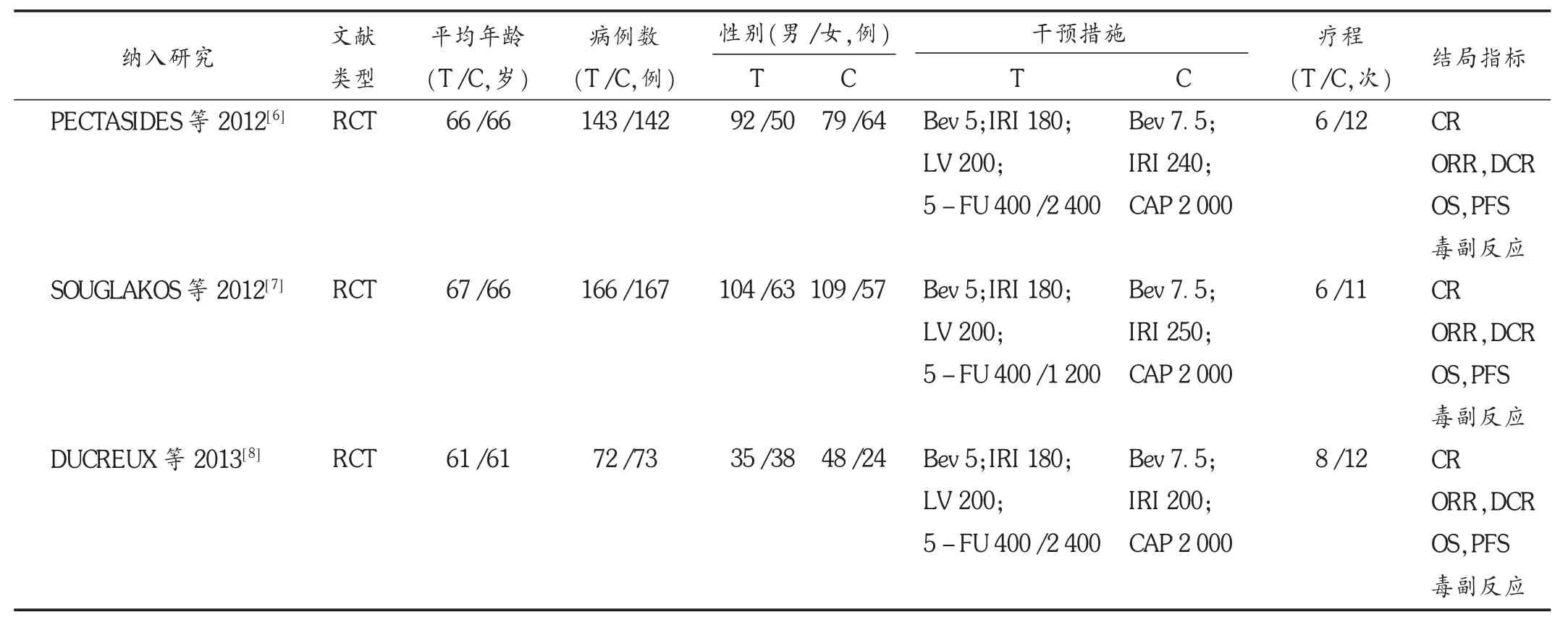
表1 纳入文献基本特征
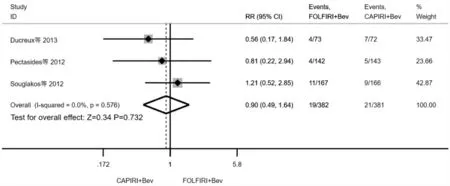
图1 FOLFIRI +Bev 与CAPIRI +Bev 治疗晚期转移性结直肠癌的CR 比较Meta 分析森林图

图2 FOLFIRI +Bev 与CAPIRI +Bev 治疗晚期转移性结直肠癌的ORR 比较Meta 分析森林图

图3 FOLFIRI +Bev 与CAPIRI +Bev 治疗晚期转移性结直肠癌的DCR 比较Meta 分析森林图
客观有效率(ORR):3 项研究均报道了ORR。异质性分析提示,各研究间无统计学异质性(I2=0.0% ,P =0.549),采用固定效应模型分析。结果显示,两组的ORR 差 异 无 统 计 学 意 义[RR =1.10,95% CI(0.94,1.29),P =0.227]。详见图2。
疾病控制率(DCR):3 项研究均报道了DCR。异质性分析提示,各研究间无统计学异质性(I2=0.0%,P =0.561),采用固定效应模型分析。结果显示,与CAPIRI +Bev 组 相比,FOLFIRI +Bev 组DCR 高[RR =1.10,95% CI(1.01,1.21),P =0.028]。详见图3。
2.4 生存指标分析
无进展生存时间(PFS):2 项研究[6-7]报道了PFS的HR 值及置信区间,另1 项研究[8]报道了详细生存数据及生存曲线,通过计算获得其HR 值及置信区间,将3 项研究的HR 值进行合并,共763 例患者。异质性分析无明显统计学异质性(I2=0.0% ,P =0.467),采用固定效应模型分析。结果显示,两组的PFS 差异无统计学 意义[ HR =0.99,95% CI(0.91,1.08), P =0.853]。详见图4。
总生存时间(OS):2 项研究[6-7]报道了OS 的HR值及置信区间,另1 项研究[8]报道了详细生存数据及生存曲线,通过计算获得其HR 值及置信区间,将3 项研究的HR 值进行合并,共763 例患者。异质性分析无明显统计学异质性(I2=0.0%,P =0.753),采用固定效应模型分析。结果显示,两组的OS 差异无统计学意义[ HR =1.05,95% CI(0.93,1.19),P =0.397]。详见图5。
2.5 安全性评价
3 项研究均报道了治疗相关不良反应(3/4 级)。异质性分析提示,仅发热型中性粒细胞减少存在较低异质性,采用固定效应模型进行分析。Meta 分析结果详见表3。
2.5 发表偏倚分析
Harbord 检验提示,发表偏倚差异无统计学意义(P =0.513,0.431),详见图6 A 和图6 B。Egger′s 检验提示,发表偏倚差异无统计学意义(P =0.960,0.234),详见图6 C 和图6 D。
3 讨论

图4 FOLFIRI +Bev 与CAPIRI +Bev 治疗晚期转移性结直肠癌的PFS 比较Meta 分析森林图
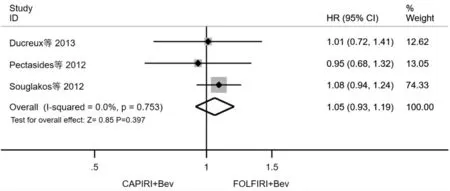
图5 FOLFIRI +Bev 与CAPIRI +Bev 治疗晚期转移性结直肠癌的OS 比较Meta 分析森林图

图6 纳入文献的偏倚风险图

表3 FOLFIRI +Bev 与CAPIRI +Bev 治疗晚期转移性结直肠癌不良反应的Meta 分析
不可切除的mCRC 患者如不接受任何全身治疗,其中位生存时间为8 个月左右[3],经过全身治疗可接近30 个月[9-10]。已有大量研究证据证实,全身治疗可延长患者的生存时间,改善生活质量,这对于mCRC 患者极为重要。分子靶向药物联合化疗治疗mCRC 近年来在临床广泛应用,并有多项研究报道,与单用Bev 或化疗相比,联合用药在延长患者的PFS 和OS 方面优势更明显[11-12],但对于联合用药的方案选择及安全性评价尚有争议[10,13]。本研究中采用Meta 分析法对FOLFIRI +Bev 和CAPIRI +Bev 2 种治疗方案的疗效与安全性进行比较,对纳入的3 项临床随机试验进行分析,结果显示,FOLFIRI +Bev 可增加mCRC 患者DCR,而两组的CR,ORR,PFS,OS 比较均无明显差异。XU 等[14]的研究显示,两组主要疗效指标无明显差异,与本研究结果一致。
DING 等[15]通 过Meta 分 析 比 较 了FOLFIRI 和CAPIRI 2 种化疗方案对mCRC 的疗效和安全性,共纳入7 项相关研究,Meta 分析结果显示,2 组方案临床疗效相似,两组间ORR,OS,PFS 差异均无统计学意义。XU等[16]通过Meta 分析比较了Bev 联合不同化疗方案后的疗效与安全性,共纳入8 项研究,结果显示FOLFIRI +Bev 方案治疗mCRC 可获得更好的ORR 及OS,但研究并未包含CAPIRI +Bev 方案。
合并分析各项研究的3 /4 级不良反应的发生率发现,FOLFIRI +Bev 方案发热型中性粒细胞减少、腹泻的发生率较CAPIRI +Bev 方案低,中性粒细胞减少的发生率较CAPIRI +Bev 方案高,而肥胖、恶心、手足综合征等不良反应的发生率差异无统计学意义。与国内外相关Meta 分析结果相似[15-17],但也有回顾性研究发现,CAPIRI +Bev 方案在手足综合征的发生率较FOLFIRI +Bev 高[18]。
综上所述,CAPIRI +Bev 方案与FOLFIRI +Bev 方案在改善不可切除mCRC 患者OS 及PFS 等方面无明显差异,但可提高其DCR,降低腹泻、发热型中性粒细胞减少的并发症。较已发表的相关系统综述,本研究中比较了CAPIRI +Bev 方案与FOLFIRI +Bev 方案,弥补既往关于贝伐单抗联合化疗研究的空隙,且纳入研究均为英文RCT,优于回顾性研究。但本研究存在一定局限性,如严格控制文献质量后,纳入文献较少,总样本量较少;各研究间的药物剂量及疗程存在差异,且研究对象的选择也不完全一致;未按区域药物剂量、疗程进行亚组分析。故需更高质量、更严谨、更大样本的RCT 支持验证。
