Pd-Cu/羟磷灰石的制备及常温常湿CO催化氧化性能
2020-07-13邢莉莎赵婉君王永钊赵永祥
李 潇, 邢莉莎, 赵婉君, 王永钊, 赵永祥
(1. 山西大学精细化学品教育部工程研究中心, 太原030006; 2. 山西大学化学化工学院, 太原030006)
CO低温催化氧化作为最常见的多相催化模型反应备受关注, 并同时涉及CO防护面具、机动车冷启动尾气排放、燃料电池及CO2激光器等应用领域, 因此, 不断探索新型高效CO催化氧化材料具有重要的理论意义与实用价值[1,2]. 在众多CO低温氧化催化剂[3~5]中, 负载型Wacker催化剂(Pd-Cu/载体)因优异的抗水性和抗卤化物中毒等优势已成为研究热点, 其中, 载体对其CO催化氧化性能的影响至关重要[6]. 目前, 用于负载型Wacker催化剂的载体主要有活性炭[7]、Al2O3[8]、凹凸棒土[9]和分子筛[10]等. 尽管负载型Wacker催化剂对含水汽条件下低温CO氧化具有良好的催化活性, 但以活性炭为载体的催化剂, 由于Cu物种活性相与载体相互作用较弱, 在CO氧化反应过程中易发生氯流失而引起催化剂不可逆失活[11]. Al2O3载体表面富含羟基, 亲水性强, 使得原料气中水汽分子不断在催化剂上吸附凝结, 覆盖在活性中心上的水分子低温下较难脱附, 并可进一步诱导Cu物种活性相Cu2(OH)3Cl晶粒聚集长大, 或相转变为CuCl, 减弱Pd与Cu之间的相互作用, 从而导致催化剂不可逆失活[12]. 以分子筛为载体的催化剂, 由于水汽分子易于充满其孔隙结构, 减少气液接触面积, 致使其催化稳定性降低[10]. 我们[9,11,13,14]前期研究发现, 以廉价的天然凹凸棒土为载体制备负载型Wacker催化剂, 通过对制备方法、焙烧条件及载体的超声处理和炭改性等改进和优化, 不仅可调控Cu物种活性相结构, 提高其稳定性, 同时可改善催化剂对原料气中不同水汽浓度的适应性. 以天然凹凸棒土为载体的催化剂虽然在实际应用方面显示出明显优势, 但凹凸棒土作为一种天然矿物, 由于开采时间、地点以及加工工艺不同, 其组成、结构存在一定差别, 对其常温常湿条件下CO催化氧化作用机制的认识尚难深入. 因此, 探索新载体的催化体系并阐明其结构性能关系, 对于设计新型高效的负载型Wacker催化剂具有重要意义.
羟磷灰石[Ca10(PO4)6(OH)2, HAP]是一种无毒且生物相容性较高的物质, 同时类沸石孔道结构使其表现出较强的离子交换能力[15]. 因此, HAP不仅广泛应用于生物医学硬组织的修复和重建, 在处理水和土壤重金属离子(Cd2+, Hg2+, Sr2+, Ba2+, Pb2+等)污染领域也备受关注[16,17]. 此外, HAP由于可调控的酸碱性和特殊的热稳定性, 在众多催化反应中被广泛用作载体或催化剂[18,19]. Yin等[20]以水热法制备的HAP 载体负载铜用于催化甘油转化. 结果发现, 与Cu/ZrO2催化剂相比, Cu/HAP催化剂上丰富的碱性位点和Cu0活性中心使其表现出较优异的催化性能. Dobosz等[21]分别以微波辅助水热法和溶胶-凝胶法制备HAP载体, 考察了其负载Co, Ce催化剂的乙醇蒸汽重整反应催化性能. 研究结果表明, 不同载体负载活性组分后均可实现较高的乙醇转化率, 但以水热法制备的HAP为载体的催化剂具有更高的产氢率, 其可归因于还原能力和氧移动性的提高以及较多的碱性位点和较高的比表面积. Wang等[22]以不同结晶度的HAP为载体, 采用沉积-沉淀法制备Au/HAP纳米催化剂. 结果显示, 以较高结晶度HAP为载体的催化剂上产生了较多的Au0, 这有助于提高其CO催化氧化活性. Huang等[23]探讨了不同焙烧气氛(H2, He和O2)对Au/HAP催化剂的CO催化氧化性能的影响. 发现O2焙烧气氛下得到的Au/HAP催化剂表现出最高的稳态活性和最佳的稳定性, 归因于催化剂表面较弱的碱性延缓了类碳酸盐物种的积累. Boukha等[24]考察了不同Pd负载量(0.5%~2%, 质量分数)的Pd/HAP催化剂催化CO完全氧化、CO优先氧化和水煤气变换反应. 结果发现, HAP较强的离子交换能力使其成为负载Pd催化剂的优良载体, 其中Pd(0.5)/HAP具有较小的Pd晶粒尺寸, 表现出较高的催化活性和稳定性.
基于上述报道可见, HAP是一种性能优良的催化剂载体, 但将其用于负载型Wacker催化剂的研究尚未见报道. 本文首先以溶胶-凝胶法和水热法获得了HAP载体, 并采用浸渍法制备Pd-Cu/HAP催化剂, 考察了该催化剂常温常湿条件下CO催化氧化性能. 研究结果为新型高效负载型Wacker催化剂的设计提供了参考.
1 实验部分
1.1 试剂与仪器
Ca(NO3)2·4H2O(分析纯), 购于天津市大茂化学试剂厂; (NH4)2HPO4(分析纯), 购于天津市北辰方正试剂厂; PdCl2·2H2O(分析纯), 购于国药集团化学试剂有限公司; CuCl2·2H2O(分析纯)和NH3·H2O(分析纯), 均购于天津市天力化学试剂有限公司; H3PO4(分析纯), 购于北京化学试剂厂.
Agilent 720型电感耦合等离子体发射光谱仪(ICP-OES), 美国Agilent公司; Micromeritics ASAP-2020型物理吸附仪, 美国Micromeritics公司; Bruker D8 Advance 型X射线衍射仪(XRD)和Bruker Tensor 27型傅里叶变换红外光谱仪(FTIR), 瑞士Bruker公司; AutochemⅡ2920型化学吸附分析仪, 美国Micromeritics公司; Escalab 250Xi型X射线光电子能谱仪(XPS)和Nicolet iS50 型傅里叶变换红外光谱仪, 美国Thermo Fisher Scientific公司; GC-930型气相色谱仪, 上海海欣色谱仪器有限公司.
1.2 载体的制备
溶胶-凝胶法制备HAP载体: 将0.1 mol Ca(NO3)2·4H2O和20 mL 3 mol/L H3PO4溶于100 mL无水乙醇中并搅拌混合. 在60 ℃下搅拌2 h后, 将30 mL 10% NH3·H2O加入上述混合溶液中逐渐形成溶胶, 在60 ℃下老化10 h, 在100 ℃下干燥24 h. 最后将干燥的凝胶在600 ℃下焙烧2 h. 获得的样品标记为HAP-SG.
水热法制备HAP载体: 将0.1 mol Ca(NO3)2·4H2O和0.06 mol(NH4)2HPO4溶于100 mL去离子水中. 将30 mL 10%(体积分数)NH3·H2O加入上述悬浮液中, 在40 ℃下搅拌3 h后, 将悬浮液转移至内衬为聚四氟乙烯的高压反应釜中并在100 ℃下保持8 h. 过滤洗涤沉淀物, 将所得样品在100 ℃下干燥, 最后在600 ℃下焙烧2 h. 获得的样品标记为HAP-HT.
1.3 催化剂的制备
采用浸渍法制备Pd-Cu/HAP催化剂: 将1.82 g CuCl2·2H2O溶于2 mL(9.97 mg/mL) PdCl2水溶液中, 然后加入5 g HAP-SG或HAP-HT载体. 老化3 h后, 在120 ℃下干燥6 h. 最后在空气气氛中于300 ℃焙烧2 h. 制得的催化剂样品分别标记为PC-SG和PC-HT.
1.4 催化剂的表征
H2-TPR实验过程如下: 称取30 mg样品放置于H2-TPR反应管内, 通入5%H2-95%N2(体积分数)混合气, 然后以10 ℃/min程序升温至500 ℃. 采用热导检测器测量H2消耗量, 并通过CuO定量还原为单质铜来校准. 样品在进行H2-TPR实验之前未经任何预处理, 尾气进入检测器前经过干燥、净化, 消除H2O和HCl等杂质的影响. CO2-TPD实验过程如下: 在He气氛中, 将100 mg样品加热至300 ℃并恒温1 h. 然后将样品冷却至50 ℃并暴露于CO2脉冲气体中吸附直至饱和, 最后设定升温程序并采用热导检测器测量脱附信号, 通过扣除未吸附CO2样品的程序升温脱附信号得到CO2-TPD曲线. XPS表征以碳的C1s结合能作为基准进行校正. CO原位红外(in-situDRIFTS)测试过程: 称取0.045 g催化剂压片, 将压好的片放入反应池中, 升温至300 ℃并通入流动的N2气处理1 h, 降温至25 ℃, 记录红外光谱(分辨率为4 cm-1, 扫描100次)扫描背景; 然后将N2气切换为CO保持30 min, 最后再将CO切换为N2气吹扫30 min, 并间隔记录样品扫描图谱.
1.5 催化活性评价
CO催化氧化活性评价在连续流动微反装置上进行[14]. 催化剂用量为0.3 g, 原料气中CO体积分数为0.5%, 空气流速(GHSV)为6000 h-1, 水蒸汽体积分数为3.3%. 通入原料气时反应温度设置为25 ℃, 反应前催化剂未进行任何预处理. 采用GC-930型气相色谱仪分析反应前后CO含量, 检测器为氢火焰离子化检测器(FID), 色谱柱为碳分子筛, 柱后与内装Ni催化剂的甲烷转化器相连. 催化活性用CO转化率(x, %)表示:
x=[(SCO-S′CO)/SCO]×100%
式中:SCO为原料气中CO的峰面积;S′CO为反应后剩余CO的峰面积.
2 结果与讨论
2.1 催化活性评价

Fig.1 Catalytic performance of supports and catalysts for CO oxidationReaction conditions: 0.5%CO, GHSV 6000 h-1, water vapor 3.3%(volume fraction), 25 ℃.
图1给出了常温常湿条件下HAP载体和Pd-Cu/HAP催化剂的CO催化氧化活性结果. 可见, 2种HAP载体在反应条件下几乎无活性. 负载活性组分Pd和Cu后, 2种催化剂上CO出现不同程度的转化. 与PC-SG相比, PC-HT表现出较高的CO催化氧化活性. 在考察时间内, PC-SG的CO转化率约为50%, 而PC-HT的CO转化率基本维持在70%左右. 此外, 2种催化剂在反应4 h后仍保持良好的催化稳定性. 由此可见, HAP是一种优良的负载型Wacker催化剂载体, 与HAP-SG相比, HAP-HT更加适合于负载Pd和Cu用于常温常湿条件下CO催化氧化.
2.2 ICP-OES分析
表1列出了2种催化剂中Pd, Cu, Ca和P等元素含量的测试结果. 可见, 2种催化剂具有相似的Pd和Cu负载量, 且均接近于理论值(Pd 0.35%, Cu 12%). PC-HT中Ca/P摩尔比为1.69, 略高于载体HAP的理论Ca/P摩尔比(1.67), 而PC-SG中Ca/P摩尔比高达1.72.

Table 1 Element content analysis of catalysts
2.3 N2物理吸附-脱附分析

Fig.2 N2 adsorption-desorption isotherms of supports and catalysts
图2为HAP载体和Pd-Cu/HAP催化剂的N2物理吸附-脱附曲线. 可见, 样品的吸附-脱附曲线均属于Ⅳ型等温线[25]. 表2列出了各载体和催化剂的比表面积、孔容和平均孔径. 由表2可见, 与HAP-SG和PC-SG相比, HAP-HT和PC-HT具有更大的比表面积和孔容, 有利于反应气体分子的吸附. 其中, HAP-SG的比表面积仅为12.8 m2/g, 而HAP-HT的比表面积为46.2 m2/g. 与载体相比, 负载活性组分后, 2种催化剂的比表面积均有所下降. 这是由于活性组分渗入到载体孔道结构中所引起的[26]. 与载体相比, PC-HT的孔容、平均孔径均减小, 但PC-SG的孔容和平均孔径反而增大, 尤其是平均孔径变化明显, 这可能是由于活性组分在HAP-SG上分布不均匀所致.

Table 2 Textural properties of supports and catalysts
2.4 XRD表征

Fig.3 XRD patterns of supports and catalysts
图3为HAP载体和Pd-Cu/HAP催化剂的XRD谱图. 从图3可见, 2种载体均在2θ=25.9°, 31.8°, 32.2°, 32.9°, 34.0°和39.8° 处出现明显的特征衍射峰, 分别对应HAP载体的(002), (211), (112), (300), (202)和(310) 晶面[27],且与HAP的标准卡片(JCPDS No.09-0432)相符. 值得注意的是, 在2θ=30°~35°范围内, HAP-SG载体的特征衍射峰强度大于HAP-HT, 表明HAP-SG载体结晶度更高.
相比于载体, 2种催化剂均在2θ=16.2° 和17.6°处出现了微弱的衍射峰, 对应Cu2Cl(OH)3(JCPDS No.25-0269) 物种. 在PC-SG的XRD谱图中2θ=8.7°和15.1°处的衍射峰则分别对应于Cu2P2O7(JCPDS No.51-0202)和Cu2(OH)PO4(JCPDS No.77-0922). 此外, 在2θ=30°~35°范围内, 负载Pd和Cu活性组分后, 与单一载体相比2种催化剂中载体特征衍射峰强度均有所减弱, 同时可看到, PC-HT中载体特征衍射峰也发生了一定程度的变化, 而PC-SG中峰型变化不明显. 推测是由于活性组分与HAP-HT间存在较强的相互作用, 且部分Cu2+通过与Ca2+发生离子交换进入了HAP结构中. 此外, 2种催化剂中均未检测到Pd物种的特征衍射峰, 表明Pd物种以良好分散的状态存在[9]. 图3插图为催化剂PC-HT反应240 min后(PC-HT-U)的XRD谱图. 可以看出, 反应后PC-HT-U中HAP载体结构保持良好, 铜物相组成与反应前一致, Cu2Cl(OH)3物种衍射峰强度略有增加. 表明反应后催化剂结构并未发生显著变化.
2.5 FTIR表征
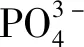

Fig.4 FTIR spectra of supports and catalysts

Fig.5 H2-TPR profiles of supports and catalysts
2.6 H2-TPR表征
图5为HAP载体和Pd-Cu/HAP催化剂的H2-TPR谱图. 可见, 载体在考察温度范围内无还原峰出现, 表明催化剂中还原峰是由Pd和Cu物种引起的, 进一步将其划分为低温区域(T<350 ℃)和高温区域(T>350 ℃). 具体而言, 在PC-SG中, 193, 258和289 ℃处出现的3个低温还原峰分别归属为Pd与高分散Cu2Cl(OH)3物种的共还原、Pd与微晶态Cu2Cl(OH)3物种的共还原以及晶态Cu2Cl(OH)3物种的还原[29]. 结合XRD表征结果, 高温427 ℃处的还原峰可与Cu2P2O7和Cu2(OH)PO4物种的还原相关联[30]. 在PC-HT中, 195和217 ℃处的2个低温还原峰分别归属为Pd与高分散Cu2Cl(OH)3物种的共还原和Pd与微晶态Cu2Cl(OH)3物种的共还原, 351 ℃处的高温还原峰则归属为离子交换形成Cu物种的还原. 图5插图还给出了催化剂PC-HT反应240 min后(PC-HT-U)的H2-TPR结果. 可以看出, 与反应前相比, 反应后催化剂的还原峰峰型和出峰温度并无显著差别, 仅观察到195 ℃处的肩峰变小, 表明部分Cu2Cl(OH)3物种由高分散变为微晶态. 此外, 表3给出了2种催化剂的H2消耗量. 由表3可知, 2种催化剂在低温区域和高温区域的还原峰均具有相近的H2消耗量. 与催化剂PC-SG相比, PC-HT中各个物种的还原峰温度均向低温方向移动, 表明催化剂PC-HT中Pd, Cu物种以及与载体之间存在更强的相互作用, 与XRD表征结果一致. 可见, 相比于PC-SG, PC-HT具有更强的氧化还原性能.

Table 3 H2 consumption of catalysts
2.7 CO2-TPD表征

Fig.6 CO2-TPD profiles of supports and catalysts
图6为HAP载体和Pd-Cu/HAP催化剂的CO2-TPD谱图. 可见, 2种载体均呈现出较微弱的CO2脱附峰, 其中, 载体HAP-HT上的脱附峰位于100~200 ℃之间, 而HAP-SG则在421 ℃处出现了一个小的CO2脱附峰. 从2种载体上CO2脱附情况可看出, HAP-SG较HAP-HT具有更强的表面碱性, 与HAP-SG组成中相对较高的Ca/P比有关. 负载Pd和Cu到载体HAP上后, PC-SG和PC-HT在100~300 ℃和350~450 ℃范围内出现了CO2脱附峰, 表明2种催化剂均存在弱碱性和中强碱性位点[25]. 相比于载体, 2种催化剂上低温处CO2脱附峰面积略有增加, 中高温度处峰的峰面积则显著增强, 同时, 脱附峰温度较载体向高温处移动. 对2种催化剂而言, 低温脱附峰温度区间相差不大, 但PC-SG的中高温脱附峰峰值温度出现在430 ℃处, 较PC-HT相应的脱附峰明显向高温方向移动, 表明PC-SG催化剂较PC-HT具有更强的表面中强碱性. 进一步根据载体和催化剂CO2脱附峰峰面积计算碱性位点数量(表4). 由表4可见, PC-SG上弱碱性位点数量仅有50.9 μmol/g, 但中强碱性位点数量高达416.2 μmol/g. 与PC-SG相比, PC-HT上弱碱性位点数量明显增多, 但中强碱性位点数量则减少. 可见, 2种催化剂上具有类似的碱性位点, 但PC-HT具有更多数量的弱碱性位点和相对较少数量的中强碱性位点[25].

Table 4 Amounts of different basic sites of supports and catalysts
2.8 XPS表征
图7为Pd-Cu/HAP催化剂的Pd3d和Cu2p3/2的XPS谱图. 由图7(A)可见, 在338.1和343.3 eV处的特征峰分别归属于Pd3d5/2和Pd3d3/2, 表明催化剂中Pd物种以Pd2+形式存在[9]. Pd2+物种通常被认为是Wacker催化剂用于吸附和活化CO的活性物种[31]. 图7(B)中, 2种催化剂在约934.7和932.5 eV处出现的特征峰分别归属于Cu2+和Cu+物种[32]. 进一步对Pd3d5/2和Cu2p3/2XPS谱图进行分峰拟合, 并根据XPS峰面积对催化剂表面Pd和Cu物种进行定量分析, 得到PC-SG和PC-HT表面上Cu+/(Cu++Cu2+)原子比分别为0.296和0.365. 与PC-SG相比, PC-HT具有更多表面Cu+物种. 此外, 根据Pd和Cu物种的峰面积和灵敏度因子计算出2种催化剂表面上Pd2+/(Cu++Cu2+)原子比, 得到PC-SG的Pd2+/(Cu++Cu2+)原子比为0.321, 其远高于PC-HT(0.145), 表明PC-SG表面上聚集着更多的Pd2+物种.

Fig.7 XPS spectra of Pd3d(A) and Cu2p3/2(B) of catalysts
2.9 In-situ CO-DRIFTS表征
采用in-situCO-DRIFTS技术测试了室温下CO在Pd-Cu/HAP催化剂上的吸附, 如图8所示. CO在Pd活性中心上具有线式吸附和桥式吸附2种吸附态[33]. 2158 cm-1处的吸附峰归属于线式Pd2+-CO[34], 1939和1998 cm-1处的吸附峰分别归属于桥式Pd+-CO和Pd2-CO[34], 其中, Pd2-CO吸附峰是CO桥式键合在金属态的钯物种引起的. 由图8(A)可见, 随着时间的延长, 2158 cm-1处CO线式吸附峰强度逐渐减弱, 而桥式吸附峰强度变化较小, 表明CO在Pd位点上的桥式吸附态比线式吸附态稳定, 与文献[33]结果一致. 值得注意的是, XPS表征结果显示2种催化剂表面仅存在Pd2+物种, 但原位红外表征结果显示, 通入CO后催化剂表面出现还原态Pd物种(Pd+-CO), 甚至在PC-HT上出现了Pd2-CO吸附峰[图8(B)], 这些还原态Pd物种可认为是室温下CO还原Pd2+物种产生的. 同时, 由图8(C)可知, PC-HT上Pd+-CO吸附峰强度明显强于PC-SG, 表明PC-HT表面更多的Pd2+物种被还原为Pd+物种, 可见相比于PC-SG, PC-HT上Pd2+物种更易于被CO还原. 对于Pd2+和Pd+2种活性中心而言, Pd+-CO吸附峰的位置(1939 cm-1)远低于Pd2+-CO(2158 cm-1), 表明前者吸附态CO的键力常数减小, Pd+对CO存在较强的反馈π键, 因此Pd+较Pd2+具有更强的活化CO能力. Shen等[32]在研究Pd-Cu-Clx/Al2O3催化剂用于CO低温氧化时也发现, 采用NH3配位浸渍法所制催化剂上的Pd+较采用普通浸渍法形成Pd2+的活性更高.

Fig.8 In-situ DRIFTS spectra of CO adsorbed over PC-SG(A), PC-HT(B) and PC-SG and PC-HT(C) at 25 ℃
图8还给出了2种催化剂中Cu物种上CO的原位红外吸附结果. 对于PC-SG而言, 在2127和2136 cm-1处的吸附峰归属为Cu+物种上CO的线性吸附, 分别对应于SI和SII吸附中心[35]. 随时间延长吸附峰强度逐渐减弱, 但SII吸附中心处的2136 cm-1吸附峰强度始终强于SI吸附中心. SII吸附中心上CO振动频率在2136 cm-1处, 接近于气态CO, 表明其与CO作用力较弱. 而2127 cm-1处SI吸附中心由于存在更强的反馈π键, 使得νCO相对降低[36]. 同时可看到, PC-HT上吸附初期只有2136 cm-1处的吸附峰, 随时间延长逐渐分裂为2136和2127 cm-12个吸附峰, 前者强度逐渐降低而后者增强, 表明SII吸附中心数量减小, SI吸附中心数量增多. Wang等[36]利用CO的红外光谱研究了Cu-ZSM-5上Cu+位置时认为, SI位于分子筛两个通道交叉处, 而SII位于分子筛通道壁靠近孔口处, 进一步研究发现SII处的Cu+由于与氧配位不如SI处紧密而更容易被氧化和还原. 对于Pd-Cu/HAP催化剂而言, 根据Cu物种上CO吸附红外光谱特征可认为, SII主要位于催化剂表面, 而SI则位于载体孔道内; 根据2种位点上CO吸附的演变情况并结合文献[36]报道, 可认为Pd-Cu/HAP催化剂上SII不如SI稳定而易被氧化或还原. 由图8(C)可见, PC-HT中Cu+物种上CO吸附峰强度明显强于PC-SG, 且Cu+物种SII吸附中心逐渐偏移至SI吸附中心, 表明PC-HT中不仅存在更多的SII吸附中心, 而且具有更强的氧化还原性质, 与XPS和H2-TPR表征结果一致.
负载型Wacker催化剂用于低温CO氧化反应时, 通常认为在水汽分子参与下Pd2+物种吸附活化CO并将其氧化为CO2, 同时自身被还原为Pd0物种, 然后Cu2Cl(OH)3或CuClOH物种氧化Pd0物种为Pd2+物种, 同时Cu2+物种被还原为Cu+物种, 最后, Cu+物种吸附O2被氧化为Cu2+物种完成催化循环[31,37]. XPS表征结果显示, 活性中心Pd物种仅以Pd2+形式存在于2种催化剂表面, PC-SG较PC-HT表面具有更多的Pd2+物种. 进一步的in-situCO-DRIFTS结果表明, 通入CO后2种催化剂表面均出现Pd2+和Pd+物种的CO吸附峰, 与PC-SG相比, PC-HT表面较多的Pd2+物种被还原为Pd+物种, 且Pd+较Pd2+具有更强的活化CO能力. 可见PC-HT表面较多且具有更强CO活化能力的Pd+物种是其具有高催化活性的首要原因. 对于Cu物种而言, XRD和FTIR结果表明, 2种催化剂上均形成了Cu2Cl(OH)3物种, 且PC-HT中该活性Cu物种含量更高, 这有利于氧化Pd0物种为Pd2+或Pd+物种[8,32]. 同时, 在Wacker催化循环中, 除Cu2+物种之外, 具有较强氧化还原能力的Cu+物种同样至关重要. XPS和in-situCO-DRIFTS结果表明, PC-HT表面上不仅含有大量的Cu+物种, 其中有更多的Cu+物种与氧配位不紧密而更具氧化还原性, 是PC-HT催化活性较高的另一重要原因. 与PC-SG相比, PC-HT较少且相对较弱的表面碱性有利于CO2的脱附, 这也是PC-HT催化剂表现出较高催化活性的原因之一. 基于上述Pd-Cu/HAP催化剂的结构性质, Scheme 1给出了该催化剂的表面模型图和CO催化氧化反应机理. 可见, 除经典的Wacker催化循环外, 部分Pd2+物种被CO还原生成更具有活性的Pd+物种, Pd+物种被CO和H2O分子进一步还原为Pd0物种. 然后Cu2+物种氧化Pd0物种为Pd+物种, 同时Cu2+物种被还原为Cu+物种, 最后, Cu+物种吸附O2被氧化为Cu2+物种, 从而实现催化循环.
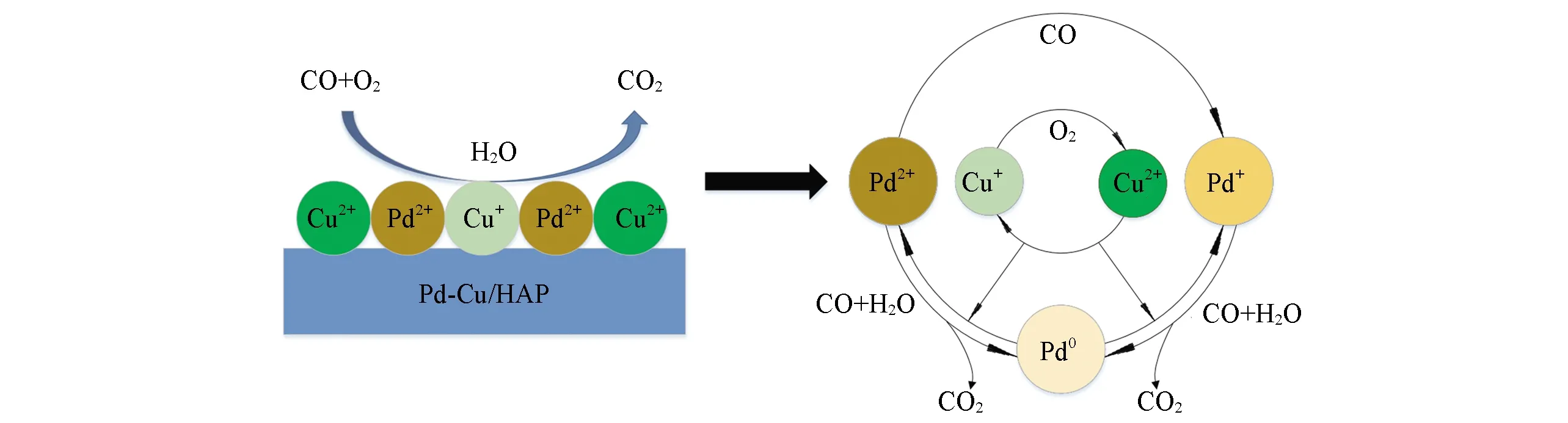
Scheme 1 Proposed surface model and reaction mechanism of CO oxidation for Pd-Cu/HAP
3 结 论
通过溶胶-凝胶法和水热法分别合成了2种HAP载体, 采用浸渍法制备了Pd-Cu/HAP催化剂, 并在连续流动微反装置上考察其对CO常温催化氧化性能. 结果表明, PC-SG和PC-HT均表现出稳定的CO催化氧化活性, 但相比于PC-SG, PC-HT表现出更高的催化氧化性能. 这是由于PC-HT具有更大的比表面积和孔容, 含有更多的Cu2Cl(OH)3物种且与Pd物种和载体直接产生了更强的相互作用; 同时, PC-HT表面易形成具有更强CO活化能力的Pd+物种和更强氧化还原性质的Cu+物种, 对于催化剂建立良好的Wacker循环具有至关重要的作用; 此外, PC-HT较少且相对较弱的表面碱性有利于反应产物CO2的脱附, 从而促进了CO常温氧化反应的进行. 研究结果为继续优化Pd-Cu/HAP催化剂的制备参数以获得常温常湿条件下具有实用价值的CO氧化催化剂奠定了基础.
