阿帕替尼在晚期非小细胞肺癌的临床疗效观察
2020-06-28孙向春刘建刚
孙向春,刘建刚
(1.安徽理工大学附属亳州市人民医院肿瘤科,安徽 亳州 236800;2.东南大学附属中大医院溧水分院肿瘤科,江苏 南京 211200)
肺癌在中国的发病率和死亡率仍然很高[1],并呈逐年上升趋势,治疗难度大,对人类健康和发展造成严重威胁。NSCLS在发现时大部分已处于晚期,5年生存率20%左右[2]。对于晚期肺癌患者,主要治疗方式为放化疗及靶向等综合治疗,当患者无法耐受化疗或者没有可选的基因突变靶向治疗时,除了姑息治疗外,无有效的治疗手段。有研究表明,血管内皮生成因子(vascular endothelial growth factor,VEGF)与肺癌发生密切相关。因此,以新生血管为靶点的抗肿瘤治疗成为近年来研究的热点。阿帕替尼是一种酪氨酸激酶抑制剂(tyrosine kinase inhibitor,TKI),对肿瘤的血管形成具有较好的抑制作用。在肺癌的治疗中已进行一定的临床研究[3]。本研究主要在前人研究基础上对不同临床特征的患者进一步分层分析,观察不同ECOG评分、年龄、性别及是否联合化疗对PFS的影响,以及不良反应及处理。现收集亳州市人民医院2017年9月至2018年9月收治的56例晚期非小细胞肺癌,评价阿帕替尼的临床疗效及安全性。
1 资料和方法
1.1 一般资料
本研究对象为亳州市人民医院收治的晚期非小细胞肺癌患者56例,所有患者过去均接受过化疗或表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)类靶向治疗。其中纳入标准:1)年龄≥18岁,男女不限;2)经病理学或细胞学诊断的非小细胞肺癌患者;3)东部肿瘤协作组织(ECOG)评分:0~2分,预计生存期≥12周;4)主要器官功能正常;5)血生化、肝肾功能无明显异常。排除标准: 1)怀孕或哺乳期妇女; 2)Karnofsky 评分小于60 分; 3)主要器管受累;4)高血压控制不佳;5)有出血倾向、凝血异常,或正在接受溶栓或抗凝治疗;6)6个月内有消化道出血史(如局部活动性溃疡病变,大便隐血以上+);7)初次应用研究药物前1月内出现肺出血(>CTCAE 2),首次用药前1月内出现其它部位出血(≥CTCAE 3级)。依据肿瘤标志物及影像学检查综合评估病情,患者基本情况见表1。患者中男性38例,女性18例,年龄49~80岁,中位年龄67岁;阿帕替尼联合用药9例(1例吉西他滨+卡铂、2例单药替吉奥、2例顺铂、1例培美曲塞+洛铂、1例吉西他滨+顺铂、1例单药多西他赛、1例联合艾克替尼),单药47例,如表1所示。
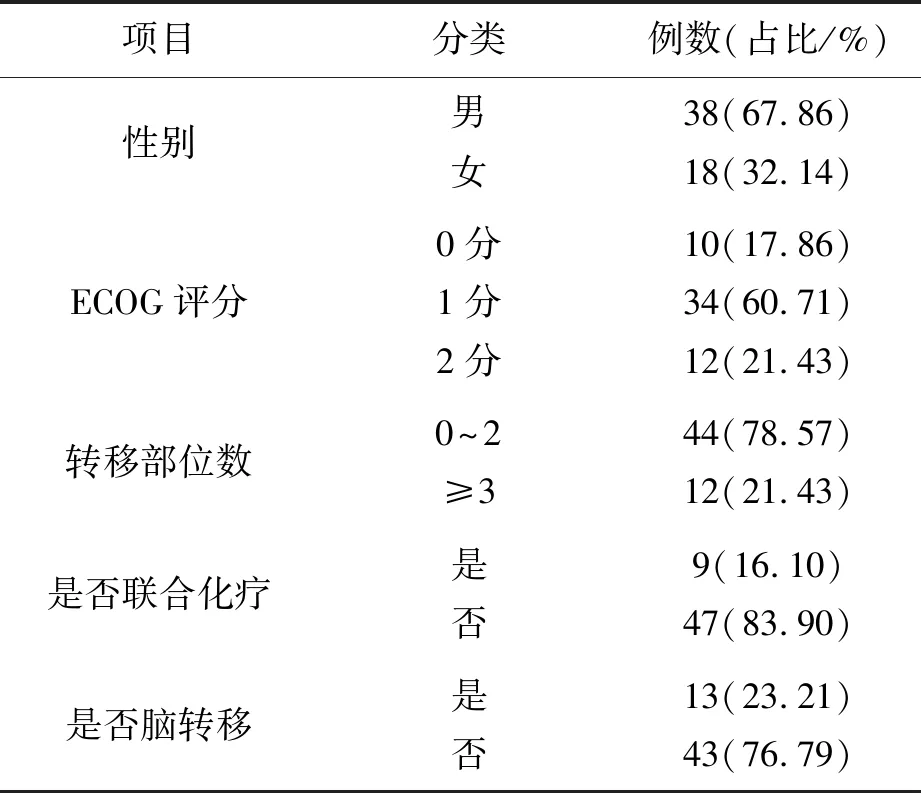
表1 患者临床特征
1.2 方法
患者口服剂量500mg/d甲磺酸阿帕替尼片(江苏恒瑞药业有限公司,国药准字:H20140103),根据患者意愿及病情加或不加化疗,之后每6周进行一次评估(影像学标准RECIST1.1和肿瘤标志物),直到病情进展(PD)或出现严重的不良反应,如果出现于阿帕替尼相关的Ⅲ度及以上不良反应可暂停药物或减量应用。本研究通过医院伦理委员会批准。
1.3 观察指标与评价
主要观察指标:PFS,从治疗开始直到疾病的进展或出现不可耐受的不良反应的发生时间,根据RECIST1.1版进行疗效评估:完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)、疾病进展(PD)。
客观观察指标:总缓解率(ORR),(CR+PR)/病例总数×100%;疾病控制率(DCR),(CR+PR+SD)/病例总数×100%。
对比患者治疗前后癌胚抗原(CEA)、细胞角蛋白 19 片段(CYFRA211)、血管内皮生长因子(VEGF) 等指标。不良反应评估参照美国国立癌症研究所制定的评价标准,随访截止时间2019年1月。
1.4 统计方法
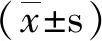
2 结果
2.1 治疗效果
56例患者中6例因严重不良反应而停药,50例可疗效评价。给予阿帕替尼治疗后,CR,0例;PR,8例;SD,26例;PD,16例;ORR为16%,DCR为68%。患者的平均 PFS为3.14月(见表2)。
表2 50例晚期NSCLC患者预后情况
2.2 生存情况
不同临床特征受阿帕替尼治疗的患者ECOG0~1分中位PFS为4.7月,95%CI(3.662~5.738),2分患者PFS为1.7月, 95%CI(1.409~2.351)(P=0.007)差异有统计学意义(见图1)。
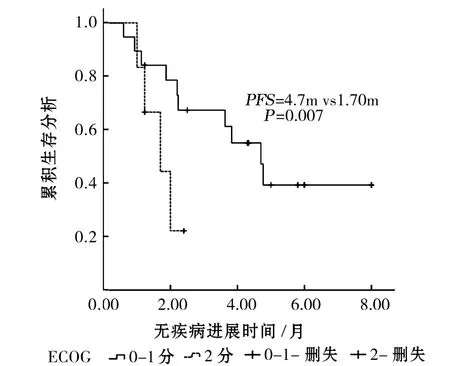
图1 ECOG评分对疗效的影响
2.3 性别、年龄、是否联合化疗均无统计学意义(P>0.05 )(见表3)。
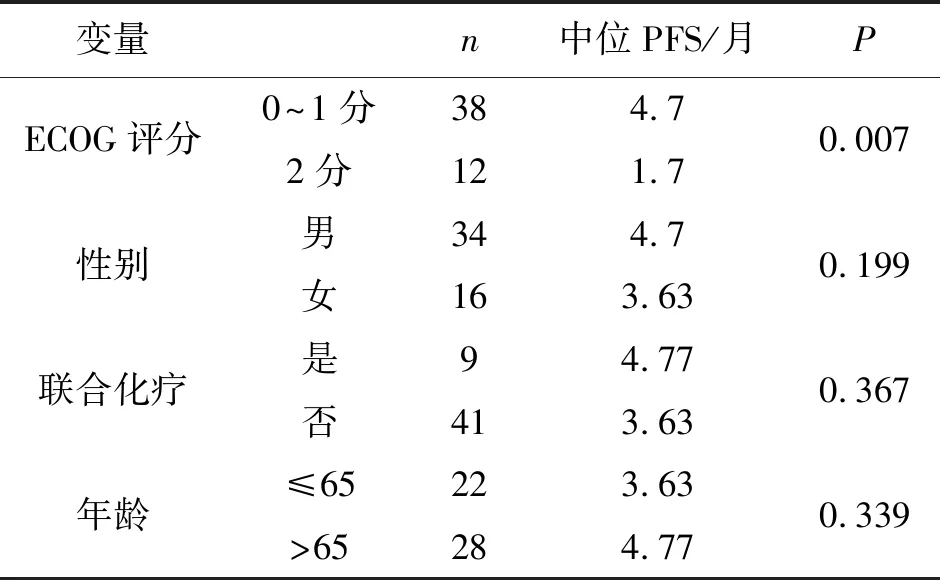
表3 不同临床特征治疗后中位PFS比较
2.4 血肿瘤标志物变化情况(见表4)。
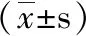
表4 晚期NSCLC治疗前后血肿瘤标志物变化
2.5 不良反应
治疗过程中常见不良反应为高血压、蛋白尿、手足综合征、乏力等,暂停用药并对症治疗后症状均获缓解。1例因胃肠道反应停药、2例因痰中带血、2例咯血家属要求停药、1例因摔伤且出现黑便停药。本研究未发现4级或更高治疗相关的不良事件,也未发现意外的不良事件(见表5)。
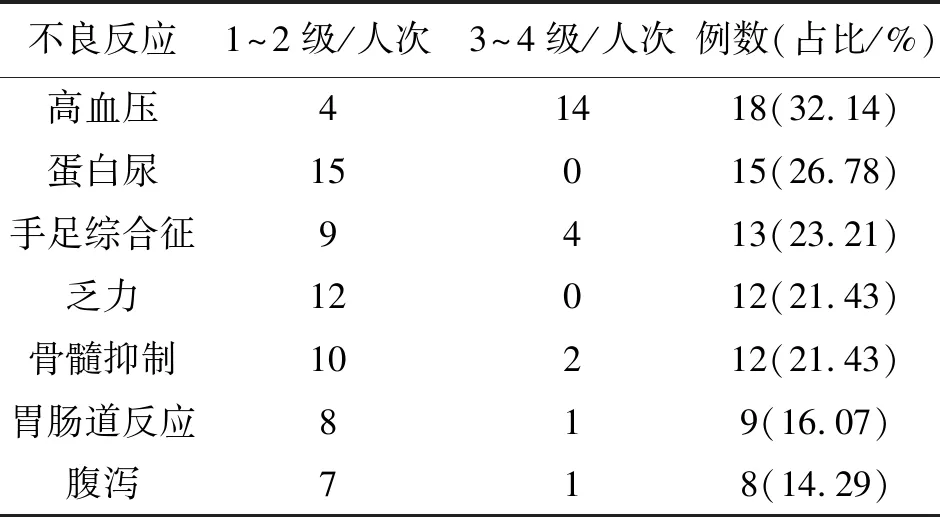
表5 患者不良反应发生情况
3 讨论
肺癌是世界上最常见的恶性肿瘤之一,目前晚期NSCLC治疗一般采用化疗或分子靶向治疗。由于患者化疗耐药或针对EGFR靶点的靶向药物耐药,抗血管生成药物正在发挥越来越重要的作用。Folkman教授于1971年提出了“肿瘤的生长依赖于血管的生成,抑制血管生成是一种治疗肿瘤的策略。”的观点。
肿瘤血管生成以不受控制和无序的方式进行的,它为肿瘤生长提供必要的氧气、生长因子和营养。VEGF信号通路被认为是肿瘤血管生成的重要途径,血管内皮生长因子受体(VEGFR)是在酪氨酸激酶诱导下的病理性血管生成的主要信号转导因子。因此,它被认为是治疗癌症的一个目标。VEGFR家族蛋白包含VEGFR-1、VEGFR-2、VEGFR-3 等。其中,VEGR-2是VEGF促进血管生成信号的主要中间介质。因此,阻断VEGFR-2信号通路是抑制肿瘤血管生成的新靶点[4-5]。一些药物在晚期非小细胞肺癌中抑制肿瘤血管生成的临床疗效已经得到证实,这些药物包括贝伐单抗、雷莫鲁单抗、安罗替尼、尼达尼布、呋喹替尼等。
阿帕替尼是我国第一种完全自主产权研发的抗癌药,甲磺酸阿帕替尼片主要作用通过抑制 VEGFR-2 与 VEGF 的结合,同时包括之后发生的 VEGFR-2 的自动磷酸化过程,可致酪氨酸激酶激活失败,从而发挥疗效抑制VEGFR-2进而抑制肿瘤生长活性[6-7]。研究表明,阿帕替尼在多种恶性肿瘤的治疗中取得较好的疗效[8-11]。
我国晚期或转移性胃癌患者在二期和三期临床试验中证实了阿帕替尼的疗效及安全性[12-13],2014年国家卫生管理局批准使用晚期胃或胃-食管结合部腺癌[14]。 在2014年ASCO年会上公布了治疗晚期非小细胞鳞状细胞癌的二期临床试验,取得了较好的效果,ORR和DCR分别为12.2%和68.9%,平均PFS为4.7月[15],该结果反映了阿帕替尼在非小细胞肺癌应用中具有广阔的前景。在本研究中,阿帕替尼也取得了较好的疗效,其中ORR为16%和DCR为68%,平均PFS为3.14月。 而且本研究根据患者的临床特征进一步分析,发现患者的中位PFS受治疗前患者ECOG评分影响较大,ECOG评分2分的患者的中位PFS显著低于0~1分的患者(P=0.007),而性别、年龄、是否联合化疗对患者的中位PFS并无影响,这也提示在今后的治疗中要更加关注患者的一般体力状况评分。治疗后患者的肿瘤标志物CEA、CYFRA211明显下降,可以作为阿帕替尼治疗患者的疗效评价参考指标。而VEGF下降不明显,可能是因为VEGF生成和作用机制较复杂,除了肿瘤患者可能升高外,炎症、凝血功能改变等因素均可引起VEGF变化。阿帕替尼应用中出现的主要副作用有高血压(32.14%)、蛋白尿(26.78%)等,与文献[16]报道一致,经过积极处理后一般都可恢复。
本研究结果显示,阿帕替尼应用于非小细胞肺癌毒性作用小、疗效较好、价格合理、患者依从性好,阿帕替尼可作为晚期NSCLC替代靶向治疗。本研究由于入组病例较少、研究时间短,对于阿帕替尼联合化疗或其他分子靶向药物的疗效需要进一步探讨。
