菠萝蛋白酶金纳米簇模拟酶活性比色法检测Hg2+
2020-06-15刘士蒙李嘉倩吕昌银刘然李诗雅杨桂英
刘士蒙,李嘉倩,吕昌银,刘然,李诗雅,杨桂英
(南华大学 公共卫生学院 衡阳市健康危害因子检验检疫新技术研究重点实验室,湖南 衡阳 421001)
近年来,纳米材料的快速发展为开发人工模拟酶提供了新思路[1]。纳米酶广泛应用于免疫测定和生物传感器等领域。其中,金纳米团簇,由于其毒性低,生物相容性好,催化性能优异,已被广泛用于生物检测[2]。菠萝蛋白酶(Bromelain)属于巯基蛋白酶,是一种植物源性蛋白质[3-4],是制备金属纳米团簇的理想模板,且很少应用于纳米材料合成。
Hg(II)离子通常被认为是毒性很强的重金属离子,严重危害人类健康和生活环境。因此,Hg2+的灵敏检测对于监测水环境非常重要,已经开发了高效液相色谱法[5]、原子吸收光谱法、ICP-MS法、冷蒸气原子荧光光谱法[6]等来检测Hg2+。然而,这些方法仪器昂贵,样品制备过程耗时、复杂,限制了在现场分析中的应用。
本文建立了检测环境水样中Hg2+的新型比色传感新方法,具有低成本、高选择性、简便等优点,并成功应用于环境水样中Hg2+的检测。目前,没有发现单独使用菠萝蛋白酶作为模板合成金纳米簇,利用其模拟酶活性检测金属离子的报道。
1 实验部分
1.1 试剂与仪器
菠萝蛋白酶(Bromelain)、氯金酸(HAuCl4)、汞标准溶液(100.0 μg/mL)、3,3′,5,5′-四甲基联苯胺(TMB)、双氧水均为分析纯;实验用水均为灭菌超纯水(电阻为18.25 MΩ·cm)。
UV-2550紫外-可见分光光度计;THERMO-SHAKER恒温混合器;Titan G2 60-300透射电子显微镜;K-Alpha 1063 X射线光电子能谱仪;HGG-1102远红外线鼓风干燥箱。
1.2 Bromelain-AuNCs的合成
取90 μL HAuCl4溶液(10 mmol/L)和400 μL菠萝蛋白酶溶液25 mg/mL(pH 8.0),充分混合,室温孵育5 min;然后加入45 μL NaOH溶液(1 mol/L),在恒温孵育仪中37 ℃、800 r/min继续孵育12 h,合成Bromelain-AuNCs。
1.3 Hg2+标准系列的紫外分光光度检测方法
在2 mL EP反应管中,依次加入pH=3.75,200 mmol/L 的NaAc-HAc缓冲液100 μL,Bro-AuNCs 25 μL,5 mmol/L TMB 30 μL,100 mmol/L H2O2110 μL以及不同浓度的Hg2+标准溶液,充分混匀后,于 37 ℃恒温混匀仪中反应 45 min。再加入 200 mmol/L H2SO4终止液 80 μL,用紫外-可见分光光度计比色测定,记录体系在450 nm波长处的吸光度值。
1.4 环境水样中Hg2+的测定
分别采集湘江水、池塘水、自来水环境水样,水样经定量滤纸过滤 3次后,置于电炉上加热煮沸持续15 min。静置冷却,使用0.22 μm微孔滤膜过滤,用1.3节的分析方法测定环境水样中的Hg2+。
2 结果与讨论
2.1 金纳米簇的表征



图1 体系紫外-可见吸收光谱和荧光光谱(A)和Bro-AuNCs 在5个月内的荧光稳定性(B)Fig.1 The UV-visible absorption and fluorescencespectra of the system of Bro-AuNCs(A) and thefluorescence stability of Bro-AuNCs within 5 months(B)
2.1.2 傅里叶变换红外光谱表征 傅里叶变换红外光谱测定结果见图2。

图2 菠萝蛋白酶和菠萝蛋白酶金纳米簇的傅里叶变换红外光谱图Fig.2 Fourier transform infrared spectrum ofbromelain and bromelain-AuNCs
由图2可知,1 600~1 700 cm-1为蛋白酶的酰胺Ⅰ谱带,其中1 629 cm-1为蛋白酶α螺旋部分的特征峰,由Bromelain稳定的金纳米簇在1 631 cm-1的特征峰有较为明显的增强,1 631.78 cm-1的特征峰位移到1 629.85 cm-1,1 000~1 200 cm-1的特征吸收峰消失,表明金纳米簇的形成主要和蛋白酶的α螺旋结构有关,蛋白质的二级结构发生了改变[9]。已有研究把酰氨Ⅰ带主要归属于C—O键伸缩振动及肽键的C—N伸缩振动。2 304 cm-1左右的 —SH特征吸收峰在金纳米簇中明显增强,表明了蛋白酶的 —SH与Au形成了Au—SH键。
2.1.3 TEM测试和XPS表征 本实验进一步用透射电子显微镜(TEM)测试表征了Bro-AuNCs的形貌和结构,由图3A表明,AuNCs呈球形,分布均匀,通过软件分析,AuNCs的粒径为0.9~2.8 nm,平均粒径(1.7±0.3)nm。X射线能量色散光谱(EDX)结果(图4A)表明,该物质主要元素为Au元素,与文献报道AuNCs的特征一致[10]。X射线光电子能谱(XPS)研究(图4B)表明,金的4f频谱被分成两个峰,结合能分别为84.02,84.77 eV,分别对应零价金和一价金,表明反应中生成了Au0和Au+,由金纳米簇的拟合数据可以看出,主要形成了Au0。




图3 TEM测试图和粒径分布图Fig.3 The TEM images and the picture size distribution figureA.Bro-AuNCs TEM;B.Bro-AuNCs粒径分布;C.Bro-AuNCs+Hg2+TEM;D.Bro-AuNCs+Hg2+粒径分布
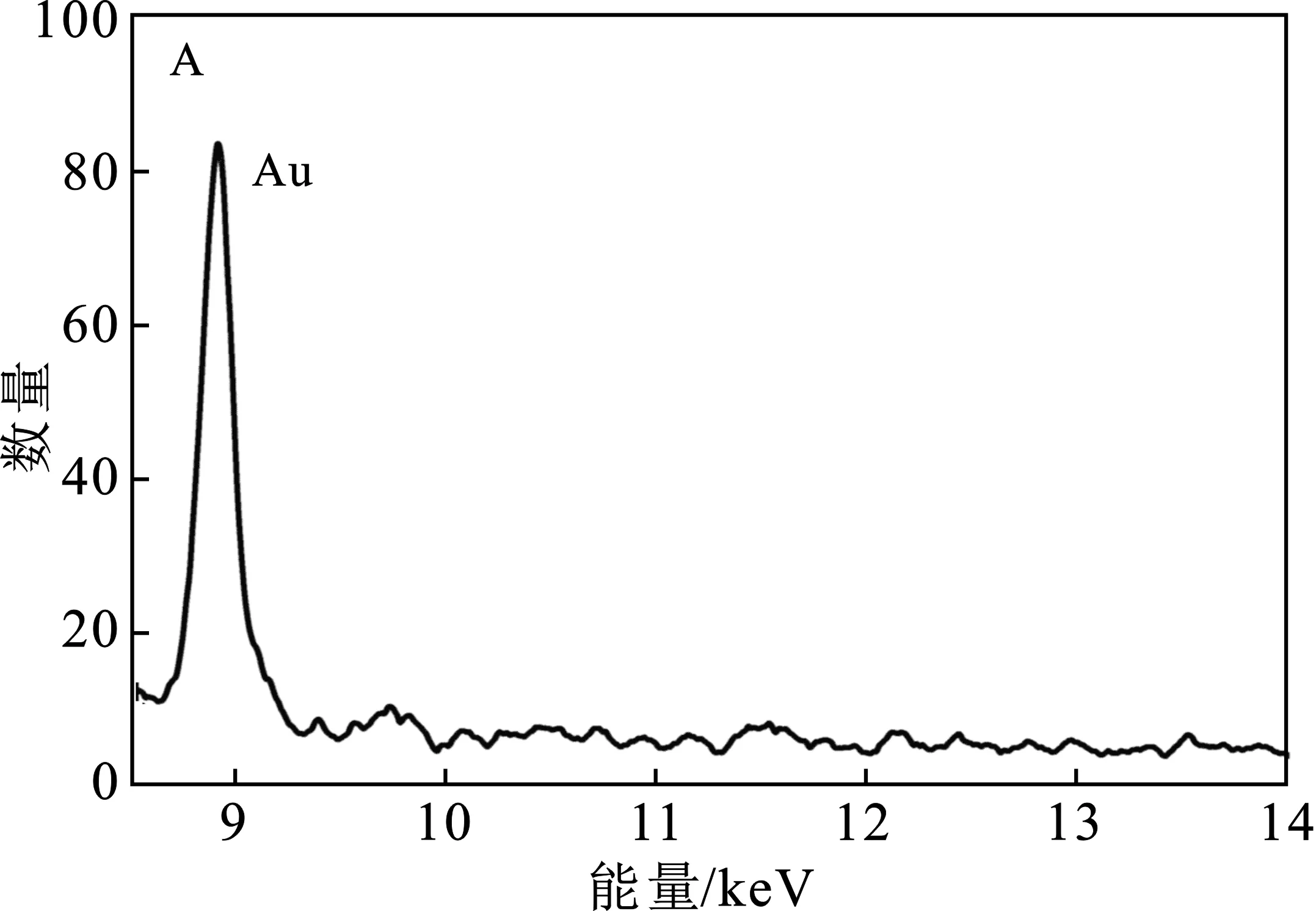

图4 金纳米簇的X射线能量色散光谱图(A)和X 射线光电子能谱图(B)Fig.4 The EDX spectrum(A) and XPSspectrum(B) of Bro-AuNCs
2.2 实验原理
构建了一种汞抑制 Bro-AuNCs模拟过氧化物酶活性新型比色传感新方法,实验原理见图5。

图5 基于Bro-AuNCs-TMB-H2O2体系检测Hg2+示意图Fig.5 Schematic diagram of detection of Hg2+ ions based on Bro-AuNCs-TMB-H2O2 system
由图5可知,Bro-AuNCs具有较高的过氧化物酶活性,当体系中存在Hg2+时,由于AuNCs表面Au+与Hg2+之间的高亲和力金属亲和作用,Hg2+会增大AuNCs的粒径并使其发生团聚,大大降低AuNCs的催化能力,使Bro-AuNCs体系颜色从蓝色转变为无色。通过测定加入Hg2+后体系吸光度值的改变量(ΔA),可以计算出汞离子的含量,在一定汞离子浓度范围内,ΔA值与汞离子浓度之间的定量关系为ΔA=Kc。据此,本文建立了基于Bro-AuNCs比色传感法定量测定Hg2+的新方法。
2.3 Hg2+抑制Bro-AuNCs介导的催化显色反应机制探讨
首先通过紫外-可见吸收光谱对加入 Hg2+后Bro-AuNCs的酶活性变化进行验证(图6A曲线a~f)。TMB溶液(曲线 a)和 H2O2-TMB溶液(曲线b)体系在450 nm 处都没有明显的吸收峰。在 Bro-AuNCs体系中,TMB-H2O2显色反应增强,A450显著增强(曲线f),这表明本研究合成的Bro-AuNCs具有较高的过氧化物酶活性;当加入Hg2+后,Bro-AuNCs-Hg2+-TMB-H2O2体系的A450值显著降低(曲线e)。这一现象可能是由于Hg2+与Bro-AuNCs发生了相互作用后,Bro-AuNCs的过氧化物酶活性减弱,从而抑制TMB氧化显色。
进一步探讨了各体系在 60 min内的时间动力学曲线(图6B),TMB-H2O2体系显色随时间增加而增强(曲线g)。当加入Bro-AuNCs后,A652吸光度值显著增强,表示Bro-AuNCs显示出较高的类过氧化物酶活性催化TMB 氧化显色(曲线i)。当加入 Bro-AuNCs和Hg2+后,0~3 000 s 内显色反应缓慢被抑制;3 000 s后,显著小于 TMB-H2O2体系(曲线h)。TEM测试结果(图3)表明,当体系中加入Hg2+后,Bro-AuNCs的平均粒径由原本的2 nm增大到7.5 nm左右。这进一步确证了由于AuNCs表面Hg2+和Au+之间的高亲和力金属亲和作用,Hg2+诱导AuNCs的粒径增大并使其团聚,抑制其过氧化物酶活性。

图6 不同体系中紫外吸收图谱(A)和体系中60 min内吸光度-时间曲线(B)Fig.6 The UV absorption spectrum mechanism ofdifferent systems(A) and absorbance-time curvein 60 min of the system(B)
2.4 共存物质影响


图7 不同金属离子对测定体系吸光度值的影响Fig.7 The effect of different interfering ions on the absorbance value of the measurement system
2.5 标准曲线、检出限与精密度
在优化后的实验条件下,配制Hg2+标准系列溶液进行定量分析实验,建立了测定Hg2+的标准曲线,见图8。


图8 Bro-AuNCs-TMB-H2O2-Hg2+传感系统的比色图、荧光光谱图和标准曲线图Fig.8 The visual observation(A),fluorescencespectrum(B) and calibration curves(C) of theBro-AuNCs-TMB-H2O2-Hg2+ sensing system
由图8可知,当Hg2+浓度在 6.25×10-9~3.5×10-6mol/L时,A450的吸光度值随着Hg2+浓度的增加而逐渐降低,溶液颜色逐渐减弱,由蓝色转变为浅蓝色。此时,体系中吸光度差值ΔA与Hg2+浓度之间呈现良好的线性关系,回归方程为ΔA=0.000 7+0.191cHg(II),相关系数r=0.996,经LOD=3Sb/k 计算,检出限为 4.3×10-3μmol/L。对汞离子浓度为0.2,1.75,3 μmol/L的三种标准溶液分别进行11次平行测定,相对标准偏差分别为0.65%,0.85%,3.0%,方法精密度良好。
2.6 环境水样分析
按照标准采样方法分别采集了5个不同来源的环境水样,对样品实施煮沸、过滤等预处理操作,按照测定Hg2+的方法分别测定 5 个环境水样中汞的含量。随后,采用真实样品中添加标准溶液的方法,对5个环境水样中分别添加浓度为0.375,1.75,3 μmol/L 的汞标准溶液进行加标回收实验,每个样品平行测定11次,结果见表1。
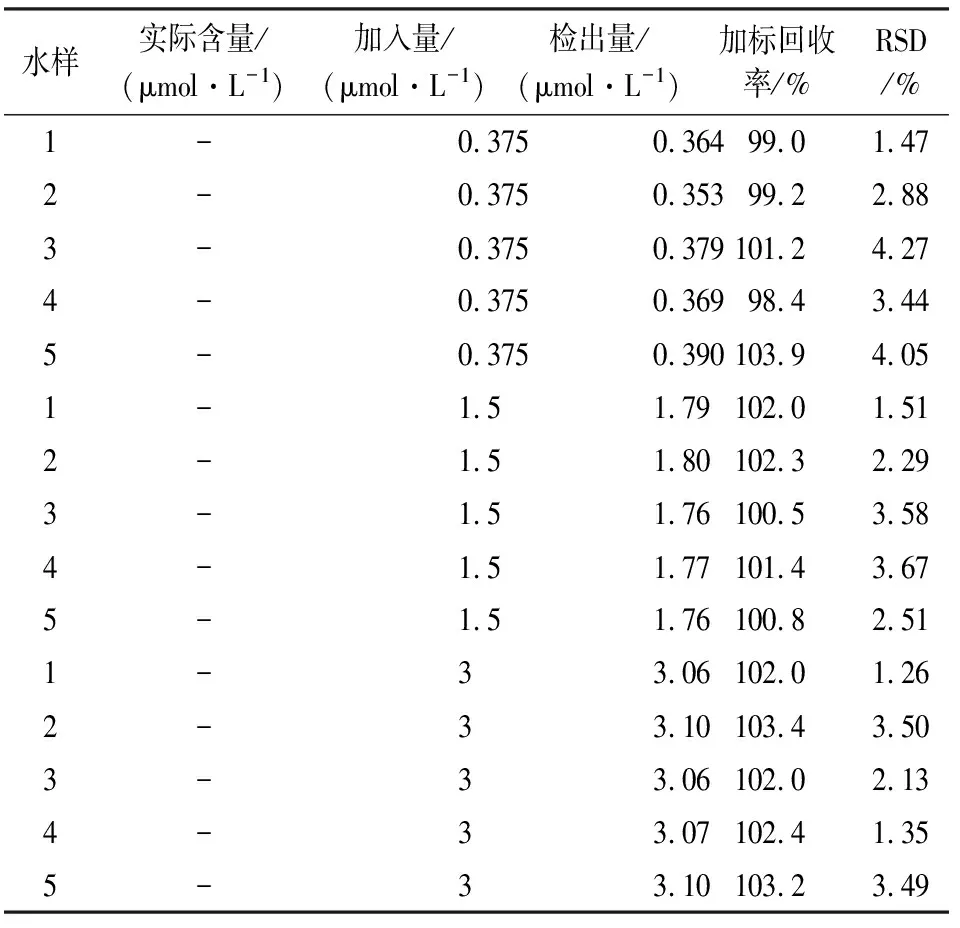
表1 环境水样中 Hg2+ 的加标回收率Table 1 Actual measurement and analysis of Hg2+ inenvironmental water samples
注:1.湘江水(上游);2.湘江水(中游);3.湘江水(下游);4.池塘水;5.实验室自来水。
由表1可知,Hg2+的测定加标回收率为98.36%~103.95%,以上结果表明本方法可用于实际环境水样中Hg2+的检测,具有实际应用价值。
3 结论
制备了一种具有优良的荧光特性、较高的过氧化物酶活性的菠萝蛋白酶金纳米簇材料(Bro-AuNCs),能够代替天然酶,有效提高了稳定性,可应用于生物传感领域。Hg2+能有效抑制Bro-AuNCs过氧化物酶活性,据此建立了高灵敏、高选择性测定环境水样中 Hg2+的比色传感平台。本文进一步探讨了Hg2+抑制Bro-AuNCs介导的催化显色反应机制,为新型蛋白质-金纳米簇的合成提供了新思路和新依据;拓宽了纳米材料模拟酶的应用。本方法操作简单、灵敏、检测效率高,有望在环境检测、生物医学、生物传感等领域广泛应用。
