丝瓜络改性方法及其对水中痕量多环芳烃的吸附特征
2020-06-15王天杰苏丹李雪普聿王鑫
王天杰,苏丹,李雪,普聿,王鑫
(1.辽宁大学 环境学院,辽宁 沈阳 110036;2.沈阳大学 区域污染环境生态修复教育部重点实验室,辽宁 沈阳 110044)
多环芳烃(PAHs)由于致癌、致畸、致突变的作用,被列入对生态系统和人类健康危害最大的化合物列表[1],美国环保总局(EPA)等也把PAHs列为优先监测污染物中的一类[2]。PAHs主要通过废水排放、废物沥滤、意外排放、大气沉降和扩散源等进入水体,因疏水性、低溶解性、难降解性及长距离迁移性,在自然水体中以痕量浓度广泛分布[3]。我国大部分地表水已经被PAHs污染[4-6],增加了PAHs通过水介质进入人体的可能性。
去除水环境痕量PAHs的方法主要包括生物降解法、植物修复法、紫外线光解法、吸附法、高级氧化法和化学去除法等[7]。由于PAHs的低溶解性,一些传统方法如光催化[8]、超声催化[9]、臭氧氧化[10]等对痕量PAHs的去除效果并不理想,而吸附法尤其是生物质吸附是一种有效方法,具有成本低、去除效率高、易于操作、易于回收等优点,成为处理环境中痕量PAHs的主要方法[11-13]。而丝瓜络是一种天然、低成本、无毒、可生物降解的材料,在地球上有着惊人的储存量,近年来成为国内外学者的研究重点和热点之一[14-18]。
本实验选择研究了改性丝瓜络对水中痕量PAHs菲(Phe)和芘(Pyr)的吸附特征,对水中痕量PAHs的去除提供理论依据。
1 实验部分
1.1 试剂与仪器
丝瓜络,购自中国科学院沈阳生态站;菲(Phe)、芘(Pyr)、丙酮、生物抑制剂(氯化钙、叠氮化钠)均为分析纯;乙腈,色谱纯。
MLS-3780高压蒸汽灭菌器;KQ5200DE超声清洗机;TDL-5-A离心机;TQZ-312台式全温振荡器;Agilent1100高效液相色谱仪,色谱柱为C-18柱。
1.2 丝瓜络改性
条状丝瓜络用蒸馏水冲洗除去灰尘,于65 ℃烘干。粉粹过筛(40目),得到丝瓜络粉末,记为UM。
1.2.1 碱化 于30%的NaOH溶液回流碱化 24 h。过滤,蒸馏水冲洗至中性,65 ℃烘干,记为AL。
1.2.2 酸解 用6 mol/L盐酸溶液回流24 h,过滤,蒸馏水冲洗至中性,65 ℃烘干,记为AH。
1.2.3 高压高温改性 130 ℃、0.125 MPa下改性5 h。蒸馏水冲洗,120 ℃下烘干,记为HC。
采用扫描电子显微镜(SEM)观察表面特征,傅里叶红外光谱仪进行红外表征。
1.3 丝瓜络对水中痕量PAHs的吸附
精确称取1 mg固体Phe、Pyr,放入两个烧杯中,加入丙酮,直至Phe、Pyr完全溶解。将溶液转置于1 000 mL容量瓶中,定容,配制初始浓度为1 mg/L Phe、Pyr两种水-丙酮溶液。
实验每个溶液设置4组,每组3个重复。将以上两种溶液分别加入250 mL锥形瓶中,每组各100 mL,加入生物抑制剂,调节pH=7,并分别加入吸附剂丝瓜络UM、AL、AH、HC(固液比为1∶2 mg/g)。在室温、避光条件下,以100 r/min振荡,每隔1 h取样。
1.4 PAHs测试
将样品离心10 min(3 000 r/min),取500 μL上清液与500 μL乙腈混合,使用高效液相色谱仪测定溶液中PAHs的浓度。测定条件:进样量为10 μL,流动相为乙腈和水,其体积比为85∶15,流速0.5 mL/min,柱温为35 ℃,两种PAHs均在其各自的检测波长下测定。
2 结果与讨论
2.1 丝瓜络表征
2.1.1 SEM 4种丝瓜络的SEM表征见图1。

图1 4种丝瓜络的SEM照片Fig.1 SEM photograph of four loofahsUM.未改性丝瓜络;AL.碱化丝瓜络;AH.酸解丝瓜络;HC.高温高压处理丝瓜络(×500倍)
由图1可知,未改性的丝瓜络UM,表层的木质素较厚,且粗糙,具有较大的比表面积;碱处理的丝瓜络AL,木质素被去除,表面光滑,且表面褶皱多于UM[15];酸处理的丝瓜络AH,表面褶皱明显减少,吸附面积减小,可能是由于酸破坏了丝瓜络的组织结构,使其比表面积减小;经高温高压改性后的丝瓜络HC,表面褶皱明显多于其他三个,表面积显著增大,吸附能力增强,可能是由于高温高压使丝瓜络中木质素受热降解,从而失去强度。
2.1.2 FTIR 4种丝瓜络在4 000~400 cm-1处的红外光谱图见图2。
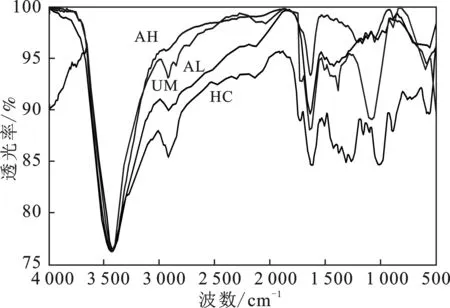
图2 4种丝瓜络的红外图谱Fig.2 Infrared spectrum four of loofahsUM.未改性丝瓜络;AL.碱化丝瓜络;AH.酸解丝瓜络;HC.高温高压处理丝瓜络

2.2 丝瓜络对Phe与Pyr的吸附量
由图3A可知,4种丝瓜络对Phe的吸附曲线走势大体一致。在第1 h内,4种丝瓜络吸附速率均最快,其中HC吸附速率最高,达0.911 3 μg/(mg·h);随后吸附速率均逐渐降低,10 h后,吸附均达到了饱和,UM、AL、AH、HC饱和吸附量分别为1.325,1.351,1.253,1.626 μg/mg,其中HC对Phe的饱和吸附量最大。
由图3B可知,对比Phe,4种丝瓜络对Pyr的吸附曲线走势更加相似。在第1 h内,4种丝瓜络吸附速率均最快,其中HC吸附速率最高,达1.145 μg/(mg·h);在2~3 h内,HC平均吸附速率0.187 4 μg/(mg·h)高于其他三种(UM为0.176 9 μg/(mg·h),AL为0.176 3 μg/(mg·h),AH为0.184 8 μg/(mg·h));5 h后吸附速率趋于平稳,12 h后吸附达到饱和,UM、AL、AH、HC饱和吸附量分别为1.777,1.799,1.689,1.886 μg/mg,其中HC对Pyr的饱和吸附量最大。
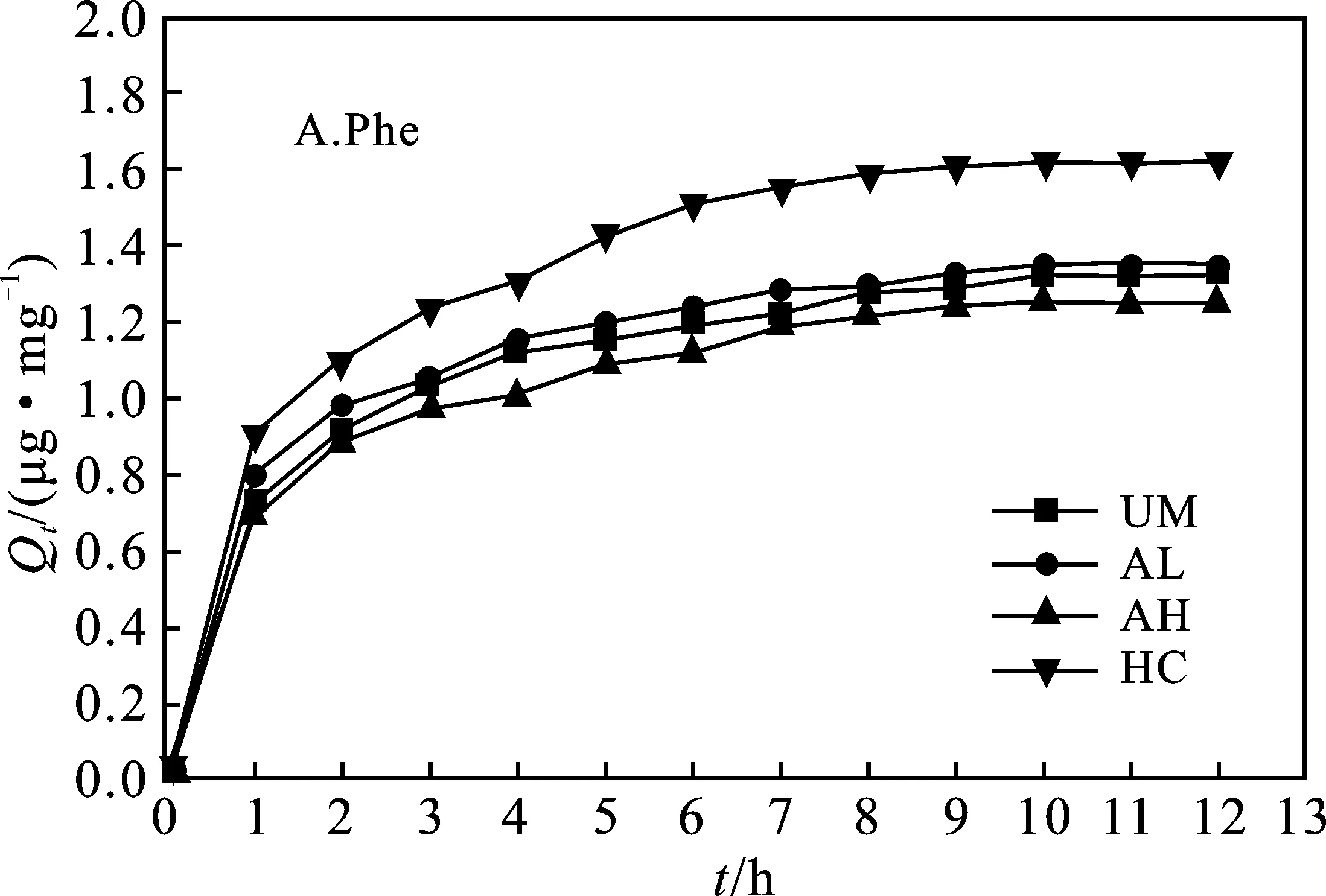
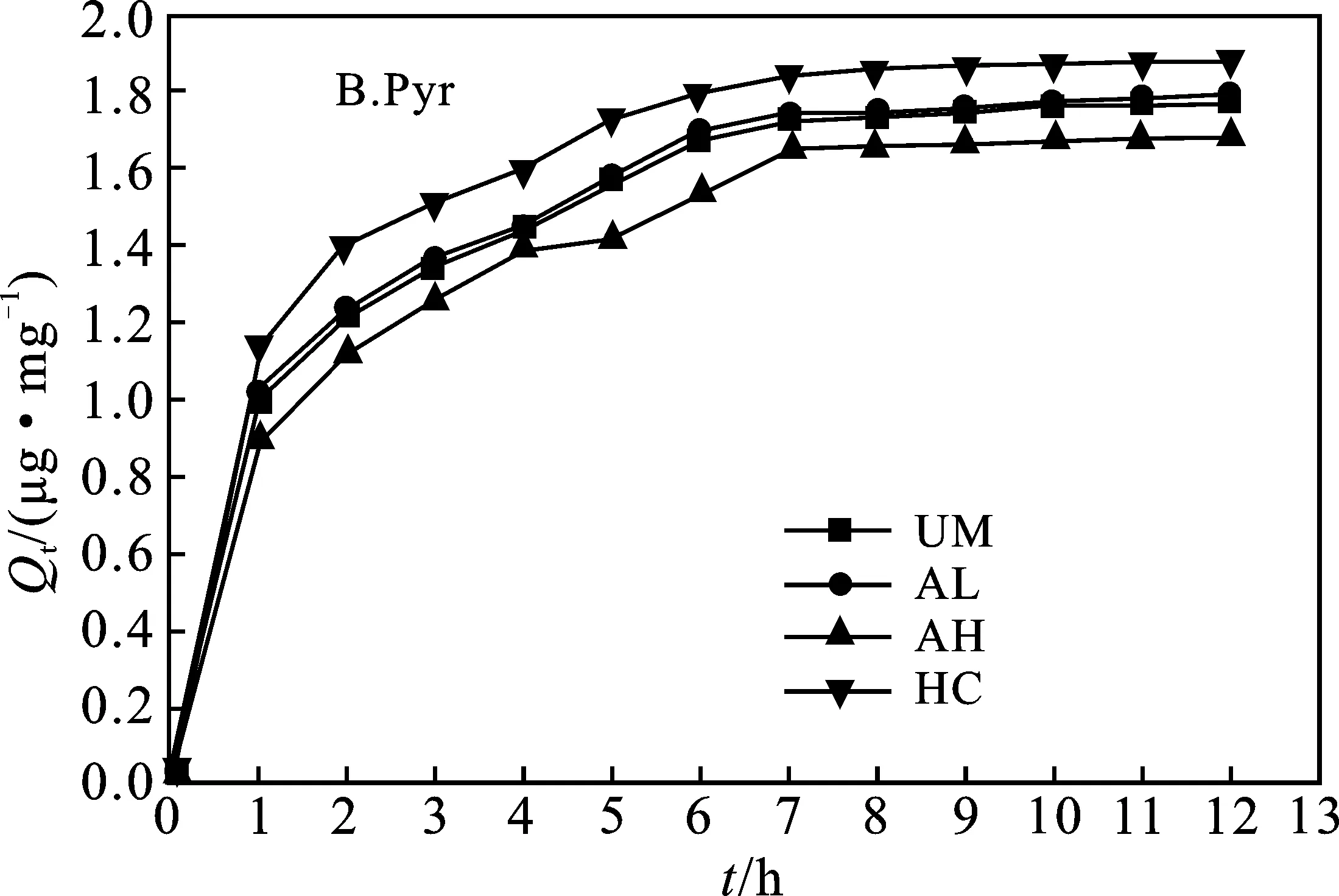
图3 不同处理的丝瓜络对Phe和Pyr的吸附量随时间变化的关系Fig.3 Relationship between the adsorption amount offour loofahs on phenanthrene and pyrene with time
由上可知,AH处理的丝瓜络对Phe、Pyr的饱和吸附量最小,可能由于稀盐酸对丝瓜络表面官能团及纤维素的腐蚀,导致褶皱减少,空隙堵塞,使得比表面积减小,导致丝瓜络对Phe、Pyr的吸附量减少,表明不能利用酸处理的方式对丝瓜络改性[22]。AL处理的丝瓜络,对Phe、Pyr的饱和吸附量高于UM处理,可能由于碱去除丝瓜络纤维表面的蜡质等憎水组分,同时脱除半纤维素及木质素,增大表面粗糙程度[23-24],比表面积增大,从而使得碱化丝瓜络吸附能力大于未改性丝瓜络的吸附能力[25]。HC处理的丝瓜络对Phe、Pyr的饱和吸附量最大,可能由于升高温度提高了生物炭的孔隙度[26],增加了其比表面积,同时,表面生成了大量的官能团,从而使其吸附能力增强[27-28]。
2.3 丝瓜络对Phe与Pyr的吸附动力学
采用准一级动力学方程和准二级动力学方程对丝瓜络的吸附过程进行拟合,结果见图4、图5和表1、表2。
准一级动力学方程:
(1)
ln(Qe-Qt)=lnQe-k1t
准二级动力学方程:
(2)
式中Qt——t时间吸附量,μg/mg;
Qe——平衡吸附量,μg/mg;
k1——准一级吸附速率常数,h-1;
k2——准二级吸附速率常数,μg/(mg·h)。


图4 4种丝瓜络对Phe吸附动力学曲线Fig.4 Adsorption kinetics curves of four loofahs on Phe
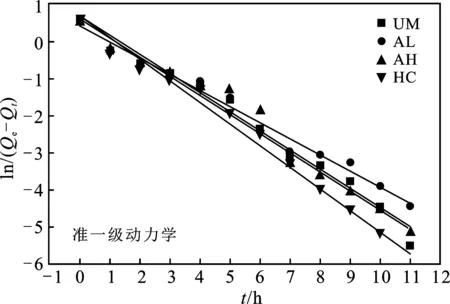
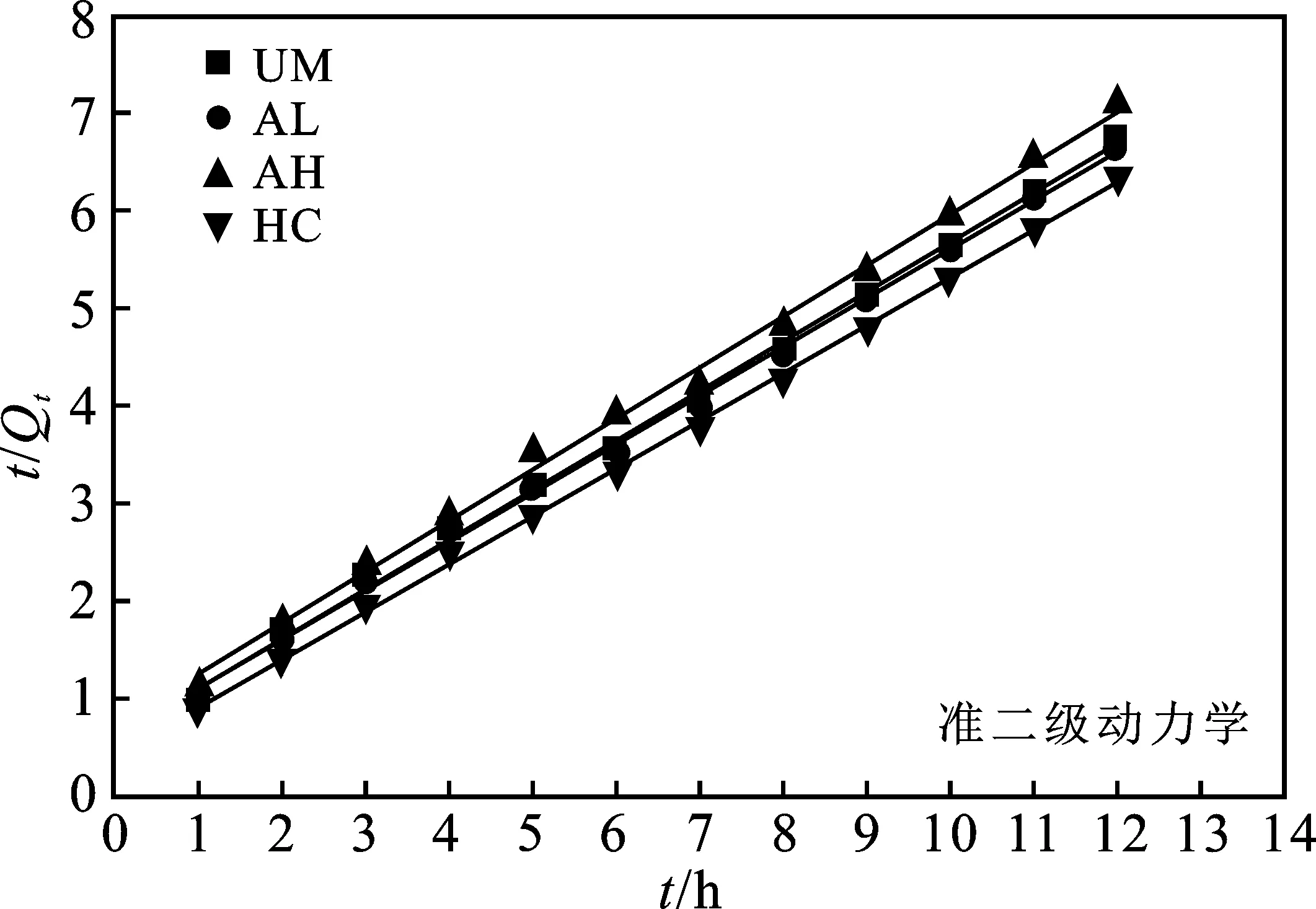
图5 4种丝瓜络对Pyr吸附动力学曲线Fig.5 Adsorption kinetics curves of four loofahs on Pyr
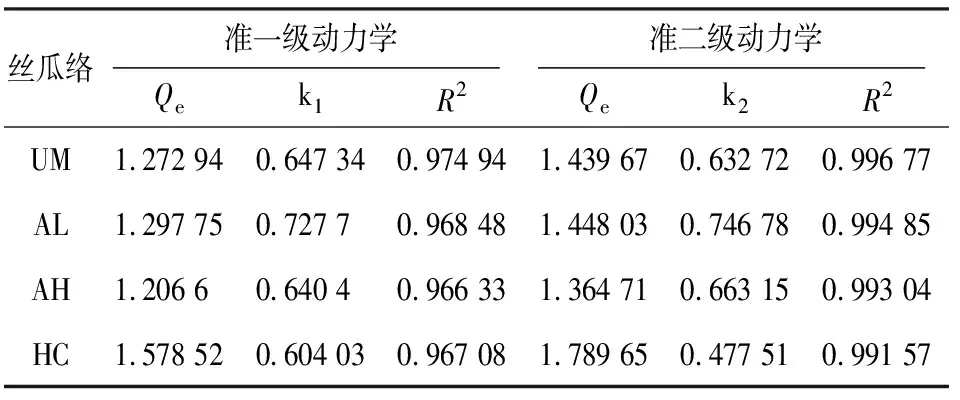
表1 动力学模型拟合参数(Phe)Table 1 Kinetic model fitting parameters

表2 动力学模型拟合参数(Pyr)Table 2 Kinetic model fitting parameters
由图4及表1可知,4种不同处理的丝瓜络对Phe吸附的准二级动力学拟合的预测平衡吸附量(Qe)接近实际实验值,且准一级动力学拟合的预测平衡吸附量(Qe)也比较接近实际实验值;而准二级动力学拟合的结果R2>0.99,拟合效果较好,并且略微高于准一级动力学拟合结果R2,这表明该吸附过程较好地服从于准二级动力学模型。
由图5及表2可知,由于UM和AH对Pyr的准一级动力学拟合结果相近,两条线接近重合,且UM和AL对Pyr的准二级动力学拟合结果相近,两条线接近重合。4种不同处理的丝瓜络对Pyr吸附的准一级动力学与准二级动力学拟合的预测平衡吸附量(Qe)均接近实际实验值,准一级动力学和准二级动力学方程拟合的结果R2均达到0.99以上,而准二级动力学方程拟合的R2略大于准一级动力学方程,这表明该吸附过程较好地服从于准二级动力学模型。
4种丝瓜络对Phe、Pyr的吸附均服从于准二级动力学模型,属于化学吸附[29]。
2.4 丝瓜络对Phe与Pyr的等温吸附
分别配制0.2,0.4,0.8,1.0,1.2 mg/L的Phe、Pyr水-丙酮溶液。精确量取100 mL于250 mL锥形瓶中,并分别加入50 mg UM、AL、AH、HC丝瓜络,在室温、避光条件下以100 r/min振荡至吸附平衡,取样,测定,吸附等温线见图6。用Langmuir方程和Freundlich方程对等温吸附数据进行拟合。
(3)
(4)
式中Qm——饱和吸附量,mg/g;
Ka——Langmuir常数;
Kf和n——经验常数;
Ce——平衡浓度,mg/L;
Qe——平衡吸附量,mg/g。

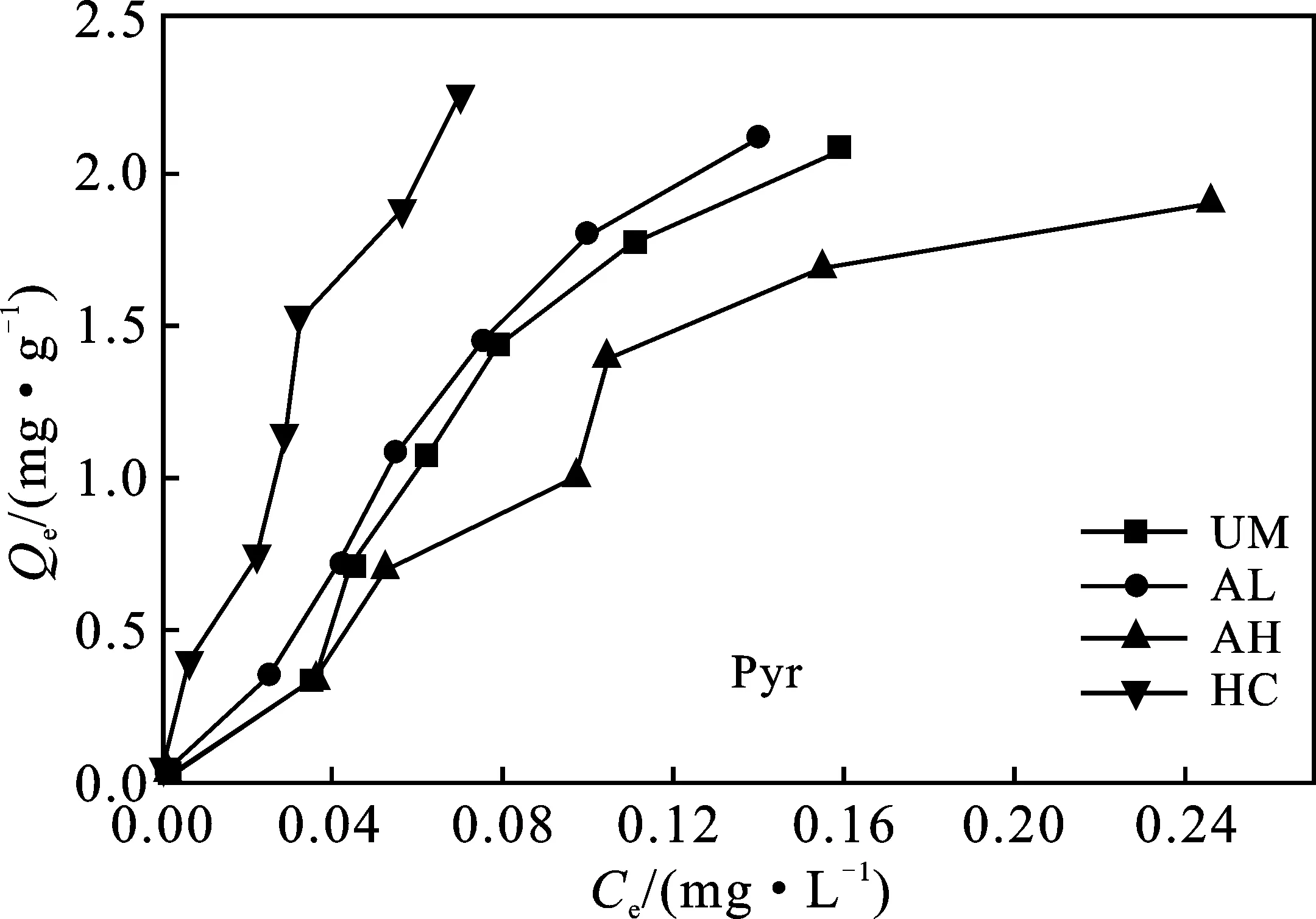
图6 4种丝瓜络对Phe和Pyr的吸附等温线Fig.6 Adsorption isotherms of four loofahs on Phe and Pyr
由图6可知,随着菲与芘初始浓度的增加,4种丝瓜络对其吸附量均随之增加。
对比图7、图8及表3,Langmuir和Freundlich吸附模型均能较好地描述4种丝瓜络对Phe和Pyr的吸附过程,且该实验结果更加符合Langmuir等温吸附模型,UM、AL、AH、HC对Phe的饱和吸附量(Qm)分别为2.177,1.967,2.195,2.274 mg/g,对Pyr的饱和吸附量(Qm)分别为2.248,2.162,2.255,6.919 mg/g。由此可以推断,4种丝瓜络对Phe和Pyr的吸附机制主要为表面吸附,且主要为单分子层吸附[30]。
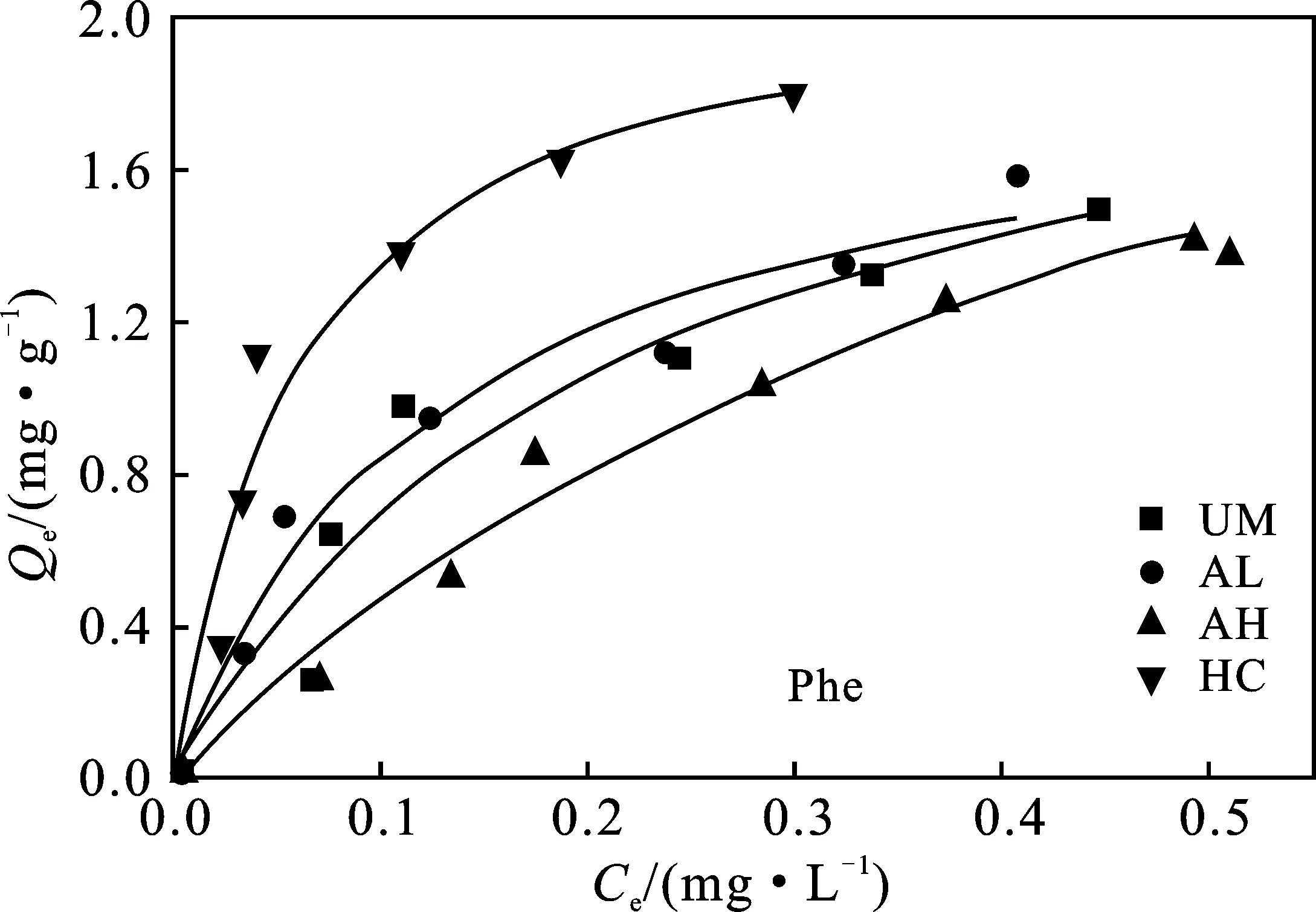

图7 4种丝瓜络对Phe和Pyr的Langmuir吸附等温线Fig.7 Langmuir adsorption isotherms offour loofahs on Phe and Pyr

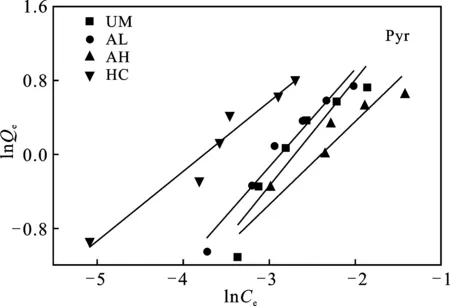
图8 4种丝瓜络对Phe和Pyr的Freundlich吸附等温线Fig.8 Freundlich adsorption isotherms offour loofahs on Phe and Pyr

表3 Langmuir和Freundlich吸附等温线模型拟合参数Table 3 Langmuir and Freundlich adsorptionisotherm model fitting parameters
3 结论


(3)4种丝瓜络对Phe与Pyr的吸附过程均服从于准二级动力学,属于化学吸附。
(4)4种丝瓜络对Phe和Pyr的吸附机制主要为表面吸附,且更符合Langmuir吸附模型,主要为单分子层吸附。
