丙戊酸相关血液系统不良反应严重程度的相关因素分析
2020-06-08刘清扬林京玉闫素英
唐 静,刘清扬,2,林京玉,闫素英
0 引言
在世界范围内大约有5 000万人患有癫痫,其中1/4的患者在使用抗癫痫药物治疗[1],欧洲一项研究对接受抗癫痫药物治疗的患者进行调查,有88%的患者至少经历过1次药物不良事件[2]。丙戊酸通过多种作用机制发挥抗癫痫作用,是临床上常用的广谱抗癫痫药,由于其具有稳定心境的作用,还适用于轻躁狂、双相抑郁等双相情感障碍的单药或联合治疗[3-4]。丙戊酸常见的不良反应包括神经系统、胃肠道系统、内分泌和代谢系统及血液系统等[3-5]。前期工作中,我们对北京市药品不良反应监测中心2004-2017年接收到的614例丙戊酸相关不良反应报告进行了分析,血液系统不良反应占22.2%,仅次于皮肤和皮下组织不良反应,位列第2位。与其他不良反应相比,丙戊酸相关的血液系统的不良反应多数仅为实验室检查结果的异常而不易被患者发现[6],但可以导致出血性卒中、严重感染等临床事件[7-8]。临床上通常认为,当血小板低于50×109/L、纤维蛋白原低于1 g/L时,严重出血风险较高,粒细胞低于1.0×109/L时,易出现感染[6,9-11]。丙戊酸作为各种类型癫痫和双相情感障碍的一线治疗药物,通常要求患者坚持长期服药,对于出现不良反应的患者是否都需要减量或者停药,值得进一步研究和探讨。目前,几乎还没有关于丙戊酸血液系统不良反应严重程度的相关研究,本文旨在分析并探讨影响丙戊酸相关血液系统不良反应严重程度的相关因素,为临床安全使用丙戊酸类药物以及出现血液系统不良反应时的处置提供指导。
1 资料来源和研究方法
1.1 资料来源 北京市药品不良反应监测中心主要负责本市药品不良反应资料和报告的收集、整理、分析、上报,发布药品不良反应的监测信息,调取其2004年1月至2017年9月接收的丙戊酸相关血液系统不良反应报告。排除标准:服药前血常规检查基线水平已经低于正常值的不良反应报告。剔除标准:在进行丙戊酸相关血液系统不良反应严重程度相关因素分析时,剔除其中未报告实验室检查结果而无法进行严重程度分级的报告。
1.2 不良反应严重程度分级标准 参考WHO抗癌药急性及亚急性毒性反应分度标准[12],对血小板减少、白细胞减少和中性粒细胞减少等各类型血液系统不良反应严重程度进行分级。分级标准为:血小板减少(单位L-1),Ⅰ度75×109≤PLT<100×109,Ⅱ度50×109≤PLT<75×109,Ⅲ度25×109≤PLT<50×109,Ⅳ度PLT<25×109;白细胞减少(单位L-1),Ⅰ度3.0×109≤WBC<4.0×109,Ⅱ度2.0×109≤WBC<3.0×109,Ⅲ度1.0×109≤WBC<2.0×109,Ⅳ度WBC<1.0×109;粒细胞减少(单位L-1),Ⅰ度1.5×109≤NEU<2.0×109,Ⅱ度1.0×109≤NEU<1.5×109,Ⅲ度0.5×109≤NEU<1.5×109,Ⅳ度NEU<0.5×109,其中Ⅰ、Ⅱ度定义为轻度,Ⅲ、Ⅳ度定义为中重度。目前临床纤维蛋白原减少严重程度尚无明确的分级方法,但研究认为,纤维蛋白原水平可以用来评估出血风险[13],研究中通常认为纤维蛋白原低于正常值2.0 g/L,一般无出血风险,为轻度减少;而当纤维蛋白原低于1.0 g/L时,可出现出血征象,为中重度减少[6,14]。
2 结果分析
2.1 丙戊酸相关血液系统不良反应总体分析 2004年1月至2017年9月,北京市药品不良反应监测中心接收到丙戊酸相关的血液系统不良反应报告136例,排除服用丙戊酸前实验室检查结果基线水平已经低于正常值报告2例,得到实际有效不良反应报告134例。
2.1.1 人口学信息特点 134例血液系统不良反应报告中,年龄最大117岁,最小1.67岁,中位数37.8(22.2,58.1)岁,按年龄划分为儿童组(<14岁)、青中年组(≥14岁且<65岁)和老年组(≥65岁);其中男62例,女72例;汉族130例,满族2例,苗族1例,1例不详。
2.1.2 疾病和药品信息特点 134例血液系统不良反应报告中,原发病主要为癫痫和双相情感障碍,其中丙戊酸用于治疗癫痫70例,用于治疗双相情感障碍62例,其他1例用于止痛,1例不详。所用药品包括丙戊酸钠和丙戊酸镁,其中使用注射剂型12例,口服缓释剂型94例,口服常释剂型23例,有5例未报告剂型;由于3例未报告剂量、10例未报告患者体重,因此选取剂量、体重信息完整的121例计算单位体重剂量,最高171.2 mg/(kg·d),最低3.63 mg/(kg·d),中位数16.7(13.3,22.9)mg/(kg·d)。根据丙戊酸说明书,其常规日剂量为20~30 mg/kg,本研究中日剂量低于常规剂量的有75例(62.0%),在常规剂量范围内的34例(28.1%),高于常规剂量的12例(9.9%)。有12例报告了血药浓度,最高168.3 mg/L,最低33.0 mg/L,中位数94.2(75.5,123.6)mg/L。丙戊酸有效血药浓度范围根据目前临床的指导方案定为50~100 μg/ml[14],其中5例(41.7%)大于有效血药浓度范围,6例(50.0%)在有效血药浓度范围内,1例(8.3%)低于有效血药浓度范围。
2.1.3 不良反应情况 134例报告中有严重不良反应12例,一般不良反应122例。由于1位患者可同时存在多种不良反应,因此共涉及162例次不良反应,包括血小板减少60例次(37.0%)、白细胞减少60例次(37.0%)、粒细胞减少24例次(14.8%)和纤维蛋白原减少18例次(11.1%)。不良反应出现时间最短1 d,最长28年,中位数16.5(7.0,31.0)d;出现不良反应的患者中约85%痊愈或有所好转,不良反应处理方式及转归情况见表1。
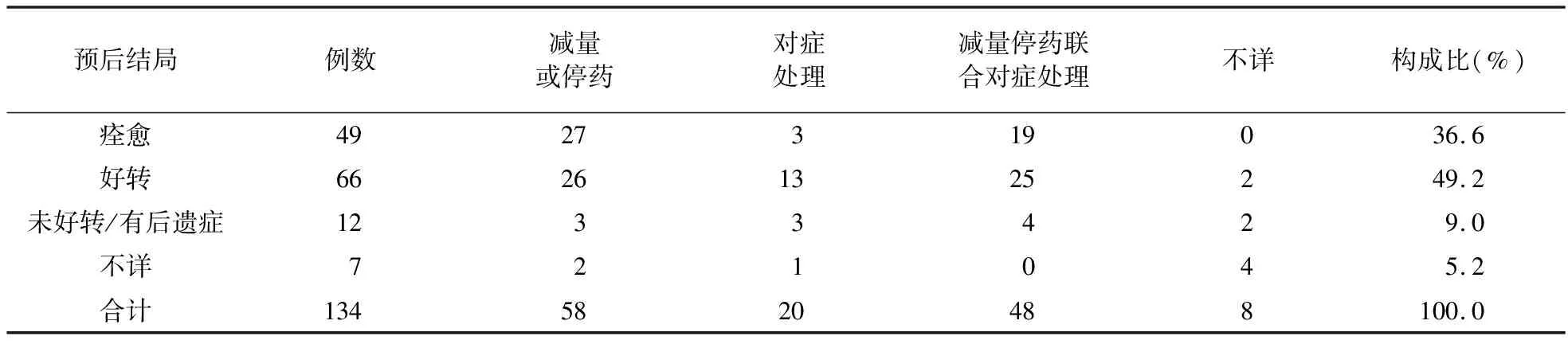
表1 丙戊酸相关血液系统不良反应处理措施及预后
2.2 丙戊酸相关血液系统不良反应严重程度的单因素分析 162例次丙戊酸相关血液系统不良反应中,8例次报告中未详细描述实验室检查结果而无法进行严重程度分级,故剔除,对剩余154例次进行严重程度分级。各类型血液系统不良反应严重程度分级结果见表2,不良反应严重程度单因素分析结果见表3(计数资料)和表4(计量资料)。

表2 丙戊酸相关血液系统不良反应严重程度分级(例)

表3 丙戊酸相关血液系统不良反应严重程度单因素分析结果[(计数资料,例(%)]

表4 丙戊酸相关血液系统不良反应严重程度单因素分析结果(计量资料)
2.3 丙戊酸相关血液系统不良反应严重程度多因素分析 对性别、年龄分组和原发疾病3个变量采用二元Logistic回归进行多因素分析。年龄分组与血液系统不良反应严重程度单因素分析结果提示,儿童组和老年组间差异无统计学意义,故多因素回归时将二组合并为“特殊人群组”,青中年组为“非特殊人群组”。最终年龄、性别两项进入方程,其中特殊人群(OR=2.260,95%CI:0.915~5.441,P=0.071),男性(OR=3.932,95%CI:1.231~8.307,P=0.003)是丙戊酸相关严重的血液系统不良反应的危险因素。
3 讨论
3.1 丙戊酸导致的血液系统不良反应的表现 丙戊酸血液系统不良反应较为常见,主要包括血小板减少、白细胞减少、粒细胞减少和纤维蛋白原减少、von Willebrand病、维生素K依赖性凝血因子缺乏症、低纤维蛋白原血症、凝血因子Ⅷ缺乏、急性早幼粒细胞白血病等[15-16]。丙戊酸导致血小板减少的发生率在5%~18%[7],纤维蛋白原减少发生率为1.3%~59.1%[6],关于白细胞减少发生率的研究报道较少,一项纳入65例癫痫患者的研究中,有57例患者白细胞及中性粒细胞较用药前降低[17]。此外,多数研究发现,丙戊酸血液系统不良反应的患者仅为实验室检查结果异常,而无明显临床表现,也有研究观察到患者出现出血等严重的临床症状[18-22],本研究中出现血液系统不良反应的患者多数均无明显的出血和感染等表现。
3.2 较低剂量和正常血药浓度仍可出现血液系统不良反应 关于剂量和血药浓度对丙戊酸血液系统不良反应的影响研究较少,唐静等[6]纳入59例患者进行纤维蛋白原减少发生的相关因素分析发现,剂量≥13.3 mg/(kg·d)是丙戊酸引起纤维蛋白原降低敏感性和特异性较好的预测指标;血药浓度与丙戊酸相关血液系统不良反应的关联性现有研究结论不一致,一些研究发现,较多患者血药浓度在正常范围内依然可以出现不良反应[19,22-23]。也有研究认为,丙戊酸血液系统不良反应发生与血药浓度相关[16,24]。曾艳等[15]研究发现,丙戊酸血药浓度在90~160 μg/ml时,并未出现严重的血液系统不良反应。本研究中约62%的患者未超过推荐剂量而出现血液系统的不良反应,考虑一方面由于患者个体差异及合并用药等因素,可能造成按照推荐剂量给药的情况下丙戊酸的血药浓度已经达到较高水平;另一方面,血液系统不良反应可能由多种机制引起,其中一些可能为非剂量依赖型的不良反应,药物少量暴露即可出现[4]。本研究中仅12例患者报告了血药浓度,样本量较小,其中7例在有效血药浓度范围内或低于有效浓度范围下限,表明在血药浓度不高的情况下依然可以出现血液系统不良反应,但这12例患者血药浓度中位数为94.2 mg/L,接近治疗浓度范围上限,因此,对于血药浓度较高的患者,应密切监测有无血液系统检查结果异常。
3.3 丙戊酸血液系统不良反应预后较好 本研究超过85%患者不良反应转归为痊愈或好转,处置措施包括停药、减量及对症处理等,对症处理常用的药物包括利可君、升白胺、小檗胺、鲨肝醇以及输注血小板、输注新鲜冰冻血浆等。多数患者经停药或减量可逆转丙戊酸所致的血液系统不良反应,且停药或减量较仅对症处理有更高比例的患者痊愈,与其他研究中丙戊酸血液系统不良反应给予停药减量的处理较对症治疗效果更好的结论一致[19,25]。因此,当发现血液系统检查结果异常时应引起重视,若患者出现检查结果重度异常、出血或感染等伴随症状,建议减量或停药处理。
3.4 临床上应更加关注严重血液系统不良反应的高危人群 本研究中轻度不良反应和中重度不良反应两组间年龄(P=0.008)和原发疾病(P=0.022)差异有统计学意义,两组患者的性别(P=0.069)也存在一定程度的差异,但“原发疾病”一项在进行二元Logistic回归时未纳入,考虑原因可能为样本量较小,且患者性别与原发病间可能存在交互作用,男性患者癫痫发生率较高所导致[26]。此外,研究中发现,丙戊酸注射剂与口服缓释剂型相比,有更容易出现严重不良反应的趋势(P=0.077),与文献报道丙戊酸静脉给药较口服给药不良反应发生率高的结果一致[27]。临床使用丙戊酸类药物时,对于男性、儿童或老年、癫痫及应用静脉剂型的患者,要更加密切监测血常规和凝血功能,并观察患者有无出血、感染等相关症状,当这些人群出现血液系统实验室检查结果异常时应谨慎处置,避免严重的血液系统不良反应发生。
4 结论
丙戊酸血液系统不良反应表现多样但常可逆转,临床在密切监测下可较为安全地应用该药。血液系统不良反应通常仅表现为实验室检查结果异常而无明显症状,用药期间应注意监测血常规和凝血功能。儿童和老年患者、男性患者使用丙戊酸易出现严重的血液系统不良反应,对于这些人群出现血液系统检查结果异常时要谨慎处置,以避免严重临床事件发生。
