多粘菌素B对鲍曼不动杆菌生物膜形成的影响研究
2020-06-08阮四维王海鑫张妙英蒋文静周训竹曹栋卿
阮四维,王海鑫,张妙英,蒋文静,周训竹,曹栋卿,周 燕*
0 引言
鲍曼不动杆菌(Acinetobacterbaumanii)是临床尤其在ICU内多重耐药和院感最主要的细菌之一[1-2],其泛耐药及多耐药特性与其生物膜的形成有关,生物膜状态下细菌可以抗消毒剂,抗人体的免疫系统,使感染持续存在且难以治疗[1]。既往对多重耐药鲍曼不动杆菌的研究多集中于其携带的耐药基因直接导致的耐药,本研究分析形成生物膜的相关特性及多粘菌素B作用于多重耐药鲍曼不动杆菌的最低抑菌浓度、与生物膜形成存在可能关联性的基因[3]、最低生物膜清除浓度以及杀菌机制,为临床治疗多重耐药鲍曼感染提供理论依据。
1 材料与方法
1.1 材料
1.1.1 标本 选取温州某三甲医院2016年2-10月ICU气管插管患者分离出的鲍曼不动杆菌42株。入选标准:①患者临床有感染症状,根据中华医学会呼吸病学分会医院获得性肺炎的诊断标准判定为医院获得性肺炎。②连续痰培养2次以上,结果为鲍曼不动杆菌优势生长。
1.1.2 主要试剂和仪器 细菌检定卡购自英国Oxoid公司,药敏纸片购自法国梅里埃公司,硫酸多粘菌素B购自上海鼓臣生物技术有限公司;氨溴索购自常州四药制药有限公司。VITEK-2全自动微生物鉴定仪由法国梅里埃公司生产,电镜由日本JOEL株式会社生产,基因扩增仪由杭州博日公司生产,凝胶成像仪为美国BIO-RAD公司生产。质控菌株采用卫生部临床检验中心提供的大肠埃希菌(ATCC 25922)、铜绿假单胞菌(ATCC 27853)、金黄色葡萄球菌(ATCC25923)。
1.2 方法
1.2.1 细菌鉴定及药敏试验 鉴定方法和结果判定均按照操作说明书进行;药敏试验应用微量肉汤稀释法,结果判断按美国临床实验室标准协会CLSI2019标准判读。
1.2.2 生物膜形成能力检测 96孔细胞培养板构建生物膜模型,结晶紫半定量法筛选出成膜能力不同的菌株,并用扫描电镜、激光共聚焦显微镜观察鲍曼不动杆菌生物膜。
1.2.3 PCR检测鲍曼不动杆菌生物膜相关基因 煮沸法提取鲍曼不动杆菌DNA,扩增abal、bfs、CsuE、ompA及blaPER-1基因,引物序列及扩增条件见参考文献[4],由上海华大公司合成。PCR扩增产物经1%琼脂糖凝胶电泳,经DNA marker对照确认是否含阳性片段,随机各挑选2株产物送至上海华大基因公司进行纯化并测序。
1.2.4 胞外多糖及蛋白含量测定 参照文献方法[5],采用苯酚-硫酸法、考马斯亮蓝染液结合法分别检测多粘菌素B用药前后鲍曼不动杆菌的胞外多糖和黏附蛋白含量。
1.2.5 药物对鲍曼不动杆菌的最低抑菌浓度、生物膜清除浓度测定 参照美国临床实验室标准协会CLSI2019标准方法,相同药物浓度多粘菌素B作用鲍曼不动杆菌生物膜。选取24 h和48 h生物膜培养物电镜扫描和激光共聚焦显微镜观察病原菌生物膜。
1.3 统计学方法 数据统计应用SPSS 18.0软件,计数、计量资料比较分别采用χ2检验及t检验。P<0.05为差异有统计学意义。
2 结果
2.1 药敏试验 试验结果显示,有2株(4.8%)鲍曼不动杆菌对所有药物均敏感,35株(83.3%)对3种以上药物耐药,具体见表1。所有鲍曼菌株头孢他啶的MIC>512 μg/ml,哌拉西林的MIC>512 μg/ml,5株鲍曼不动杆菌对亚胺培南的MIC>512 μg/ml,2株鲍曼不动杆菌对亚胺培南的MIC为512 μg/ml,美罗培南的MIC>512 μg/ml,头孢吡肟的MIC>512 μg/ml,阿米卡星和环丙沙星的MIC>512 μg/ml,左氧氟沙星的MIC≥256 μg/ml,具体药敏结果见表1。多粘菌素B的MIC有梯度,7株(16%)鲍曼不动杆菌的MIC为0.5 μg/ml,19株(46%)鲍曼不动杆菌的MIC为1 μg/ml,6株(15%)鲍曼不动杆菌的MIC为2 μg/ml,10株(23%)鲍曼不动杆菌的MIC>128 μg/ml,比例见图1。

表1 鲍曼不动杆菌药敏试验结果[株(%)]
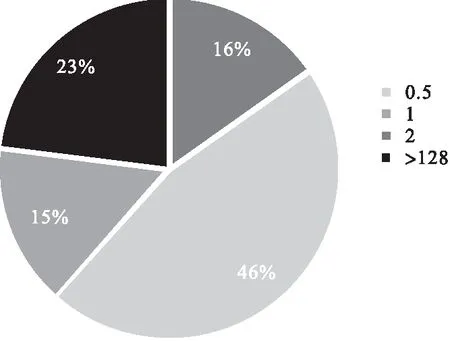
图1 鲍曼不动杆菌多粘菌素B的MIC(μg/ml)
2.2 鲍曼不动杆菌生物膜形成能力分析 多重耐药鲍曼不动杆菌与敏感株24 h、48 h吸光度检测显示其成膜能力有差异,多重耐药株更容易形成生物膜。见表2。

表2 鲍曼不动杆菌耐药菌和非耐药菌不同培养时间OD550值
注:*1t=16.008,P<0.001;*2t=7.214,P<0.001
2.3 PCR检测鲍曼不动杆菌生物膜相关基因 42株鲍曼不动杆菌检出abal、bfs、CsuE、ompA及blaPER-1基因均在70%左右,χ2检验显示,5种基因在多重耐药株和敏感株中差异无统计学意义。具体结果及统计学分析见表3。
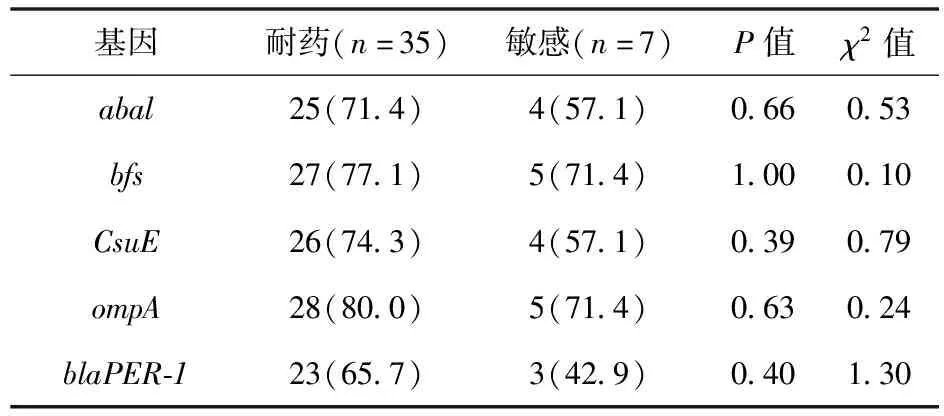
表3 鲍曼不动杆菌生物膜相关基因及统计学分析[株(%)]
2.4 胞外多糖及蛋白含量 多重耐药鲍曼不动杆菌胞外多糖和胞外蛋白的测定结果见表4。从表4可以发现,多粘菌素B对鲍曼不动杆菌胞外蛋白和胞外多糖的形成均有明显作用。

表4 多重耐药鲍曼不动杆菌胞外多糖(A490)蛋白(A595)测定结果(μg/ml)
2.5 扫描电镜、激光共聚焦显微镜观察和测定药物作用前后生物膜 耐药鲍曼不动杆菌经培养后,形成形状不同的条索状或斑片状固着物,成团或相互交叉的生物膜。用药后可见大部分斑片状固着物相互聚集成团固缩,附着面积减小,小部分固着物剥离,无规律散在。见图2、图3。
本实验采用2种染料对所研究的鲍曼不动杆菌进行双重染色:用FITC标记的刀豆蛋白A(FITC-Con A)与生物膜中的多糖结合发出绿色荧光,碘化吡啶(PI)与菌体内的DNA结合,可发出红色荧光,在盖玻片上形成生物膜,在用药前和用药后取出玻片,采用双重免疫荧光技术标记多糖和细菌,并用激光共聚焦显微镜(CLSM)观察生物膜形成情况。由图4、图5可观测到耐药鲍曼不动杆菌在用药前后成膜量的变化,结果表明,成膜能力随着用药剂量的增长而下降。

图2 耐药株用药前扫描电镜生物膜形态

图3 耐药菌用药后扫描电镜生物膜形态
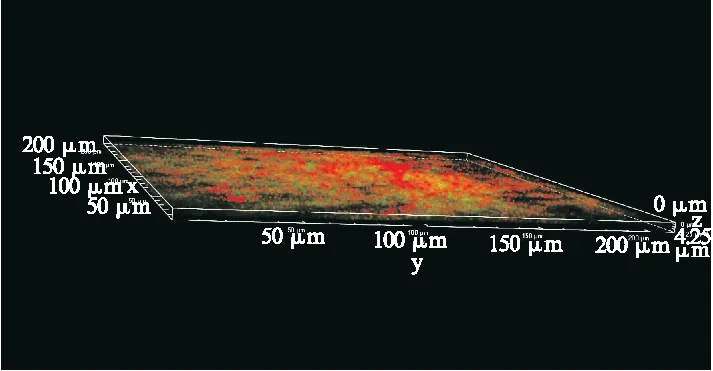
图4 耐药株用药前共聚焦生物膜形态
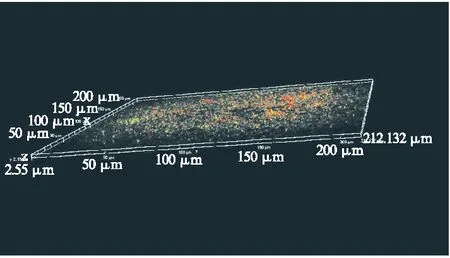
图5 耐药菌用药后共聚焦生物膜形态
3 讨论
生物膜的形成是细菌耐药的机制之一,50%的院内感染与医疗器械装置上的生物膜相关联[6-7],生物膜保护细菌免受宿主的获得性免疫应答以及吞噬细胞的捕食,使其耐药性提高10~1 000倍[8]。本研究菌株来自ICU气管插管,其体外培养均显示极易形成生物膜。而多重耐药菌较敏感菌株更易形成生物膜,显示其多重耐药与生物膜形成的协同效应,与其他研究结果一致[9-10]。研究显示,形成生物膜的菌株对不同药物的耐药性存在一定差异,对氨苄西林-舒巴坦、阿米卡星、环丙沙星、头孢他啶有较高耐药性,而对亚胺培南和哌拉西林的耐药性较低[11-12],但本次分离菌株对不同药物没有明显差别,要考虑其他耐药机制导致对药物的耐药性。
abal、bfs、CsuE、ompA、blaPER-1为菌毛装配、形成和黏附生物表面的相关基因,研究表明,鲍曼不动杆菌依靠菌毛黏附物体表面,其黏附力强,不易被外力清除,继而形成微菌落,随着菌落扩大,生物膜进一步成熟[13],因此,这些基因也被认为是生物膜的相关基因,有一个或数个基因缺失的鲍曼不动杆菌则不易形成生物膜[14]。本研究35株多重耐药菌中,23株(65.71%)均检测到了所有的基因,在7株敏感株中均存在一定的基因缺失。因而影响其生物膜形成能力,但结果也需要排除实验特异性的影响因素,可能存在一定的不足。
多粘菌素B是从多粘杆菌培养液中分离得到的一种环肽类抗生素,主要作用于革兰阴性菌细胞壁,能与其外膜的脂多糖(LPS)结合,导致外膜通透性改变,最终通过细菌的“自发摄取通路”达到杀菌的目的[15]。多粘菌素B通过破坏鲍曼不动杆菌的细胞膜,对细菌外膜具有快速穿透性的特点,导致细胞膜内主要物质外漏[16]。同时,有研究表明,类多粘菌素B与RND外排泵AcrAB-TolC和AdeABC以及非RND外排泵Norm具有最高的结合亲和力[17],外排泵是一种位于细菌细胞膜上的胞外蛋白质,能将进入细菌内的抗菌药物泵出,同时也是构成细菌生物膜的重要组成部分。本研究显示,用药后多重耐药鲍曼不动杆菌胞外多糖和胞外蛋白含量均明显减少,电镜和激光共聚焦显微镜下均可观察到生物膜明显缩小,因此,可用于临床鲍曼不动杆菌的治疗。但多粘菌素B对肾脏的损害较多见,肾功能不全者应减量。
综上所述,生物膜的形成是鲍曼不动杆菌耐药的重要机制之一,多粘菌素B对易形成生物膜的多重耐药菌有较好的抑制作用,适宜在普通抗菌药物治疗效果不明显时选择使用。
