甲基丙烯酸聚乙二醇双酯的合成研究
2020-06-07任秀云张丽华代淑兰
任秀云,张丽华,代淑兰
(中北大学 化学工程与技术学院,太原 030051)
随着对身管武器性能要求的不断提高,发射药作为其发射能源,在各种环境中的力学性能对其使用的影响日益突出,改善其力学性能(尤其是在低温环境中的力学性能)的一条途径是使用增韧剂[1-4]。聚乙二醇是一种聚醚类高分子化合物,分子链的柔顺性好[5-6],聚乙二醇与甲基丙烯酸的酯化产物[7]可作为增韧剂对发射药进行增韧,改善其力学性能[8-9]。
聚乙二醇与甲基丙烯酸的酯化反应是一个可逆过程,其特点是反应温度较高,反应速率缓慢[10-11]。聚乙二醇酯类可采用直接酯化法和酯交换法进行酯化反应[12]。直接酯化法通常采用带水剂苯、甲苯等进行除水,但它们有较高的毒性。本研究采用减压蒸馏来替代带水剂功能进行除水,通过正交实验考察了在酯化反应减压蒸馏过程各条件的影响程度法进行除水,得到了酯化反应较佳条件。
1 实验
1.1 实验试剂及仪器
实验药品:聚乙二醇(PEG),AR,上海麦克林生化科技有限公司;甲基丙烯酸(MAA),AR,国药试剂上海化学试剂公司;对苯二酚(C6H6O2)(简称氢醌),AR,天津市光复精细化工研究所;浓硫酸(H2SO4),98%,天津市大陆化学试剂厂;无水乙醇,AR,天津市富宇精细化工有限公司;氘代二甲基亚砜(DMSO),阿拉丁试剂公司。
实验仪器:DZF-6210真空干燥箱(北京市永光明医疗仪器有限公司);ME104电子分析天平(梅特勒-托利多公司);SG-5407油浴锅(上海硕光电子科技有限公司); SHZ-D(Ⅲ)循环水真空泵(河南予华仪器有限公司);Bruker AVANCE III 600 型核磁共振仪(瑞士布鲁克公司);Perkin Elmer 1000红外光谱仪(美国珀金埃尔默公司)。
1.2 反应原理和反应步骤
聚乙二醇与甲基丙烯酸的酯化反应是一个可逆过程,反应温度较高,反应速率缓慢,采用反应物(甲基丙烯酸)过量,需及时除去反应生成的水来提高酯化率。为避免聚乙二醇在反应过程中与空气中的氧发生反应,反应过程中应通氮气。酯化反应方程式如下:
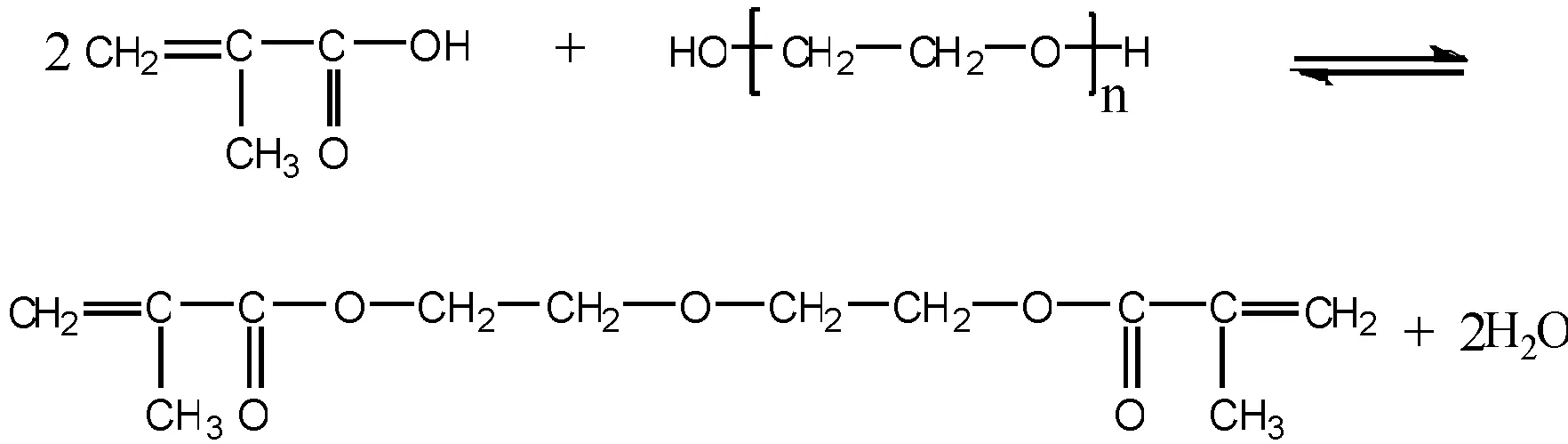
准确称取规定量的聚乙二醇、催化剂与阻聚剂,并将其加入三口烧瓶中,搅拌均匀。取样滴定,称量反应前反应液总质量。缓慢滴加一半甲基丙烯酸。加热反应,冷凝回流反应1 h,减压蒸馏除水1 h。继续滴加剩余的甲基丙烯酸,再冷凝回流反应1 h,减压蒸馏1 h,反应过程中通氮气。称量反应后反应液总质量,再次取样滴定。将得到的产物用碳酸氢钠溶液调至中性,水洗,将酯层分离出来,再次进行减压蒸馏,得到产物。
滴定测试:准确称取反应液试样1 g左右于锥形瓶中(3个平行试样),溶于10 mL无水乙醇中,加4~5滴酚酞,用NaOH标准溶液进行滴定。
酯化率计算公式如下:
m1+(MMAA-MH2O)·n1
(1)
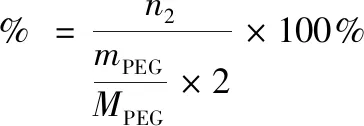
(2)
式(2)中:c为NaOH标准溶液的浓度(mol/L);n1为减压蒸馏法酯化反应消耗的甲基丙烯酸物质的量(mol);m1为反应前反应液的总质量(g);m2为反应后反应液的总质量(g);ma为反应前称取滴定试样的质量(g);mb为反应后称取滴定试样的质量(g);mPEG为反应前,反应液中聚乙二醇的质量(g);MMAA为甲基丙烯酸的摩尔质量(g/mol);MH2O为水的摩尔质量(g/mol);MPEG为反应前反应液中聚乙二醇的摩尔质量(g/mol);V1为滴定反应前试样消耗的NaOH标准溶液体积(mL);V2为滴定反应后试样消耗的NaOH标准溶液体积(mL)。
1.3 正交实验设计与表征方法
本研究确定反应时间为4 h,采用正交实验设计方法,选取了甲基丙烯酸和聚乙二醇的摩尔比、反应温度、催化剂用量、阻聚剂用量这4个影响因素,以酯化率为考察指标,建立4因素3水平的正交实验,即L9(34)正交表(甲基丙烯酸和聚乙二醇的摩尔比用A表示,反应温度用B表示,催化剂用量用C表示,阻聚剂用量用D表示,以下同),见表1。
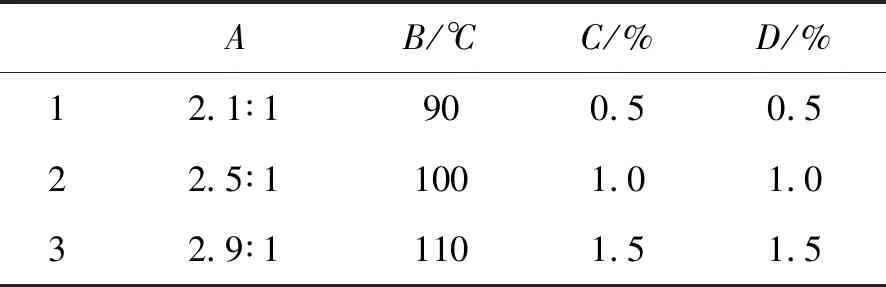
表1 正交实验设计
FT-IR:溴化钾(KBr)压片。称取2 mg样品,加入 200 mg KBr,于红外灯下在玛瑙研钵中研磨均匀,装入压片模具,用油压机以20 MPa的压力压制3 min,然后取下压片(厚度约1 mm)装入样品架。仪器扫描范围:4 000~400 cm-1。
1H- NMR:取20 μL样品置于核磁管中,选用氘代二甲基亚砜(DMSO-d6)作为溶剂,以DMSO-d6内标物的峰作为化学位移零点,样品扫描次数:64次;空扫次数:2次;采集时间:5 min;工作频率:600 MH。
DSC:试样量约 0.5~1.0 mg,温度范围-70~30 ℃,升温速率为10 ℃·min-1。
2 结果与讨论
2.1 正交实验结果分析
正交实验结果及极差分析见表2。
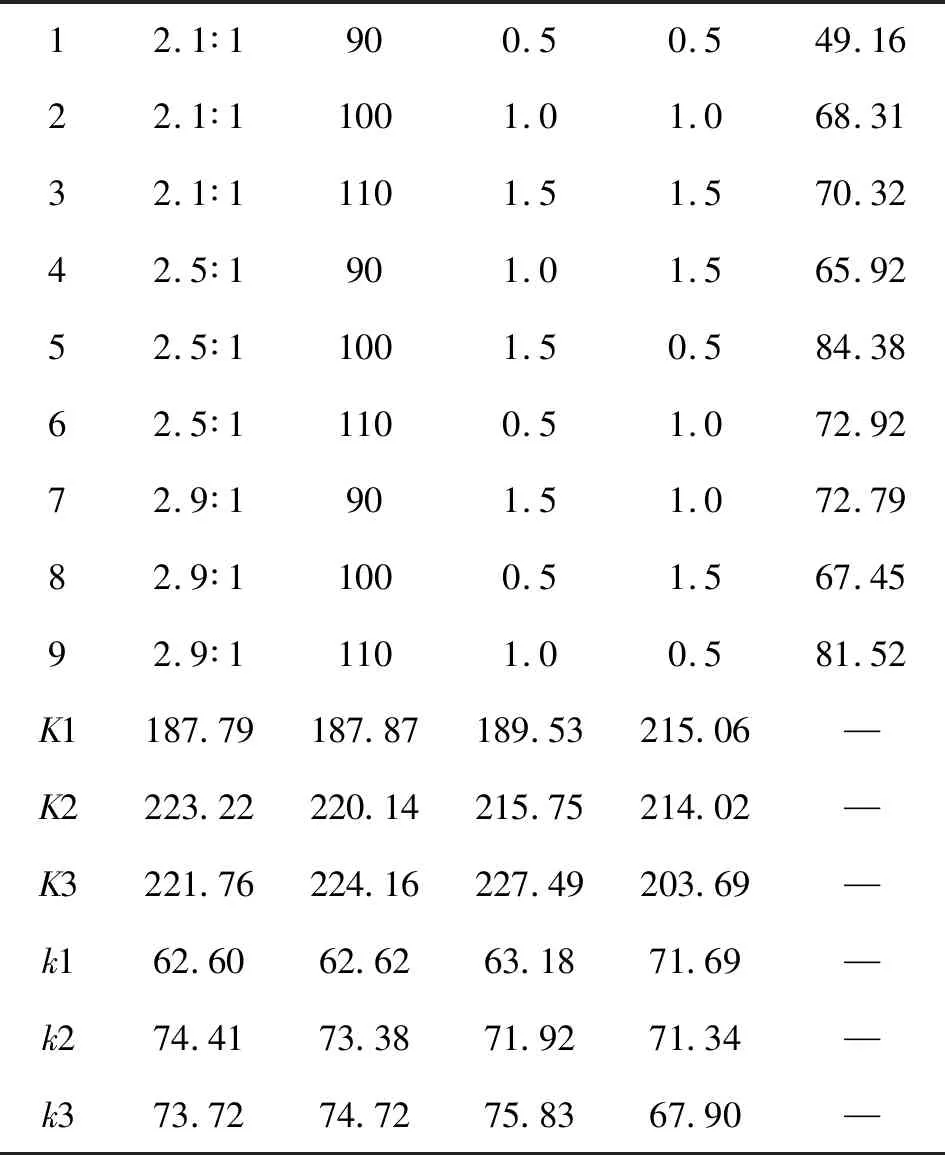
表2 正交实验结果数据
由表2的极差分析中可以看出:RC>RB>RA>RD,即催化剂用量对合成甲基丙烯酸聚乙二醇双酯的酯化率影响最大,反应温度和酸醇摩尔比次之,阻聚剂用量影响最小。
由表2可以看出,合成甲基丙烯酸聚乙二醇双酯的较佳条件为A2B3C3D1,即酸醇摩尔比2.5∶1,反应温度110 ℃,催化剂用量1.5%,阻聚剂用量0.5%。
2.2 验证实验
根据2.1得到的较佳反应条件进行验证实验。
对实验得到的较佳条件A2B3C3D1进行验证,反应酯化率为86.99%。证明正交实验得到的反应条件确实为较佳。
2.3 红外分析结果
酯化反应的反应物及产物的红外光谱图如图1。
红外分析表明:3 370 cm-1、3 433 cm-1处的吸收峰为O-H键的伸缩振动峰,1 244 cm-1处的吸收峰为O-H面弯曲振动峰,1 716 cm-1处的吸收峰为C=O键的伸缩振动峰,1 172 cm-1和1 132 cm-1为酯基特有的C-O键的双峰。
与甲基丙烯酸和聚乙二醇相比,酯化产物中的O-H键的振动峰减弱,说明聚乙二醇上的羟基被取代。1 716 cm-1、1 172 cm-1、1 132 cm-1处的吸收峰证明有酯基生成。
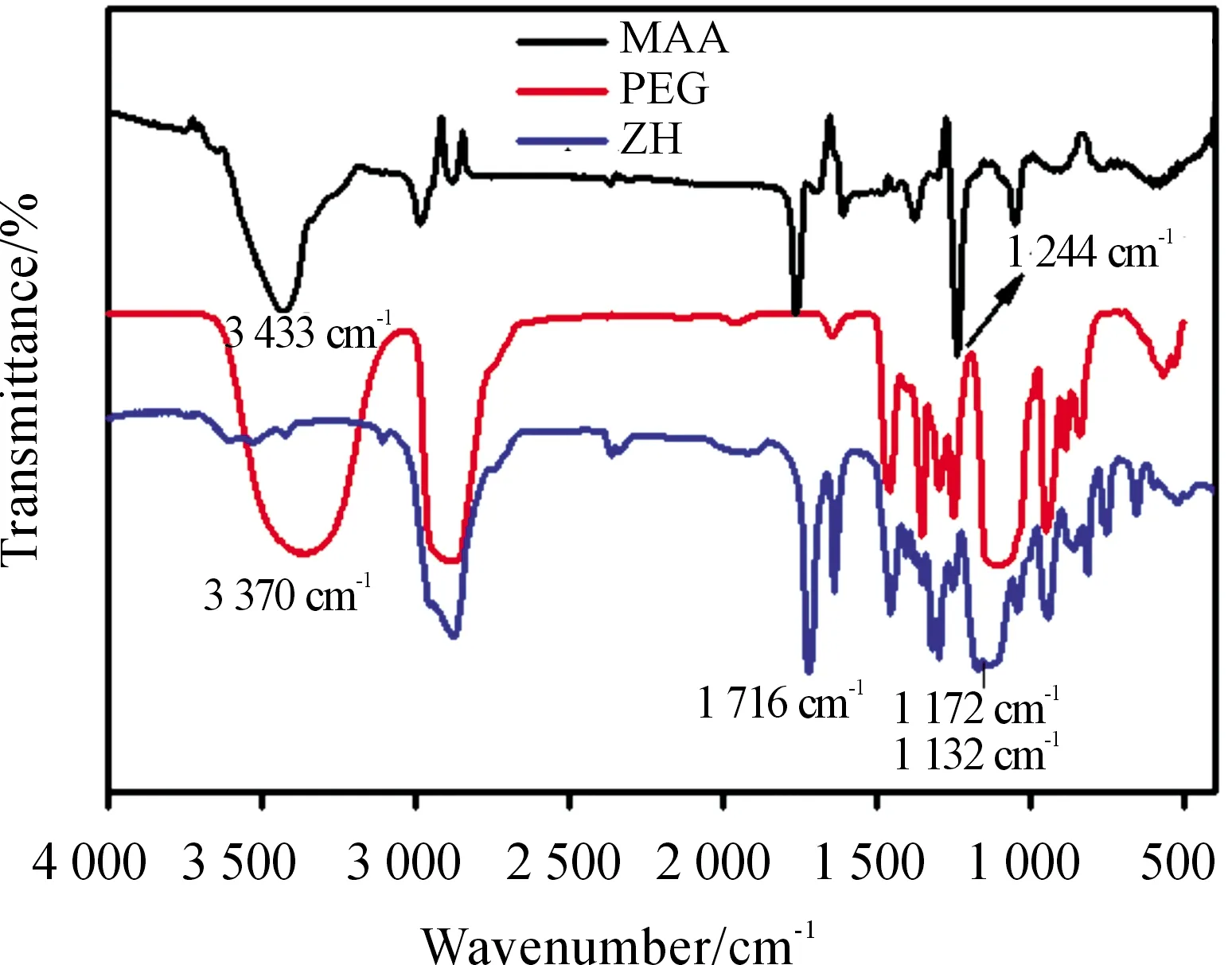
(MAA-甲基丙烯酸;PEG-聚乙二醇;ZH-酯化产物)
2.4 DSC分析结果
采用 DSC方法对聚乙二醇及酯化物的玻璃化转变温度和熔融点进行表征。(实验条件:温度范围-70~30 ℃,升温速率为10 ℃·min-1,试样量约 0.5~1.0 mg,试样皿为铝盘),实验结果如图2所示。
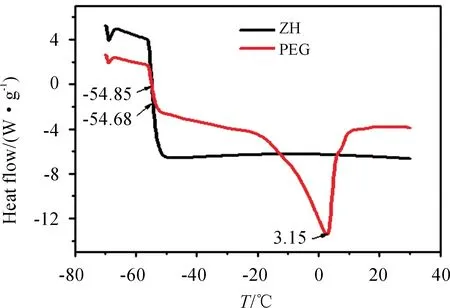
(PEG-聚乙二醇;ZH-酯化产物)
DSC分析表明:T=-54.85 ℃为聚乙二醇的玻璃化转变温度,T=-54.68 ℃为酯化产物的玻璃化转变温度。证明酯化反应没有明显改变聚乙二醇的玻璃化温度。T=3.15 ℃为聚乙二醇的熔融温度,酯化产物没有出现熔融温度,证明,与聚乙二醇相比,酯化产物没有结晶现象,物质结构发生了改变。
2.5 核磁分析结果
采用核磁共振氢谱对合成的酯化产物进行表征,如图3所示。
核磁分析表明,δ=3.3和δ=2.5分别是氘代DMSO的水峰和溶剂峰,产物共有5种不同化学环境的氢,其中化学位移δ=6.03对应图中的H2,为烯烃=CH2中靠近甲基的2个氢的共振峰;化学位移δ=5.69对应图中的H1,为烯烃=CH2中远离甲基的2个氢的共振峰;化学位移δ=4.22对应图中的H4,为图中与酯基相连的亚甲基中4个氢的共振峰;化学位移δ=3.52~3.66对应图中的H5,为图中与醚键相连的亚甲基中20个氢的共振峰;化学位移δ=1.88对应图中的H3,为图中甲基中6个氢的共振峰。由此可见,产物分子结构中的氢原子与1H-NMR谱图中的峰相互对应。
结合产物的FT-IR和1H-NMR测试结果,合成产物的化学结构得以确认。
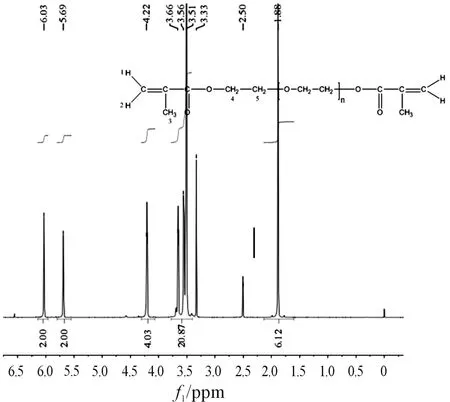
图3 产物的1H-NMR光谱
3 结论
本文采用减压蒸馏法成功制备了甲基丙烯酸聚乙二醇双酯,采用FT-IR和1H-NMR对酯化产物进行表征,采用正交试验法对酯化条件进行优化,确定了较佳的反应条件:酸醇摩尔比2.5∶1,温度110 ℃,催化剂用量1.5%,阻聚剂用量0.5%,酯化率为86.99%。合成后的产物有望用于发射药的增韧,改善其力学性能,提升相关武器系统的安全稳定性。
