丝棉木种子化学成分及其抗肿瘤活性
2020-06-02左亚奇张冠腾
庞 策,左亚奇,张冠腾,甄 攀
(1.河北北方学院药学系,河北 张家口075000; 2.河北北方学院应用化学研究所,河北 张家口075000)
丝棉木Euonymus maackiiRupr.系卫矛科卫矛属植物,又名华北卫矛、白杜卫矛,主要分布在东北南部至长江流域北部暖温带地区。丝棉木的根和皮均可用作药物,其性寒,味苦涩,有小毒[1]。前期研究报道可知,其化学成分主要包括三萜类[2-4],其提取物有显著的昆虫拒食活性[5]。为进一步发掘该植物中的化学成分,本实验对丝棉木种子的乙醇提取物进行了分离纯化,共分离鉴定了10 个化合物,其中,化合物1 为新化合物。经过体外药理活性筛选发现,化合物6 对Hela 细胞有一定的抑制作用,IC50为9.76 μg/mL。
1 材料
WNMR-Ⅰ500 核磁共振仪(中科牛津波普有限公司);AV600 ⅢHD 核磁共振仪(瑞士布鲁克拜尔斯宾有限公司);IMPACT-400 型傅里叶变换红外光谱仪(美国Nicolet 公司);Agilent 1100 高效液相色谱仪、Agilent 1200 制备色谱仪 (美国Agilent 公司);紫外可见分光光度计(北京普析通用仪器有限责任公司);WZZ-1 自动旋光仪(申光有限公司);反相柱色谱硅胶RP18(40~60 μm)(德国Merck 公司);薄层色谱硅胶GF254及柱色谱硅胶(200~300 目)(青岛海洋化工厂);YMC C-18(260 mm×4.6 mm,5 μm,美国Thermo 公司)。
丝棉木种子于2016 年9 月采自张家口市长城西大街景观树种,由河北北方学院医学院魏会平教授鉴定为丝棉木Euonymus maackiiRupr.。
2 提取与分离
取丝棉木种子764 g,干燥,粉碎,95% 乙醇浸泡,回流提取,重复提取2 次,合并提取液,减压浓缩得膏状物约100 g。膏状物用100~200 目硅胶柱分离,分别用石油醚、二氯甲烷、乙酸乙酯洗脱,各洗脱液减压浓缩,分别得膏状物21.24、29.58、41.27 g。乙酸乙酯洗脱部分用D101 大孔吸附树脂柱进一步分离,以乙醇-水洗脱(30%、50%、70%、90%、100%),各洗脱液减压浓缩。70%和100%乙醇-水洗脱部分,分别用C18色谱柱进一步分离,甲醇-水(30%、50%、60%、70%、90%、100%) 洗脱,每10 mL 收集一试管,用薄层板检识,相同部分合并。最后用制备色谱仪纯制,甲醇-水为流动相,得到单体化合物。取100%乙醇部分,再用C18色谱柱分离,从90%甲醇-水洗脱部分,得到化合物1~4。取70%乙醇洗脱部分,再用C18色谱柱分离,从70%甲醇-水洗脱部分,得到化合物5~7;从90%甲醇-水洗脱部分,得到化合物8~10。
3 结构鉴定
化合物 1: 白色固 体。[α]D20=-315(0.286 g/100 mL,CH3OH );HR-ESI-MSm/z:707.266 2 [M+Na]+(计算值 707.268 0,C36H44NaO13),结 合 NMR 推测其 分子式 为C36H44O13,不饱和度 为15。其IR 谱显示羟基(3 300 cm-1)、羰 基 (1 645 cm-1)、苯 环(1 416.6,1 468.3 cm-1) 吸收峰。1H-NMR (500 MHz,CDCl3)δ:6.2 (1H,s,H-9),5.75 (1H,m,H-2),5.70 (1H,d,J=3.6 Hz,H-1),5.28 (1H,d,J=6.01 Hz,H-6),5.25/4.53 (2H,AB(13.2),H-12),2.58 (1H,s,H-7),2.21 (2H,s,H-3),2.2 (2H,s,H-8),1.56 (3H,s,H-15),1.51 (3H,s,H-13),1.49 (3H,s,H-14);13CNMR (150 MHz,CDCl3)δ: 91.3 (C-5),84.7 (C-11),78.2 (C-9),69.6 (C-4),69.2 (C-6),69.0(C-2),67.6 (C-1) 66.2 (C-12),55 (C-10),49.3(C-7),42.0 (C-3),34.7 (C-8),29.5 (C-15),25.7 (C-13),25.7 (C-14)。表明含有一个1,2,4,6,9,12 -六取代的β 二氢沉香呋喃倍半萜[6]。
此外,含有2 个乙酰基1H-NMR (500 MHz,CDCl3)δ:2.10 (H-9′,3H,s,-CH3),2.30 (H-7′,3H,s,-CH3);13C-NMR (150 MHz,CDCl3)δ:21.3(C-7′),170.4 (C-6′),21.7 (C-9′),170.8 (C-8′)。1 个甲基 正丁酰氧基1H-NMR (500 MHz,CDCl3)δ: 1.25 (H-12′,2H,m),0.90 (H-11′,2H,q,J=7.09 Hz),0.80 (H-14′,3H,d,J=7.05 Hz),0.56 (H-13′,3H,t,J=7.98 Hz);13C-NMR(150 MHz,CDCl3)δ: 174.6 (C-10′),41.0 (C-12′),25.4 (C-11′),16.1 (C-14′),11.4 (C-13′)。1 个苯甲酰氧基1H-NMR (500 MHz,CDCl3)δ: 8.11 (H-22″,2H,d,J=7.18 Hz),8.11 (H-6″,2H,d,J=7.18 Hz),7.57 (H-4″,1H,m),7.50(H-3″,2H,d,J=7.18 Hz),7.50 (H-5″,2H,d,J=7.18 Hz);13C-NMR (150 MHz,CDCl3)δ:165.7(C-15′),133.6 (C-4″),129.9 (C-6″),129.9(C-2″),129.4 (C-1″),128.9 (C-3″),128.9 (C-5″)。1 个呋喃甲酰基1H-NMR (500 MHz,CDCl3)δ: 8.01 (H-4′,1H,s),7.41 (H-3′,1H,s),6.73(H-2′,1H,m);13C-NMR (150 MHz,CDCl3)δ:161.1 (C-5′),148.5 (C-4′),143.9 (C-3′),118.2 (C-1′),109.8 (C-2′)。
H-1/H-2/H-3 和H-6/ H-7/H-8/H-9 出现1H-1H COSY 相关信号,结合CH3-4 与C-5,H-6 与C-10,H-9 与C-5,H-12 与C-1、C-9 的HMBC 相关,进一步确证了母核结构为β 二氢沉香呋喃倍半萜。此外,在HMBC 谱图中,H-1 与MeButO 羰基碳(174.6) 相关,H-2 与苯甲酰基羰基碳(165.7)相关,H-6 与呋喃酰基羰基碳(161.1) 相关,H-9与甲酰基羰基碳(170.4) 相关,H-12 与甲酰基羰基碳(170.8) 相关,由此确定了平面结构。在NOESY 谱中,H-12 与H-1、H-9 相关,H-2 与H-1相关,确定H-1、H-2、H-9 的相对构型均为β 型。综合上述信息,确定该化合物的结构为1β-甲基正丁酰氧基-2β-苯甲酰氧基-4α-羟基-6α-呋喃酰氧基-9β,12-二乙酰氧基-β-二氢沉香呋喃,为一新化合物。结构见图1。

图1 化合物1 的结构和重要的HMBC 和NOESY 相关Fig.1 Structure and key HMBC and NOESY correlations of compound 1
化合物2: 白色无定形固体。HR-ESI-MSm/z:757.284 6[M+H]+(计算值757.777 3,C42H45O13),结合NMR 推测其分子式为C42H44O13。根据1H-NMR和13C-NMR 分析,该化合物具有β-二氢沉香呋喃型基本母核结构。母核1H-NMR (500 MHz,CDCl3)δ:6.93 (6-H,1H,s),6.03 (H-1,1H,d,J=3.80 Hz),5.83 (H-2,1H,m),5.76/4.65 (H-12,A/Bq,2H,J=13.01/12.99 Hz),5.67 (H-8,1H,dd,J=3.9/6.5 Hz),5.62 (H-9,1H,d,J=5.9 Hz),2.67 (H-7,1H,d,J=3.80 Hz),2.44 (H-4,1H,m),1.62 (H-14,3H,s),1.53 (H-15,3H,s),1.25 (H-13,3H,d,J=6.6 Hz);13C-NMR(150 MHz,CDCl3)δ: 90.2 (C-5),81.3 (C-11),77.7 (C-9),74.7 (C-8),72.2 (C-6),70.8 (C-2),69.9 (C-1),61.2 (C-12),53.5 (C-7),50.9(C-10),32.6 (C-4),31.9 (C-3),30.4 (C-15),24.7 (C-14),16.8 (C-13)。
取代 基1H-NMR (500 MHz,CDCl3)δ: 1.62(3H,s,-CH3),1.53 (3H,s,-CH3),1.25 (3H,d,J=6.6 Hz,-CH3),1.40、1.99、2.14 (3×3H,3×s),δ7.30-8.17 (15H,m,-C6H5);13C-NMR(150 MHz,CDCl3)δ: 20.0、21.3、21.3 (3 ×-CH3),δ128.40-133.40 (-C6H5),171.4,169.9,169.2,166.4,166.0,165.0 (6×-COO-)。以上数据与文献[7] 基本一致,故鉴定为6α,9β,12-三乙酰氧基-1β,2β,8β-三苯甲酰氧基-β-二氢沉香呋喃。
化合物3: 白色无定形固体。HR-ESI-MSm/z:773.313 4 [M+Na]+(计算值 774.076 0,C41H50O13Na),结 合 NMR 推测其 分子式 为C41H50O13。根据1H-NMR 和13C-NMR 分析,该化合物具有β-二氢沉香呋喃型基本母核结构。母核1HNMR (500 MHz,CDCl3)δ: 6.94 (H-6,1H,s),5.82 (H-1,1H,d,J=3.96 Hz),5.65 (H-8,1H,dd,J=3.8/5.9 Hz),5.57 (H-9,1H,d,J=5.79 Hz),5.53 (H-2,1H,m),5.51/4.72 (H-12,A/Bq,2H,J=12.96/12.98 Hz),2.62 (H-7,1H,d,J=3.18 Hz),1.62 (H-14,3H,s),1.50 (H-15,3H,s),1.14 (H-13,3H,d,J=7.4 Hz);13C-NMR(150 MHz,CDCl3)δ: 90.8 (C-5),80.9 (C-11),80.0 (C-9),74.9 (C-8),72.6 (C-6),70.8 (C-2),68.6 (C-1),61.2 (C-12),53.5 (C-7),51.3(C-10),33.0 (C-3),32.8 (C-4),30.4 (C-15),24.6 (C-14),16.8 (C-13)。
取代基1H-NMR (500 MHz,CDCl3)δ: 2.22、1.96、1.47 (3×3H,3×s),2.37 (2H,q,J=6.84 Hz,-CH2-),1.24 (6H,d,J=8.39 Hz,3×-CH2-),0.86 (3H,t,J=6.56 Hz,),7.38-8.11 (10H,m,2×-C6H5);13C-NMR (150 MHz,CDCl3)δ: 22.25、21.70、20.10、12.99 (4×-CH3),34.13、31.56、24.56、22.25 (4×-CH2-),128.4-133.4 (-C6H5),172.55、170.72、169.78、169.24、166.33、164.96 (6×-COO-)。以上数据与文献[7] 基本一致,故鉴定为6α,9β,12-三乙酰氧基-1β,8β-二苯甲酰氧基-2β-正己酰氧基-β-二氢沉香呋喃。
化合物4: 白色无定形固体。HR-ESI-MSm/z:801.344 8 [M+Na]+(计算值 801.848 6,C43H54NaO13),结 合 NMR 推测其 分子式 为C43H54O13。根据1H-NMR 和13C-NMR 分析,该化合物具有β-二氢沉香呋喃型基本母核结构。母核的1H-NMR (500 MHz,CDCl3)δ:6.95,(H-6,2H,s),5.87 (H-1,1H,d,J=3.96 Hz),5.69 (H-8,1H,dd,J=3.51/5.52 Hz),5.58 (H-2,1H,m),5.57 (H-9,1H,d,J=5.49 Hz),5.51/4.61 (H-12,A/Bq,2H,J=13.02/13.03 Hz),2.60 (H-7,1H,d,J=3.49 Hz),1.63 (H-14,3H,s),1.50(H-15,3H,s),1.17 (H-13,3H,d,J=6.9 Hz);13C-NMR (150 MHz,CDCl3)δ: 90.3 (C-5),81.1 (C-11),77.3 (C-9),74.8 (C-8),72.2 (C-6),71.6 (C-2),70.1 (C-1),61.2 (C-12),53.7(C-7),51.2 (C-10),32.7 (C-4),31.7 (C-3),30.4 (C-15),24.6 (C-14),16.8 (C-13)。
取代 基1H-NMR (500 MHz,CDCl3)δ: 1.62(3H,s,-CH3),1.42 (3H,s,-CH3),1.22 (3H,d,J=7.4 Hz,-CH3),2.16、1.96、1.38 (3×3H,3×s,3×-CH3),7.49-8.21 (10H,m,2×-C6H5);13C-NMR (150 MHz,CDCl3)δ: 21.3、20.8、20.1(3×-CH3),128.4-133.4 (-C6H5),170.7、169.7、169.1、166.3、165.8、164.9 (6×-COO-)。以上数据与文献[8] 基本一致,故鉴定为6α,9β,12-三乙酰氧基-1β,8β-二苯甲酰氧基-2β-正辛酰氧基-β-二氢沉香呋喃。
化合物5: 白色无定形固体,HR-ESI-MSm/z:827.360 3 [M+Na]+(计算值 827.884 4,C45H56O13Na),结 合 NMR 推测其 分子式 为C45H56O13。根据1H-NMR 和13C-NMR 分析,该化合物有β-二氢沉香呋喃型基本母核结构。母核的1HNMR (500 MHz,CDCl3)δ: 6.92 (H-6,2H,s),5.83 (H-1,1H,d,J=3.96 Hz),5.67 (H-8,1H,dd,J=3.53/5.53 Hz),5.56 (H-2,1H,m),5.54(H-9,1H,d,J=5.51 Hz),5.52/4.62 (H-12,A/Bq,2H,J=13.03/12.98 Hz),2.59 (H-7,1H,d,J=3.50 Hz),1.61 (H-14,3H,s),1.51 (H-15,3H,s),1.15 (H-13,3H,d,J=6.8 Hz);13C-NMR(150 MHz,CDCl3)δ: 90.3 (C-5),81.1 (C-11),77.3 (C-9),74.8 (C-8),72.2 (C-6),71.6 (C-2),70.1 (C-1),61.2 (C-12),53.7 (C-7),51.2(C-10),32.7 (C-4),31.7 (C-3),30.4 (C-15),24.6 (C-14),16.8 (C-13)。
取代 基1H-NMR (500 MHz,CDCl3)δ: 2.10(3H,t,J=6.23 Hz,-CH3),1.95 (3H,d,J=2.81 Hz,-CH3),1.61 (3H,s,-CH3),1.47 (3H,d,J=4.97 Hz,-CH3),1.37 (3H,d,J=17.42 Hz,-CH3),1.24 (3H,d,J=7.22 Hz,-CH3),7.49-8.20 (10H,m,2×-C6H5);13C-NMR (150 MHz,CDCl3)δ: 128.1-133.1 (-C6H5),170.7、170.0、169.6、166.2、164.9、164.9 (6×-COO-)。以上数据与文献[8] 基本一致,故鉴定为6α,9β,12-三乙酰氧基-1β,8β-二苯甲酰氧基-2β-正癸酰氧基-β-二氢沉香呋喃。
化合物6: 无色无定形固体,HR-ESI-MSm/z:762.236 1 [M+H]+(计算值 762.719 4,C36H44O17N),结 合 NMR 推测其 分子式 为C36H43O17N。根据1H-NMR 和13C-NMR 分析,该化合物具有β-二氢沉香呋喃型基本母核结构。母核1H-NMR (500 MHz,CDCl3)δ: 6.75 (H-6,1H,s),5.67 (H-1,1H,s),5.55 (H-9,1H,s),5.27(H-2,1H,m),4.77 (H-3,1H,d,J=2.7 Hz),4.55,4.80 (H-12,2H,dd,J=13.09/14.93 Hz),3.73,6.03 (H-15,2H,dd,J=11.40/11.66 Hz),3.02 (H-7,1H,br,s),1.62 (H-14,3H,s),1.60(H-13,3H,s);13C-NMR (150 MHz,CDCl3)δ:196.3 (C-8),94.5 (C-5),85.6 (C-11),78.2 (C-9),75.0 (C-3),73.8 (C-6),71.7 (C-1),70.4(C-4),70.3 (C-15),68.2 (C-2),61.0 (C-7),60.1 (C-12),52.4 (C-10),23.0 (C-13),19.8(C-14)。
取代 基1H-NMR (500 MHz,CDCl3)δ: 4.70(H-7′,q,J=8.75/17.4 Hz),8.10 (H-4′,d,J=7.02 Hz),8.69 (H-6′,d,J=3.29 Hz),7.26 (H-5′,dd,J=7.92/14.92 Hz),2.59 (H-8′,q,J=7.99 Hz),1.40 (H-9′,d,J=6.9 Hz),1.19 (H-10′,d,J=6.04 Hz),2.22、2.15、2.09、2.04、1.88 (15H,5×s,5×-CH3);13C-NMR (150 MHz,CDCl3)δ: 174.0 (C-11′),168.5 (C-12′),164.2(C-2′),151.1 (C-6′),137.6 (C-4′),125.4 (C-3′),121.3 (C-5′),44.5 (C-8′),36.2 (C-7′),11.0 (C-9′),8.7 (C-10′),169.6、169.58、169.4、168.91、168.6 (5 ×-CO-),19.8、19.2、19.1、19.0、18.8 (5×-CH3)。以上数据与文献[9] 基本一致,故鉴定为卫矛羰碱。
化合物7: 白色无定形固体,HR-ESI-MSm/z:697.245 4 [M+Na]+(计算值 697.663 3,C34H42NaO14),结 合 NMR 推测其 分子式 为C34H42O14。根据1H-NMR 和13C-NMR 分析,该化合物具有β-二氢沉香呋喃型基本母核结构。母核1HNMR (500 MHz,CDCl3)δ: 6.18 (H-6,1H,s),5.72 (H-1,1H,d,J=3.41 Hz),5.67 (H-2,1H,d,J=3.42 Hz),5.35 (H-9,1H,d,J=7.76 Hz),5.05/4.54 (H-12,A/Bq,2H,J=13.07/13.08 Hz),2.58 (H-7,1H,m),2.02-2.32 (H-3,2H),2.02-2.32 (H-8,H-3,2H),1.57 (H-15,3H,s),1.55 (H-14,3H,s),1.50 (H-13,3H,s);13CNMR (150 MHz,CDCl3)δ: 90.1 (C-5),84.3 (C-11),78.2 (C-9),70.8 (C-6),69.6 (C-4),68.7(C-2),68.0 (C-1),65.3 (C-12),55.1 (C-10),49.0 (C-7),41.4 (C-3),34.2 (C-8),27.8 (C-15),25.8 (C-14),24.3 (C-13)。
取代基1H-NMR (500 MHz,CDCl3)δ: 2.14、2.31 (6H,2×s,2×-CH3),2.42 (1H,m,-CH-),1.51 (2H,m,-CH2-),1.13 (3H,d,J=6.49 Hz,-CH3),0.83 (3H,t,J=7.05 Hz,-CH3);13C-NMR(150 MHz,CDCl3)δ: 20.16、19.78、19.07 (3×CH3),170.99、170.23、169.77、166.52、165.58(5×-COO-)。以上数据与文献[6] 基本一致,故鉴定为6α,12-二乙酸基-1β,9α-二乙酸(β-呋喃羧氧基) -4α-羟 基-2β-2-甲基丁 酯-β-二氢沉 香呋喃。
化合物8: 白色无定形固体,HR-ESI-MSm/z:653.258 7 [M+H]+(计算值 653.683 5,C35H42O12),结合NMR 推测其分子式为C35H40O12。根据1H-NMR 和13C-NMR 分析,该化合物具有β-二氢沉香呋喃型基本母核结构。母核1H-NMR (500 MHz,CDCl3)δ: 6.89 (H-6,1H,s),5.77 (H-1,1H,d,J=2.97 Hz),5.65/4.67 (H-12,ABq13,2H,J=14.3/13 Hz),5.65 (H-8,1H,dd,J=3.8/6.2 Hz),5.54 (H-9,1H,d,J=5.53 Hz),4.29(H-2,1H,s),2.59 (H-7,1H,d,J=3.18 Hz),1.59 (H-14,3H,s),1.47 (H-15,3H,s),1.21(H-13,3H,d,J=7.13 Hz);13C-NMR (150 MHz,CDCl3)δ:90.9 (C-5),80.6 (C-11),80.0 (C-9),74.8 (C-8),72.3 (C-6),70.8 (C-2),67.5 (C-1),61.1 (C-12),53.3 (C-7),51.5 (C-10),33.1(C-3),33.1 (C-4),29.4 (C-15),23.3 (C-14),15.9 (C-13)。
取代基1H-NMR (500 MHz,CDCl3)δ: 2.14、1.95、1.42 (3×H,3×s,3×-CH3),2.60 (1H,brs,-OH),7.4-8.13 (10H,m,2 ×-C6H5);13C-NMR(150 MHz,CDCl3)δ: 20.2、19.8、19.1 (3 ×CH3),128.1-133.1 (-C6H5),171.0、170.2、169.8、166.6、165.6 (5×-COO-)。以上数据与文献[7] 基本一致,故鉴定为6α,9β,12-三乙酰氧基-1β,8β-二苯甲酰氧基-2β-羟基-β-二氢沉香呋喃。
化合物9: 白色无定形固体,HR-ESI-MSm/z:697.245 6 [M+Na]+(计算值 697.663 3,C34H42NaO14),结 合 NMR 推测其 分子式 为C34H42O14。根据1H-NMR 和13C-NMR 分析,该化合物具有β-二氢沉香呋喃型基本母核结构。母核1HNMR (500 MHz,CDCl3)δ: 6.15 (H-6,1H,s),5.66 (H-1,1H,s),5.66 (H-2,1H,s),5.29 (H-9,1H,d,J=6.62 Hz),5.23/4.43 (H-12,ABq13,2H,J=12.3/12.3 Hz),2.53 (H-7,1H,m),2.11-2.36 (H-3,2H),2.11-2.36 (H-8,2H),1.56 (H-15,3H,s),1.49 (H-14,3H,s),1.47(H-13,3H,s);13C-NMR (150 MHz,CDCl3)δ:90.5 (C-5),84.5 (C-11),78.0 (C-9),69.9 (C-4),69.5 (C-6),69.0 (C-2),68.3 (C-1),65.6(C-12),54.9 (C-10),49.0 (C-7),40.8 (C-3),34.1 (C-8),28.0 (C-15),25.3 (C-14),24.6(C-3)。
取代基1H-NMR (500 MHz,CDCl3)δ: 2.30、2.11 (6H,2×s,2×-CH3),1.98 (1H,m,-CH-),1.25 (2H,m,-CH2-),0.83 (3H,d,J=6.79 Hz,-CH3),0.60 (3H,t,J=7.38 Hz,-CH3);13C-NMR(150 MHz,CDCl3)δ: 19.98、19.62 (2×-CH3),174.52、171.17、170.98、170.72、161.76 (5×-COO-)。以上数据与文献 [6] 基本一致,故鉴定为6α,12-二乙酸基-1β,9α-二乙酸 (β-呋喃羧氧基) -4α-羟 基-1β-2-甲基丁 酯-β-二氢沉 香呋喃。
化合物10: 白色无定形固体,HR-ESI-MSm/z: 696.268 9 [M+H]+(计算值696.719 4,C37H44O13),结合NMR 推测其分子式为C37H43O13。根据1H-NMR 和13C-NMR 分析,该化合物具有β-二氢沉香呋喃型基本母核结构。母核1H-NMR (500 MHz,CDCl3)δ: 6.89 (H-6,1H,s),5.83 (H-1,1H,d,J=2.78 Hz),5.81 (H-2,1H,m),5.67(H-8,1H,dd,J=3.8/6.3 Hz),5.55 (H-9,1H,d,J=5.15 Hz),5.46/4.60 (H-12,ABq13,2H,J=5.1/12.4 Hz),2.59 (H-7,1H,J=3.25 Hz),1.59 (H-14,3H,s),1.47 (H-15,3H,s),1.17(H-13,3H,d,J=7.15 Hz);13C-NMR (150 MHz,CDCl3)δ:90.1 (C-5),80.8 (C-11),77.4 (C-9),74.5 (C-8),72.0 (C-6),70.6 (C-1),70.6 (C-2),60.5 (C-12),53.3 (C-7),50.9 (C-10),32.8(C-4),30.8 (C-3),30.6 (C-15),23.1 (C-14),15.5 (C-13)。
取代基1H-NMR (500 MHz,CDCl3)δ: 2.15、2.09、1.98、1.42 (4×3H,4×s,4×-CH3),7.39-8.13 (10H,m,2×-C6H5);13C-NMR (150 MHz,CDCl3)δ: 20.0、20.0、19.6、18.9 (4×-CH3),170.8、170.0、170.0、169.6、166.3、164.9 (6×-COO-),128.1-133.1 (-C6H5)。以上数据与文献[7] 基本一致,故鉴定为6α,9β,12-四乙酰氧基-1β,8β-二苯甲酰氧基-β-二氢沉香呋喃。
4 药理活性筛选
采用MTT 法[10-14]研究10 种化合物对Hela 细胞的体外抑制作用,采用5-氟尿嘧啶做阳性对照。取对数期生长的Hela 细胞,经胰酶消化,用RPMI 1640 完全培养基稀释成单细胞悬液,调整细胞密度为5×104个/mL,以每孔100 μL 加到96 孔板中,常规培养过夜。次日加入以上10 个受试化合物并 设5 个不同 质量浓 度 (0.1、1、5、10、15 μg/mL) 作用24 h 后终止培养,设置正常组并分别设置6 个复孔。于每孔中分别加入10 μL MTT试剂,继续培养4 h 后,弃去上清液,每孔加入DMSO 100 μL,轻度振荡10 min 后,用酶标仪测定各孔在490 nm 下的吸光度,计算细胞增值率和IC50值。结果显示化合物6 对Hela 细胞有一定的抑制作用,其IC50为9.76 μg/mL,其他化合物没有抑制作用,结果见表1。
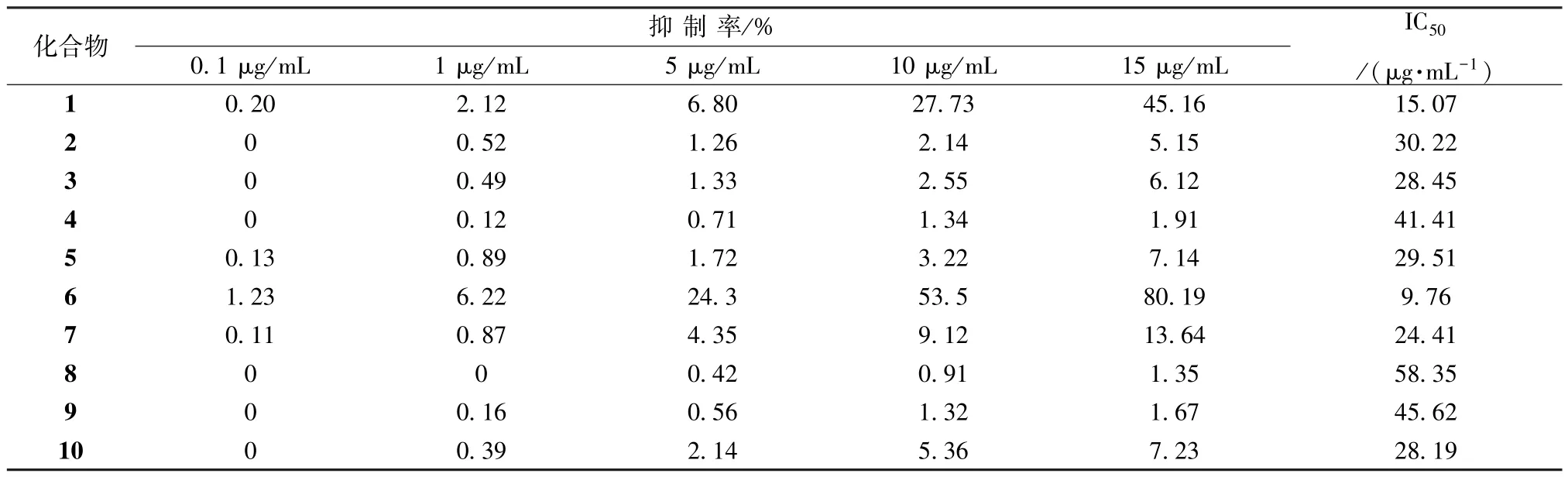
表1 各化合物对Hela 细胞的抑制作用Tab.1 Inhibition of various compounds on Hela cells
5 讨论
丝棉木是民间常用的活血通络的草药之一,关于其化学成分及活性筛选的研究较少,但关于β-二氢沉香呋喃类化合物的研究较多,张海艳等[15]从苦皮藤种子中提取了6 个β-二氢沉香呋喃多醇酯类化合物;朱辉等[16]发现卫矛属植物中含有β-二氢沉香呋喃类化合物;赵兴增等[17]研究了永瓣藤茎叶中的β-二氢沉香呋喃型的化合物;贺正山等[18]对灯油藤进行了研究,发现种子中β-二氢沉香呋喃型化合物较多。
本研究从中分离得到10 个化合物,其中化合物1 为新化合物。采用体外抗肿瘤的方法,研究10 个化合物对Hela 细胞的抑制作用,其中化合物6 对Hela 细胞有抑制作用,其他化合物对Hela 细胞无抑制作用,表明化合物6 对于Hela 细胞的抑制可能有良好的发展前景。
