四神丸中3 种成分在正常大鼠及抑郁大鼠体内药动学的比较
2020-06-02宋珊珊居文政
孙 红,宋珊珊,井 汶,张 优,谷 雨,居文政
(南京中医药大学附属医院,江苏 南京210029)
抑郁症具有高发病、高自杀、高复发和低识别、低就诊、低治疗等特点,已成为21 世纪最主要的精神疾病,据WHO 统计,全球抑郁症患者达12.8%,预计2030 年将成为仅次于心血管疾病的第二大疾病[1-2],我国患病率高达6.1%[3]。目前,抗抑郁西药以单胺类抑制剂为主[4],但这些药物起效慢,不良反应明显,而且30%~50%的患者不敏感。近年来,中医药在防治抑郁症上获得较好的临床疗效。
四神丸出自 《证治准绳》,由肉豆蔻、补骨脂、五味子、吴茱萸、大枣等药材组成[5],具有温补脾肾的功能,组方加减后用于治疗脾肾阳虚患者有一定疗效[6]。原发性抑郁、内源性抑郁、恶劣心境中的抑郁情绪在本质上“属虚”,五脏阳气不足是其病理基础[7],根据中医郁证病机中“阳虚致郁” 的理论[8-9],四神丸可改善脾肾阳虚所致的抑郁状态,动物实验表明[10-14],方中补骨脂和五味子中主要成分补骨脂素、异补骨脂素、五味子醇甲具有抗抑郁作用,但作用机理尚不明确,虽然已有方中补骨脂素、异补骨脂素在正常大鼠中的药动学研究[15],但尚未见在抑郁大鼠中的相关报道。因此,本实验将比较四神丸中上述3 种成分在正常大鼠和抑郁大鼠体内的药动学,探索其作用机理。
1 材料
1.1 仪器 Agilent 1200 高效液相色谱仪,配置API 4000 LC-MS/MS 三重四级杆质谱仪 (美国Agilent 公 司);MS105 电子天 平 (瑞 士Mettler-Toledo 公司);Centrifuge-5417R 冷冻离心机(德国Eppendorf 公司);Advantage A10 超纯水机(法国Millipore 公司);MIX-25P 旋涡混合仪(杭州米欧仪器有限公司);Labconco 离心浓缩仪 (美国Labconco 公司);RE-52CS 旋转蒸发仪(上海亚荣生化仪器厂)。
1.2 试剂与药物 肉豆蔻(煨) (批号171001)、补骨脂(盐炒) (批号180404006)、五味子(醋制) (批号170513001)、吴茱萸(制) (批号160623)、大枣(去核) (批号170520001) 均购于北京同仁堂南京药店,经江苏省中医院药学部副主任中药师张倩鉴定为正品,符合《中国药典》标准。对照品补骨脂素(批号17092820)、异补骨脂素 (批 号18062910)、五味子醇甲 (批 号17021905) 均购于成都曼思特生物科技有限公司,纯度均≥98.5%;替硝唑 (批号100126-200402)购于中国食品药品检定研究院,纯度≥95%。四神丸根据2015 年版《中国药典》 处方自制,补骨脂、肉豆蔻、五味子、吴茱萸、大枣比例为4 ∶2 ∶2 ∶1 ∶2,上述药材用10 倍量75% 乙醇浸泡30 min,回流提取2 h,滤渣再加8 倍量75%乙醇回流提取1 h,合并滤液,减压浓缩至无醇味,-20 ℃下保存,1 100 g 药材浓缩至785 mL,即每1 mL 药液含1.4 g 原药材(分别含补骨脂素、异补骨脂素、五味子醇甲1.60、1.36、0.65 mg)。甲醇、乙腈购自德国Merck 公司;水为超纯水。
1.3 动物 SD 大鼠,雄性,12 只,体质量(190±10)g,由南通大学实验动物中心提供,动物生产许可证号SCXK (苏) 2019-0001。实验前大鼠适应性饲养1 周,保持12 h 昼夜节律,室温(22±2) ℃,自由摄食饮水。
2 方法与结果
2.1 色谱、质谱条件 ACE Excel 3 C18-PFP 色谱柱(100 mm×3.0 mm);流动相乙腈-0.1% 甲酸(36 ∶64);体积流量500 μL/min;柱温40 ℃;离子源ESI+,多反应检测模式(MRM);离子源电压4 000 V;离子源温度400 ℃。质谱参数见表1。
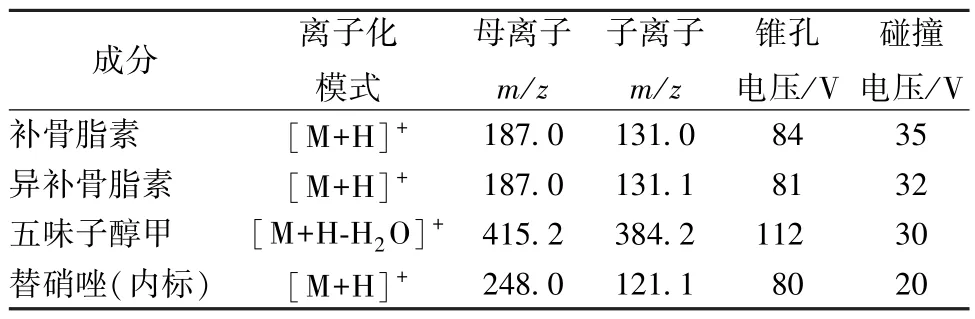
表1 各成分质谱参数Tab.1 MS parameters for various constituents
2.2 溶液制备 精密称取补骨脂素、异补骨脂素、五味子醇甲对照品适量,甲醇分别溶解定容至2.07、2.14、2.00 mg/mL,以此为母液,临用前稀释。再精密称取替硝唑适量,配制成100 ng/mL内标液。
2.3 血浆样品处理 取100 μL 空白血浆,加入10 μL 内标溶液,涡旋混匀30 s,加入800 μL 乙酸乙酯,振荡3 min,12 000 r/min 离心10 min,取700 μL 上清液,40 ℃下离心浓缩,加入100 μL 50%乙腈复溶,振荡3 min,12 000 r/min 离心10 min,取5 μL 上清液进样分析。
2.4 造模及血浆样品采集 大鼠按体质量均衡和随机的原则分为正常组和模型组,每组6 只,正常组每笼3 只,模型组单笼饲养,并在21 d 内接受10 种刺激因子,包括禁食、禁水、潮湿垫料、昼夜颠倒、闪光、4 ℃冰水游泳、热刺激5 min、束缚应激6 h、水平振荡10 min、触摸陌生异常物品。确认造模成功后,第22 天大鼠禁食不禁水12 h,灌胃给 予四神 丸混悬 液 6.48 g/kg (即4.63 mL/kg),于给药前及给药后5、15、30、45、60、90、120、180、240、360、480、720、960、1 440 min眼眶取血各约0.3 mL,置于肝素化EP 管中,4 000 r/min 离心10 min,取上层血浆保存于-80 ℃冰箱中待测。
2.5 行为学实验 在造模3 周后开始。
2.5.1 糖水消耗实验 大鼠在适应性期间给予2瓶2%蔗糖溶液适应3 d 后,才进行实验。大鼠禁水18 h,每只给予体积相同的1 瓶2%蔗糖溶液和1 瓶纯水,测试4 h,其中每2 h 2 瓶水交换位置。实验结束后,计算糖水消耗率,公式为糖水消耗率= [(蔗糖消耗量) / (纯水消耗量+蔗糖消耗量)] ×100%。
2.5.2 旷场实验 实验前需提前将大鼠搬入测试室使其适应环境1 h,再放入长、宽、高均为50 cm,内壁涂黑的纸箱中心,底面平均分为25个10 cm×10 cm 的小方格。以5 min 内大鼠三爪以上穿越底面的方格数为水平得分,穿越1 格得1 分;以大鼠双前肢抬起1 cm 以上次数为垂直得分,离地一次得1 分。实验过程进行摄像和计时。
2.5.3 强迫游泳实验 正式实验前1 d 大鼠进行预游泳,将其放入(24±2)℃水中并保持悬浮,四肢不能触及桶底,15 min 后取出,擦干放回笼中,整个实验过程保持安静。次日在相同条件下大鼠强迫游泳5 min,记录后4 min 内不动时间(大鼠仅有头部露出水面,呈漂浮状态,四肢可有微动)。
2.5.4 结果分析 经过21 d 造模后,与正常组比较,模型组大鼠糖水消耗率、水平得分、竖直得分降低 (P<0.05,P<0.01),不动时 间延长(P<0.05),显示造模成功,见表2。
表2 各组大鼠行为学实验结果(, n=6)Tab.2 Results of behavioral tests for rats in various groups (, n=6)

表2 各组大鼠行为学实验结果(, n=6)Tab.2 Results of behavioral tests for rats in various groups (, n=6)
注:与正常组比较,∗P<0.05,∗∗P<0.01。
2.6 方法学考察
2.6.1 专属性考察 取空白大鼠血浆、空白大鼠血浆+对照品+内标(替硝唑)、给药1 h 后血浆样品,按“2.3” 项下方法处理,在“2.1” 项条件下进样测定,结果见图1。由此可知,补骨脂素、异补骨脂素、五味子醇甲、内标(替硝唑) 保留时间分别为4.72、5.24、7.34、1.5 min,各成分与内标色谱峰峰形良好而且互不干扰,同时血浆中杂峰也无干扰,基线平稳,表明该方法专属性良好。

图1 各成分LC-MS/MS 色谱图Fig.1 LC-MS/MS chromatograms of various constituents
2.6.2 线性关系考察 取100 μL 空白大鼠血浆,加入对照品、内标溶液各10 μL,按“2.3” 项下方法处理,在“2.1” 项条件下进样测定。以各成分峰面积与内标峰面积的比值为纵坐标(Y),溶液质量浓度为横坐标(X) 进行回归,以S/N≥10为最低定量限,结果见表3,可知各成分在各组范围内线性关系良好。

表3 各成分线性关系Tab.3 Linear relationships of various constituents
2.6.3 准确度、精密度试验 取100 μL 空白大鼠血浆,制成低、中、高3 个质量浓度的样品(补骨脂素3.2、80、1 200 ng/mL,异补骨脂素1.6、40、600 ng/mL,五味子醇甲0.32、8、120 ng/mL),按“2.3” 项下方法处理,在“2.1” 项色谱条件下进样测定,连续3 d,结果见表4,可知该方法准确度、精密度良好。

表4 各成分准确度、精密度、基质效应试验结果Tab.4 Results of accuracy,precision and matrix effect tests for various constituents
2.6.4 基质效应试验 精密加入低、中、高质量浓度对照品溶液及内标溶液各10 μL,复溶到80 μL,振荡3 min,12 000 r/min 离心10 min,取上清液5 μL,在“2.1” 项色谱条件下进样测定,峰面积为A1;按“2.3” 项下方法提取空白血浆(不加内标),离心浓缩后同法操作,峰面积为A2,计算基质效应,公式为基质效应=A2/A1×100%,结果见表4,可知内源性物质对3 种成分无影响。
2.6.5 稳定性试验 取100 μL 空白大鼠血浆,按“2.6.3” 项下方法制成低、中、高3 个质量浓度的样品各3 份,分别在室温下放置12 h、-20 ℃下反复冻融3 次、-80 ℃下保存30 d 后,在“2.1”项色谱条件下进样测定。结果,补骨脂素、异补骨脂素、五味子醇甲峰面积RSD 分别为0.99%~5.16%、1.09%~4.78%、0.90%~4.24%,表明该方法稳定性良好,符合生物样品分析要求。
2.6.6 提取回收率 取100 μL 空白大鼠血浆,按“2.6.3” 项下方法制成低、中、高3 个质量浓度的质控样品,各5 份,在“2.1” 项色谱条件下进样测定,峰面积为A3,计算提取回收率,公式为提取回收率=A3/A2×100%。结果,补骨脂素、异补骨脂素、五味子醇甲提取回收率分别为66.33%~70.28%、61.28%~74.45%、61.93%~68.16%。
2.7 药动学研究 各成分在正常大鼠、抑郁大鼠体内的血药浓度-时间曲线见图2,经DAS1.0 软件处理分析后主要药动学参数见表5。由此可知,各成分药动学均符合一室模型;与正常组比较,模型组各成分Cmax、AUC0~t升高(P<0.05,P<0.01),以异补骨脂素更明显。

图2 各成分血药浓度-时间曲线Fig.2 Plasma concentration-time curves for various constituents
表5 各成分主要药动学参数(, n=6)Tab.5 Main pharmacokinetic parameters for vairous constituents (, n=6)

表5 各成分主要药动学参数(, n=6)Tab.5 Main pharmacokinetic parameters for vairous constituents (, n=6)
注:与正常组比较,∗P<0.05,∗∗P<0.01。
3 讨论
本实验在测定大鼠血浆中补骨脂素、异补骨脂素、五味子醇甲含有量时发现,补骨脂素、异补骨脂素是同分异构体,质荷比相同,质谱无法区分,故应用液相色谱将两者分离开。在考察流动相时发现,乙腈作为有机相峰形和出峰时间较好,而0.1%甲酸作为水相同分异构体峰形良好。再通过考察不同型号和品牌色谱柱,确定ACE Excel 3 C18-PFP色谱柱(100 mm×3.0 mm) 能满足分析要求。
在血浆样本处理过程中,本实验考察了蛋白沉淀(甲醇、乙腈、10% 三氯乙酸) 和液液萃取(乙酸乙酯、丙酮、二氯甲烷),发现甲醇、乙腈蛋白沉淀的提取回收率与乙酸乙酯萃取的相近,且后者萃取后能明显减少血浆样本内源性物质干扰,提高基质效应,故选择乙酸乙酯萃取作为前处理方法。
不同文献报道的补骨脂素、异补骨脂素药动学参数并不一致[15],其原因可能是本实验采用75%乙醇作为提取溶剂,而文献采用水煎煮法,提取出来成分相差较大,给药剂量也有所差异。与正常组大鼠比较,模型组补骨脂素、异补骨脂素、五味子醇甲t1/2无明显差异;异补骨脂素、五味子醇甲Tmax无明显差异,而补骨脂素Tmax高于正常组;3种成分在抑郁大鼠体内的Cmax分别为在正常大鼠体内的1.36、1.30、1.47 倍,AUC0~t分别为1.38、1.27、1.40 倍,AUC0~∞分别为1.38、1.26、1.33倍,表明各成分吸收程度在抑郁大鼠体内明显提高,而消除速度无明显变化,其原因可能是疾病状态导致其吸收过程发生改变[16-17]。综上所述,大鼠在抑郁状态下四神丸中补骨脂素、异补骨脂素、五味子醇甲血药浓度明显改变,对临床上抑郁症患者用药量具有一定参考意义。
