香蕉纤维素-壳聚糖/聚丙烯酰胺双网络水凝胶的制备及吸附性能
2020-05-19宋传捷郑丽丽郑晓燕艾斌凌郝凤岭盛占武
宋传捷,郑丽丽,郑晓燕,艾斌凌,杨 旸,钟 爽,校 导,郝凤岭,盛占武※
(1.吉林化工学院石油化工学院,吉林132022;2.中国热带农业科学院海口实验站,海口571101)
0 引 言
水凝胶是水和聚合物的聚合体[1],由高分子主链和亲水性官能团通过共价键、离子键、氢键或者是物理缠绕交联等方式形成[2]。许多聚合物均可形成水凝胶并携带各种官能团,赋予水凝胶各种性质,应用于组织工程、药物载体、光学和流体致动器、生物细胞基质的体外模型、水处理等领域[3-6]。然而,由于大量水分子的存在,聚合物网络是稀疏的,水凝胶中聚合物网络结构呈现不均匀性,表现出较差的力学性能,在外力作用下极易破碎,大大限制了其应用范围[7]。因此,保持水凝胶高含水量的基本特性不变,改变水凝胶网络结构是提升其力学性能的有效手段和重要途径。
目前高强度高韧性的水凝胶材料主要有拓扑水凝胶[8],纳米复合水凝胶[9-11],离子交联水凝胶[12]以及双网络水凝胶(double network hydrogel,DN)[13]。其中双网络水凝胶因其简单的制备方法和卓越的力学性能,受到广泛关注。DN水凝胶是由两层相互贯穿的聚合物网络构成,第一层网络是高交联密度的刚性网络;第二层网络为低交联密度的柔性网络[14]。在外力作用下,第一层刚性网络断裂牺牲,第二层柔性网络抑制裂隙的扩展,两种相互渗透的网络之间的应力转移、能量耗散起到增韧作用[15]。DN水凝胶的合成一般采用多步连续自由基聚合工艺。第一层刚性网络聚合形成以后浸入第二层柔性聚合物溶液中,通过溶胀、扩散、聚合等多步完成,聚合过程繁琐且耗时,很难控制2个网络的准确摩尔比,造成第二层网络聚合物溶液的大量浪费。而“一锅法”是将2种聚合物水凝胶的前体溶液充分混合渗透,满足2种网络聚合反应的条件下,同时形成第一层网络和第二层网络且相互渗透和贯穿,大大简化合成工艺,缩短反应时间,且有利于提升双网络水凝胶结构的均匀性和形状的随意性[16]。
纤维素 (cellulose,Ce)、壳聚糖 (chitosan,Cs)是地球上最丰富的天然高分子材料,他们具有优良的生物相容性、生物降解性、低毒性、抗菌止血活性和螯合能力,分子链上存在大量的羟基和氨基活性位点,在一定的试验条件下(如pH值、离子强度、温度)通过改变表观电荷密度,氢键在聚合物链之间相互作用可生成水凝胶[16-20]。然而,壳聚糖在酸性溶液中溶剂化程度很高,溶解不受控制,分子内氢键被破坏,其分子链很难保持刚性链构象。前期研究结果表明:壳聚糖中添加香蕉纤维素可使水凝胶结构更加紧密,可作为重金属离子吸附剂[21]。但这些天然多糖制备的水凝胶是单网络刚性结构,其结构不均匀、不稳定,表现出较差的机械性能,在吸附重金属的应用过程中不利于多次重复利用[22-23]因此,本文利用从废弃香蕉茎秆中提取的香蕉纤维,预处理后得到香蕉纤维素,再引入到壳聚糖网络中以增加第一层网络刚性,聚丙烯酰胺(polyacrylamide,PAAM)作为第二层柔性网络,采用“一锅法”制备出香蕉纤维素-壳聚糖/聚丙烯酰胺双网络水凝胶,考察了其结构、机械性能、溶胀性能和吸附性能,并将其应用于水体中重金属离子的吸附。本研究不仅为水处理中重金属的吸附提供理论参考,也将为香蕉茎秆废弃物的利用提供新的途径。
1 材料与方法
1.1 试剂与仪器
主要试剂:香蕉茎秆纤维素(cellulose,Ce),中国热带农业科学院海口实验站;壳聚糖(chitosan,Cs)(Beijing Solarbio Science&Technology Co.,Ltd);丙烯酰胺(acrylamide,AAM)、N,N-亚甲基双丙烯酰胺(N,N-methylene bisacrylamide,MBA)、α-酮戊二酸,均为分析纯(成都艾科达化学试剂有限公司);乙酸(acetic acid,AA)、过硫酸钾(potassium persulfate,PPS),分析纯(西陇科学股份有限公司);环氧氯丙烷(epichlorohydrin,ECH),分析纯 (Aladdin Industrial Corporetion);四甲基乙二胺(Shanghai Macklin Biochemic al.Co.,Ltd.)。
主要仪器:DF-101D型集热式恒温磁力搅拌器(巩义市予华仪器有限责任公司);AL-104型精密电子天平紫外工作台(梅特勒-托利多仪器(上海)有限公司);QSDC-Ⅱ型紫外灯车(常州市戚墅堰医疗器械有限公司)。
1.2 水凝胶的制备
1.2.1 聚丙烯酰胺(polyacrylamide,PAAM)水凝胶的制备
称取4.26 g丙烯酰胺加入到10 mL去离子水中溶解,完全溶解后加入0.02 g MBA、0.2 g PPS、0.2 g α-酮戊二酸和2 μL四甲基乙二胺,然后将溶液放在紫外灯(功率8 W,波长254 nm)光照下反应1 h,之后将其置于室温下24 h,得到白色透明聚丙烯酰胺水凝胶(反应机理如图1)。
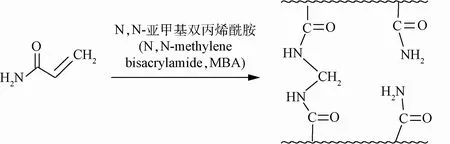
图1 聚丙烯酰胺(PAAM)水凝胶的合成Fig.1 Synthesis of polyacrylamide(PAAM)hydrogel
1.2.2 香蕉纤维素-壳聚糖(cellulose-chitosan,Ce-Cs)水凝胶的制备
称取0.5 g香蕉纤维素和0.5 g壳聚糖加入到20 mL离子液体中,60℃下搅拌2 h,得到淡黄色黏稠液体,冷却至室温后用去离子水浸泡7 d,每天换2次水,去除离子液体,得到淡黄色香蕉纤维素-壳聚糖凝胶(反应机理如图2)。
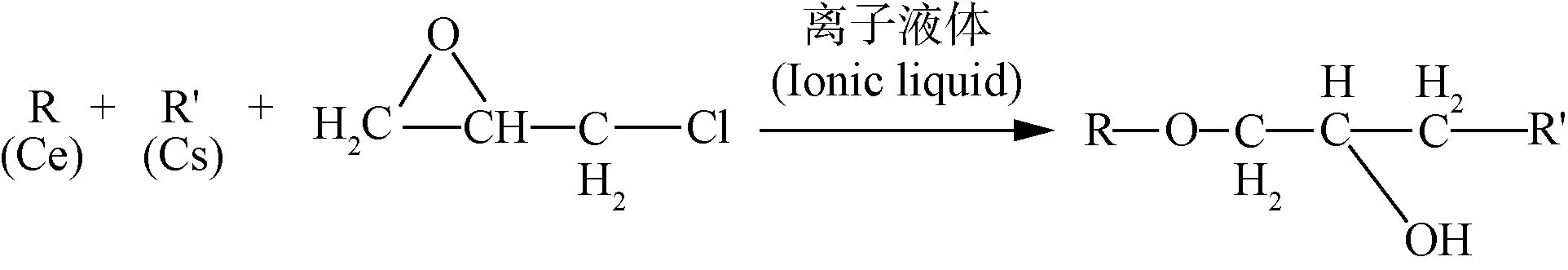
图2 纤维素-壳聚糖(Ce-Cs)水凝胶的合成Fig.2 Synthesis of cellulose-chitosan(Ce-Cs)hydrogel
1.2.3 香蕉纤维素-壳聚糖/聚丙烯酰胺(cellulose-chitosan/polyacrylamide,Ce-Cs/PAAM)双网络水凝胶的制备
称取0.5 g香蕉纤维素和0.5 g壳聚糖加入到20 mL 0.1 mol/L乙酸中,60℃下搅拌5 h;加入4.26 g丙烯酰胺和3 mL环氧氯丙烷,室温下搅拌1 h;加入0.02 g N,N-亚甲基双丙烯酰胺、0.02 g过硫酸钾、0.2 g α-酮戊二酸搅拌反应15 min;室温下放置24 h使反应达到平衡,之后放在紫外光照下6 h,然后用去离子水洗涤7 d,每天换2次水,得到白色不透明香蕉纤维素-壳聚糖/聚丙烯酰胺双网络凝胶(反应机理如图3)。
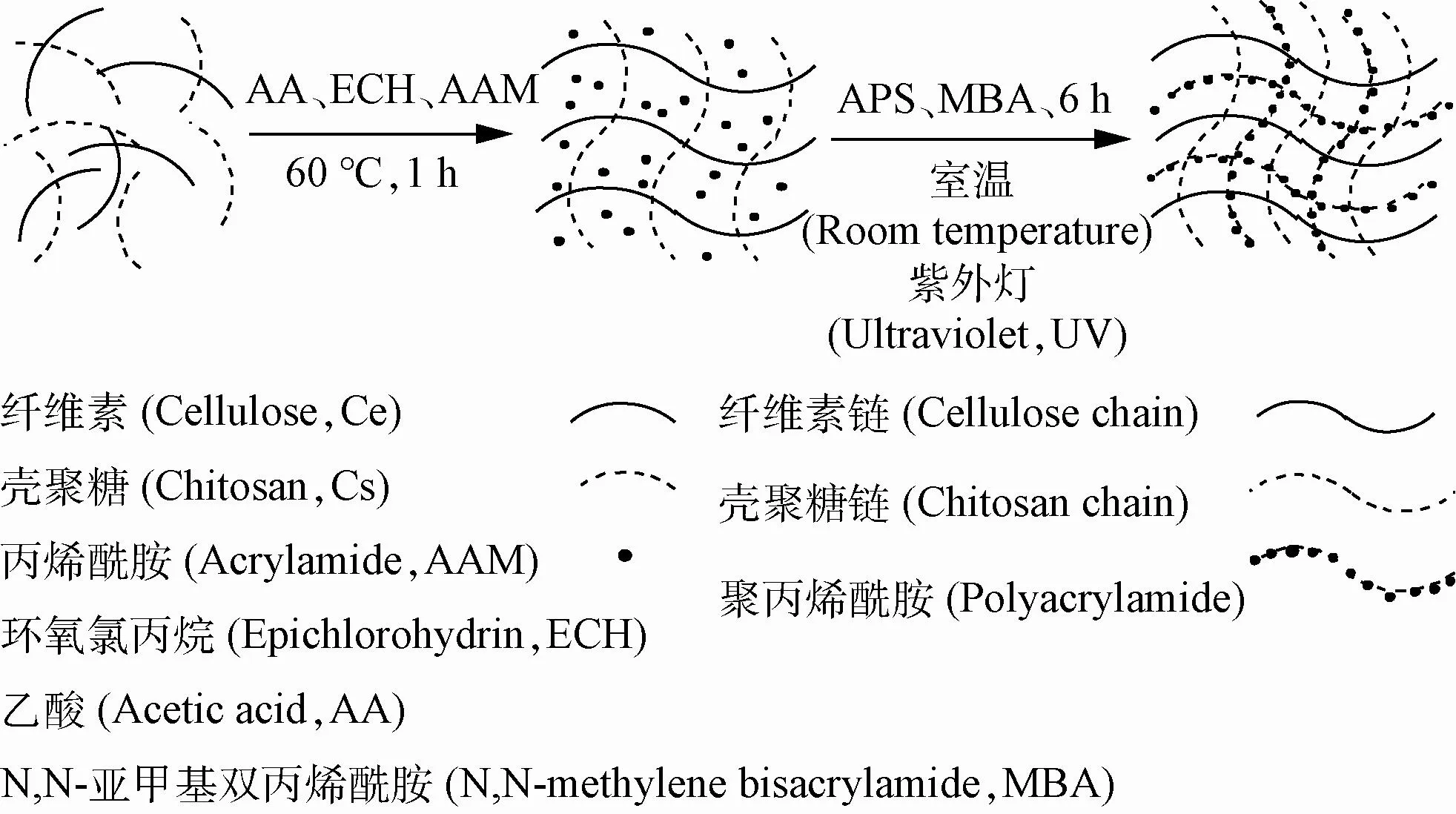
图3 纤维素-壳聚糖/聚丙烯酰胺(Ce-Cs/PAAM)双网络水凝胶的形成示意图Fig.3 Schematic diagram of formation of cellulose-chitosan/polyacrylamide(Ce-Cs/PAAM)double network hydrogel
1.3 测试与表征
1.3.1 傅里叶红外光谱(Fourier transform infrared,FTIR)
将冷冻干燥后的水凝胶研磨成粉末状,使用德国Bruker,Tensor 27型傅立叶变换红外光谱仪,用KBr压片法对样品进行测试,测试波长范围为500~4000 cm-1。
1.3.2 扫描电子显微镜(scanningelectronmicroscope,SEM)
水凝胶样品经过冷冻干燥后,采用美国Thermo Scientific,Helios NanoLab 600i扫描电子显微镜SEM观察Ce-Cs、PAAM和Ce-Cs/PAAM水凝胶的表面形貌。冷冻干燥前将样品放入-20℃预冷24 h,以免产生表面裂纹。测试时样品表面经过喷金处理。
1.3.3 X射线衍射(X-ray diffractometer,XRD)
采用日本理学公司UltimaⅣ型X射线衍射仪对水凝胶进行XRD分析,测量时采用Cu射线(λ=0.154 06 nm),在加速电压为40 kV,加速电流为30 mA的条件下扫描速度为 5º/min,扫描范围为5°~40°。得到的图谱用Jade 6软件处理。
1.3.4 溶胀性能
将预先称得一定质量的Ce-Cs、PAAM和Ce-Cs/PAAM水凝胶,室温下在一定量的蒸馏水中浸泡7 d,使其充分溶胀,将溶胀的水凝胶从蒸馏水中取出,用滤纸对其表面干燥并称质量。溶胀性能用溶胀度R表示,R的计算公式如下:

式中R是溶胀度;mt是水凝胶溶胀后的质量,mg;m0是干燥的水凝胶质量,mg。
1.3.5 力学性能
Ce-Cs/PAAM水凝胶的压缩测试是通过万能试验机(SHIMADZU AGS-X 10KN)在室温下测得的。万能试验机压缩测试样品为直径13 mm,高度8 mm的圆柱体。测试过程中,压缩速率恒定,为2 mm/min。水凝胶的压缩应变与压缩强度同样由破裂点得到。
压缩强度计算公式如下:

式中σ为压缩强度,MPa;P为最大载荷,N;r为圆柱半径,mm。
压缩应变计算公式如下:

式中ε为压缩应变;L为压缩机压缩的距离,mm;L0为样品柱原始高度,mm。
1.3.6 吸附性能
用硫酸铜配制含铜离子(Cu2+)的水样,根据需要在使用过程中逐级稀释。采用紫外分光光度法测定溶液的吸光度,利用标准曲线法计算出Cu2+的质量浓度。
通过计算水凝胶对Cu2+的吸附效率来评价其吸附效果。计算公式如下:

式中Qe表示吸附量,mg/g;C0表示Cu2+初始浓度,mg/L;Ce表示水凝胶吸附后Cu2+浓度,mg/L。
2 结果与分析
2.1 FTIR结果分析
PAAM水凝胶光谱中3 100和3 010 cm-1处的峰是NH的伸缩振动,1 704 cm-1处的峰是C=O的拉伸振动,1 583 cm-1是N-H cm-1变形振动,1 454 cm-1是C-N拉伸,1 091 cm-1处是-NH2面内摇摆振动。1 583和1 330 cm-1处的峰分别指定酰胺的-N2H弯曲振动和仲酰胺的C-N拉伸[24]。Ce-Cs水凝胶的红外光谱显示,壳聚糖结构中-NH2基团的弯曲振动在1 730 cm-1处有一条带(图4)。此外,3 425 cm-1处的谱带与-NH2和-OH基团的拉伸振动有关,这些官能团使得形成均匀的Ce-Cs共混水凝胶成为可能[25]。1 065 cm-1处的峰对应于来自糖苷单元的C-O-C。1 374、2 885和1 566 cm-1处的峰值分别是-OH、-CH和C=O。在1 590和1 320 cm-1处,分别为二次酰胺的酰胺弯曲振动(N-H)和C-N拉伸峰值。此外,在Ce-Cs/PAAM双网络水凝胶的光谱中,3 300~3 000 cm-1(O-H和N-H拉伸振动)附近的峰变得更宽,这是由于形成氢键所导致的。可能是由于第一层网络与第二层网络之间新增了分子间氢键作用。此外,与Ce-Cs和PAAM相比,Ce-Cs/PAAM水凝胶并没有出现明显特征峰的移动或增加,表明他们之间并没有新的化学键出现。也就是说,在Ce-Cs/PAAM双网络水凝胶中,第一层网络与第二层网络没有发生其他化学反应,由此得到了Ce-Cs/PAAM双网络混合水凝胶[26]。
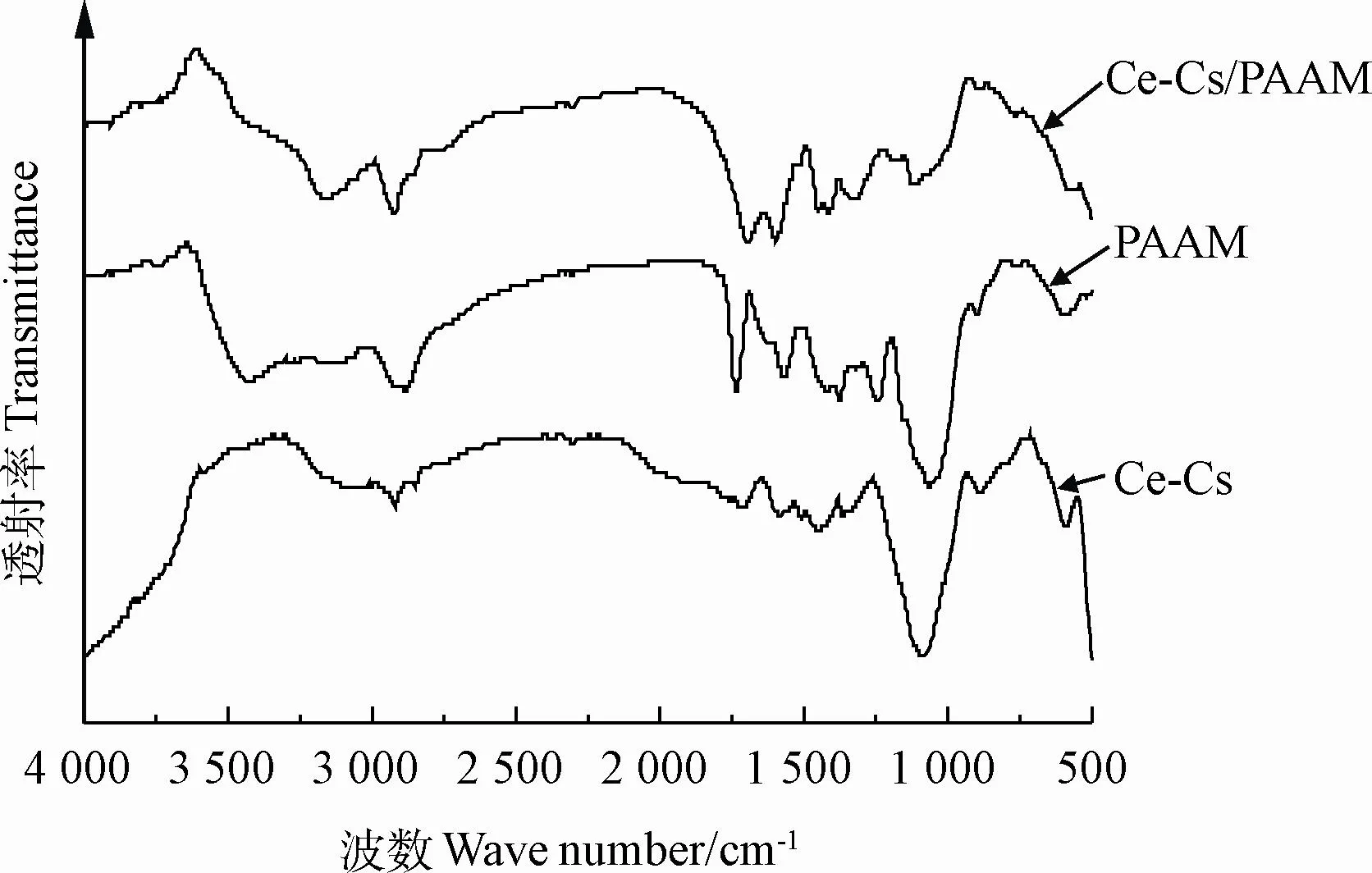
图4 不同水凝胶傅里叶红外测试(FTIR)谱图Fig.4 Fourier transform infrared(FTIR)spectra of different hydrogels
2.2 SEM结果分析
图5 a、5b可以看出,Ce-Cs水凝胶具有三维相互贯通的孔隙结构,孔洞清晰可见,孔洞壁光滑,表明该水凝胶透气性好,孔隙性较高。在图5a中,可以清晰地看出,纤维素作为支点连接孔洞结构,使得成孔结构更加稳定。从图5c、5d中可以看出PAAM水凝胶为层状结构,且表面光滑,与文献[27-28]报道结果相似;也可以看到样品有些粘连,可能是由于它们具有较大的内比表面积而极易吸潮所致。图5e、5f为Ce-Cs/PAAM水凝胶截面的SEM照片。与Ce-Cs水凝胶比较,Ce-Cs/PAAM水凝胶的孔状结构更加密集,孔隙大小更加均匀,与PAAM水凝胶相比较,Ce-Cs/PAAM水凝胶的结构变得粗糙,这是因为少量纤维素和壳聚糖嵌入孔壁中,从而起到增强水凝胶机械强度的作用。
2.3 XRD结果分析
从PAAM图像中可以看出,PAAM基本为非晶结构,只在衍射角(2θ)为20°~23°出现了特征弥散衍射峰(图6),说明PAAM由大部分非晶和少量结构松散的晶体组成[28]。与Ce-Cs图像相比较,Ce-Cs/PAAM图像中,纤维素I型的结晶衍射峰基本消失,表明在有交联剂环氧氯丙烷存在的情况下,纤维素的结晶结构在复合物的制备过程中受到了破坏,纤维素的结晶度下降,这种结构利于吸附过程中重金属离子进入到水凝胶内部网络中,从而提高水凝胶对重金属离子的吸附量[29]。
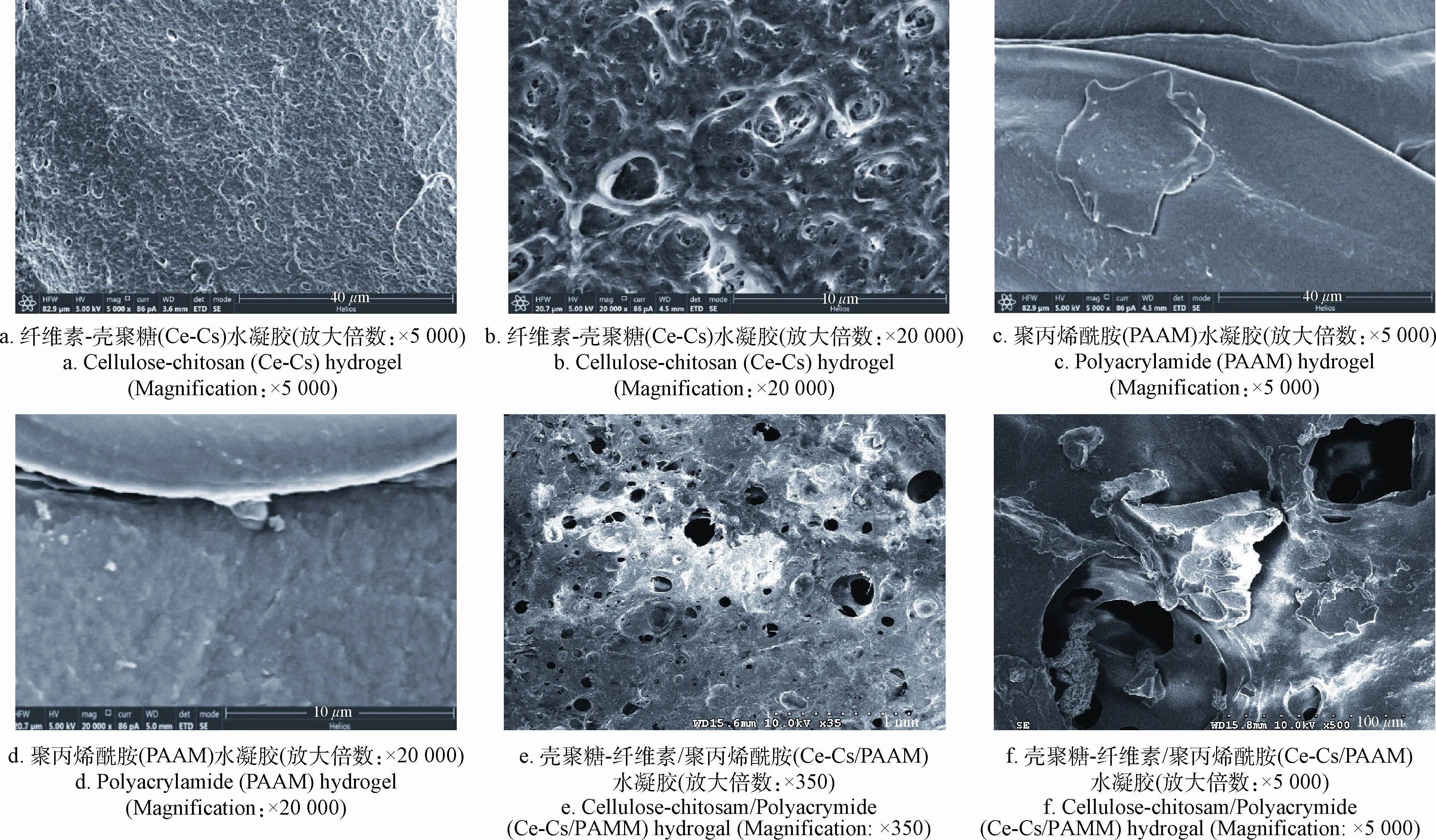
图5 不同水凝胶扫描电镜分析Fig.5 Scanning electron microscope analysis different hydrogel
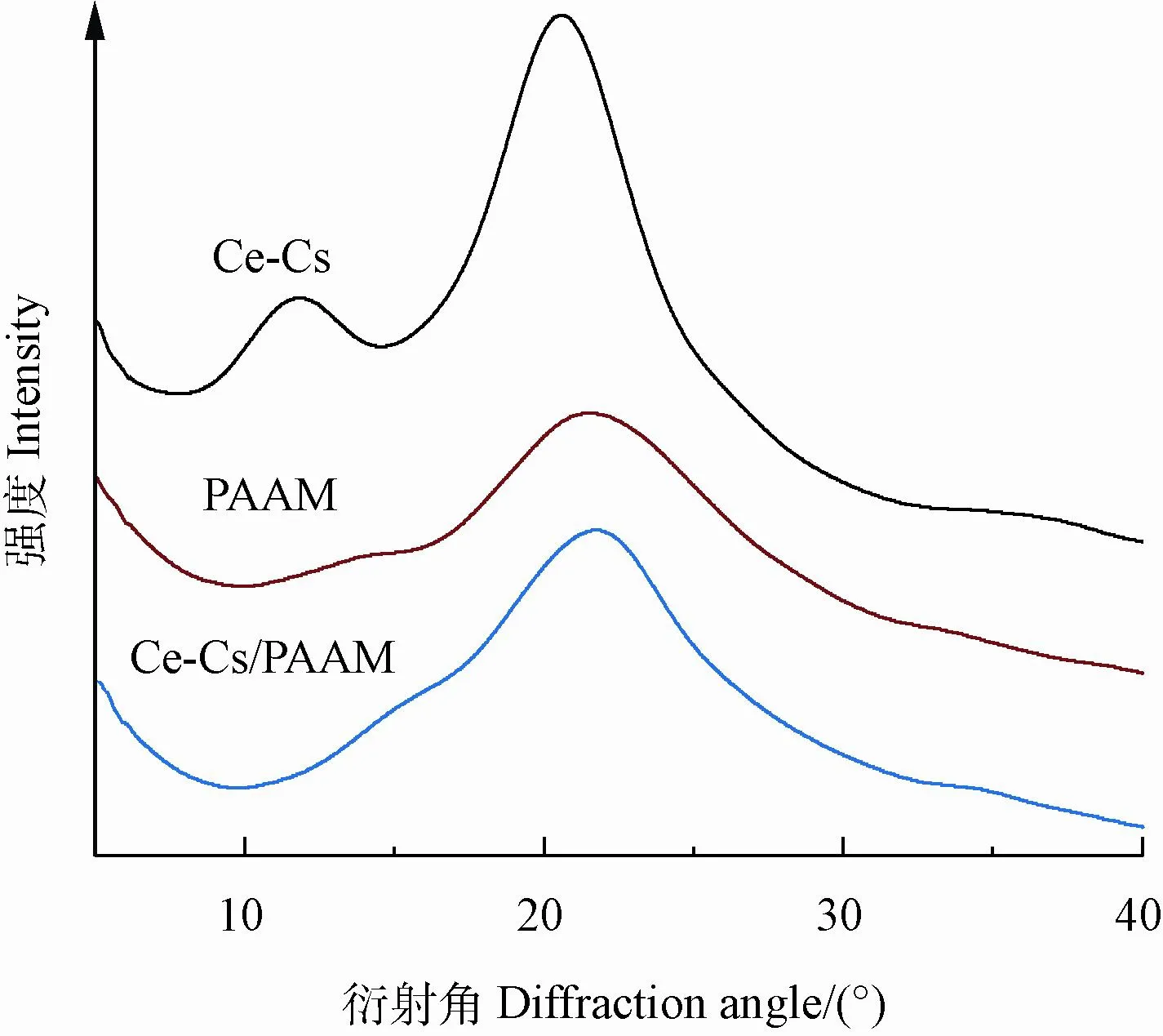
图6 不同水凝胶XRD谱图Fig.6 X-ray diffractometer(XRD)spectra of different hydrogel
2.4 力学性能结果分析
如图7所示,在压缩应变达到80%时,其压缩强度随着应变的增加而显著增大,当压缩应变达到90%时,压缩强度达到最大值60 MPa,是Ce-Cs水凝胶的强度的127倍[30],是PAAM水凝胶的强度的60倍[31],是聚丙烯酰胺/纤维素纳米纤维双网络水凝胶的强度的25倍[32]。这是因为纤维素接枝在壳聚糖网络作为第一层网络增加水凝胶的密度,交联反应可以增加水凝胶的化学稳定性,增加其刚性结构,同时,我们将聚丙烯酰胺作为第二层网络,使Ce-Cs/PAAM水凝胶的韧性也得到了很大提升,在压缩应变达到90%时,其结构依然没有被破坏掉。这些结论说明了Ce-Cs/PAAM水凝胶具有优异的机械性能,为其在诸多应用上提供良好保障。
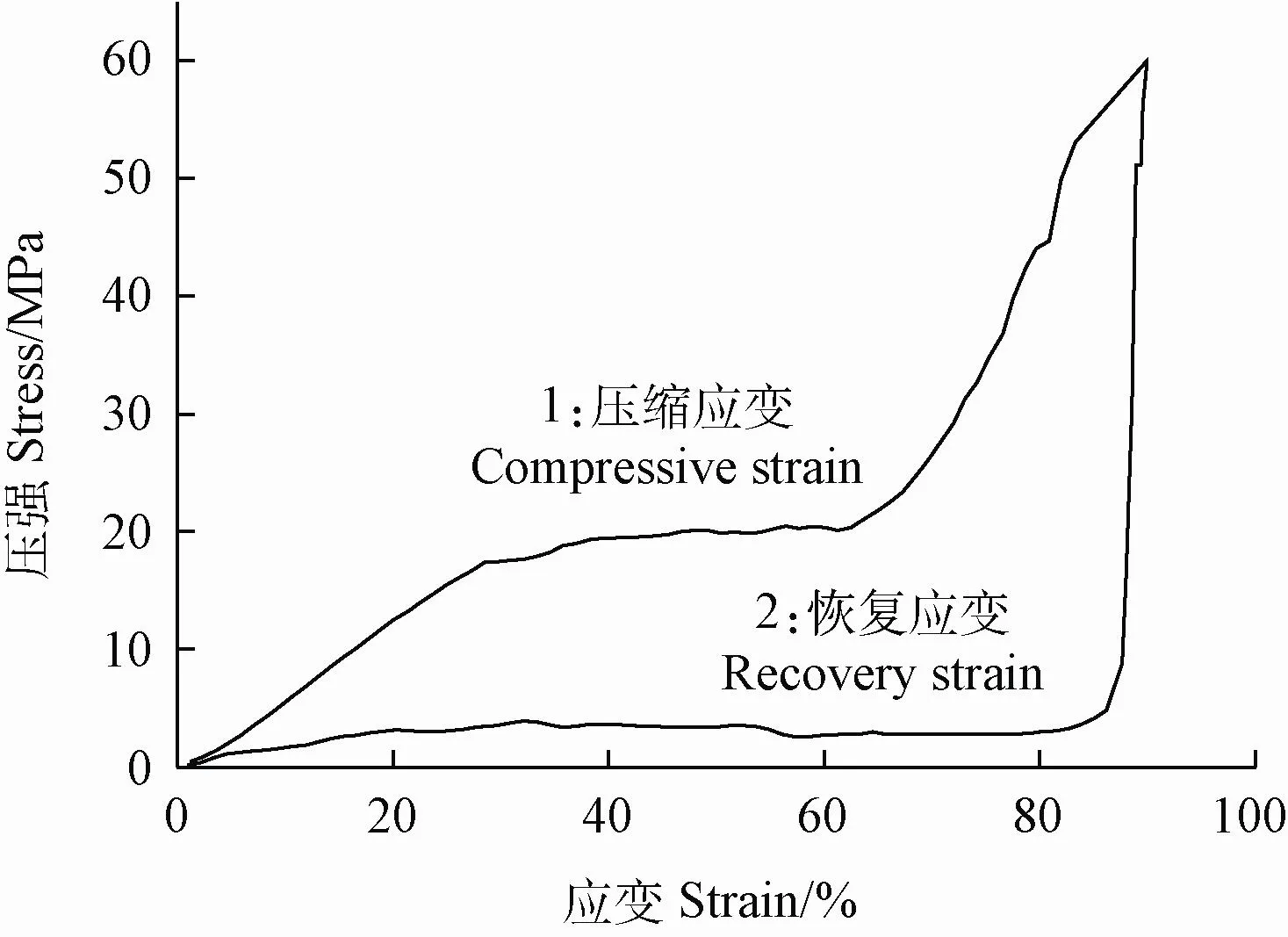
图7 壳聚糖-纤维素/聚丙烯酰胺(Ce-Cs/PAAM)水凝胶压缩应力-应变曲线Fig.7 Compressive stress-strain curves of cellulose-chitosan/polyacrylamide(Ce-Cs/PAAM)hydrogel
2.5 溶胀性能结果分析
图8 a显示了3种水凝胶在室温下浸入超纯水中7 d充分溶胀后的溶胀度。Ce-Cs水凝胶的溶胀度为8.66 mg/mg,因为纤维素和壳聚糖中存在更多的N-H基团,这些基团增加了Ce-Cs混合水凝胶对水分子的亲和力[33];由于引入柔性PAAM网络,Ce-Cs/PAAM水凝胶的溶胀度提高至9.56 mg/mg,可能是PAAM与Ce-Cs形成双层网络的过程中形成较强的氢键,使凝胶网络变得紧密,水分子进入水凝胶网络结构比较困难,限制了水凝胶的膨胀。特别是与PAAM水凝胶相比,显示出较低的溶胀度[34]。溶胀性结果进一步证实了柔性PAAM网络填充于Ce-Cs刚性网络的空隙中形成了结构更加紧密的双网络结构,这与SEM、XRD的分析结果一致。
由图8b可以看出,Ce-Cs/PAAM水凝胶在不同pH值缓冲溶液中的溶胀性能的变化,在pH值2.0~6.0时,水凝胶的平衡溶胀度基本保持在相对较低的水平,这可能是因为在较低pH值缓冲溶液中存在大量的质子氢会与水凝胶中的酰胺基团结合形成-NH3+,使得水凝胶网络结构的静电斥力增加,但同时低pH值环境中,水凝胶内部网络结构的氢键作用力也会增强,从而抑制水凝胶的溶胀率,随着缓冲溶液pH值的升高,氢键作用力减弱,同时溶液提供质子氢的能力也随之降低,形成-NH3+的数量就越少,水凝胶网络的静电斥力减弱,在pH值为6.0~10.0的缓冲溶液中,这2种相反方向的作用力在水凝胶中达到平衡状态,使其溶胀率没有明显变化;当pH值>10.0时,水凝胶的溶胀率急剧增加,这可能因为水凝胶中的酰胺基团在强碱环境中水解为-COO-,水凝胶网络中的静电斥力增加,且在高pH值环境下,水凝胶的氢键作用力减弱,使得静电斥力作用明显处于优势地位,水凝胶的溶胀率显著增加[35]。当pH值为12时,Ce-Cs/PAAM双网络水凝胶的溶胀度增加至15.34 mg/mg。

图8 溶胀性能分析Fig.8 Swelling property analysis
2.6 吸附性能结果分析
Ce-Cs/PAAM水凝胶对Cu2+的吸附作用受离子初始浓度、吸附时间、pH值等因素的影响,图9a所示,Ce-Cs/PAAM水凝胶对Cu2+的吸附随着Cu2+初始浓度的升高而呈上升趋势。在较低的初始Cu2+浓度下,吸附量随初始Cu2+浓度呈线性增加,表明在这些情况下,Ce-Cs/PAAM水凝胶结构存在大量的吸附位点,水凝胶的吸附量取决于Cu2+溶液输送到水凝胶表面的Cu2+的数量;然而在较高的初始Cu2+浓度下,吸附量不再与初始Cu2+浓度成比例增加,表明Ce-Cs/PAAM水凝胶表面上的吸附位点的实际数量限制了吸附量;当初始Cu2+初始浓度C0达到350 mg/L时,Ce-Cs/PAAM水凝胶结构中吸附位点趋于饱和状态,这时Ce-Cs/PAAM水凝胶的吸附量趋于平衡,最大吸附量为298.67 mg/g。
如图9b所示,随着吸附时间的延长,Ce-Cs/PAAM水凝胶对Cu2+的吸附量也随之增加,且在Ce-Cs/PAAM水凝胶与Cu2+溶液接触时间的前10 min,水凝胶的吸附量增加的非常迅速。这是由于Ce-Cs/PAAM水凝胶表面有充足的活性结合位点,有助于水凝胶和重金属离子的结合。Cu2+在初始阶段很容易与这些位置相互作用,吸附速率比很多报道的其他吸附剂快得多[28,36]。随着时间的推移,吸附速率逐渐趋于平衡,在90 min时Ce-Cs/PAAM水凝胶对Cu2+的吸附达到吸附平衡,最大吸附量为312.4 mg/g。与聚丙烯酸/腐殖质双网络水凝胶[29]对Cu2+的吸附量151.00mg/g相比,大幅提高。
如图9c所示,当溶液的pH值从1.5增加到5.5时,Ce-Cs/PAAM水凝胶对Cu2+的吸附能力逐渐增加。在较低的pH值下,Ce-Cs/PAAM水凝胶中的活性胺基很容易被质子化,导致Cu2+离子的静电排斥。pH值为4.5时,由于胺基脱质子化,吸附能力增加。当pH值为5.5时,表面吸附位点达到饱和,最大吸附量为312.4 mg/g。根据酸碱理论,脱氢胺基与Cu2+相互作用强烈,因此,水凝胶的吸附原理应该更准确地描述为螯合作用,而不是静电作用[37]。当pH值为6.5时Cu2+溶液会发生沉淀,吸附量发生急剧下降。

图9 不同条件下壳聚糖-纤维素/聚丙烯酰胺(Ce-Cs/PAAM)水凝胶对Cu2+的吸附性能Fig.9 Adsorption properties of chitosan-cellulose/polyacrylamide(Ce-Cs/PAAM)hydrogel on Cu2+under different conditions
3 结 论
1)本文通过“一锅法”制备了香蕉纤维素-壳聚糖/聚丙烯酰胺双网络水凝胶(Ce-Cs/PAAM),(Ce-Cs/PAAM)双网络水凝胶具有三维多孔网络结构,其中纤维素的结晶结构在复合物的制备过程中受到了破坏,纤维素的结晶度下降,这些结构特点有助于吸附重金属离子;
2)刚柔网络互穿缔合大大提升了Ce-Cs/PAAM双网络水凝胶的机械性能,在压缩应变为90%的情况下,其压缩强度能够达到60 MPa;
3)Ce-Cs/PAAM双网络水凝胶具有较好的溶胀性能,尤其在强碱性环境下(pH值为12时),Ce-Cs/PAAM双网络水凝胶的溶胀性能最好,溶胀度达到15.34 mg/mg;
4)吸附试验结果表明,Ce-Cs/PAAM双网络水凝胶对Cu2+的吸附受Cu2+初始浓度、吸附时间、Cu2+溶液pH值的影响,最优吸附条件为:Cu2+初始浓度350 mg/L、吸附时间90 min、pH值为5.5,此时最大吸附量为312.4 mg/g。
此外,本文制备的Ce-Cs/PAAM双网络水凝胶所用材料香蕉纤维素(Ce)、壳聚糖(Cs)都是世界上最丰富的天然高分子材料,数量大、来源广、价格低,所使用的溶剂是常规乙酸(AA),另外,丙烯酰胺(AAM)、N,N-亚甲基双丙烯酰胺(MBA)、α-酮戊二酸,过硫酸钾(PPS),环氧氯丙烷(ECH)都是常规试剂,反应条件不需要高温高压高辐射,“一锅法”大大简化制备工艺,因此作为重金属吸附剂具有成本低、强力好的优点。其吸附机理、解析以及重复吸附性能将在后续研究中陆续报道。
